紫杉醇注射液杂质检查方法建立①
于俊清
摘 要:目的 对有关物质检查方法筛选,建立紫杉醇注射液有关物质检查方法。方法 采用高效液相色谱法,色谱柱为Ultimate柱(250mm*4.6mm,5μm),以乙腈:水为流动相,进行梯度洗脱,柱温40℃,流速为1.0mL/min,检测波长为230nm。结果 辅料对有关物质测定无干扰,耐用性试验表明色谱条件微小变化杂质检出基本一致,溶液稳定性研究结果表明溶液在8h内稳定,该品检测限溶液溶度为97ng/mL,专属性试验结果表明各条件下降解产物与主峰可有效分离。结论 梯度洗脱检查杂质更准确,方法学试验各项指标符合规定,可用于该品有关物质检查。
关键词:紫杉醇 方法学 含量测定
中图分类号:R284.1 文献标识码:A 文章编号:1672-3791(2015)03(b)-0214-01
紫杉醇是红豆杉属植物中的一种复杂的次生代谢产物,也是目前所了解的惟一一种可以促进微管聚合和稳定已聚合微管的药物。同位素示踪表明,紫杉醇只结合到聚合的微管上,不与未聚合的微管蛋白二聚体反应。细胞接触紫杉醇后会在细胞内积累大量的微管,这些微管的积累干扰了细胞的各种功能,特别是使细胞分裂停止于有丝分裂期,阻断了细胞的正常分裂。目前已上市紫杉醇制剂厂家较多,有关物质检查方法较多,除文献方法外[1-6],《中国药典》2010年版二部收载紫杉醇制剂有关物质检查方法,通过对各检查方法比较,发现色谱条件对杂质检出情况有明显差别,普通的等度洗脱无法有效检出全部杂质,本文对梯度洗脱方法进行优化,建立梯度方法检查本品有关物质,并对方法进行详细验证。
1 仪器与试药
日本岛津高效液相色谱仪LC-20A(DAD检测器),色谱柱Ultimate AQ-C18 5 μm 4.6×250 mm,乙腈为色谱纯(Dima),紫杉醇(含量:99.6%,使用前不需干燥,批号:100382-201102)、紫杉醇杂质Ⅰ(7-表-10-去乙酰基紫杉醇,批号:100925-201102)、杂质Ⅱ紫杉醇杂质Ⅱ(7-表-10-去乙酰基紫杉醇,批号:100926-201102)和杂质Ⅲ(7-表-紫杉醇,批号:100927-201102)购自中国食品药品检定研究院。
紫杉醇注射液由哈药集团生物工程公司提供,乙腈为色谱纯,其它试剂均为分析纯。
2 方法与结果
2.1 色谱条件
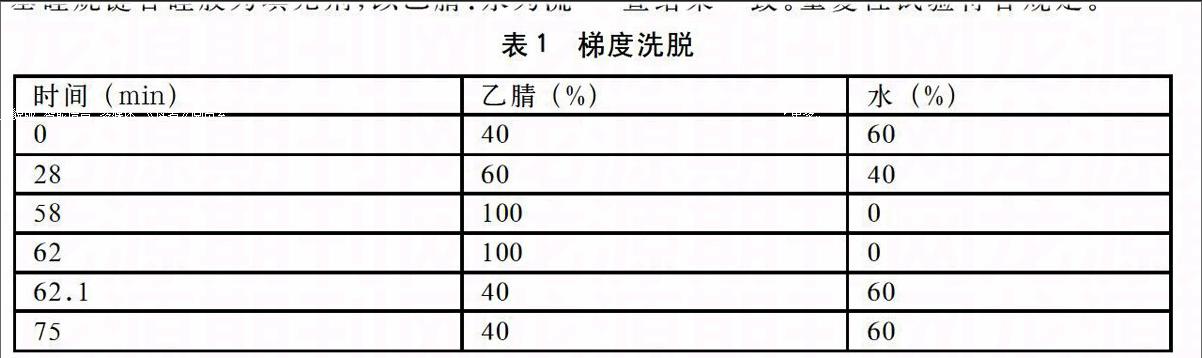
分别取紫杉醇、紫杉醇杂质对照品、空白辅料、起始物料及中间体,加乙腈使溶解,制成单一溶液及混合溶液,按照文献方法分别进样,根据杂质检出及分离情况对方法进行优化,结果如表1,紫杉醇与其它物质可有效分离,紫杉醇峰纯度符合规定,辅料、中间体及起始物料不干扰含量测定。
色谱条件与系统适用性试验用十八烷基硅烷键合硅胶为填充剂,以乙腈:水为流动相,进行梯度洗脱,柱温为40℃,检测波长为230 nm。理论塔板数不低于5000,紫杉醇与杂质Ⅰ、杂质Ⅱ及杂质Ⅲ的分离度应符合规定。
测定法 取该品2.5 mL置10 mL量瓶中,用乙腈稀释并定容至刻度,作为供试品溶液,精密量取供试品溶液1.0 mL于50 mL量瓶中,加乙腈稀释至刻度,作为对照溶液,精密量取空白辅料溶液2.5 mL于10 mL量瓶中,加乙腈至刻度,作为空白辅料溶液,精密量取上述溶液各20 μL注入液相色谱仪,记录色谱图。
2.2 系统适用性试验
取紫杉醇对照品、紫杉醇与杂质Ⅰ、杂质Ⅱ及杂质Ⅲ加乙腈使溶解,作为系统适用性溶液,按照拟建立色谱条件进样,结果杂质Ⅰ、杂质Ⅱ及杂质Ⅲ与紫杉醇分离度符合规定。
2.3 耐用性试验
改变柱温(35℃、4015℃、45℃)、色谱柱(相同品牌不同批号的3根色谱柱)及流速(0.8 mL/min、1.0 mL/min、1.2 mL/min),评价各项指标改变对有关物质检查结果的影响,同时评价各色谱条件下系统适用性,结果表明各项指标变化对有关物质结果无影响,耐用性试验符合规定。在各种色谱条件下对称因子在0.9至1.1之间,塔板数均大于10000。
2.4 检测限
取紫杉醇对照品,7-表-10-去乙酰基紫杉醇对照品,7-表-10-去乙酰基紫杉醇对照品,7-表-紫杉醇对照品,制成系列浓度溶液,进样,当信噪比约为3:1时,各进样浓度为检测限浓度。结果紫杉醇、7-表-10-去乙酰基紫杉醇、7-表-10-去乙酰基紫杉醇及7-表-紫杉醇检测限分别为97 ng/mL、86 ng/mL、91 ng/mL、164 ng/mL, 供试品溶液浓度可有效检出杂质。
2.5 重复性试验
取供试品溶液,重复测定6次,结果6次测定结果杂质Ⅰ、杂质Ⅱ及杂质Ⅲ与紫杉醇分离度均符合规定,6次测定有关物质检查结果一致。重复性试验符合规定。
2.6 溶液稳定性试验
精密量取供试品溶液,加乙腈稀释至刻度,作为供试品溶液;取供试品溶液1.0 mL于50 mL量瓶中加乙腈稀释至刻度,作为对照品溶液。室温条件下放置放置8 h,分别于0 h、1 h、2 h、4 h、6 h及8 h进样。结果对照溶液峰面积变化的标准偏差为0.26%,保留时间相对标准偏差为0.41%,符合规定,供试品溶液放置8 h无新的杂质峰产生,各杂质峰无明显变化,供试品溶液及对照品溶液在8小时内稳定。
2.7 专属性试验
取紫杉醇注射液样品,对样品进行酸(0.1 mol/mL)、碱(0.1mol/mL)、氧化(30%过氧化氢溶液)、高温(100℃)及强光(5000LX)破坏试验,使用DAD检测器,全波长监测,考察各种破坏条件下杂质检出情况。结果230 nm为该品最佳检测波长,确定供试品检测波长为230 nm,供试品在各条件下降解产物约为5%,杂质与主峰可有效分离,峰纯度符合规定,各破坏条件下物料平衡。说明梯度洗脱方法可行。
上述方法学试验结果表明所建立方法可行,杂质与主峰可有效分离。
3 讨论
对检查方法进行优化,新方法运行时间较长,但优化后的杂质检查方法可有效检出起始物料、中间体及降解产物,主峰与杂质峰分离度符合规定,分离识别效果更优。
参考文献
[1] 骆泽宇.紫杉醇的药理与临床研究进展[J].现代中西医结合杂志,2006,15(24):3457-3458.
[2] 吴健敏,张才煜,张启明.关于HPLC法测定紫杉醇有关物质方法的探讨[J].中国药事,2009(11):1072-1075.
[3] 张艳霞,孙磊.紫杉醇有关物质检测HPLC法色谱条件优化[J].首都医药,2011(22):53-54.
[4] 杨雪梅,徐江平.紫杉醇注射液含量及其有关物质的检测[J].中国药学杂志,2001,36(11):841-842.
[5] 赵亮,徐炳欣,石晓晓,等.RP-HPLC法测定紫杉醇注射液的含量及有关物质[J].中国实用医药,2014,9(5).
[6] 杨蓓,郑璐侠,段更利,等.高效液相色谱法测定多西紫杉醇注射液含量及其有关物质[J].复旦学报,2006,33(5):701-702.

