环戊醇制备工艺研究进展
蒋方红 周 飞 王继媛 吴忠平 奚 军
(中国石化上海石油化工股份有限公司精细化工部,200540)
国内外行业发展动态
环戊醇制备工艺研究进展
蒋方红 周 飞 王继媛 吴忠平 奚 军
(中国石化上海石油化工股份有限公司精细化工部,200540)
环戊醇是重要的医药、农药精细化工产品中间体,应用较为广泛。环戊醇制备路线按照原料的不同分为己二酸法、环戊烯法和环戊烷法,这几种方法各有优缺点,文章对这些方法进行了详细的技术比较。环戊烷氧化法因其原料价格优势、环境友好的催化剂体系和工艺会是今后环戊醇的制备方向。
环戊醇 己二酸 环戊烯 环戊烷 催化剂
环戊醇为无色液体,具有芳香性气味,是重要的医药、农药精细化工产品中间体。环戊醇溶于乙醇,微溶于水,主要用于药物、染料和香料的生产,是制备环戊酮、卤代环戊烷、治疗水肿及高血压的药物环戊甲噻嗪及新型非巴比妥静脉麻醉药开他敏不可缺少的原料,也可在药物和香料合成中用作溶剂[1-2]。自然界中环戊醇仅存在于少量植物中且含量较低,提取较困难。环戊醇的国外生产企业主要是印度碱金属有限公司、法国Rhodia公司、日本Zeon 公司和德国BASF公司。目前,环戊醇制备路线按照原料的不同分为己二酸法、环戊烯法和环戊烷法。
1 己二酸法
国内目前主要采用己二酸法生产环戊酮,再加氢获得环戊醇。从化学反应看,环戊酮可以加氢生成环戊醇、己二酸及其衍生物热解法生产环戊酮技术相对成熟,约占世界总产量的90%以上。将己二酸在以化学计量的氢氧化钡存在下加热至285~295 ℃,生成粗环戊酮,再经水蒸气蒸馏、萃取、精馏得到高纯度的环戊酮[3],也可用氟化锂做催化剂。己二酸的脂类衍生物,如己二酸二甲酯、己二酸二乙酯等,在高温条件下也可以发生环化作用生成环戊酮,所用的催化剂主要有MnO2、Al2O3及CeO2等。该法虽然收率较高,但由于原料价格昂贵,且产生大量污染物,工艺路线长,所以此工艺的进一步发展受到限制[4]。
2 环戊烯法
2.1 环戊烯硼氢化-氧化法
环戊烯可通过硼氢化-氧化法制备环戊醇。Brown[5]将一定量的乙硼烷和1,4-噻恶烷在室温下反应,然后降温至0 ℃,得到结晶的1,4-噻恶烷硼化物。它与环戊烯反应生成产率较高的烷基硼化物,在碱性过氧化物的作用下氧化得到环戊醇。其化学方程式如下:
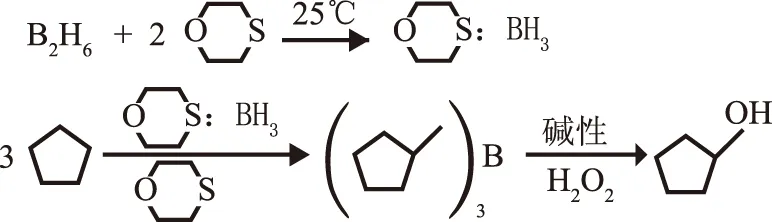
此法环戊醇的收率可达到95%,虽然收率较高,但是原料乙硼烷的资源有限,价格昂贵,且毒性较大,对环境污染严重,因此不适宜工业化。
2.2 环戊烯直接氧化法
环戊烯先直接氧化成环戊酮,再加氢得环戊醇。C5馏分是石油炼制的副产物,资源丰富,价格低廉,以C5馏分为原料生环戊醇的研究虽然起步较晚,却受到广泛的关注,成为国内环戊醇合成新途径研究的焦点。
Starokon等[6-8]在不使用任何催化剂下,研究了N2O液相氧化链烯、环烯、杂环烯及其衍生物生成羰基化合物的反应。实验结果表明:烯烃的结构和组成是影响反应选择性的主要因素,重氮甲烷的生成是端烯烃发生氧化反应的特征产物;在N2O压力2.5 MPa,温度200 ℃,反应时间约20 h时,环戊烯具有较好的氧化效果,转化率为67%,环戊酮选择性达99%。Dubkov等[7-9]则更进一步,使环戊烯转化率达94.2%,环戊酮选择性接近100%。
非催化剂直接氧化法虽然不需要任何催化剂而且环戊酮收率较高,但反应需在高温、高压条件下进行,初始压力一般为6 MPa,随着反应温度的升高,压力进一步增大,当温度为230 ℃时,反应器内的压力可达11.5 MPa。因此对反应设备及操作的要求比较高,实际应用困难较大。
2.3 环戊烯wacker氧化法
自从wacker 型催化剂(PdCl2-CuCl2)催化乙烯氧化制备乙醛取得成功后, wacker法已成为目前烯烃氧化羰基化的重要方法之一。 wacker型催化剂用于环戊烯氧化制环戊酮时,由于氯化钯水溶液在环戊烯中的溶解度很差,很难与环戊烯有效配位,需选择一种合适的溶剂体系,增加钯与烯的接触,在合适的温度及压力条件下,制备环戊酮,再加氢得环戊醇。
Takehira等[10-11]在乙醇溶剂中,考察了氧气压力对PdCl2-CuCl2、PdCl2-FeCl3催化环戊烯氧化的影响。在1.01×105Pa下,PdCl2-CuCl2、PdCl2-FeCl3催化氧化环戊烯,其转化率分别为98%和50%,环戊酮选择性分别为70%和90%。
由于反应体系中含有大量的氯离子,传统Wacker反应不仅设备腐蚀严重,还会引起含氯副产物的生成,既导致了产品收率的下降,又造成了产品分离和废水处理方面的困难。同时由于烯烃结构上的空间效应和钯催化反应的异构化,因此Wacker催化剂催化较高碳数的端烯烃、内烯烃、环烯烃的催化活性较之于乙烯的氧化来说要低得多,因此,改进的Wacker类催化剂的催化活性已引起人们广泛的注意。一些新型的不含氯离子的钯配合物催化体系的研究也非常活跃。通过选择合适的共溶剂、共氧化剂、钯配合物,或采用固载化的Wacker类催化剂,相转移催化剂均可一定程度地改进Wacker类催化剂的催化活性。
目前国内的研究大多停留在实验室的水平,应该加强相关的研究,尽快实现产业化。
2.4 环戊烯水合工艺法
烯烃水合法是制备相应醇的一种重要方法,水合方法有直接法和间接法两种。间接法是将烯烃用硫酸或磺酸磺化,然后水解获得相应的醇;直接法是采用强酸性阳离子交换树脂、杂多酸、分子筛或固体酸作为催化剂,把烯烃直接水合得到相应的醇。
2.4.1 环戊烯间接水合法
在传统的由烯烃生产有机醇的工艺中,原料烯烃与一定浓度的硫酸反应生成硫酸酯,再水解制得相应的醇。
郭世卓[12]对环戊烯水合制备环戊醇工艺进行了研究。当硫酸浓度为75%,环戊烯与硫酸的物质的量比为(1~1.2)︰1,搅拌速度大于220 r/min,磺化温度为30~35 ℃,水解硫酸浓度小于30%时,环戊烯的单程转化率为60%左右,环戊醇的选择性在95%左右。
间接水合工艺除了固有的硫酸对设备的腐蚀外,稀硫酸的浓缩所消耗能源较大和回收硫酸质量不稳定,都是该路线的不足之处,为此,Knudsen等[13]对稀硫酸的浓缩进行了改进。通过在废硫酸中加入氧化剂,使有机物氧化得以脱除,再经脱水后得到可以循环使用的硫酸,从而减少了环境污染,Robert等[14]研究了以0.05%~40%的硫酸为磺化剂进行烯烃水合的过程。此外,Ernst等[15]对烯烃间接水合工艺进行了改进,但仍然无法从根本上解决间接水合工艺的缺陷。因此,这种工艺除用于某些特定结构醇的生产外,大部分产品均改为烯烃直接水合工艺。
2.4.2 环戊烯直接水合法
为了解决烯烃间接水合存在的问题,开发了使用多相催化剂催化烯烃直接水合制备有机醇的技术。在各种酸性催化剂作用下,烯烃与水直接反应生成有机醇,虽然在直接水合法中,烯烃的单程转化率较低,但由于保持了较好的选择性,回收的烯烃可以循环使用,仍然达到了较高的反应收率,更重要的是从工艺上解决了硫酸对设备的腐蚀和环境污染。
直接水合工艺合成环戊醇是以环戊烯为原料,在酸性催化剂的作用下进行水合反应生成环戊醇。与硫酸间接水合法相比,直接水合法虽然单程转化率较低,但是由于环戊烯沸点低,回收循环使用简单且能耗少,对环境的污染少,属于环境友好工艺。
环戊烯直接水合工艺的研究中酸性催化剂的筛选尤为重要。目前已见文献报道环戊烯水合制环戊醇所用固体酸催化剂有:强酸性阳离子交换树脂、杂多酸类、分子筛、铌酸催化剂和固体超强酸等。
3 环戊烷法
从天然气和石油中得到的原料很大一部分是以烷烃形式存在,烃类的选择氧化一直是催化和环境化学领域具有挑战性的研究课题,而烷烃氧化作为较难的一类氧化反应,其氧化中间产物是精细化工和石油化工等各个领域的重要生产原料,因此烷烃的高效选择性氧化已经成为化学工业的重要课题之一,引起了众多科研工作者的高度关注。
Gopal S. Mishra 等[16]开发了以氧气为氧化剂、环戊烷和环辛烷为氧化催化剂,采用含过渡金属的钒氧化物制备催化剂,在压力为1.0~1.4 MPa,温度150~160 ℃的反应条件下,环戊酮的收率达到10%,选择性达75%。专利CN101547881[17]提供了一种环烷烃氧化的方法,在一种含有氮原子的环状化合物存在下,首先将环戊烷氧化得到环戊烷氧化产物,环戊烷的转化率只有3.8%,环戊酮选择率为24.1%,环戊醇选择率为12.3%,环戊基过氧氢选择率为34.2%。再将氧化产物中的环戊基过氧氢分解得到环戊醇和环戊酮,过氧化物转化率可以达92.7%。专利CN102382025[18]公开了一种环烷烃氧化的方法,以臭氧为氧化剂,在含钛催化剂存在下,环戊烷转化率为27%,环戊酮选择性为4%。
针对环戊烷的氧化研究比较少,主要是参照环己烷的工艺和催化剂。但是由于五元环和六元环结构的不同,催化剂需要更加针对性的开发。
3.1 环己烷氧化法
环己烷氧化反应制备环己醇和环己酮(俗称KA油)是工业上的一类重要反应。环己酮是制备己内酰胺和己二酸进而制得尼龙-6和尼龙-66 的主要中间体, 世界90%以上的环己酮采用该法生产。环己烷氧化制备环己醇和环己酮的方法可以分为非催化氧化法和催化氧化法。所用氧化剂可以是空气、纯氧、H2O2等,根据氧化剂的不同又可分为氧气法和其他氧化剂法。非催化氧化工艺中环己烷转化率低于5%,醇酮选择性约80%,产生大量难于处理的碱渣,不符合当今对环境保护方面的要求。因此如何同时维持高转化率和高选择性,降低污染和能耗一直是国内外研究的难点和热点。寻找一种高活性、高选择性的催化体系是实现这一目标的重要途径。
3.2 环己烷氧化催化剂
环己烷氧化的工艺中,催化剂的改进是研究的重点。环己烷催化氧化所用的催化剂体系主要包括钴盐法催化剂体系、硼酸法催化剂体系、Gif体系、仿生催化剂、过渡金属氧化物和分子筛催化剂等。其中钴盐法催化剂体系、硼酸法催化剂体系已应用到工业化生产中[19]。
3.2.1 硼系列催化剂
该法以硼酸或偏硼酸为催化剂,其用量为环己烷的5%~l0%。该催化剂可以提高环己烷的转化率和环己酮、环己醇的选择性。在空气氧化过程中,硼酸或偏硼酸与环己基过氧化物形成过硼酸环己醇酯,然后再转变为环己醇酯,或者与环己醇结合生成硼酸环己醇酯和偏硼酸环己醇酯。氧化产物中含环己醇硼酸酯,用水处理,硼酸酯水解生成环己醇和硼酸,形成水相和油相,水相中主要溶有硼酸,而油相主要是环己烷、环己醇及少量环己酮。油相经水洗、皂化和蒸馏后得环己醇。
硼酸催化法环己烷利用率高,环己酮收率高,耗碱少,但是此法必须有水解过程和硼酸的回收系统,使设备投资比钴盐催化法高。
3.2.2 钴盐法催化剂体系
钴盐催化法一般采用环烷酸钴、辛酸钴、油酸钴、硬脂酸钴、环烷酸钴铬复合物等钴盐为催化剂。环己烷在催化剂作用下与空气发生氧化反应,生成主要产物环己酮和环己醇。氧化反应的过程是首先通过游离基反应形成环己基过氧化氢,然后过氧化物在催化剂作用下受热而分解,生成环己酮和环己醇,同时由于环己酮和环己醇比环己烷更容易氧化,有许多副产物生成。
为了减少副产物的生成,提高产物的选择性及收率,必须控制环己烷的转化率,以及环己酮和环己醇的停留时间。但是,如果转化率太低,大量的环己烷未反应,分离过程投资大,经济效益差,停留时间太长,环己酮、环己醇被深度氧化,其选择性和收率均下降。因此一般将转化率控制在5%~10%,停留时间为5~ 30 min。
钴盐催化法反应条件温和,反应温度和压力都较低,停留时间短,对设备要求不严格。世界上许多工厂如巴斯夫、杜邦等都利用钴盐催化剂实现了工业化。但是钴盐催化氧化环己烷时会生成一些一元酸和二元酸等副产物,这些酸会与钴离子形成盐, 从而在反应设备及管道中结渣。此外,由于环己醇和环己酮很容易被氧化生成羧酸副产物,因此降低了该催化体系中产物的收率。
3.2.3 Gif 体系
Gif体系是由Barton 等人在20 世纪90年代初期提出的,是用FeCl3、Zn、O2、乙酸和吡啶组成的氧化体系,它的特点在于可以在低温或者室温下以非自由基历程将烷烃氧化。GoAggⅡ体系是Gif体系中最具代表性和氧化效率最高的一个体系,它由吡啶、乙酸、FeCl3和H2O2等组成,对酮具有更高的选择性。
3.2.4 金属配合物催化剂
非生物模拟配合物体系自20世纪90年代开始由研究者应用于环己烷催化氧化反应。金属配合物是一类重要的均相烷烃氧化剂,具有很高的活性和选择性,在环己烷氧化反应中得到了大量应用。Velusamy等[20]以乙腈为溶剂,双氧水为氧化剂,配合物CuⅡsalen为催化剂催化氧化环己烷,在80 ℃下反应5 h,环己酮收率可达18%。这类配合物担载量很低,在反应过程中金属流失很大,因而限制了它们的应用。
3.2.5 过渡金属氧化物
过渡金属氧化物具有较强的氧化性能,可以作为氧化催化剂,因此在环己烷氧化反应中也得到了应用,特别是纳米金属氧化物,因其较大的比表面积,具有较高的催化活性,近年来得到了广泛的应用。原伟伟[21]对纳米金属氧化物催化氧化环己烷做了比较系统的研究,结果表明该类催化剂具有很高的催化活性,如以叔丁基过氧化氢和异丁醛为引发剂,纳米无定形氧化铁为催化剂,在70 ℃的常压下反应3 h,环己烷转化率可以达到16.8%,醇酮选择性可以达到94.5%。
3.2.6 分子筛催化剂
分子筛催化剂具有优良的催化性能,被广泛的应用于催化氧化反应中。在催化氧化环己烷中,国内外研究较多的是钛硅分子筛。钛硅分子筛催化体系采用双氧水为氧化剂,还原产物是水,无污染物生产,是典型的环境友好催化剂。
Spinacé 等以水热法合成德分子筛Ts-1 为催化剂,丙酮为溶剂催化氧化环己烷,在150 ℃下反应8 h,环己烷转化率达到了12%。研究表明,环己烷氧化产物环己醇和环己酮在Ts-1分子筛外表面进一步发生非选择性地氧化生成己二酸等深度氧化产物,而在分子筛孔道内环己醇可以选择性的氧化为环己酮。在反应体系中加入2,6-二叔丁基-4-甲基苯酚(BHT)后,可以有效抑制分子筛外表面的非选择性氧化反应,提高环己酮选择性。
除了钛硅分子筛,研究者将其他过渡金属掺杂到各种分子筛中,制备出各种氧化还原分子筛并将其用于环己烷催化氧化反应。赵培庆等[22]以H2O2为氧化剂,Ti-MMM-1 分子筛为催化剂在100 ℃下催化氧化环己烷,环己烷的转化率可达10 % ,环己醇和环己酮的总选择性为100 %。中国石油化工股份有限公司石油化工科学研究院自主研发了空心钛硅分子筛HTS,氧化活性高,活性稳定性好[23]。在反应温度60~80 ℃,催化剂质量分数5%~10%,n(Cyclohexane)/n(H2O2)=0.5,n(Acetone)/n(Cyclohexane)=12,反应时间6~10h。在此条件下,酮醇产率和产物酮/醇(物质的量比)分别可超过40%和2.0。
但是由于五元环和六元环结构的不同,环戊烷氧化制环戊醇催化剂需要更加针对性的开发。
4 结语
目前,环戊醇制备路线按照原料的不同分为己二酸法、环戊烯法和环戊烷法。己二酸热解法约占世界环戊酮总产量的90%以上,但该法存在原料短缺、价格高和污染大等缺点,亟待开发新的环戊酮生产方法从而来制备环戊醇。环戊烯水合制环戊醇工艺路线较长,间接水合法因为用到强酸对设备要求高,直接水合法酸性催化剂的筛选尤为重要。环戊烯氧化法分为非催化氧化法和催化氧化法,非催化氧化法采用N2O,高温高压,对设备有较高的要求,但若能够稳定地获得N2O,则将是一个有意义的方法。负载型我wacker催化剂具有分离容易和催化性能良好的优点,但目前负载wacker型催化剂尚存在有效成分在反应过程容易流失的问题,亟待研发新的负载方法和相应的反应体系。环戊烷氧化法原料有价格优势,如采用双氧水作氧化剂,氧化副产物只有水,不对环境造成污染,此工艺还在研究阶段。所以,若能从中找到一种低成本、高效率、环境友好的催化剂体系和工艺,并将其工业化,必为环戊醇生产带来巨大的进步。
[1] 张思规. 精细有机化学品技术手册(上册)[M]. 北京: 科学出版社, 1991: 3-16.
[2] 徐克勋.精细有机化工原料及中间体手册[M].北京:化学工业出版社,1998.2-15.
[3] 陈甘棠. 化学反应工程[M]. 北京: 化学工业出版, 2000: 11-33.
[4] 侯玲, 许绍东, 于大伟. 一种环戊醇的制备方法:中国,1762943 [P]. 2006-04-26.
[5] Brown H. C. Borane-1, 4-thioxane: US, 4298750A[P]. 1981-11-03.
[6] Starokon E V,Dubkov K A,Babushkin D E,et al. Liquid phase oxidation of alkenes with nitrous oxide to carbonyl compounds [J].Adv. Synth. Catal.,2004,346(2):268-274.
[7] Panov G I,Dubkov K A,Starokon E V,et al. Method for producing monocyclic ketones C4-C5:US,20060106258[P]. 2006-05-18.
[8] Parmon V N,Panov G I,Uriarte A,et al. Nitrous oxide in oxidation chemistry and catalysis:application and production [J]. Catal. Tod.,2005,100(2):115-131.
[9] Dubkov K A,Panov G I,Starokon E V,et al. Non-catalytic liquid phase oxidation of alkenes with nitrous oxide. 2. oxidation of cyclopentene to cyclopentanone [J]. React. Kinet. Catal. Lett.,2002,77(1):197-205.
[10] Takehira K, Hayakawa T.Orita H.Mono-oxygenation of cyclopentene by molecular oxygen catalyzed by PdCl2-CuCl2in ethanol[J].J. M. Catal., l989,53(3):15-21.
[11] Takehira K Orita H,Oh I H.Palladium(II)-catalyzed oxidation of cyclopentene in the presence of copper(Ⅱ)一chloride and molecular oxygen[J].J.M.Catal.,1987,42(2):247-255.
[12] 郭世卓. 环境友好的环戊醇和环戊酮制备工艺研究 [D]. 上海: 华东理工大学, 2004.
[13] Knudsen G A, Scotch D, Savini C W. Verfahren zur Verbesserung der verbruchten Schwefelsaeurestroemen:DE,3243007A1[P].1983-07-07.
[14] Robert J S, Hoffman E, Tamotsu Imal. Hydration of olefinic compounds with dilute sulfuric acid and cobalt sulfate:US,4267397[P].1981-05-11.
[15] Ernst J. Improvements in the manufacture of alcohols:GB,1373211[P]. 1974-11-06.
[16] Gopal S.M.,Joao J.R.,Fra’usto da Silva,et al.Supported bis(maltolato)oxovanadium complexes as catalysts for cyclopentane and cyclooctane oxidations with dioxygen[J].Journal of Molecular Catalysis A: Chemical,2007, 265(1):59-69.
[17] 大森匠,佐藤靖.环烷烃氧化产物的制备方法:中国,101547881[P].2007-11-30.
[18] 朱斌,史春风,林民,等. 一种环烷烃氧化的方法:中国, 102382025[P].2012-03-21.
[19] 吴鑫干,刘含茂. 环己烷催化氧化反应及工艺的研究进展[J]. 化工科技, 2002, 10(2):48-53.
[20] Velusamy S, Punniyamurthy T. Copper(II)-catalyzed C-H oxidation of alkylbenzenes and cyclohexane with hydrogen peroxide [J].Tetrahedron Lett., 2003, 44(50):8955-8957.
[21] 原伟伟. 金属纳米催化剂的制备及其对环已烷氧化反应的影响[D]. 北京:北京化工大学, 2008.
[22] 赵培庆,于超英,彭志光,等. 新型分子筛Ti-MMM-1 的合成及其催化性能的研究[J] . 分子催化,2004,18(3) :208 - 212.
[23] 史春风,朱斌,林民.空心钛硅分子筛在环己烷温和氧化反应中的催化性能[J].石油学报(石油加工),2014,30(5):792-797.
Advance of Study on Preparation Process of Cyclopentanol
Jiang Fanghong,Zhou Fei,Wang Jiyuan,Wu Zhongping,Xi Jun
(FineChemicalDivision,SINOPECShanghaiPetrochemicalCo.,Ltd. 200540)
Cyclopentanol is an important fine chemical intermediate for medicine and pesticide, which has extensive application. The preparation routes of cyclopentanol include adipic acid method, cyclopentene method and cyclopentane method based on the raw materials, which each have advantages and disadvantages. Technical comparisons were made among the above methods. It was concluded that cyclopentane oxidation method would be a direction for preparation of cyclopentanol due to its superiority in raw material price, environmentally friendly catalyst system and process.
cyclopentanol, adipic acid, cyclopentene, cyclopentane, catalyst
2015-09-15。
蒋方红,女,1969年出生,1987年毕业于上海科技大学应用化学专业,高级工程师,长期从事精细化工研究工作。
1674-1099 (2015)05-0058-05
TQ233.1
A

