纳米银在水环境中的环境行为和毒性效应研究进展
衣俊,黄俊,程金平,2,*
1. 华东师范大学河口海岸学国家重点实验室,上海200062 2. 香港城市大学深圳研究院,深圳518057
纳米银在水环境中的环境行为和毒性效应研究进展
衣俊1,黄俊1,程金平1,2,*
1. 华东师范大学河口海岸学国家重点实验室,上海200062 2. 香港城市大学深圳研究院,深圳518057
纳米材料的环境行为和生态效应是目前国内外研究的热点,其中纳米银颗粒(AgNPs)是使用量最高的纳米材料。本文主要总结了AgNPs在水环境中的赋存、AgNPs的环境行为、AgNPs对不同种类微生物的毒性效应以及影响AgNPs毒性效应的因素,最后对AgNPs在河口区的研究进行了展望。
纳米银颗粒;微生物;环境行为;毒性效应
当Richard Feynman在1959年的美国物理学会(American Physical Society)上首次提出用近似原子的尺度合成并控制物质的概念时,纳米技术开始逐渐被人们关注[1]。纳米材料被定义为维度小于100 nm的材料,而纳米颗粒被定义为至少有2维在1~100 nm的材料,它们特殊的理化性质使其应用广泛[2]。根据伍德罗威尔逊数据库的统计,截止到2013年10月,全世界有1 628种消费品中含纳米材料,其中含有纳米银颗粒(AgNPs)的产品占383种,是使用量最高的纳米材料[3]。
Ag自身有强杀菌抑菌作用,这使得AgNPs在卫生和医疗等方面有着广泛应用[4-6]。但是随着该类产品的大量使用,进入水环境中的AgNPs对水生生态系统中的生产者和分解者,如微生物、藻类和无脊椎动物等产生很强的毒性。Choi等[7]的研究表明AgNPs能够抑制硝化细菌的生长,在1 mg·L-1的浓度下,AgNPs对自养硝化细菌的呼吸抑制率高达约86%;Miao等[8]通过研究证明人工合成的AgNPs严重抑制海洋硅藻(Thalassiosira weissflogii)的细胞生长、光合作用以及叶绿素合成;Griffitt等[9]发现AgNPs对枝角水蚤(Daphnia pulex)、网纹水蚤(Ceriodaphnia dubia)和羊角月牙藻(Pseudokirchneriella subcapitata)有很强的毒性,其半致死浓度(LC50)分别是0.040 mg·L-1、0.067 mg·L-1和0.19 mg·L-1。同时,含有AgNPs的产品会向环境中释放Ag+[10-11]。尽管Ag+在环境中的背景浓度极低,在自然水体中的浓度范围仅达到0.03~500 ng·L-1[12],但是Ag+在环境中具有持久性和生物积累效应,对水生生物有很强的毒性。有研究表明,一些微型浮游植物在受50~100 ng·L-1的Ag污染后,其生殖能力受到抑制[13]。而90~170 ng·L-1的Ag+就能导致鳟鱼慢性中毒[14]。因此在这个缓慢积累和持续的过程中,AgNPs给环境造成的不利影响无法预计。
微生物是生态系统的基础,也是食物网的基础,同时调控全球生物地球化学循环。水环境中的微生物如细菌、藻类、真菌等容易在水中形成生物膜(biofilm),生物膜是微生物细胞附着在固体表面形成的生物与非生物群体,对水中污染物有吸附和降解功能,在水体自净方面起着重要作用[15-16]。近年来随着长江流域经济的飞速发展,大量污染物通过河口输入至水环境,对水质造成了严重污染,对河口环境的生态系统的结构和功能造成不良影响,并且在一定程度上对长江流域战略水源地青草沙水库造成威胁。除此以外,在水环境中的纳米颗粒不但自身有较强的毒性效应,其特殊的理化性质和吸附性,使其能与水中其他污染物相互作用,成为污染物的传输工具,通过自身的迁移转化改变其他污染物的环境行为,进一步产生污染物复合毒理效应。本文简介了AgNPs在水环境中的赋存和环境行为,重点阐述了AgNPs对水中微生物的毒性效应,为新型纳米颗粒物的环境风险评价提供科学参考。
1 AgNPs在水环境中的赋存和环境行为
在AgNPs的生产、加工和使用等过程中,AgNPs不可避免地进入环境中。水环境中AgNPs的“源”主要有污水排放和大气沉降,排放的污水是最大的污染源,从河口流入的AgNPs在水环境中会经历一系列迁移转化(图1),环境条件如光照、溶解氧、天然有机质等同样影响AgNPs的环境行为,主要过程包括AgNPs团聚和沉降、价态转变、络合作用和生物利用等过程。纳米颗粒在海水中的环境行为与其在淡水中不同,海水离子强度更高,更容易导致纳米颗粒团聚现象,团聚的纳米颗粒最终会聚集在沉积物中,对附着或栖息在沉积物中的底栖生物带来潜在影响[2]。
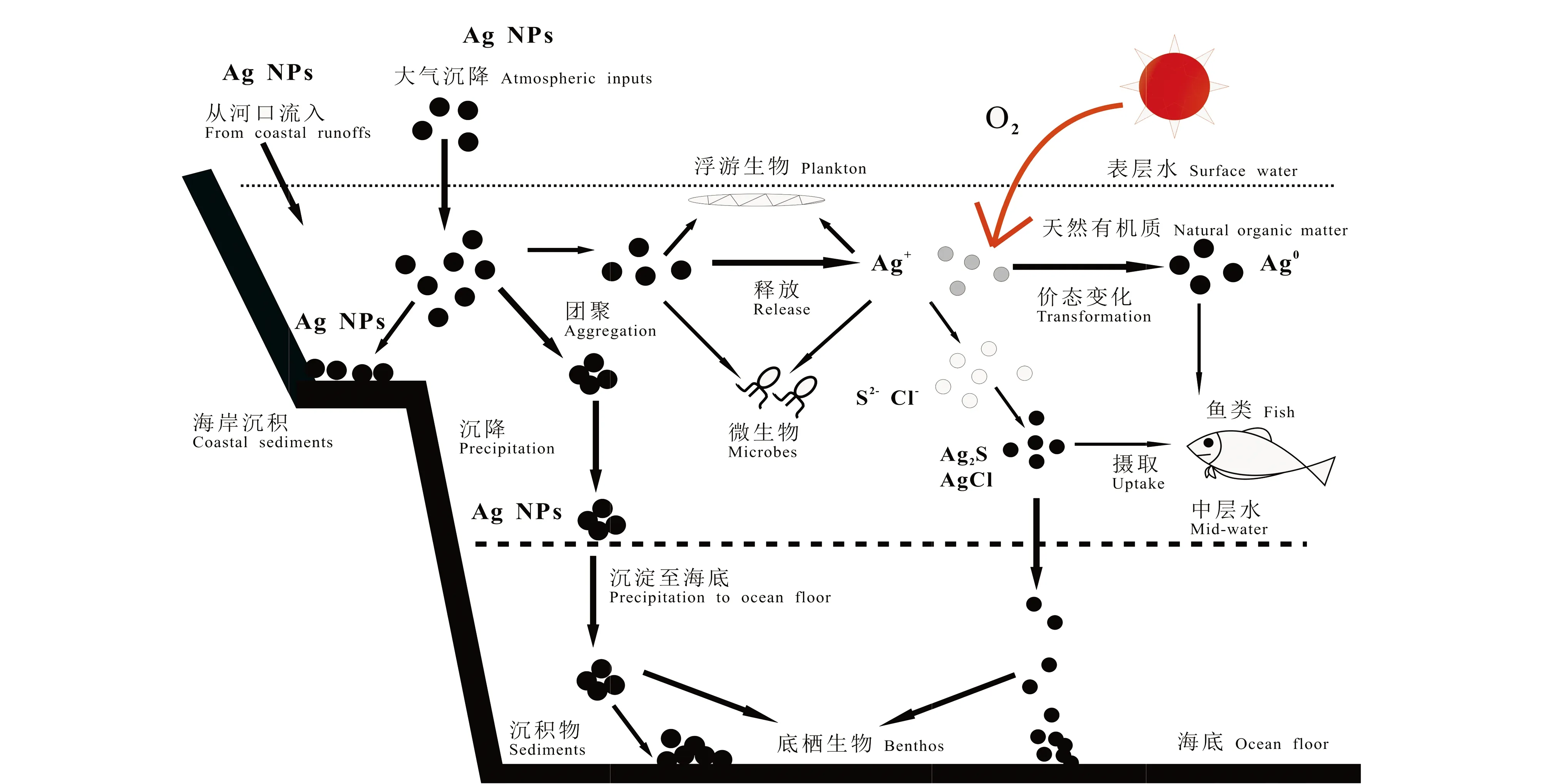
图1 纳米银颗粒(AgNPs)在水环境中的环境行为和归趋[2,17-18]Fig. 1 Environmental behavior and fate of silver nanoparticles (AgNPs) in the aquatic environment[2,17-18]
1.1 AgNPs在水环境中的赋存
Ag是地壳中极其稀缺的元素,环境背景浓度极低。因此由于人类活动所导致的水中Ag浓度的变化,即便是细微的变化,也能导致偏离自然条件的巨大波动,Benn等[19]的研究表明在清洗纳米银袜子的水中可检测到Ag的浓度高达1.3 μg·mL-1。
水环境中AgNPs的潜在风险很大程度上由其浓度决定,并且AgNPs在生产、加工、运输、消费和处置的整个生命周期中可能以不同的形式进入环境中。人工合成的AgNPs已经广泛存在于水环境中。英国生态与水文中心(Centre for Ecology and Hydrology)的报告表明英国污水处理厂排放的污水中胶体态Ag(包括AgNPs)的平均浓度是6 ng·L-1,总颗粒态Ag的浓度为78 ng·L-1[20]。Flegal和Sanudo-Wilhelmy[21]通过分析圣地亚哥湾和南旧金山湾的金属浓度发现Ag+浓度范围是7~33 ng·L-1。即使在开放的海洋中,也有研究证明Ag的存在,Ranville和Flegal[22]认为海洋中Ag处于生物地球化学循环状态,由于亚洲地区工业排放,导致北太平洋表层水中检测到Ag的最高浓度可达到1.296 ng·L-1,比背景浓度(0.027 ng·L-1)高出近50倍。Ag在污水中的浓度比在自然水体中要高得多,Wen等[23]在美国科罗拉多州5个城市收集水样,其研究结果显示其中3个城市的污水中,Ag+浓度范围是64.1~327 ng·L-1,远超过在上游地区Ag+的浓度;而科罗拉多州的一家影像公司排出的废水中,Ag的浓度竟高达33 400 ng·L-1。Hoque等[24]对加拿大彼得伯勒一家污水处理厂排放的污水进行分析,结果显示AgNPs的粒径是9.3 nm,浓度是1 900 ng·L-1。Matzke等[25]的研究表明,AgNPs对恶臭假单胞菌的EC05为0.13~3.41 μg·L-1,而AgNO3对其的EC05为0.043 μg·L-1。Völker等[26]研究发现,在21 d的长期暴露中,AgNPs对大型溞(Daphnia magna)的EC10为0.92 μg·L-1。从上述世界各地检测到的Ag浓度范围可知,Ag在水环境中不断积累,而其较强的急性或慢性毒性效应将给环境与健康带来一定的风险。
目前分析环境中AgNPs含量的相关研究在国内外都鲜有报道,Maynard等[27]科学家曾表示,追求合理化安全的纳米科技面临着5大挑战,而现阶段挑战的内容就包括运用模型预测环境中和人体内人工合成纳米材料的行为。所以目前大部分文献中出现的AgNPs浓度基本都是模型预测的结果。即便如此,在复杂的环境条件或是生物作用下,由于缺少检测、定量以及表征AgNPs的方法,AgNPs暴露模型的研究存在瓶颈。所以,今后的发展方向很可能是综合多种方法,侧重环境中AgNPs的痕量分析[28-29]。
Gottschalk等[30]通过模型计算了欧洲、美国和瑞士等国家和地区的AgNPs环境预测浓度(predicted environmental concentrations)(表1)。但Boxall等[31]指出即使用最保守的模型预计,天然水环境中AgNPs的浓度同样是痕量级,浓度远低于产生毒性效应的浓度范围。但由于模型本身存在局限,同时缺乏详细实测数据的比对,因此AgNPs的潜在风险不可忽视。
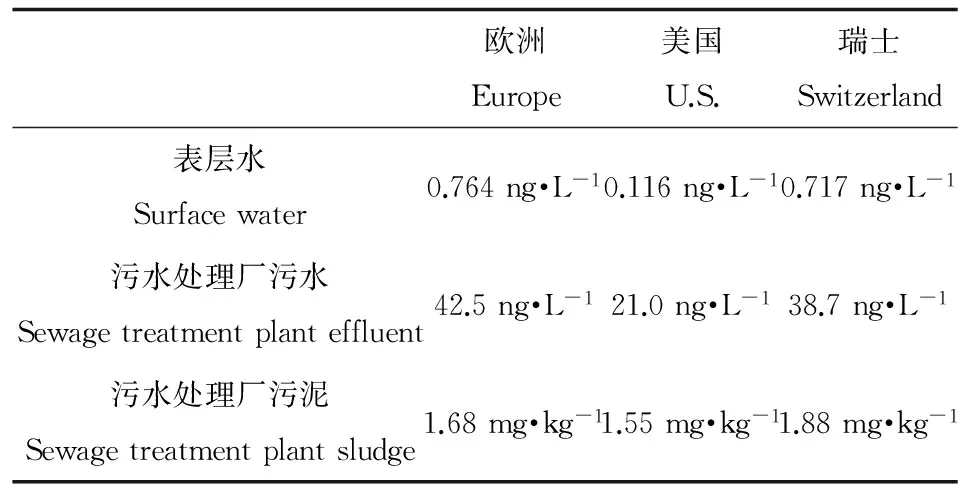
表1 AgNPs环境浓度预测值[30]
1.2 AgNPs在水环境中的环境行为
在海洋或河口环境中,Ag化学性质和生物可利用性决定Ag的毒性。海水中的Cl-结合Ag+能力很强,同时形成的氯化银类化合物有很强的生物可利用性,能被鱼类摄入体内。所以相比于河流湖泊这类淡水域,海洋中的生物对Ag利用性更高,对Ag的环境承载能力更弱[29, 32]。
近年来分析水环境中AgNPs行为的相关研究成为热点和难点[33],其中很大的难题在于区分Ag的形态(Ag+和AgNPs),因为环境中Ag+能与阴离子如S2-、Cl-形成Ag2S、AgCl,此外环境中存在的天然有机配体如腐殖酸(HA)等也能与Ag+络合,所以上述过程将给AgNPs的分析带来干扰。另外,在富含溶解有机质(DOM)的水体中,溶解氧(DO)在光照条件下能产生超氧阴离子(O2·-),进一步将Ag+转化成AgNPs[18],这表明环境中AgNPs不仅来源于人为活动,也可能来自环境中Ag+的转化。因此,对不同形态的Ag进行区分,是分析AgNPs浓度不可轻视的问题之一。目前分析和表征AgNPs的方法主要包括扫描电镜、透射电镜、动态光散射、紫外可见吸收光谱、电感耦合等离子质谱(或发射光谱)等方法[24,28,34-35]。
由于AgNPs有不同的形状,不同的电荷,这使得它与其他物质的结合方式也有所不同,因此每一个因素都有可能改变AgNPs的环境行为和毒性[12]。比如,AgNPs释放Ag+的过程受AgNPs粒径的影响,粒径小(<10 nm)的AgNPs释放Ag+速率较快,粒径较大的AgNPs(>50 nm)释放Ag+速率慢,但持续时间长,所以更像是一个稳定的Ag+排放源。同时,AgNPs表面包裹物不同,对整个释放过程也有影响[11],进一步影响AgNPs颗粒的毒性[36]。Kittler等[37]的研究也表明AgNPs释放Ag+的速率和程度取决于温度、AgNPs浓度及其表面基团功能;并且AgNPs放置时间越长,释放Ag+含量越高,产生的毒性越强。
AgNPs具有极大的比表面积,有很强的吸附能力。同时水体中大多数颗粒物带负电荷,能吸附水中带正电荷的金属阳离子,因此AgNPs可能与水体中的颗粒物发生相互作用。Kaegi等[38]认为从污水处理厂中排放的AgNPs能有效地在廊道中传输,并最终沉降至底泥。因为AgNPs更能吸附在水体中悬浮物(TSS)上面而不是在污水生物膜上面。所以在河口区这种含沙量较大的环境中,水中的泥沙和悬浮颗粒可能会影响AgNPs的环境行为和归趋。
虽然近年来国内外学者对水环境中AgNPs的环境行为开展了探索性研究,但天然水体理化条件复杂多变,AgNPs的形态和行为更具有差异性,这使得要想进一步研究AgNPs的环境行为,就需要新的分析技术和方法。Glover等[39]提出一个新方法分析固体表面AgNPs的转变,通过实验发现银制品暴露在湿润的空气或水中能产生AgNPs,整个过程包括3部分:(1) Ag0离子化以及Ag+溶解;(2) Ag+扩散至吸附水层;(3) Ag+在周围环境条件下被还原。这不但使AgNPs的表面动力学重新被认识,并且暗示人类在长时间接触纳米材料后可能成为环境中纳米材料的潜在来源。Zhou等[40]发现AgNPs直接碰撞电极后产生的电氧化结果可以量化,可用于表征并定量AgNPs,该研究正在继续深入并计划用于公共卫生和环境监测中。
AgNPs在生态系统中的生物和非生物作用下会产生复杂的环境行为,有学者发现人工合成的纳米材料与在自然环境中形成的纳米颗粒相差无几,意味着在复杂的自然环境中纳米物质普遍存在。水环境中AgNPs的行为例如氧化还原反应、团聚、溶解及其与生物大分子的作用等,可能改变AgNPs的毒性效应,所以相关研究对解释AgNPs毒理机制有科学指导意义[41-43]。
2 AgNPs对水环境中微生物和生物膜的毒性效应
早在20世纪,Ag及其化合物对水环境中微生物(如藻类、细菌等)的生物积累效应和毒性效应已有研究,同时由于环境条件(尤其是海洋环境)的不同,Ag的毒性效应也随之发生变化[44]。同样在含有纳米颗粒的环境介质中,微生物也很可能扮演着调节纳米颗粒迁移转化和毒性效应的角色[17]。因此,对纳米材料的微生物毒性的深入研究,既能推动纳米技术的发展,又能帮助设计安全合理的纳米材料,在提升材料功能的同时降低环境风险。
2.1 水环境中的微生物和生物膜的作用
生物膜中包含多种微生物如细菌、原生动物、真菌以及藻类等,微生物之间处于竞争与合作的平衡状态[45]。生物膜中丰度最高的是细菌,因此细菌是生物膜的一个重要组成组分。与悬浮状态的浮游细菌相比,附着在生物膜中的浮游细菌由于生物膜的保护作用,更能抵抗吞噬细胞、抗生素和抗体的攻击[46]。生物膜中有一个重要组成部分是胞外聚合物(EPS),EPS中含有蛋白质、多糖、脂质和核酸等,为微生物细胞提供天然屏障[47]。复杂的生命结构使得生物膜能够吸附甚至降解无机污染物和有机污染物[48-49]。
AgNPs进入细胞内的过程可能是由AgNPs的粒径和细胞膜的通透性和孔隙度决定的。有研究表明,粒径小于80 nm的AgNPs能进入绿脓杆菌细胞中,并且随着细胞膜的通透性和孔隙度的增加,AgNPs在细胞中的积累也随之增加[50]。但Kloepfer等[51]尝试用腺嘌呤和单磷酸腺苷(AMP)标记枯草杆菌和大肠杆菌,发现只有在量子点(QDs)小于5 nm的情况下,细菌才能被标记。
2.2 AgNPs对微生物和生物膜的毒性效应
若评价AgNPs对微生物和生物膜的毒性效应,要考虑的因素之一便是AgNPs在其中的扩散情况。Peulen和Wilkinson[52]选取包括AgNPs在内的3种纳米颗粒,研究AgNPs在荧光假单胞菌生物膜中的扩散规律,结果发现,纳米颗粒在环境中的迁移很大程度上受生物膜的影响,AgNPs容易富集在更密集的生物膜上。Martinez-Gutierrez等[53]则证明AgNPs能抑制绿脓杆菌生物膜的形成,并且能杀死生物膜内的细菌。Fabrega等[54]以天然海洋生物膜为研究对象,发现当AgNPs的暴露浓度达到200 μg·L-1,生物膜的体积和生物量明显减少,进一步通过分子水平分析证明AgNPs能抑制生物膜的形成与进化。
早在2004年就有实验证明AgNPs有很强的抗菌能力,Sondi等[55]发现当AgNPs的暴露浓度达到10 mg·L-1时,70%的大肠杆菌生长受到抑制;暴露在AgNPs中的大肠杆菌细胞壁遭到破坏,形成了凹陷(pits),这些纳米颗粒富集在细胞壁上,增强细胞壁的渗透性,使其不能有效调节质膜运输,从而导致细胞死亡。
AgNPs在水环境中可以游离出Ag+,Ag+有很强的毒性,因此有关AgNPs抑菌性的文章,得到的结论是Ag+起到决定性的作用[56]。Xiu等[57]通过对比AgNPs商品和Ag+对大肠杆菌的毒性,发现Ag+的毒性明显高于AgNPs。但是,也有研究将AgNO3与AgNPs对藻类的毒性作用进行对比,发现AgNPs对藻类的毒性比AgNO3强,即使在比环境中Ag+浓度低的条件下,AgNPs也有同等效果的抑制效率[58]。但是Burchardt等[59]的研究表明当AgNPs的暴露浓度达到10 μmol·L-1时,聚球藻(Synechococcus sp.)在72 h后生长完全受到抑制,而达到同样抑制效果所对应的AgNO3暴露浓度为2 μmol·L-1。Kim等[60]的研究表明AgNPs能抑制大肠杆菌和枯草芽孢杆菌菌落的生长,当AgNPs的暴露浓度为10 mg·L-1时,大肠杆菌和枯草芽孢杆菌的菌落形成比例与对照组相比分别为0.5%和77.5%,同时实验明确证实AgNPs存在于细菌细胞内并破坏细菌细胞膜,这是其产生毒性效应的主要原因。有研究者认为,AgNPs是间接产生毒性效应,因为检测到的Ag+浓度不足以解释毒性效应,所以这可能是一个连续的缓慢的释放过程。但是如果没有AgNPs的存在,产生的毒性不会那么明显[61]。
近期不断有研究探讨AgNPs抗菌特性的可能机制,Radzig等[62]认为AgNPs会吸附在细菌细胞膜表面,破坏细胞渗透性,抑制细胞呼吸,孔蛋白(porin)可能在这个过程中起到关键性作用。该实验选取生物膜中革兰氏阴性菌(大肠杆菌AB1157、铜绿假单胞菌PAO1、沙雷菌94)作为研究对象,结果表明:(1)纳米银(Ag0/Ag+)抑制细菌生长和生物膜的形成。(2)上述抑制结果的原因不单单是Ag+的作用,过程中出现的DNA氧化损伤也可能有所贡献。(3)Ag+的产生可能是生物膜释放的H2O2(产生·OH)与AgNPs相互作用的结果。(4)孔蛋白参与Ag+的传输,与对照组相比,突变组中细菌对AgNPs的抵抗力更强,分子水平的分析表明参与合成孔蛋白的基因表达上调。孔蛋白形成的气孔直径(约1 nm)比实验中所用AgNPs直径(约8.6 nm)小,这表明AgNPs的抗菌机制是Ag+透过细胞壁进入细胞引起的。Xiu等[63]也通过实验证明Ag+是明确的分子毒物,实验通过设置严格的厌氧条件限制Ag0的氧化以及Ag+的释放,结果显示AgNPs在厌氧状态下对大肠杆菌的毒性明显低于需氧状态,并且AgNPs的毒性效应与Ag+浓度呈一定的剂量效应关系。但是,目前有关AgNPs的抗菌机制还没有确凿的结论,需要进一步实验证明。
2.3 影响AgNPs对微生物和生物膜毒性效应的因素
AgNPs对微生物的毒性效应可能因为环境条件的变化而受到影响,绝大多数水环境中都存在天然有机质(NOM),能和AgNPs发生相互作用。Wirth等[64]发现腐殖酸(HA)能缓解Ag对荧光假单胞菌生物膜的毒性,原因是HA能结合Ag+,降低Ag+的毒性,但是HA对稳定的胶体态Ag的毒性短期内没有显著影响,反而增加了其对生物膜的接触,导致慢性毒性的变化。Fabrega等[65]依据萨旺尼河的富里酸(SRFA)设定对照实验,结果表明在含有SRFA的实验组中,恶臭假单胞菌细胞脱落的速率降低,并且SRFA提升了生物膜摄取以及富集AgNPs的可能性。在后续的实验中,Fabrega等[66]进一步通过实验证明天然有机大分子 (humic substances, HS)能够短期缓解AgNPs对荧光假单胞菌的毒性。Levard等[67-68]通过实验证明,AgNPs的硫化作用能降低自身毒性。与对照组相比,在AgNPs发生硫化作用的实验组中,4种受试生物的EC50和LC50都有明显的下降。除上述条件以外,García-Alonso等[69]的研究表明处于生命周期早期的海洋生物沙蚕(Platynereis dumerilii)相对于成熟期,在AgNPs暴露下出现更多的死亡或发育异常现象。
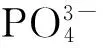
在与微生物的相互作用中,AgNPs自身的特征如形状、尺寸和表面包裹物等,同样对整个过程起着重要作用。Jose Ruben等[34]发现只有粒径为1~10 nm的AgNPs才能直接与微生物相互作用,这样的颗粒能吸附在细菌细胞膜上并破坏其功能。Park等[71]的研究表明Ag表面包裹物不同,对细菌的毒性也不同,用蛋白质包裹的Ag(Biogenic-Ag)毒性明显高于化学合成的胶态Ag(Colloidal-Ag)。Zhou等[72]通过比较AgNPs和AuNPs对大肠杆菌和卡介苗(Bacillus Calmette-Guérin, BCG)的抑制作用发现,2种纳米颗粒均表现出有效的抗菌能力。相同形状和粒径的AuNPs,用PAH包裹能导致细胞溶解,而用柠檬酸盐包裹的纳米颗粒则没有该现象。此外,光照强度、水体温度和pH值等环境条件有可能影响AgNPs的微生物毒性效应。综上所述,影响AgNPs对微生物和生物膜毒性效应的因素可能主要有2方面,一是AgNPs所处的环境条件因素,包括自然环境条件如光照、温度、溶解氧、pH值、盐度、阴离子和天然有机质等;也包括实验条件如不同种类的培养基、营养盐溶液和受试生物选择等。二是AgNPs自身的特征因素,包括AgNPs的形状、粒径、表面包裹物或是修饰物等。
3 问题与展望
随着纳米科技的不断发展以及含AgNPs商品的广泛使用,其对生态系统的危害以及对人类健康的潜在风险逐渐得到关注。目前国内外有关AgNPs在水环境中的环境行为及其对微生物的毒性效应研究已经取得了较大进展。但是仍然存在着一些问题没有被解决或证实,具体表现在以下几个方面:
(1) AgNPs对微生物的毒性机制。目前针对AgNPs抗菌机制的研究没有明确结论,有观点证明Ag+在其毒性效应中起主要作用,但另有观点证明AgNPs的毒性机制是进入微生物体内NPs导致的。因此,今后相关研究需要探索新的实验方法和技术,结合不同学科(如化学的成分分析和生物的基因表达分析等)研究AgNPs抗菌机制。
(2) AgNPs慢性毒性实验研究。Ag具有持久性和生物富集性,并且纳米颗粒的自身特性使得AgNPs能长期积累在生物体内,因此AgNPs慢性或长期毒性效应不容忽视。然而目前研究多针对AgNPs的急性毒性,缺乏慢性毒性实验数据的对比,如果低浓度(ng·L-1)AgNPs长期暴露对受试生物产生毒性效应或抑制作用,同样对环境风险评价有重要借鉴意义,因此亟待开展相关研究。
(3)评价天然水体中AgNPs的环境行为和毒性效应。目前多数AgNPs的毒理研究所得结论是建立在特定实验条件基础上的,但AgNPs在相对复杂的自然环境下的环境行为和毒性效应很可能发生变化,因此有必要开展相关研究。
此外,有关AgNPs进入环境后,在生态系统中的迁移转化规律和潜在危害的研究比较有限,特别作为地球上最富有生机、具有独特生态价值和资源潜力的河口滨岸生态系统,相关研究更是稀缺。因此这方面的研究也有待开展。
[1] Feynman R P. There's plenty of room at the bottom [J]. Engineering and Science, 1960, 23(5): 22-36
[2] Klaine S J, Alvarez P J J, Batley G E, et al. Nanomaterials in the environment: Behavior, fate, bioavailability, and effects [J]. Environmental Toxicology and Chemistry, 2008, 27(9): 1825-1851
[3] Woodrow Wilson International Center for Scholars. The project on emerging nanotechnologies [DB]. [2014-03-14]. http://www.nanotechproject.org
[4] Bryaskova R,Pencheva D,Nikolov S, et al. Synthesis and comparative study on the antimicrobial activity of hybrid materials based on silver nanoparticles (AgNps) stabilized by polyvinylpyrrolidone (PVP) [J]. Journal of Biological Chemistry, 2011, 4(4): 185-191
[5] Silver S. Bacterial silver resistance: Molecular biology and uses and misuses of silver compounds [J]. FEMS Microbiology Reviews, 2003, 27(2-3): 341-353
[6] Hamouda I M. Current perspectives of nanoparticles in medical and dental biomaterials [J]. Journal of Biomedical Research, 2012, 26(3): 143-151
[7] Choi O, Deng K K, Kim N J, et al. The inhibitory effects of silver nanoparticles, silver ions, and silver chloride colloids on microbial growth [J]. Water Research, 2008, 42(12): 3066-3074
[8] Miao A J, Schwehr K A, Xu C, et al. The algal toxicity of silver engineered nanoparticles and detoxification by exopolymeric substances [J]. Environmental Pollution,2009, 157(11): 3034-3041
[9] Griffitt R J, Luo J, Gao J, et al. Effects of particle composition and species on toxicity of metallic nanomaterials in aquatic organisms [J]. Environmental Toxicology and Chemistry, 2008, 27(9): 1972-1978
[10] Geranio L, Heuberger M, Nowack B. The behavior of silver nanotextiles during washing [J]. Environmental Science & Technology, 2009, 43(21): 8113-8118
[11] Dobias J, Bernier-Latmani R. Silver release from silver nanoparticles in natural waters [J]. Environmental Science & Technology, 2013, 47(9): 4140-4146
[12] Luoma S N. Silver nanotechnologies and the environment: Old problem or new challenges [R]. Washington D C, USA:Woodrow Wilson International Center for Scholars, 2008: 72
[13] Hook S E, Fisher N S. Sublethal effects of silver in zooplankton: Importance of exposure pathways and implications for toxicity testing [J]. Environmental Toxicology and Chemistry, 2001, 20(3): 568-574
[14] Hogstrand C,Wood C M. Toward a better understanding of the bioavailability, physiology, and toxicity of silver in fish: Implications for water quality criteria [J]. Environmental Toxicology and Chemistry, 1998, 17(4): 547-561
[15] 王文军, 王文华, 张学林, 等. 水环境中生物膜对污染物环境化学行为的影响[J]. 环境科学进展, 1999, 7(6): 58-65
Wang W J, Wang W H, Zhang X L, et al. Effect of biofilms in the aquatic environment on the environmental chemical behavior of pollutants [J]. Advancesin Environental Science, 1999, 7(6): 58-65 (in Chinese)
[16] 张金莲, 吴振斌. 水环境中生物膜的研究进展[J]. 环境科学与技术, 2007, 30(11): 102-106, 121
Zhang J L, Wu Z B. Progress on biofilm studies [J]. Environmental Science and Technology, 2007, 30(11):102-106, 121
[17] Wiesner M R, Lowry G V, Alvarez P, et al. Assessing the risks of manufactured nanomaterials [J]. Environmental science & technology, 2006, 40(14): 4336-4345
[18] Yin Y, Liu J, Jiang G. Sunlight-induced reduction of ionic Ag and Au to metallic nanoparticles by dissolved organic matter [J]. ACS Nano, 2012, 6(9): 7910-7919
[19] Benn T M,Westerhoff P. Nanoparticle silver released into water from commercially available sock fabrics [J]. Environmental Science & Technology, 2008, 42(11): 4133-4139
[20] Centre for Ecology and Hydrology. Exposure assessment for engineered silver nanoparticles throughout the rivers of England and Wales (CB0433)[R/OL]. (2011-11-06) [2014-03-14]. http://randd.defra.gov.uk
[21] Flegal A R, Sanudo-Wilhelmy S A.Comparable levels of trace metal contamination in two semienclosed embayments: San Diego Bay and south San Francisco Bay [J]. Environmental Science & Technology, 1993, 27(9): 1934-1936
[22] Ranville M A, Flegal A R. Silver in the North Pacific Ocean [J]. Geochemistry, Geophysics, Geosystems, 2005, 6(3): Q03M01
[23] Wen L S, Santschi P H, Gill G A, et al. Silver concentrations in Colorado, USA, watersheds using improved methodology [J]. Environmental Toxicology and Chemistry, 2002, 21(10): 2040-2051
[24] Hoque M E, Khosravi K, Newman K, et al. Detection and characterization of silver nanoparticles in aqueous matrices using asymmetric-flow field flow fractionation with inductively coupled plasma mass spectrometry [J]. Journal of Chromatography A, 2012, 1233: 109-115
[25] Matzke M, Jurkschat K, Backhaus T. Toxicity of differently sized and coated silver nanoparticles to the bacterium Pseudomonas putida: Risks for the aquatic environment? [J]. Ecotoxicology, 2014: 1-12
[26] Völker C, Boedicker C, Daubenthaler J, et al. Comparative toxicity assessment of nanosilver on three Daphnia species in acute, chronic and multi-generation experiments [J]. PloS one, 2013, 8(10): e75026
[27] Maynard A D, Aitken R J, Butz T, et al. Safe handling of nanotechnology [J]. Nature, 2006, 444(7117): 267-269
[28] Hassellöv M, Readman J, Ranville J, et al. Nanoparticle analysis and characterization methodologies in environmental risk assessment of engineered nanoparticles [J]. Ecotoxicology, 2008, 17(5): 344-361
[29] Fabrega J, Luoma S N, Tyler C R, et al. Silver nanoparticles: Behaviour and effects in the aquatic environment [J]. Environment International, 2011, 37(2): 517-531
[30] Gottschalk F,Sonderer T,Scholz R W, et al. Modeled environmental concentrations of engineered nanomaterials (TiO2, ZnO, Ag, CNT, Fullerenes) for different regions [J]. Environmental Science & Technology, 2009, 43(24): 9216-9222
[31] Boxall A, Chaudhry Q, Sinclair C, et al. Current and future predicted environmental exposure to engineered nanoparticles [R]. Central York, UK: Science Laboratory, 2007
[32] Luoma S N, Ho Y B, Bryan G W. Fate, bioavailability and toxicity of silver in estuarine environments [J]. Marine Pollution Bulletin, 1995, 31(1-3): 44-54
[33] Cherrie M W, Matteo Dalla V, Kevin C J, et al. Challenges in assessing the environmental fate and exposure of nano silver [J]. Journal of Physics: Conference Series, 2011, 304(1): 012070
[34] Jose Ruben M, Jose Luis E, Alejandra C, et al. The bactericidal effect of silver nanoparticles [J]. Nanotechnology, 2005, 16(10): 2346
[35] Liu J F, Chao J B, Liu R, et al. Cloud point extraction as an advantageous preconcentration approach for analysis of trace silver nanoparticles in environmental waters [J]. Analytical Chemistry, 2009, 81(15): 6496-6502
[36] Yang X, Gondikas A P, Marinakos S M, et al. mechanism of silver nanoparticle toxicity is dependent on dissolved silver and surface coating in Caenorhabditis elegans [J]. Environmental Science & Technology, 2011, 46(2): 1119-1127
[37] Kittler S, Greulich C, Diendorf J, et al. Toxicity of silver nanoparticles increases during storage because of slow dissolution under release of silver ions [J]. Chemistry of Materials, 2010, 22(16): 4548-4554
[38] Kaegi R,Voegelin A,Ort C, et al. Fate and transformation of silver nanoparticles in urban wastewater systems [J]. Water Research, 2013, 47(12): 3866-3877
[39] Glover R D,Miller J M,Hutchison J E. generation of metal nanoparticles from silver and copper objects: Nanoparticle dynamics on surfaces and potential sources of nanoparticles in the environment [J]. ACS Nano, 2011, 5(11): 8950-8957
[40] Zhou Y G, Rees N V, Compton R G. The electrochemical detection and characterization of silver nanoparticles in aqueous solution [J]. Angewandte Chemie International Edition, 2011, 50(18): 4219-4221
[41] Bone A J, Colman B P,Gondikas A P, et al. Biotic and abiotic interactions in aquatic microcosms determine fate and toxicity of Ag nanoparticles: Part 2 toxicity and Ag speciation [J]. Environmental Science & Technology, 2012, 46(13): 6925-6933
[42] Unrine J M, Colman B P, Bone A J, et al. Biotic and abiotic interactions in aquatic microcosms determine fate and toxicity of Ag nanoparticles. Part 1. aggregation and dissolution [J]. Environmental Science & Technology, 2012, 46(13): 6915--6924
[43] Lowry G V,Gregory K B, Apte S C, et al. Transformations of nanomaterials in the Environment [J]. Environmental Science & Technology, 2012, 46(13): 6893-6899
[44] Ratte H T. Bioaccumulation and toxicity of silver compounds: A review [J]. Environmental Toxicology and Chemistry, 1999, 18(1): 89-108
[45] Nadell C D,Xavier J B,Foster K R. The sociobiology of biofilms [J]. FEMS Microbiology Reviews,2009, 33(1): 206-222
[46] Costerton J W, Stewart P S, Greenberg E P. Bacterial biofilms: A common cause of persistent infections [J]. Science, 1999, 284(5418): 1318-1322
[47] Sutherland I W.Biofilm exopolysaccharides: A strong and sticky framework [J]. Microbiology, 2001, 147(1): 3-9
[48] 董德明, 纪亮, 花修艺, 等. 自然水体生物膜吸附Co, Ni和Cu的特征研究[J]. 高等学校化学学报, 2004, 25(2): 247-251
Dong D M, Ji L, Hua X Y, et al. Stuies on the characteristics of Co, Ni and Cu adsorption to natural surface coatings [J]. Chemical Journal of Chinese Universities, 2004, 25(2): 247-251
[49] Bohuss I, Rékasi T, Szikora S, et al. Interaction of acetochlor and atrazine with natural freshwater biofilms grown on polycarbonate substrate in lake Velence (Hungary) [J]. Microchemical Journal, 2005, 79(1-2): 201-205
[50] Xu X-H N, Brownlow W J, Kyriacou S V, et al. Real-time probing of membrane transport in living microbial cells using single nanoparticle optics and living cell imaging [J]. Biochemistry, 2004, 43(32): 10400-10413
[51] Kloepfer J A, Mielke R E, Nadeau J L. Uptake of CdSe and CdSe/ZnS quantum dots into bacteria via purine-dependent mechanisms [J]. Applied and Environmental Microbiology, 2005, 71(5): 2548-2557
[52] Peulen T-O, Wilkinson K J. Diffusion of nanoparticles in a biofilm [J]. Environmental Science & Technology,2011, 45(8): 3367-3373
[53] Martinez-Gutierrez F, Boegli L, Agostinho A, et al. Anti-biofilm activity of silver nanoparticles against different microorganisms [J]. Biofouling, 2013, 29(6): 651-660
[54] Fabrega J, Zhang R, Renshaw J C, et al. Impact of silver nanoparticles on natural marine biofilm bacteria [J]. Chemosphere, 2011, 85(6): 961-966
[55] Sondi I, Salopek-Sondi B. Silver nanoparticles as antimicrobial agent: A case study on E. colias a model for Gram-negative bacteria [J]. Journal of Colloid and Interface Science, 2004, 275(1): 177-182
[56] Lok C-N,Ho C-M,Chen R, et al. Silver nanoparticles: Partial oxidation and antibacterial activities [J].Journal of Biological Inorganic Chemistry, 2007, 12(4): 527-534
[57] Xiu Z M, Ma J, Alvarez P J J. Differential effect of common ligands and molecular oxygen on antimicrobial activity of silver nanoparticles versus silver ions [J]. Environmental Science & Technology, 2011, 45(20): 9003-9008
[58] Navarro E, Piccapietra F,Wagner B, et al. Toxicity of silver nanoparticles to Chlamydomonas reinhardtii [J]. Environmental Science & Technology, 2008, 42(23): 8959-8964
[59] Burchardt A D, Carvalho R N,Valente A, et al. Effects of silver nanoparticles in diatom Thalassiosira pseudonanaand cyanobacterium Synechococcus sp. [J]. Environmental Science & Technology, 2012, 46(20): 11336-11344
[60] Kim S, Baek Y-W, An Y-J. Assay-dependent effect of silver nanoparticles to Escherichia coli and Bacillus subtilis [J]. Applied Microbiology and Biotechnology, 2011, 92(5): 1045-1052
[61] Lubick N. Nanosilver toxicity: Ions, nanoparticles or both? [J]. Environmental Science & Technology, 2008, 42(23): 8617--8617
[62] Radzig M A, Nadtochenko V A, Koksharova O A, et al. Antibacterial effects of silver nanoparticles on Gram-negative bacteria: Influence on the growth and biofilms formation, mechanisms of action [J]. Colloids and Surfaces B: Biointerfaces, 2013, 102: 300-306
[63] Xiu Z M, Zhang Q B, Puppala H L, et al. Negligible particle-specific antibacterial activity of silver nanoparticles [J]. Nano Letters, 2012, 12(8): 4271-4275
[64] Wirth S M, Lowry G V, Tilton R D. Natural organic matter alters biofilm tolerance to silver nanoparticles and dissolved silver [J]. Environmental Science & Technology, 2012, 46(22): 12687-12696
[65] Fabrega J, Renshaw J C, Lead J R. Interactions of silver nanoparticles with Pseudomonas putida biofilms [J]. Environmental Science & Technology, 2009, 43(23): 9004-9009
[66] Fabrega J, Fawcett S R, Renshaw J C, et al. Silver nanoparticle impact on bacterial growth: Effect of pH, concentration, and organic matter [J]. Environmental Science & Technology, 2009, 43(19): 7285-7290
[67] Levard C, Hotze E M, Lowry G V, et al. Environmental transformations of silver nanoparticles: Impact on stability and toxicity [J]. Environmental Science & Technology, 2012, 46(13): 6900-6914
[68] Levard C, Hotze E M, Colman B P, et al. Sulfidation of silver nanoparticles: Natural antidote to their toxicity [J]. Environmental Science & Technology, 2013, 47(23): 13440-13448
[69] García-Alonso J, Rodriguez-Sanchez N, Misra S K, et al. Toxicity and accumulation of silver nanoparticles during development of the marine polychaete Platynereis dumerilii [J]. Science of the Total Environment, 2014, 476 477: 688-695
[70] Li M, Zhu L, Lin D. Toxicity of ZnO nanoparticles to Escherichia coli: Mechanism and the influence of medium components [J]. Environmental Science & Technology, 2011, 45(5): 1977-1983
[71] Park H-J, Park S, Roh J, et al. Biofilm-inactivating activity of silver nanoparticles: A comparison with silver ions [J]. Journal of Industrial and Engineering Chemistry,2013, 19(2): 614-619
[72] Zhou Y, Kong Y, Kundu S, et al. Antibacterial activities of gold and silver nanoparticles against Escherichia coliand bacillus Calmette-Guérin [J]. Journal of Nanobiotechnology, 2012, 10(1): 1-9
◆
Review of Environmental Behavior and Toxicity of Silver Nanoparticles in the Aquatic Environment
Yi Jun1,Huang Jun1,Cheng Jinping1,2,*
1. State Key Laboratory of Estuarine and Coastal Research, East China Normal University, Shanghai 200062, China 2. City University of Hong Kong Shenzhen Research Institute, Shenzhen 518057, China
14 March 2014 accepted 7 May 2014
The environmental behaviour and ecological impact of nano-materialshave attracted increasing attention in recent years. Silver nanoparticles (AgNPs) are the most frequently used nano-materials. This review summarizes research progress on the behavior and toxicity of AgNPs in the aquatic environment. Occurrence, environmental behavior, toxicity to various microorganisms, and the factors influencing toxicity of AgNPs are summarized. Finally, perspectives for future research regarding AgNPs in estuarine environment are discussed.
silver nanoparticles; microorganisms; environmental behavior; toxicity
国家自然科学基金(41101489);广东省自然科学基金(s2012010010847);教育部新世纪优秀人才计划项目(NECT-12-0181);华东师范大学高层次人才经费(No.79631916);河口海岸学国家重点实验室自主课题(2012RCDW-01)
衣俊(1990-),男,硕士,研究方向为生态毒理学,E-mail: 51132601029@ecnu.cn
*通讯作者(Corresponding author),E-mail: jpcheng@sklec.ecnu.edu.cn
10.7524/AJE.1673-5897.20140314003
2014-03-14 录用日期:2014-05-07
1673-5897(2015)1-101-09
X171.5
A
程金平(1978—),女,博士,研究员,主要研究方向为生态毒理学。
衣俊, 黄俊, 程金平. 纳米银在水环境中的环境行为和毒性效应研究进展[J]. 生态毒理学报, 2015, 10(1): 101-109
Yi J, Huang J, Cheng J P. Review of environmental behavior and toxicity of silver nanoparticles in the aquatic environment [J]. Asian Journal of Ecotoxicology, 2015, 10(1): 101-109 (in Chinese)

