Eu3+掺杂纳米TiO2的制备及光催化性能的研究
黄正喜,龙剑英,吴腊梅,刘献平
(中南民族大学 化学与材料科学学院, 武汉 430074)
Eu3+掺杂纳米TiO2的制备及光催化性能的研究
黄正喜,龙剑英,吴腊梅,刘献平
(中南民族大学 化学与材料科学学院, 武汉 430074)
通过溶液法制备了不同铕(Eu3+)掺杂量TiO2纳米颗粒(Eu3+/TiO2),利用XRD、TEM、XPS对其进行了表征.在可见光照射下,以光催化降解常用的工业染料为目标反应,探讨了Eu3+掺杂量、催化剂用量、溶液pH值和催化剂重复利用对催化活性的影响,以优化光催化条件.结果表明:煅烧温度为500 ℃,Eu3+/TiO2光催化剂晶型为锐钛矿型,其晶粒尺寸为14 nm;Eu3+离子的最佳掺杂摩尔比r(Eu3+︰TiO2)=3%,样品加入量为1.25 mg/mL,pH=10.75时样品光催件性能最佳;其3次循环降解甲基紫,60 min内降解率仍保持在约96%,说明Eu3+/ TiO2光催化剂具有良好的稳定性.
纳米颗粒Eu3+/ TiO2; 光催化降解; 染料
纳米TiO2是具有光催化活性的半导体氧化物,因其化学性质稳定、难溶于水、无毒、成本低而倍受关注[1, 2],它能将有机物较为彻底的氧化,最终的产物为CO2、H2O等简单的无机物,没有二次污染,是近年来绿色环保技术中研究热点[3]. 但TiO2是一种宽带隙的半导体(Eg = 3.12 eV),只能用紫外光作为激发光源,不能很好地利用太阳光,光激发产生的电子和空穴易复合,光量子效率不高,限制了其应用范围[4].
国内外学者为提高TiO2光催化性能,采取掺杂、半导体复合、贵金属沉积、染料敏化等[5-8]等手段对TiO2进行改性,其中金属离子掺杂是常用的方法. 稀土元素存在多个化合价,并有未完全充满的d和f轨道,故在TiO2半导体中掺杂少量稀土元素,使其捕获光生电子-空穴对,抑制光生电子与空穴的复合,提高了TiO2的光催化活性[9-11].
本文采用溶液法制备了不同铕(Eu3+)掺杂量的TiO2纳米颗粒(Eu3+/TiO2)并对其物理特性进行了初步表征.在可见光照射下,以光催化降解常用的工业染料为目标反应,探讨了Eu3+的掺杂量、催化剂的用量、溶液的pH值和催化剂的重复利用对催化活性的影响,优化获得了高活性的光催化条件.
1 实验部分
1.1 试剂和仪器
钛酸四丁酯C16H36O4Ti(CP,沪试),NaOH(AR,天津市凯通化学试剂有限公司),氧化铕Eu2O3(高纯试剂,沪试),HNO3、HCl (AR,沪试),乙醇(AR,国药),罗丹明B、百里香酚蓝、酸性铬蓝K、甲基蓝、甲基紫(AR,阿拉丁),亚甲基蓝、甲酚红、溴酚蓝(AR,天津市科密欧化学试剂有限公司),实验用水均为二次蒸馏水.
X-射线衍射仪(D8 ADVANCE型, 德国 Bruker),透射电子显微镜(Tecnai G 20型, 荷兰 FEI),X-射线光电子能谱仪(VG Multilab 2000型, 美国 Thermal Electron),双光束紫外-可见分光光度计(Lambda Bio35型, 美国 PE).
1.2 Eu3+/ TiO2纳米粒子的制备
TiO2纳米粒子的合成方法:将5 mL C16H36O4Ti缓慢滴加到 70 mL 10 mol/L NaOH溶液中,接着将其转入水热釜,放置于马弗炉中,160℃下恒温反应 24 h.待反应结束,将反应液过滤并用0.1 mol/L HCl和去离子水反复洗涤沉淀,直至pH值为7.0.最后在烘箱中 60℃下将沉淀物干燥 24 h,即可制备得到TiO2纳米粒子.为了提高TiO2结晶度,使用前将其高温煅烧,煅烧条件为:空气氛围下,升温速率 5 ℃/min,500 ℃煅烧1 h.
称取适量的TiO2粉末加入至30 mL的50%(V/V)的乙醇水溶液中,搅拌30 min,并缓慢滴加入一定量的Eu(NO3)3溶液,于80℃恒温,反应12 h停止,所得溶液分别用蒸馏水和乙醇洗涤、离心,60 ℃下干燥.
1.3 光催化实验
容器中加入80 mL 10 mg/L的染料溶液和适量的Eu3+/TiO2纳米粒子,暗箱中搅拌30 min以达到吸附-脱附平衡.以70 W的金卤灯作为光源进行光催化降解反应,每隔10 min取适量样品,离心,取上层清液,用分光光度计测其吸光度. 根据朗伯-比耳定律,在低浓度时溶液浓度与吸光度呈良好的线性关系.故可用相对吸光度值的变化来表征降解过程中目标染料浓度的变化,即:

式中ρ0、ρt分别为初始和t时刻目标染料的浓度(mg/L).A0和At分别为染料的初始和t时刻的吸光度.
2 结果与讨论
2.1 样品的表征
图1 为Eu3+/TiO2催化剂XRD谱图.样品谱图中2θ为 25.4°, 37.8°, 47.99° , 特征峰分别对应的(101), (004), (200)晶面,其中(101)晶面特征衍射峰强度最大,故晶型为锐钛矿型. 根据Scherrer公式:

其中,θ为衍射角,λ为X射线的波长(nm),β为衍射峰极大值一半处的半峰宽,D为平均晶粒大小(nm).分别计算以上3个特征峰对应的不同晶面的晶胞大小,其晶粒尺寸为14 nm.稀土掺杂TiO2的XRD图谱中并未出现氧化铕的特征峰,由于掺杂的稀土离子含量较低而未能检测到.
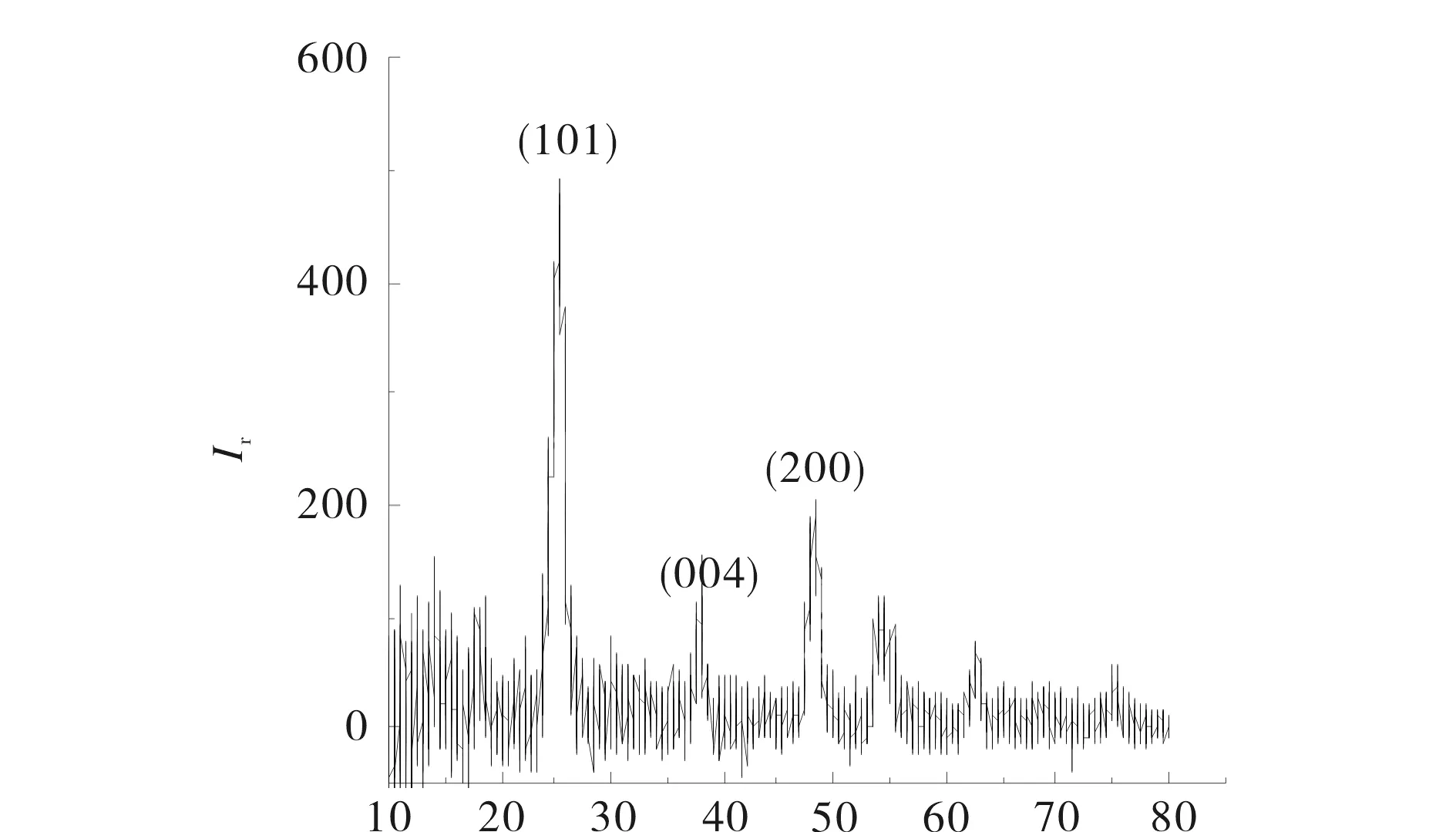
2θ/(°)图1 Eu3+/ TiO2纳米粒子的XRD谱图Fig.1 XRD spectra of the Eu3+/ TiO2 nanoparticles
图2为Eu3+/ TiO2纳米粒子TEM图.图2中催化剂粒度均匀,出现少量团聚,但总体上分散性较好,平均晶粒尺寸约15 nm.

图2 Eu3+/ TiO2纳米粒子的电镜图Fig.2 TEM spectra of the Eu3+/ TiO2 nanoparticles
图3 为Eu3+/ TiO2催化剂XPS谱图.图3a中除C、Ti、O、Eu元素特征能谱峰外,无其他元素能谱峰,表明样品有较高纯度;图3b为Ti的2p3/2和2p1/2结合能,分别为458.76 eV和464.48 eV,为Ti4+离子的特征峰;图3c中O的1s结合能是530.23eV.图3d中Eu的3d5/2结合能是1136.03 eV.根据结合能分析,键能1136.03 eV为Eu3+的特征峰(键能为1133~1136 eV),表明Eu主要以三价形态存在,且Eu3+可能在TiO2表面形成Eu-O-Ti键,Eu的3d3/2特征峰相比较弱,主要考虑Eu的3d5/2特征峰[13].

a)全谱; b) Ti2p; c) O1s; d) Eu3d图3 纳米粒子Eu3+/TiO2的XPS谱图Fig.3 XPS spectra of the Eu3+/ TiO2 nanoparticles
2.2 光催化反应
2.2.1 Eu3+离子的掺杂对RhB溶液降解的影响
图4为不同Eu3+掺杂浓度对RhB溶液降解影响.由图4可知,Eu3+掺杂能不同程度地提高TiO2的光催化活性,其活性随着掺杂的Eu3+离子浓度的升高而增强,掺杂摩尔比r(Eu3+︰TiO2)=3%,样品的催化活性最高,光照60 min,RhB溶液的降解率为98%.随着掺杂浓度的升高,催化活性反而下降,说明稀土元素掺杂浓度存在一个最佳值.
Eu3+离子掺杂在TiO2晶格中引入了缺陷位置,抑制电子-空穴对复合. Eu3+离子最外层电子组态为[Xe]4f6,很容易获取一个电子成为稳定[Xe]4f7电子态的Eu2+离子,电子转移过程导致电荷的不平衡进一步阻止电子-空穴对的复合而提高催化剂活性.若Eu3+掺杂成为电子或空穴的陷阱则抑制复合,若成为电子-空穴对的复合中心则加快了复合.故当Eu3+浓度较低时,捕获电子或空穴的能力不足,不能使光生电子-空穴对有效地分离;当Eu3+浓度过量,导致TiO2表面光生载流子复合中心增加,复合的几率增大,只有达到最佳掺杂比时,光催化活性才最强.
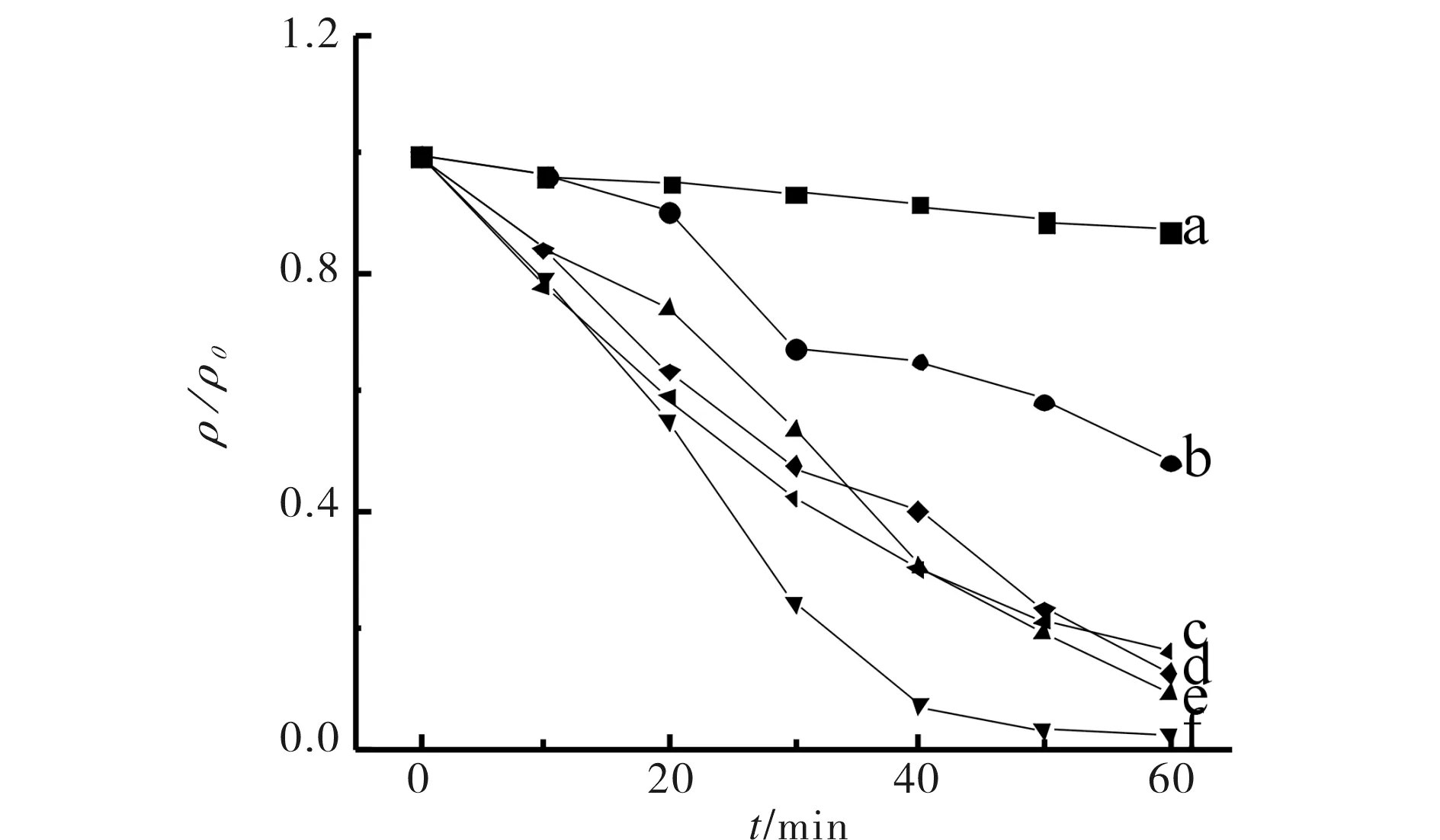
a) TiO2 ; b) 1% Eu3+/ TiO2 ; c) 5% Eu3+/ TiO2 ; d) 4% Eu3+/ TiO2 ;e) 2% Eu3+/ TiO2 ;f) 3% Eu3+/ TiO2图4 不同Eu3+掺杂浓度对RhB溶液降解的影响Fig.4 The activity of photocatalytic degradation on RhB with various Eu3+ doped content
2.2.2 催化剂用量对RhB溶液降解的影响
光催化反应中,催化剂用量对RhB溶液降解影响结果如图5所示,80 mL(10 mg/L)RhB溶液中若催化剂用量少,则不能充分利用光能,被光激发产生的电子少;随着催化剂从0.01 g增至0.1 g,提高了光能利用率,产生更多有效的光生电子和空穴,光催化效率提高,30 min内降解RhB溶液效率达到97%;而过多的催化剂对光线的漫反射和散射降低了光线的透过率,降低了催化剂对光能的利用率;同时反应器中催化剂质量太大,被光激发的催化剂之间的距离较小,导致光生载流子复合的机率增大,光催化效率降低.故催化剂加入量存在一个最佳值即1.25 mg/mL.
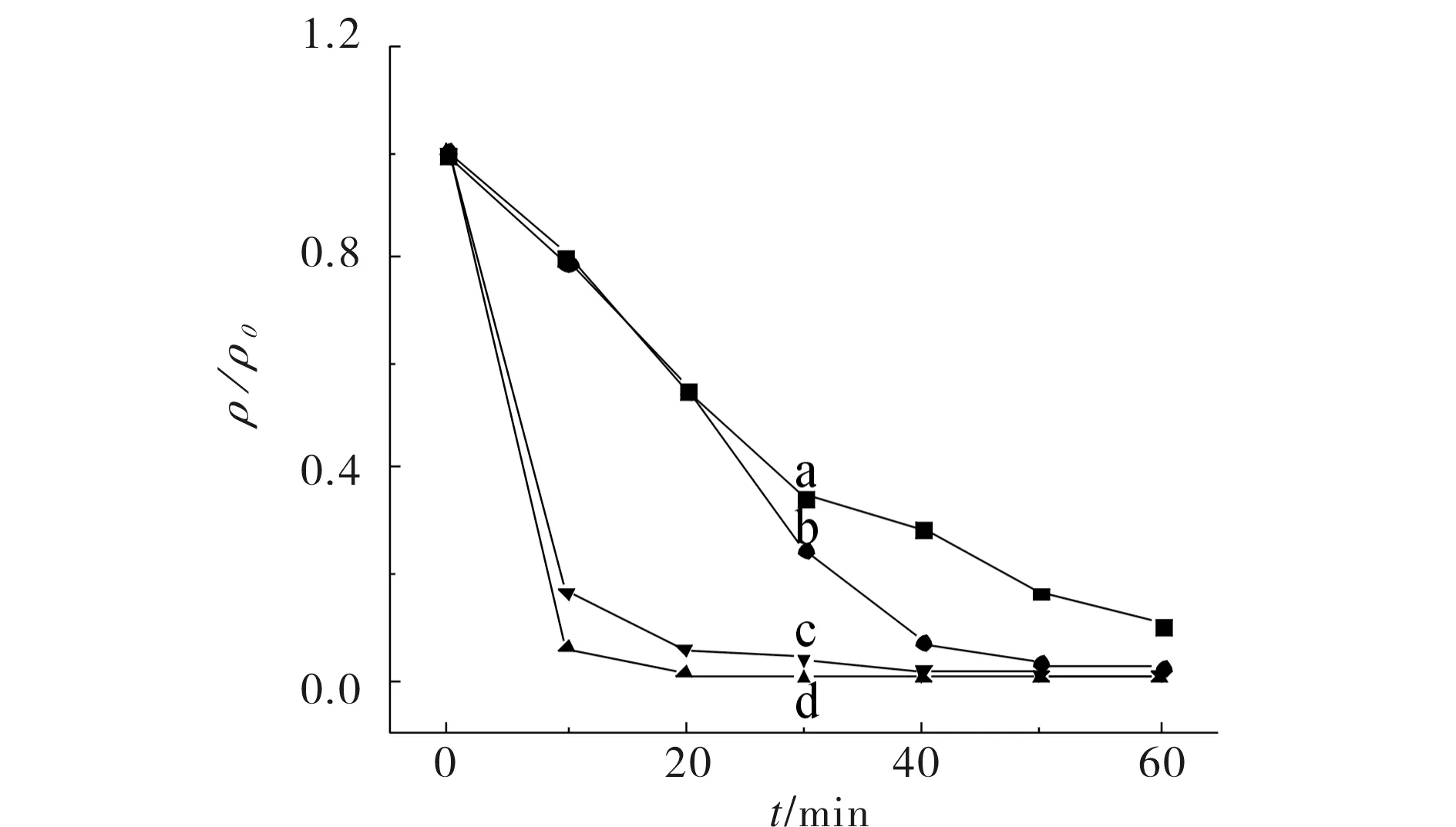
a ~ d ) 80 mL溶液催化剂用量分别为0.01,0.05, 0.15, 0.1g图5 催化剂的用量对RhB溶液降解的影响Fig. 5 The effect of catalyst dosage on the degradation of RhB
2.2.3 Eu3+/ TiO2对不同染料的降解效果
Eu3+/TiO2对不同染料的降解效果如图6和表1所示,所制备的Eu3+/TiO2催化剂对许多常用工业染料均没有选择性,在60 min内均具有一定的降解效果.

a)甲基蓝;b)甲酚红;c)百里香酚蓝;d)酸性铬酸K; e)亚甲基蓝;f)罗丹明B; g)溴酚蓝; h)甲基紫图6 不同染料对降解的影响Fig.6 The photocatalytic degradation results of the different dyes

染料ρ/(mg·L-1)*λmax/nm降解率/%酸性铬蓝K1052089.28亚甲基蓝1066494.66罗丹明B1055497.90溴酚蓝1059098.57百里香酚蓝2038078.03甲基紫1058099.30甲基蓝2030824.72甲酚红2043675.67
*ρ为初始浓度, 测试体积为80 mL
2.2.4 RhB溶液pH对光催化活性的影响
浓度为10 mg/L RhB溶液,分别用HCl和NaOH调节溶液pH值为1.02, 5.85, 10.75,13.09,结果如图7所示,pH变化对光催化反应影响较大,在酸性环境降解率为76%,在碱性环境中,Eu3+/TiO2在60 min降解RhB溶液的效率为98%. pH>7时,TiO2粒子的表面带负电[13],有利于空穴迁向TiO2表面,与电子供体OH-、H2O等反应,生成强氧化性的·OH;同时碱性环境中有利于催化剂吸附RhB,使RhB更容易被降解.在酸性环境中,催化剂不能有效地吸附RhB分子,故在酸性溶液中催化活性不高.

a~d) PH值分别为:1.02, 5.85, 10.75, 13.09图7 不同PH值对RhB溶液降解的影响Fig. 7 The effects of different pH on the degradation of RhB
2.2.5 催化剂的稳定性
在光催化降解染料污染物实际应用过程中,催化剂的循环降解能力是一个非常重要的参数.图8为Eu3+/TiO2光催化剂循环3次降解甲基紫溶液.如图8所示,循环3次的降解率分别为96%, 98%, 97%,催化效果并未随着循环次数的增加而下降,说明所制备Eu3+/TiO2催化剂稳定性很好.

图8 Eu3+/ TiO2光催化剂3次循环对甲基紫的降解Fig. 8 Photodegradation of methyl violet with 3 cycled Eu3+/ TiO2 nanoparticles
3 结语
本文采用溶液法制备了Eu3+/TiO2催化剂,与未掺杂纳米TiO2比较,Eu3+/TiO2具有可见光光催化活性.结果表明:掺杂摩尔比r(Eu3+︰TiO2)=3%,样品的催化活性最强,60 min内对RhB溶液的降解率达到了98%;Eu3+/ TiO2光催化剂对几种常用的工业染料无选择性,都具有一定的降解效果;在其3次循环降解甲基紫后,降解率仍保持在96%,说明Eu3+/ TiO2光催化剂具有良好的稳定性.
[1] Choi W, Termin A, Hoffmann M R. The role of metal ion dopants in quantum-sized TiO2: correlate-on between photworeactivity and charge carrier re-combination dyanmics[J]. J Phys Chem, 1994, 98(51):13669-13679.
[2] Iwasaki M, Hara M, Kawada H, et al. Cobalt ion-doped TiO2photocatalyst response to visible light[J].J Colloid Interface Sci, 2000, 224(1):202-204.
[3] Lee A C, Lin H R, Yang C Y, et al. Preparations and characterization of novel photocatalysts with mesoporous titanium dioxide (TiO2) via a sol-gel method[J]. Mater Chem Phys, 2008, 109(6):275-280.
[4] Zhu H Y, Lan Y, Gao X P, et al. Phase transition between nanostructures of titanate and titanium dioxides via simple wet-chemical reactions [J]. J Am Chem Soc, 2005, 127(18): 6730-6736.
[5] Asahi R, Morikawa T, Ohwaki T, et al. Visible light photocatalysis in nitrogen-doped titanium oxides [J].Science , 2001 , 293(5528) : 269-271.
[6] Yang G D, Yang B L, Xiao T C ,et al. One-step solvothermal synthesis of hierarchically porous nanostructured CdS/TiO2heterojunction with higher visible light photocatalytic activity[J]. Appl Surf Sci, 2013, 283:402-410.
[7] 毛立群, 冯彩霞, 金振声, 等.Au/TiO2的制备及其光催化氧化丙烯的研究[J].感光科学与光化学, 2005,23(1): 61-65.
[8] Ramarkrishna G, Ghosh H N. Emission from the charge transfer state of xanthene dye-sensitized TiO2nanoparticles : a new approach to determining back electront ransfer rate and verifying the marcus inverted regime [J]. J Phys Chem B,2001,105(29):7000-7008.
[9] 黄正喜, 龙剑英, 吴腊梅, 等. Nb2O5/CdS纳米粒子的制备及其光催化性能研究[J].中南民族大学学报:自然科学版,2014,33(4):26-30.
[10] Asal S, Saif M, Hafez H, et al. Photocatalytic generation of useful hydrocarbons and hydrogen from acetic acid in the presence of lanthanide modified TiO2[J].Int J Hydrogen Energ, 2011, 36(11): 6529-6537.
[11] Zhou W, Zheng Y H, Wu G H. Novel luminescent RE/TiO2(RE = Eu, Gd) catalysts prepared by insituation sol-gel approach construction of multi-functional precursors and their photo or photocatalytic oxidation properties[J]. Appl Surf Sci, 2006, 253 (3) :1387-1392.
[12] El-Bahy Z M, Ismail A A, Mohamed R M. Enhancement of titania by doping rare earth for photodegradation of organic dye (Direct Blue)[J]. J Hazard Mater, 2009,166 (1) :138-143.
[13] Leostean C, Stefan M , Pana O, et al. Properties of Eu doped TiO2nanoparticles prepared by using organic additives[J]. J Alloy Compd, 2013, 575:29-39.
[14] 李芳柏, 古国榜. 亚甲基蓝溶液的光催化脱色及降解[J].环境污染与防治,1999,21(6):1-4.
Preparation and Photodegradation Properties of Eu3+doped TiO2Nanoparticles
HuangZhengxi,LongJianying,WuLamei,LiuXianping
(College of Chemistry and Materials Science, South-Central University for Nationalities, Wuhan 430074, China)
Eu3+/TiO2nanoparticles were prepared by aqueous solution method with various Eu3+doping concentration. The samples were characterized by XRD, TEM and XPS. Using the photocatalytic degradation of industrial dye under visible light as target reaction, the effects of Eu3+doping concentration, catalyst dosage, solution pH and reutilization on photocatalytic activity were studied to obtain the optimized condition. The results showed that the structure of the Eu3+/TiO2catalyst was of anatase phase with a grain size of 14 nm when calcined at 500 ℃.The best photocatalytic activity were achieved with a Eu3+doping concentration of 3%, 1.25 mg/mL of catalyst dosage and at pH=10.75. The photocatalysts remained active after 3 cycles, with the degradation rate for methyl violet in 60 min maintained at about 96%.
Eu3+/ TiO2; photocatalytic degradation; dyes
2014-10-20
黄正喜(1978-), 女, 副教授,博士,研究方向:纳米粒子的性能研究,E-mail:zxhuang2005@126.com
国家民委科研基金资助项目(09ZN02), 中央高校基本科研业务费专项资金项目(CZY15004)
TQ034; O634
A
1672-4321(2015)03-0010-05

