芬苯达唑混悬剂的制备与含量测定方法的建立
张粉丽,党丽梅,杨小怀,张要齐,孙雪峰,童光年,贾维彬,杨小凡,李引乾*
(1.西北农林科技大学动物医学院,陕西杨凌712100;2.陕西蓝牧生物科技有限公司,陕西西安710000;3.岐山县蔡家坡镇畜牧兽医工作站,陕西岐山722450,4.河南惠通天下生物工程有限公司,河南郑州451162)
芬苯达唑(fenbendazole,FBZ)又名硫苯咪唑,为白色或类白色粉末,无臭,无味,不溶于水,可溶于二甲亚矾和冰醋酸[1-3],在国内外已经得到了广泛的应用[4]。芬苯达唑与虫体的微管蛋白结合,阻止微管的聚合,从而导致幼虫或成虫的表皮层与肠细胞质的微管损伤,降低虫体的消化和营养吸收的速率[5-6]。芬苯达唑可以有效防治牛、禽动物胃肠道线虫成虫及幼虫如毛圆线虫等所致的疾病。同时,该药对绦虫、猪蛔虫、牛前后盘吸虫童虫等的感染也有一定的疗效。现已广泛应用于羊、牛、马、猪、犬、猫和野生动物如鹿、鸵鸟、骆驼等多种动物胃肠道寄生虫病的防治[7-9]。
芬苯达唑不溶于水及一般有机溶剂,其在临床常用的制剂主要有畜用片剂、丸剂和水产用颗粒剂等。在应用过程中,常有药片被吐出的情况,造成实际剂量不足,而且投服费时费力,操作使用不方便[1-2]。悬剂系指难溶性固体药物以微粒状态分散于分散介质中形成的非匀相的液体药剂。在混悬剂中,药物以微粒状态分散,分散度较大,胃肠道吸收迅速,有利于提高生物利用度[10]。本试验对以芬苯达唑为主药制备出芬苯达唑混悬剂,建立起紫外-可见分光光度计测定芬苯达唑混悬剂有效成分含量的方法,旨在为该制剂的质量控制和临床应用提供理论依据。
1 材料与方法
1.1 材料
1.1.1 仪器 SPECORD50紫外-可见分光光度计,德国耶拿分析仪器有限公司产品;BS-210S型电子分析天平,德国赛多利斯股份公司产品;pH-S3B型pH计,上海精密科学仪器有限公司产品;78-1型磁力加热搅拌器,江苏金坛保庆分析设备厂产品;QL-901型漩涡振荡器,其林贝尔仪器制造公司产品。
1.1.2 试剂与药品 芬苯达唑原料,山东亚康药业股份有限公司产品,批号:20130519;芬苯达唑对照品,中国兽医药品监察所产品,批号:20130515;冰乙酸,天津市百世化工有限公司产品,批号:20121124;无水乙醇,成都市科龙化工试剂厂产品,批号:20120711;其他试剂均为分析纯。
1.2 方法
1.2.1 处方组成与制备工艺流程 根据预试验结果,芬苯达唑混悬剂按以下处方采用分散法,用高速均质分散机制备。即每25mL混悬剂中含1.25g芬苯达唑,0.25g羧甲基纤维素钠,0.025mL聚山梨酯-80,0.25g柠檬酸,0.025g苯甲酸钠。按筛选确定的芬苯达唑混悬剂配方,先将助悬剂、润湿剂、絮凝剂、抗氧化剂溶于适量的蒸馏水中,待溶胀或溶解后备用。取润湿剂溶于少量的蒸馏水中,然后加入芬苯达唑润湿后,用高速均质分散机混匀,转移至25mL量筒,用蒸馏水均质机数次,转移至量筒,加蒸馏水定容至25mL,密封筒口,混匀后在室温下静置保存备用[11-12]。
1.2.2 芬苯达唑混悬剂含量测定方法
1.2.2.1 测定波长的确定 精密称取芬苯达唑标准品10.80mg,置于100mL容量瓶中,先加入2.0 mL冰醋酸溶解,再以无水乙醇稀释至刻度,振荡摇匀,作为标准品储备液。精密量取标准品储备液0.10mL,置于50mL的容量瓶中,加无水乙醇稀释至刻度,摇匀,制成0.216μg/mL的溶液备用。以无水乙醇作为空白对照,用分光光度法在190nm~450nm波长对阿苯达唑标准品进行扫描[13-14]。
1.2.2.2 标准工作曲线的绘制 用移液管分别精密吸取上述标准品储备液0.10、0.30、0.50、0.80、1.0mL,置于10mL容量瓶中,用无水乙醇稀释至刻度,配制成1.08、3.24、5.40、8.64、10.80μg/mL的系列对照品溶液备用。以无水乙醇作为空白对照,在选择的最大波长处测定上述标准品的吸光度。以芬苯达唑标准品质量浓度C为横坐标,吸光度为纵坐标,绘制吸光度-质量浓度标准曲线,求得标准曲线的回归方程。
1.2.2.3 回收率试验与精密度试验 精密称取适量芬苯达唑和其他辅料,按1.2.2方法制备成芬苯达唑理论浓度为10.0、30.0、50.0μg/mL的混悬剂样品。按上述样品处理方法处理后,在已选择的最大波长处测定OD值,采用标准曲线计算芬苯达唑测定浓度,计算其回收率。分别在同一天测定3次;1周内隔天测定,共测定3次,分别计算日内精密度和日间精密度。
2 结果
2.1 芬苯达唑混悬剂制备结果
试验制备的混悬剂外观为乳白色,静置分层后,上清为无色透明液体,沉淀物为乳白色。放置过程中pH无明显改变,变化范围为5.5~6.2。
2.2 芬苯达唑混悬剂含量测定方法
2.2.1 测定波长的确定 芬苯达唑标准品紫外测定波长见图1。由图1可知,芬苯达唑标准品在217nm波长处有最大吸收峰,故确定217nm为芬苯达唑混悬剂的检测波长。
2.2.2 标准曲线的绘制 以吸光度为纵坐标、浓度(μg/mL)为横坐标,绘制标准曲线:y=0.099 2x-0.033 6,R2=0.995 3。结果表明,芬苯达唑在1.08μg/mL~10.80μg/mL浓度范围内呈良好的线性关系(图2)。

图1 芬苯达唑紫外吸收谱图Fig.1 UV absorption spectra of fenbendazole

图2 芬苯达唑质量浓度-吸光度标准曲线Fig.2 Standard curve for mass concentration of fenbendazole
2.2.3 回收率试验结果 回收率试验结果见表1。由表1可以看出,芬苯达唑的平均回收率为98.60%,变异系数为0.48%,说明该方法稳定、可靠。因此可以使用紫外-可见分光光度法测定混悬剂中有效成分的含量。
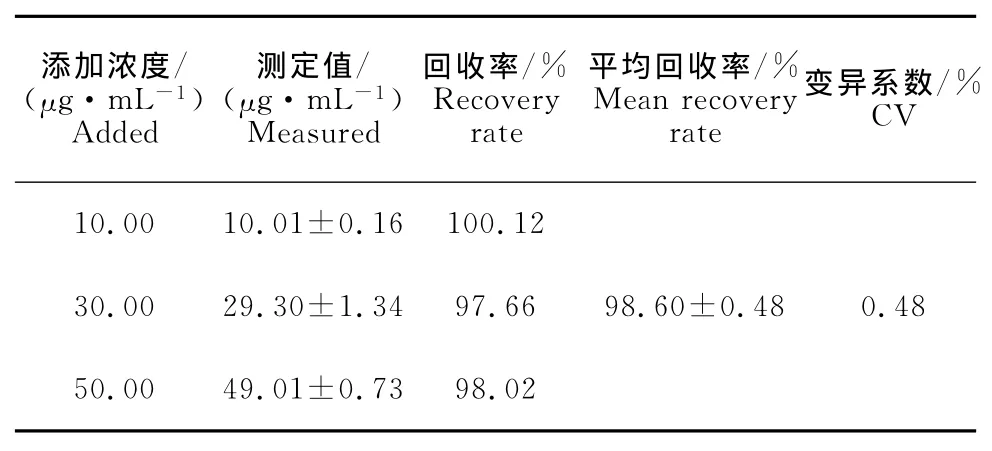
表1 混悬剂中芬苯达唑的回收率Table 1 The recovery rate of fenhendazole in the suspension
2.2.4 精密度试验结果 精密度试验结果见表2。由表2可以看出,混悬剂中芬苯达唑的日内和日间平均精密度分别为1.30%和1.35%,日内和日间精密度RSD均小于5%,说明测定方法稳定性较好,可用于芬苯达唑混悬剂中芬苯达唑含量的测定。

表2 混悬剂中芬苯达唑精密度测定结果Table 2 The precision of fenbendazola in the suspension
3 讨论
混悬剂一般含有主药、助悬剂、防腐剂、抗氧化剂等,本试验通过正交试验发现,影响混悬剂沉降体积比、重分散性、通针性等的主要因素是助悬剂、润湿剂等成分的比例。通常在混悬剂中添加适量的助悬剂可在一定程度上提高介质的黏稠度,使药物容易分散和减缓颗粒沉降。若助悬剂选用不当,介质黏度过大,虽可增大制剂沉降比,但久贮易板结,并易产生黏壁现象。芬苯达唑混悬剂制备时选用羧甲基纤维素钠为助悬剂,所制得的混悬剂有速释相和缓释相两部分,通过延缓释放和延缓吸收的方法,既保留了常规制剂见效快的优点,又具有长效的特点。为了获得絮状物的最佳均化,可添加低黏度或中等黏度的羧甲基纤维素钠。润湿剂可以使分散相分散度大、稳定性好、不易受外界因素影响。分散相浓度增大时不转相,不受微生物的分解和破坏,同时可以使不同的未溶解物质之间保持足够的静电斥力,防止其碰撞后产生聚合,从而保证溶液的稳定性。合适的润湿剂对于防止不同相之间的分离具有重要作用,本试验选用聚山梨酯-80表面活性剂作为润湿剂。
目前,芬苯达唑含量的测定方法包括旋光法、紫外-可见分光光度法、高效液相色谱法等。本研究采用紫外-可见分光光度法测定混悬剂中芬苯达唑的含量,但由于芬苯达唑难溶于水,易溶于无水乙醇,且无水乙醇与芬苯达唑无相似的吸收峰,对含量测定不存在干扰,故在本试验中,建立含量测定方法时选择无水乙醇作为溶剂和空白对照,从而排除了辅料对测定的干扰。根据中国兽药典(2010年版)使用紫外-可见分光光度法测定芬苯达唑含量,具有操作简便快速,结果稳定可靠等特点。本试验配制的标准品溶液,在190nm~450nm波长范围内扫描,混合物仅在217nm处有明显的吸收峰,在其他波长处未出现明显的吸收峰,与吴剑平[15]等的报道一致。
本研究采用紫外-可见分光光度法直接测定芬苯达唑混悬剂中芬苯达唑含量,结果显示,本法简单快速,在一定的浓度范围内,线性关系良好,灵敏度和准确度高,适用于芬苯达唑混悬剂中芬苯达唑含量的测定,可为芬苯达唑混悬剂的进一步研究提供参考方法。
[1]陈杖榴.兽医药理学[M].3版.北京:中国农业出版社,2009:317-318.
[2]中国兽药典委员会.中华人民共和国兽药典·兽药使用指南·化学药品卷[M].北京:中国农业出版社,2011:135-136.
[3]Short C R,Flory W,Hsieh L C,et al.The oxidative metabolism of fenbendazole:acomparative study[J].J Vet Pharmacol Therap,1988,(11):50-55.
[4]Landoni M F,Soraci A L,Delatour P,et al.Enantioselective behaviour of drugs used in domestic animals:a review[J].J Vet Pharmacol Therap,1997,(20):1-16.
[5]Morgen U M,Reynoldson J A,Thompson R C.Activities of several benzimidazoles and tubulin inhibitors againstGiardiaspp[J].InvitroAntimicrob Agents Chemother,1993,37(2):328-331.
[6]高学军,李庆章.广谱抗蠕虫药物奥芬达唑研究进展[J].动物医学进展,2004,25(3):53-55.
[7]Landoni M F,Soraci A L,Delatour P,et al.Enantioselective behaviour of drugs used in domestic animals:a review[J].J Vet Pharmacol Therap,1997(20):1-16.
[8]Jacobs D.Anthelmintics for dogs and cats[J].Inter J Parasitol,1987(17):511-518.
[9]Beier E,Lehenbauer T W,Sangiah S.Clinical effcacy of fenbendazole against gastrointestinal parasites in llamas[J].Small Ruminant Res,2000(36):17-23.
[10]胡功政.兽医药剂学[M].北京:中国农业出版社,2008.
[11]王敏儒,杨少林,杨 鸿,等.恩诺沙星注射混悬剂的研制及药物含量测定[J].中国兽医科技,2002,32(10):30-32.
[12]史同瑞,许腊梅,于万才,等.土霉素混悬剂的研制及药物质量指标测定[J].现代畜牧兽医,2005,10(9):9-11.
[13]路 宽,吴秀兰.药物阿苯达唑固体新剂型研究[J].医药前沿,2012,6(3):4-5.
[14]李华日,孙 睿,李青梅,等.复方盐酸土霉素注射液的制备[J].西北农林科技大学学报:自然科学版,2013,41(3):55-60.
[15]吴剑平,商 军.对2005年版中国兽药典芬苯达唑鉴别方法的商榷[J].中国兽药杂志,2010,44(7):25-27.

