精制胃乐胶囊长期毒性实验研究
姚观平,余丽梅,范振海,吴 芹
(遵义医学院 1.贵州省细胞工程重点实验室;2.基础药理省部共建教育部重点实验室,贵州 遵义 563099;3.遵义医学院附属医院 生殖医学中心,贵州 遵义 563099)
基础医学研究
精制胃乐胶囊长期毒性实验研究
姚观平1,2,3,余丽梅1,范振海1,吴 芹2
(遵义医学院 1.贵州省细胞工程重点实验室;2.基础药理省部共建教育部重点实验室,贵州 遵义 563099;3.遵义医学院附属医院 生殖医学中心,贵州 遵义 563099)
目的 通过SD大鼠长期毒性实验观察精制胃乐胶囊(rWLC)可能产生的毒性反应,以评价rWLC的安全性,为临床安全用药提供依据。方法 120只SD大鼠随机分为4组(空白组、rWLC高、中、低剂量组),每组30只,3个给药剂量组分别为4.00、1.41和0.50 g·kg-1·d-1(分别是成人临床日用量50 mg·kg-1·d-1的80、28和10倍),每天灌胃1次,连续给药90 d。停药日及14 d后,分别检测大鼠体重、血液学和血液生化指标,计算重要脏器指数,并进行组织病理检查。结果 与空白组比较,rWLC 3个剂量组对大鼠的一般状况、体重、血液学、血液生化指标、重要脏器指数和脏器组织结构等均未见明显改变。停药14 d后,检测rWLC 3个组大鼠上述各项指标也未见明显异常。结论 长期大剂量连续灌胃给予rWLC,对大鼠无明显毒性作用,停药14 d后也未见药物的延迟性毒性反应,表明该药临床拟用剂量安全,未见明显长期毒性。
精制胃乐胶囊;长期毒性;大鼠
精制胃乐胶囊(refine Wei Le capsule,rWLC)由白芍、苍术、元胡、肉桂等6味中药组成,源于贵州省黔东南地区,在原胃乐散的组方和炮制工艺基础上,结合现代药物制剂工艺研制而成的新制剂,采用原方精制、水提、醇提,按工艺1、工艺2、工艺3分别将其命名为rWLCI、rWLC2和rWLC3。其中工艺1生产的rWLC对消化性溃疡疗效最佳,可通过多靶点发挥作用,保护黏膜,促进损伤修复。具有温中和胃、降逆止呕、解痉之功效,用于气滞所致胃脘疼痛,腹胀纳差,反酸嗳气等症。我们前期药效学实验研究表明对实验性胃溃疡有较好的防治作用。为保证临床用药的安全性,我们按疗程进行了90d及停药14 d后的大鼠毒性反应实验研究[1-2],现将结果总结报告如下。
1 材料与方法
1.1 材料
1.1.1 动物 选用清洁级SD大鼠120只,体重130~150g,雌雄各半,购于购自第三军医大学大坪医院动物实验中心,许可证号:SCXK(渝)2007-0005,合格证号:0004256。
1.1.2 药物 rWLC主要按胃乐散原方精制(原生粉过80目筛),由遵义医学院药理教研室与贵阳春科药物研发股份有限公司联合研制而成。实验前用蒸馏水配制所需浓度的混悬液,并能保持较好的流动性及可操作性,可配制最大浓度为0.2 g/mL[5-6]。
1.1.3 主要仪器 电子分析天平为北京赛多利斯电子天平有限公司,Leica光学显微镜(德国Leica 公司),全自动全血细胞分析仪(日本Sysmex,XE-2100),全自动血细胞分析仪(美国ADVIA2120)和全自动生化分析仪(日本Olympus,AU5421)。
1.2 方法 取SD大鼠120只,按体重随机分为4组,每组30只,雌雄各半。rWLC高、中、低剂量组分别为4.00、1.41、0.50 g·kg-1·d-1,给药体积均为10 ml·kg-1;空白对照组给予等体积的生理盐水,定时灌胃1次/d,给药6d/周,称量体重1次/周,每日观察大鼠外观体征、行为、饮食、呼吸、二便、皮毛光泽等一般情况,于第90天各组随机麻醉15只大鼠,腹主动脉取血,分别送遵义医学院附属医院检验科,采用全自动全血细胞分析仪和全自动生化分析仪检测血液学、血液生化指标,称重法称量大鼠体重和脏器重量,计算脏器指数,留取各类组织器官标本,送遵义医学院形态学实验室切片、染色,进行组织病理学检查。各组剩余大鼠停药14 d,按照新药注册要求和有关文献方法对上述各项指标进行检测[3-4]。

2 结果
2.1 一般状况 连续灌胃给药9d过程中,rWLC各给药组与空白组大鼠的外观体征、行为活动、腺体分泌、呼吸、粪便等状况均正常;停药14 d后,亦未见异常,说明rWLC连续灌胃给药90 d,对大鼠一般状况无明显毒性反应。
2.2 体重变化 连续灌胃给药90 d和停药后14 d过程中,各剂量组不同性别大鼠随着时间延长体重逐渐增加,且各组间比较无统计学意义(见图1)。

图1 rWLC给药90 d和停药14 d后对雌(B)雄(A)大鼠体重的影响
2.3 血液学指标变化 大鼠连续服用rWLC 90d过程中和停药14 d,分别检测rWLC高、中、低剂量组大鼠血液中白细胞(WBC)、红细胞(RBC)、血红蛋白(HB)、平均红细胞血红蛋白浓度(MCHC)、平均红细胞血红蛋白量(MCH)、血小板(PLT)、红细胞容积(HCT)、平均红细胞容积(MCV)、凝血酶原时间(PT)、网织红细胞计数(Ret)等血液学指标。结果:除给药90 d后雌性低剂量组Hb、MCHC含量较空白组明显增高(P<0.01),但无剂量依赖关系,高、中剂量组未见明显改变,其他各剂量组的各项指标与空白组比较,均无统计学意义(P>0.05);停药14 d中、低剂量雄性大鼠WBC、RBC、PT、Ret计数较空白组明显增加(P<0.01),但无剂量依赖关系,其他各剂量组的各项指标与空白组比较,均无统计学意义(见表1~2)。综上所述,以血象观察rWLC未出现明显毒性反应。
表1 rWLC给药90 d对大鼠血液学指标的影响(n=8)
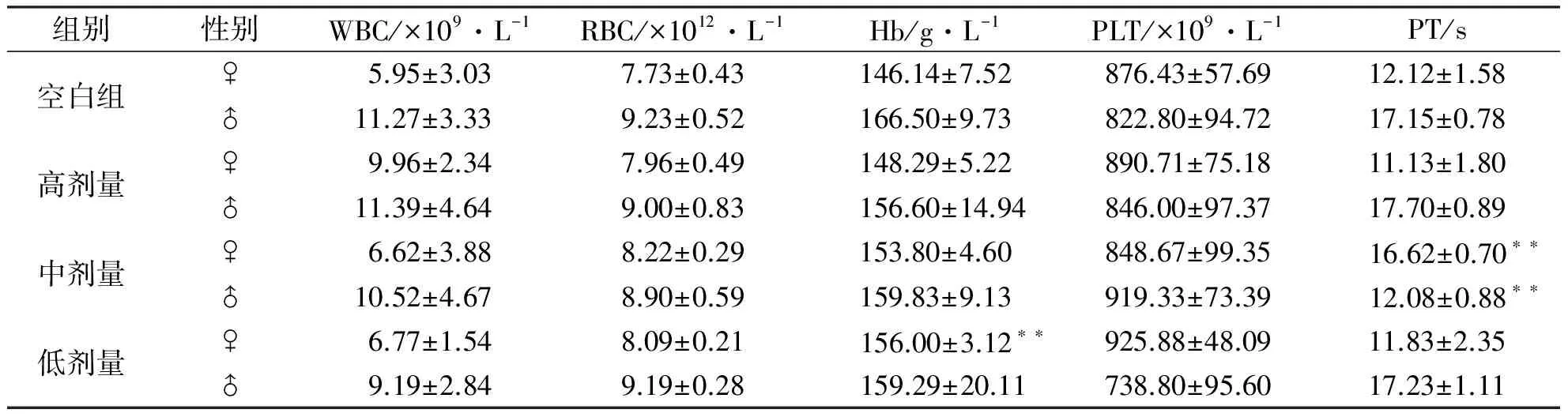
组别性别WBC/×109·L-1RBC/×1012·L-1Hb/g·L-1PLT/×109·L-1PT/s空白组♀5.95±3.037.73±0.43146.14±7.52876.43±57.6912.12±1.58♂11.27±3.339.23±0.52166.50±9.73822.80±94.7217.15±0.78高剂量♀9.96±2.347.96±0.49148.29±5.22890.71±75.1811.13±1.80♂11.39±4.649.00±0.83156.60±14.94846.00±97.3717.70±0.89中剂量♀6.62±3.888.22±0.29153.80±4.60848.67±99.35 16.62±0.70∗∗♂10.52±4.678.90±0.59159.83±9.13919.33±73.39 12.08±0.88∗∗低剂量♀6.77±1.548.09±0.21 156.00±3.12∗∗925.88±48.0911.83±2.35♂9.19±2.849.19±0.28 159.29±20.11738.80±95.6017.23±1.11
与空白组比较,**P<0.01。
表2 rWLC停药恢复期14 d大鼠血液学指标的变化(n=7)

组别性别WBC/×109·L-1RBC/×1012·L-1Hb/g·L-1PLT/×109·L-1PT/s空白组♀5.96±1.778.31±0.66154.00±7.54860.60±70.8415.58±0.44♂17.96±2.758.39±0.77159.00±4.55713.75±85.8817.26±0.62高剂量♀7.52±1.298.81±0.68163.75±8.66864.40±93.1115.84±0.98♂19.76±1.438.17±0.76159.67±12.90823.50±27.5818.20±0.42中剂量♀7.64±2.637.47±0.21147.25±6.19872.25±54.8316.83±0.81∗♂9.75±3.18∗∗8.99±0.43167.00±10.27816.75±83.3017.10±0.40∗低剂量♀7.89±0.998.10±0.64158.00±4.85898.00±34.5816.45±0.66♂8.49±2.67∗∗9.58±0.48∗∗175.67±7.99∗∗811.75±81.3916.37±1.62
与空白组比较,*P<0.05,**P<0.01。
2.4 血液生化学指标变化 大鼠连续用rWLC 90d过程中和停药恢复14 d,检测其血清钾离子浓度(K+)、钠离子浓度(Na+)、氯离子浓度(Cl-)、丙氨酸氨基转换酶(ALT/U·L-1)、天门冬氨酸氨基转换酶(AST/U·L-1)、碱性磷酸酶(ALP/U·L-1)、总胆红素(T-BIL/μmol·L-1)、总蛋白(TP/g·L-1)、白蛋白(ALB/g·L-1)、尿素氮(BUN/mmol·L-1)、肌酐(Cr/μmol·L-1)、甘油三酯(TG/mmol·L)、总胆固醇(T-CHO/mmol·L-1) 、血糖(GLU/mmol·L-1)等指标水平。结果:给药90 d后雌性高剂量组TP、BUN,中剂量ALP、GLU,低剂量BUN有所升高(P<0.01),但各剂量组数值均在正常范围,且无剂量依赖关系,故认为rWLC给药90d对各项血液生化指标没有明显影响。停药后14d,高、中、低剂量rWLC各组与空白组比较Cl-、AST 、ALP、CREA、GLU有一定升高(P<0.01),但各剂量组数值也均在正常值范围,且无组间差异,故认为停药后的升高是正常范围波动。提示rWLC对大鼠血液生化指标没有明显毒性改变(见图2)。
2.5 重要脏器指数的变化 大鼠连续服用rWLC 90d和停药14d,留取心、肝、脾、肺、肾、肾上腺、胸腺、脑、子宫、卵巢、睾丸、附睾等重要要脏器组织,肉眼观察其大小、形状、色泽、质地、包膜等与空白组比较均无异常改变,称重,计算脏器指数。结果:给药90d后,可见雌性大鼠中剂量肝、胸腺,低剂量脾脏脏器指数明显增加,但无明显肝脏功能及血象改变,各组脏器指数均在正常范围;停药14 d,雌性高剂量卵巢、肝,中剂量脾脏脏器指数明显增大(P<0.01);雄性高剂量脑、睾丸脏器指数明显增大,而高剂量肾上腺、低剂量胸腺以及中、低剂量肺脏器指数反而降低(P<0.01),但这些升降变化与剂量均未显示剂量依赖关系,各组的脏器指数也均在正常范围(见表3~4)。上述变化仍属正常波动范围。提示rWLC对大鼠主要脏器指数无明显影响。

A:rWLC给药90 d对雌性大鼠血液生化学指标影响;B:rWLC给药90 d对雄性大鼠血液生化学指标影响;C:rWLC停药恢复期14 d雄性大鼠血液生化学指标变化。D:rWLC停药恢复期14 d雄性大鼠血液生化学指标变化。与空白组比较,*P <0.05,**P <0.01。
表3 rWLC对给药90d大鼠主要脏器指数的影响(n=8)

组别性别 心 肝 脾 肺 肾 脑空白组高剂量中剂量低剂量♀0.33±0.022.96±0.230.19±0.030.61±0.050.64±0.070.74±0.07♂0.25±0.013.22±0.300.17±0.020.55±0.090.64±0.060.49±0.08♀0.35±0.033.13±0.210.22±0.030.65±0.050.67±0.060.79±0.07♂0.27±0.023.57±0.250.15±0.020.54±0.060.72±0.060.53±0.03♀0.30±0.013.83±0.25∗∗0.23±0.060.58±0.030.60±0.020.68±0.03♂0.28±0.013.01±0.150.16±0.040.53±0.090.71±0.080.52±0.09♀0.32±0.022.95±0.200.58±0.09∗∗0.64±0.060.68±0.060.75±0.07♂0.28±0.023.07±0.300.16±0.030.50±0.040.63±0.030.50±0.07
与空白组比较,**P<0.01。
表4 rWLC停药恢复期14 d大鼠主要脏器指数的变化(n=7)

组别性别 心 肝 脾 肺 肾 脑空白组高剂量中剂量低剂量♀0.35±0.032.80±0.040.22±0.020.57±0.040.64±0.040.76±0.07♂0.30±0.022.76±0.320.30±0.050.66±0.060.67±0.070.47±0.05♀0.33±0.023.14±0.21∗∗0.24±0.060.60±0.020.68±0.050.78±0.05♂0.32±0.012.80±0.130.30±0.100.56±0.080.74±0.04 0.59±0.03∗∗♀0.34±0.052.95±0.150.54±0.06∗∗0.60±0.050.63±0.040.79±0.07♂0.30±0.032.81±0.140.31±0.080.52±0.06∗∗0.72±0.060.50±0.05♀0.33±0.012.93±0.230.19±0.010.58±0.060.64±0.030.78±0.04♂0.28±0.012.60±0.110.24±0.080.53±0.04∗∗0.73±0.040.55±0.07
与空白组比较,**P<0.01。
2.6 各脏器组织病理学变化 HE染色,各重要脏器和组织病理检查结果显示,rWLC给药90d和停药14d后,各组大鼠的心、肝、脾、肺、肾、脑(大脑、小脑、脑干) 、垂体、脊髓(颈、胸、腰段) 、骨髓、肾上腺、甲状腺、甲状腺旁腺、胸腺、唾液腺、食管、气管、主动脉、胃肠(大肠、小肠) 、胰、膀胱、子宫、卵巢、淋巴结、坐骨神经、乳腺、睾丸、附睾、前列腺等脏器的肉眼和组织病理学检查均未见明显异常,与空白组比较无统计学意义(见图3)。

A:空白组;B:rWLC高剂量组;1:心肌;2:肝脏;3:脾;4:肺;5:肾。
3 讨论
以往的研究表明,原方胃乐散及rWLC对消化性溃疡及急性化脓梗阻性胆管炎等具有明显治疗效果[6-7],按照参照急性毒性实验最大耐受剂量及其治疗有效剂量和消化性溃疡用药剂量的疗程[8],rWLC慢性毒性实验中给药剂量为4.00、1.41和0.50 g·kg-1·d-1,分别相当于成人临床用量80、28和10倍(临床用药剂量为50mg·kg-1·d-1),连续灌胃给药90d和停药恢复14 d,观测rWLC个剂量组与空白组正常大鼠一样,一般状况良好,体重逐渐正常增长[9-10];血液学和血液生化学检查各项指标及脏器指数,给药组与空白组之间差异也无统计学意义,表明rWLC长期大剂量用药未见明显的血液系统、肝肾肺及肠功能异常;心、肝、脾、肺、肾、脑等重要脏器和胃肠、多种腺体、生殖泌尿及骨和骨髓等组织也未见明显病理学改变及延迟性毒性,进一步确证了rWLC未见明显慢性毒性,表明同许多临床已经应用的中药复方制剂一样,rWLC按临床拟用的剂量、途径及疗程应用其安全性较为可靠。
[1] 徐叔云.药理实验方法学[M].第3版.北京:人民卫生出版社,2002:231-232.
[2] 国家食品药品监督管理局.中药天然药物长期毒性试验技术指导原则[S].国家食品药品监督管理局,2005.
[3] 王菊凤,杨道德,李鹄鸣.蛹虫草富锗胞外多糖对大鼠长期毒性研究[J].中国药理学通报,2014,30(9):1329-1330.
[4] 马晓玲,魏鸿雁,贾晓光,等.骆驼刺胶囊对大鼠的长期毒性[J].中药药理与临床,2014, 30(2):113-115.
[5] 余丽梅,邓江,文国容,等.胃乐胶囊对实验性溃疡的作用[J].遵义医学院学报,2001,24(5): 388-399.
[6] 王雨波,余丽梅,姚观平,等. 精制胃乐胶囊促进大鼠乙酸性胃溃疡修复的作用与机制[J].中成药,2014,36(7):1533-1535.
[7] 舒涛,范振海,吴芹,等.胃乐散治疗急性化脓性梗阻性胆管炎的实验研究[J].第三军医大学学报,2010,32(11):1235-1236.
[8] 姚观平,余丽梅,杨平花,等. 精制胃乐胶囊的抗炎镇痛作用与急性毒性研究[J].遵义医学院学报,2013,36(6):511-514.
[9] 朱斌,蒋平,杨阳,等.养胃颗粒对大鼠的长期毒性试验[J].中国医院药学杂志,2014,34(3):181-186.
[10] 徐步强,黄正明,李瑞生,等.水芹总酚酸胶囊对Wistar大鼠的长期毒性研究[J].中药药理与临床, 2014,30(2):82-86.
[收稿2014-07-11;修回2014-12-12]
(编辑:谭秀荣)
Chronic toxicity experimental study of refined wei le capsule in rats
YaoGuanping1,2,3,YuLimei1,2,FanZhenhai1,WuQin2
(1. The Key Laboratory of Cell Engineering of Guizhou Province;2.Key Laboratory of Basic Pharmacology of Ministry of Education, Zunyi Medical University,Zunyi Guizhou 563099,China; 3. Human Reproductive Medicine Center,The Affiliated Hospital of Zunyi Medical University, Zunyi Guizhou 563099,China)
Objective To evaluate the safety of refined wei le capsule (rWLC) and to provide evidence for the clinical safely drug-use through long-term toxicity test in rats .Methods 120 SD rats were randomly divided into 4 groups (control group,high,middle and low dosage of rWLC groups),30 rats in each group.Rats were treated with rWLC at three doses of 4.00, 1.41, and 0.50 g·kg-1·d-1(equivalent to 80, 28 and 10 times of adult clinic daily dose of 0.05 g·kg-1·d-1) by gavage, once a day for 90 days. The body weights, the indexes of hematology and biochemistry, organ weight index, and the pathological examination were measured at 90 days of administration and 14 days after stopping the medicine, respectively .Results The general animal health body weights,the indexes of hematology and biochemistry,organ weight index,and pathological examination of major organs of rats had no significant difference comparing with control group after 90 days of administration;14 days after stopping the medicine, no evident abnormal changes of above indexes were observed in administration groups.Conclusion rWLC has no significant toxicity or delayed toxicity after long-term of high dosage continuous oral gavage in rats, which indicates that the clinic dose is safe.
refine wei le capsule ;long-term toxicity;rat
贵州省科技厅中药现代化专项(NO:黔科合社字[20085023])。
余丽梅,女,博士,教授,硕士生导师,研究方向:药理学,E-mail:ylm720@sina.com。
R251
A
1000-2715(2015)01-0032-05

