不同剂量右美托咪定对心肺转流风心瓣膜置换术患者心肌损伤的影响
符 炜,顾尔伟,王 宏,梅 玫,陈庆书,赵 浩
(1.安徽医科大学第一附属医院麻醉科,合肥 230032;2.蚌埠医学院第一附属医院,安徽蚌埠 233000)
论著·临床研究
不同剂量右美托咪定对心肺转流风心瓣膜置换术患者心肌损伤的影响
符 炜1,2,顾尔伟1△,王 宏2,梅 玫2,陈庆书2,赵 浩2
(1.安徽医科大学第一附属医院麻醉科,合肥 230032;2.蚌埠医学院第一附属医院,安徽蚌埠 233000)
目的 比较不同剂量右美托咪定对心肺转流(CPB)风心瓣膜置换术患者围术期心肌损伤的影响。方法 随机、双盲将择期风心二尖瓣狭窄瓣膜置换术患者分为3组: 对照组(C组)、低剂量右美托咪定组(DEX1组)、高剂量右美托咪定组(DEX2组)。3组患者分别于全身麻醉诱导前(T0)、CPB后2 h(T1)、CPB后24 h(T2)、CPB后48 h(T3)、CPB后72 h(T4)抽取患者中心静脉血,监测各时点血浆肌钙蛋白I(cTnI)、肌酸激酶同工酶(CK-MB)水平、平均动脉压(MAP)和心率(HR)的变化。并记录气管导管拔除时间、ICU停留时间、术后24 h时心肌收缩力评分、术后24 h引流量、心脏自动复跳及心血管不良事件发生的情况。结果 与T0相比,DEX2组HR在T1时间点明显降低。与C组相比,DEX1组在T1时间点HR、血浆CK-MB明显降低,术后24 h时心肌收缩力评分和心血管不良事件发生率显著降低(P<0.05),但心脏自动复跳率没有明显改善;DEX2组在T1时间点HR显著减少,在T1和T2时间点血浆CK-MB值明显降低,在T2~T4时间点血浆cTnI值显著减少,心脏自动复跳率明显增加,术后24 h时心肌收缩力评分和心血管不良事件发生率明显降低(P<0.05);DEX1组和DEX2组的气管导管拔除时间、ICU停留时间和术后24 h引流量没有明显变化。结论 右美托咪定对风心瓣膜置换术患者围术期心肌损伤具有保护作用,负荷量0.6 μg/kg继之以0.6 μg·kg-1·h-1输注的给药方法更佳。
风湿性心脏病;右美托咪定;心肌保护
右美托咪定是α2受体高选择性激动剂。研究显示α2受体激动剂参与调节自主神经系统和心血管系统[1]。Ren等[2]应用右美托咪定于不停跳冠状动脉搭桥术中,发现右美托咪定对心肌具有保护作用。本研究的目的是观察不同剂量右美托咪定对风心瓣膜置换术患者心肌损伤的影响。
1 资料与方法
1.1 一般资料 本研究已获医院医学伦理委员会批准,并与患者或家属签署知情同意书。临床资料选择择期风心瓣膜置换手术患者60例,年龄50~70岁,ASA Ⅱ~Ⅲ级,心功能Ⅱ~Ⅲ级。患者均无严重肝肾衰竭、无麻醉药过敏史、无精神病史、无严重房室传导阻滞(阻滞小于Ⅱ度)。将患者随机双盲分为3组,低剂量右美托咪定组(DEX1组)、高剂量右美托咪定组(DEX2组)和对照组(C组),每组20例。
1.2 方法 TCI 系统采用思路高公司的TCI-Ⅰ型注射泵。BIS监测采用AspectTM Medical system BISXP监测仪,额部电极采用SpectTM BISXP Sensor。所有患者麻醉前30 min肌内注射吗啡0.1~0.2 mg/kg和东莨菪碱0.006 mg/kg。入室后面罩吸氧常规监测平均动脉压(MAP)、心率(HR)、ECG、SpO2和BIS,开放外周静脉通路,局部麻醉下行左侧桡动脉穿刺置管监测有创血压,诱导后置入中心静脉导管备静脉采样。血浆靶控输注丙泊酚1.5~2.0 μg/mL,待患者入睡后舒芬太尼0.6 ng/mL血浆靶控输注和顺式阿曲库铵0.2 mg/kg行麻醉诱导,DEX1组和DEX2组于气管插管成功后10 min分别开始静输右美托咪定(批号:20130301,江苏恩华药业有限公司)0.3 μg/kg或0.6 μg/kg,输注时间10 min,随后分别以0.3 μg·kg-1·h-1,0.6 μg·kg-1·h-1持续输注至关胸。C组静脉输注同等量生理盐水作对照,方法同DEX1组和DEX2组。麻醉维持:舒芬太尼0.6 ng/mL血浆靶控输注,丙泊酚1.5~2.0 μg/mL血浆靶控输注,术中调整血浆靶浓度维持BIS于40~60,间断静脉注射顺式阿曲库铵0.05 mg/kg。体外循环期间维持ACT>480 s,MAP 50~80 mm Hg,复温开始时静脉输注多巴胺(4~10) μg·kg-1·min-1。非体外循环期间维持MAP 60~90 mm Hg、HR 70~100次/分。当MAP<60 mm Hg时,静脉注射去氧肾上腺素40~80 μg;当MAP>90 mm Hg时,静脉注射尼卡地平0.01 mg/kg。当HR<50次/分时,静脉注射阿托品0.3~0.5 mg;当HR>100次/分时,静脉注射艾司洛尔0.5~1.0 mg/kg。
1.3 观察指标 于全身麻醉诱导前(T0)、CPB后2 h(T1)、CPB后24 h(T2)、CPB后48 h(T3)、CPB后72 h(T4)时抽取中心静脉血5 mL检测血浆肌钙蛋白I(cTnI)和肌酸激酶同工酶(CK-MB)浓度,并记录各时点的MAP和HR。记录气管导管拔除时间、ICU停留时间、术后24 h时心肌收缩力评分、术后24 h引流量、心脏自动复跳及心血管不良事件(包括非致死性心肌梗死、再次心肌梗死、卒中、充血性心力衰竭、微血管事件、猝死等)发生的情况。

2 结果
3组患者一般情况各指标、体外循环时间和主动脉阻断时间比较差异无统计学意义(P>0.05),见表1。所有病例均安全完成了手术。60例患者取得完整数据。
与T0时间点相比,C组、DEX1组和DEX2组MAP值在T1~T4时间点差异无统计学意义(P>0.05);与C组相比,DEX1组和DEX2组MAP值在T0~T4各个时间点差异无统计学意义(P>0.05)。与T0时间点相比,DEX2组HR在T1明显降低(P<0.05);与C组相比,在T1时间点DEX1组和DEX2组HR都显著减少(P<0.05),见表2。
与C组相比,DEX1组血浆CK-MB在T1时间点明显降低(P<0.05),术后24 h时心肌收缩力评分和心血管不良事件发生率显著降低(P<0.05),心脏自动复跳率、气管导管拔除时间和ICU停留时间没有显著改变。与C组相比,DEX2组血浆CK-MB值在T1和T2时间点明显降低,血浆cTnI值在T2~T4时间点显著减少,心脏自动复跳率明显增加,术后24 h时心肌收缩力评分和心血管不良事件发生率明显降低(P<0.05),气管导管拔除时间、ICU停留时间和术后24 h引流量没有明显改变(P>0.05)。见表3、4。
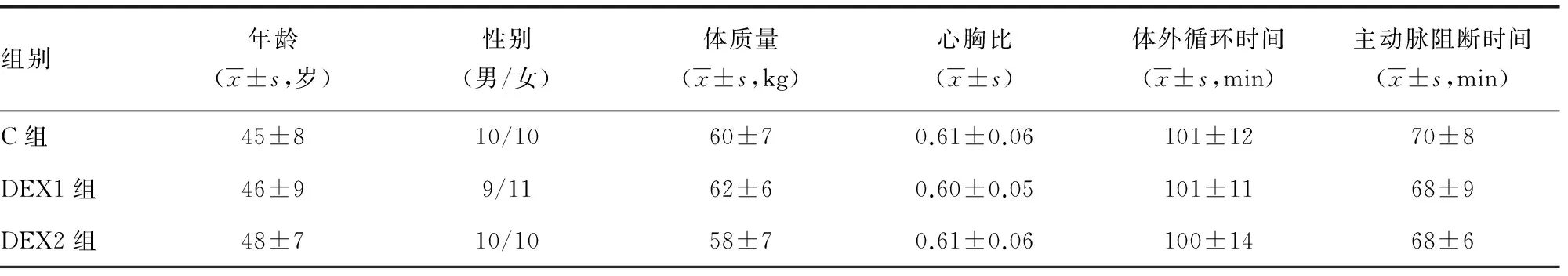
表1 3组患者一般情况和术中各指标的比较(n=20)
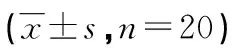
表2 3组各时点血流动力学比较
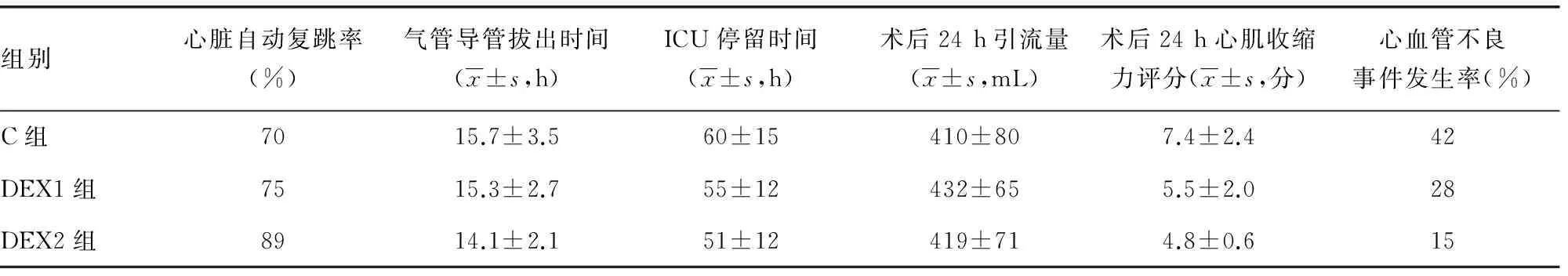
表3 3组患者术中及术后各指标比较(n=20)
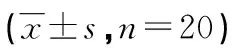
表4 3组各时间点CK-MB和cTnI比较
3 讨论
本实验通过观察风心瓣膜置换手术患者应用右美托咪定对体外循环后心肌损伤的影响,结果发现在本研究计量范围内应用右美托咪定能剂量依赖性地抑制体外循环后心肌cTnI和CK-MB值的增加,心脏自动复跳率、术后24 h时心肌收缩力评分和心血管不良事件发生率明显改善,提示右美托咪定对体外循环后心肌损伤具有保护作用。
目前认为右美托咪定心肌保护效应可能通过多重机制发挥作用。研究已经显示短时间的缺血再灌注会对随后心肌长时间缺血再灌注损伤提供心肌保护作用,这即为缺血预处理效应。注射药物也可以产生缺血预处理的效应,这即为药物预处理。腺苷、二氮嗪和吸入麻醉药能诱发药物预处理的心肌保护作用[3-4]。由于缺血预处理通过复杂的信号级联介导,因此,单独的药物预处理并不能完全模拟缺血预处理效应[5]。然而,Okada等[6]在大鼠心肌缺血再灌注前预注右美托咪定导致大鼠心肌缺血再灌注后梗死范围减小,预注α2受体拮抗剂育亨宾能取消这种保护作用。同时发现右美托咪定能显著减少冠状动脉血流量,注射育亨宾亦能逆转此效应。因此,单独注射右美托咪定发挥心肌保护作用可能通过激活α2受体减少冠状动脉血流量而模拟缺血预处理效应。与此实验相一致,新近研究表明[7]冠状动脉低灌注缺血预处理能导致心肌梗死范围减少。因此,提示在缺血再灌注损伤前使用右美托咪定具有心肌保护作用[8]。但是Mimuro 等[9]在离体小鼠心脏缺血再灌注损伤后使用右美托咪定得出了相反的结论。其原因可能为缺血再灌注损伤后,冠状动脉对右美托咪定没有应答,因而冠状动脉血流没有变化,同时右美托咪定可能是通过α2受体的激活增加了梗死面积。
右美托咪定改善心肌氧平衡可能与右美托咪定心肌保护机制有关。有文献报道右美托咪定通过增加缺血心肌/非缺血心肌的血流比率改善心肌氧平衡和维持局部缺血心脏的氧平衡[10]。有研究也发现右美托咪定能维持山羊和猪非缺血心脏心肌的氧平衡[11]。右美托咪定减少儿茶酚胺释放导致心肌氧需的降低也可能是右美托咪定心肌保护的另一机制。Yoshitomi等[12]观察右美托咪定对猪心肌缺血再灌注损伤的效应,发现冠状动脉内注射右美托咪定显著减少再灌注后心肌室性心律失常的发生率,显著改善再灌注心肌收缩力的恢复,同时发现冠状动脉内注射右美托咪定显著抑制心肌缺血区冠状静脉内去甲肾上腺素释放的增加,提示右美托咪定对缺血再灌注心肌具有保护作用,这种保护作用可能与抑制心肌再灌注后血浆去甲肾上腺素的增加有关。
总之,试验证实了在本观察剂量范围内右美托咪定持续输注剂量依赖性地抑制心肌缺血再灌注损伤,对风心瓣膜置换术损伤心肌具有保护作用。
[1]Chrysostomou C,Schmitt CG.Dexmedetomidine: Sedation,analgesia and beyond[J].Expert Opin Drug Metab Toxicol,2008,4(7):619-627.
[2]Ren J,Zhang H,Huang L,et al.Protective effect of dexmedetomidine in coronary artery bypass grafting surgy[J].Exp Ther Med,2013,6(2):497-502.
[3]Pain T,Yang XM,Critz SD,et al.Opening of mitochondrial K(ATP) channels triggers the preconditioned state by generating free radicals[J].Circ Res,2000,87(5):460-466.
[4]Piriou V,Chiari P,Knezynski S,et al.Prevention of isoflurane-induced preconditioning by 5-hydroxydecanoate and gadolinium: possible involvement of mitochondrial adenosine triphosphate-sensitive potassium andstretch-activated channels[J].Anesthesiology,2000,93(8):756-764.
[5]Yellon DM,Downey JM.Preconditioning the myocardium: from cellular physiology to clinical cardiology[J].Physiol Rev,2003,83(20):1113-1151.
[6]Okada H,Kurita T,Mochizuki T,et al.The cardioprotective effect of dexmedetomidine on global ischaemia in isolated rat hearts[J].Resuscitation,2007,74(3):538-545.
[7]Ibacache M,Sanchez G,Pedrozo Z,et al.Dexmedetomidine preconditioningactivates pro-survival kinases and attenuates regional ischemia/reperfusioninjury in rat heart[J].Biochim Biophys Acta,2012,1822(4):537-545.
[8]Hausenloy DJ,Yellon DM.Reperfusion injury salvage kinase signalling:taking a RISK for cardioprotection[J].Heart Fail Rev,2007,12(3/4):217-234.
[9]Mimuro S,Katoh T,Suzuki A,et al.Deterioration of myocardial injury due to dexmedetomidine administration after myocardial ischaemia[J].Resuscitation,2010,81(12):1714-1717.
[10]Willigers HM,Prinzen FW,Roekaerts PM,et al.Dexmedetomidine decreases perioperative myocardial lactate release in dogs[J].Anesth Analg,2003,96(7):657-664.
[11]Lawrence CJ,Prinzen FW,de Lange S.Hemodynamic and coronary vascular effects of dexmedetomidine in the anesthetized goat[J].Acta Anaesthesiol Scand,1997,41(9):830-836.
[12]Yoshitomi O,Cho S,Hara T,et al.Direct protective effects of dexmedetomiding against myocardial ischemia-reperfusion injury in anesthetized pigs[J].Shock,2012,38(1):92-97.
Effect of different doses of dexmedetomidine on myocardial injury on cardiopulmonary bypass in patients with rheumatic heart valve replacement surgery
FuWei1,2,GuErwei1△,WangHong2,MeiMei2,ChenQingshu2,ZhaoHao2
(1.DepartmentofAnesthesiology,theFirstAffiliatedHospitalofAnhuiMedicalUniversity,Hefei,Anhui230032,China;2.theFirstAffiliatedHospitalofBengbuMedicalCollege,Bengbu,Anhui233000,China)
Objective To investigate the effect of different doses of dexmedetomidine on myocardial injury (in perioperative period) on cardiopulmonary bypass (CPB) in patients with rheumatic heart valve replacement surgery.Methods Patients undertook rheumatic heart valve replacement surgery with mitral stenosis were divided into three groups (n=20) in randomized and double-blind method: control group (group C),dexmedetomidine 0.3 μg/kg group (DEX1 group),dexmedetomidine 0.6 μg/kg group (DEX2 group).Central venous blood was drawn respectively before anesthesia induction (T0),2h after CPB (T1),24 h after CPB (T2),48 h after CPB (T3),72 h after CPB (T4).Plasma muscle calcium protein I (cTnI) and creatine kinase (CreatineKinase MB,CK-MB) were measured and mean arterial pressure and heart rate were recorded at each time point.Furthermore,extubation time,ICU stay,postoperative inotropic score 24 h after operation,drainage 24 h after operation,cardio auto-resuscitation rates and adverse cardiovascular events were recorded.Results Compared with T0,HR was significantly lower in the T1time point in DEX2 group.Compared with group C,HR,plasma CK-MB,inotropic score 24 h after operation and cardiovascular adverse events was significantly reduced in the T1time points in DEX1 group (P<0.05),but the heart auto-resuscitation rate did not significantly improved.HR at T1,plasma CK-MB values at T1and T2,and plasma cTnI values at T2-T4were significantly reduced;the heart resuscitation significantly increased,myocardial contraction power ratings 24 h after operation and the incidence of cardiovascular events was significantly lower in DEX2 group (P<0.05).The extubation time,ICU stay time and drainage 24 h after operation did not change significantly in both groups.Conclusion Dexmedetomidine has a protective effect on perioperative myocardial injury in patients with rheumatic heart valve replacement surgery,and the effect would be better when the dexmedetomidine was infused at 0.6 μg·kg-1·h-1after a loading dose of 0.6 μg/Kg continuously.
rheumatic heart disease;dexmedetomidine;cardiac protection
符炜(1982-),主治医师,本科,主要从事心血管麻醉研究工作。△
,E-mail:ay_guew_mz@163.com。
10.3969/j.issn.1671-8348.2015.04.021
R971.2
A
1671-8348(2015)04-0492-03
2014-10-08
2014-11-26)

