HPLC—ELSD法测定肉制品中山梨糖醇
甘凝岚

摘 要:建立肉制品中山梨糖醇的高效液相色谱-蒸发光散射检测器(high performance liquid chromatography-evaporation light scattering detector,HPLC-ELSD)测定法。实验采用乙腈-水溶液(7∶3,V/V)作为流动相直接超声提取样品,经Agilent ZORBAX NH2(4.6 mm×250 mm,5 ?m)色谱柱分离,蒸发光散射检测器检测;优化ELSD检测器参数为飘移管温度90 ℃,氮气流速2.0 L/min。结果表明:山梨糖醇含量在0.2~5.0 mg/mL范围内有良好的线性,方法相对标准偏差(relative standard deviation,RSD)在1.28%~2.02%之间,回收率在88.3%~99.0%之间。本方法具有样品前处理简便、方法检出限低、方法重现性好的特点,适用于肉制品中山梨糖醇含量的测定。
关键词:山梨糖醇;肉制品;高效液相色谱-蒸发光散射法
Determination of Sorbitol in Meat Products by HPLC-ELSD
GAN Ninglan
(Jiangsu Product Quality Testing and Inspection Institute, Nanjing 210007, China)
Abstract: A high performance liquid chromatography with evaporative light-scattering detection (HPLC-ELSD) method was developed for the determination of sorbitol in meat products .The samples were ultrasonically extracted using acetonitrile water (7:3, V/V) as mobile phase and separated on ZORBAX NH2 Agilent column, then detected by evaporative light scattering detector (ELSD). Optimized ELSD detector parameters such as drift tube temperature and nitrogen flow rate were set at 90 ℃ and 2.0 L/min, respectively. The results showed that sorbitol displayed good linearity relationship over the concentration range of 0.2 to 10 mg/mL. The method precision (relative standard deviation, RSD) ranged from 1.28% to 2.02%, and the recovery was between 88.3% and 99.0%.This method has the advantages of simple sample pretreatment, low detection limit and good reproducibility. So it is useful for the determination of sorbitol in meat products.
Key words: sorbitol; meat products; high performance liquid chromatography-evaporation light scattering detector (HPLC-ELSD)
中圖分类号:O657.7 文献标志码:A 文章编号:
doi: 10.7506/rlyj1001-8123-201508001
山梨糖醇又名山梨醇、蔷薇醇、清凉茶醇、六羟基醇[1],主要是由葡萄糖催化加氢法和淀粉糖化直接加氢法生产,也可用蔗糖为原料进行生产[2]。山梨糖醇在食品工业中功能性很多,主要包括高黏性(促使食品增浓与定型)、吸湿性(使食品有润滑性和柔软性)、甜味或凉爽的味觉、多价螯合剂、结晶改性剂(延迟结晶)和膨黏性能等[3]。因此,山梨糖醇的添加可使食品在整个保质期内各种品质都保持不变。山梨糖醇是一种半天然、营养型甜味剂,其甜度只有蔗糖(食糖)的60%,其发热量也比食糖降低了1/3,是一种非生龋性物质,现已广泛用于糖尿病人专用的无糖型食品[4]。研究发现,在肉制品的加工过程中,山梨糖醇的添加能够增强肉制品体系对外加水分和自身水分的保持,提高体系的持水力,可以作为一种优异的持水剂使用。例如,在相同的加工时间内山梨糖醇的添加能够降低肉制品的水分活度,有利于产品的贮藏;添加山梨糖醇还可以显著缩短产品的生产周期,提高产品的得率及水分含量;同时,山梨糖醇的添加也能改善产品的品质,使其硬度降低,更易咀嚼[5]。近年来,部分肉制品生产商开始在肉制品的加工过程中加入山梨糖醇,作为持水剂使用。
据报道,美国要求在相应食品包装上说明,山梨糖醇最大日摄入量为50 g。欧洲要求当糖醇使用比例超过10%时,则须在相应食品包装上说明可能引起轻度腹泻。我国现有的食品安全国家标准GB2760—2011《食品安全国家标准 食品添加剂使用标准》中规定肉制品中不得添加山梨糖醇,而调味品中的山梨糖醇可以“按生产需要适量使用”,但没有明确限制其添加量。肉制品中常使用调味料来改善口感,若肉制品中测得山梨糖醇则必须符合带入原则,且不得对食用者造成损害。由于内服过量的山梨糖醇,会导致食用者腹泻和消化紊乱,因此需要建立检测肉制品中山梨糖醇的分析方法,为肉制品行业的规范发展提供标准依据。
目前,檢测山梨糖醇常用的方法有高效液相色谱法[6-11]、液质联用法[12-14]、气相色谱法[15-18]、气质联用法[19]、离子色谱-质谱联用法[20]、离子交换色谱-脉冲安培法[21]等。示差折光检测器对外部环境要求较高,实验室的温度、湿度以及流动相的流速都会对其有较大影响,因此,实验过程要求相对严格。用气相色谱法检测山梨糖醇前必须对山梨糖醇经行衍生化处理,但是这种处理很容易改变山梨糖醇的性质。离子色谱法用于山梨糖醇含量的检测研究较多,其灵敏度较好,但是山梨糖醇在电极表面会发生氧化还原反应,从而影响方法的准确性。运用质谱检测器检测山梨糖醇,虽然灵敏度高,但样品前处理操作复杂。本实验选用蒸发光散射检测器法,具有样品处理简单、基线稳定、检出限低、针对性强等优点。本方法的建立旨在为肉制品中山梨糖醇含量的测定做出基础性的探索工作。
1 材料与方法
1.1 材料与试剂
香肠制品、火腿肠、猪肉脯、牛肉干、酱卤肉等共10 批次市售样品均购于南京各大超市。
乙腈(色谱纯) 美国Tedia公司;去离子水 美国Millipore公司;山梨糖醇(99%) 美国Sigma公司。
1.2 仪器与设备
AL204型电子天平 梅特勒-托利多(上海)有限公司;A25实验室高剪切分散乳化机 上海乔荣电子科技有限公司;XW-80A漩涡混合器 上海青浦沪西仪器厂;KQ-300E型超声波清洗机 昆山市超声波仪器有限公司;Heraeus Multifuge XIR型离心机 美国Thermo Fisher公司;1260型高效液相色谱仪、380型蒸发光散射检测器 美国Agilent公司。
1.3 方法
1.3.1 样品制备
取5.00 g粉碎后的肉制品于50 mL具塞离心管中,准确加入20.0 mL流动相,涡旋混合均匀,超声提取30 min,以8 000 r/min离心3 min,取适量上清液,经0.22 μm微孔滤膜过滤,滤液待上机分析。
1.3.2 色谱条件
色谱柱:Agilent ZORBAX NH2柱(4.6 mm×250 mm,5 μm);流动相:乙腈-水(7∶3,V/V);流速:1.0 mL/min;柱温箱温度:40 ℃;进样体积:10 μL;漂移管温度:90 ℃;氮气流速:2.0 L/min。
1.3.3 标准溶液配制
1.3.3.1 标准储备液的配制
精确称取山梨糖醇标准品100.00 mg于10 mL容量瓶中,配制成质量浓度为10 mg/mL的标准储备液。
1.3.3.2 标准工作液的配制
分别准确吸取不同体积山梨糖醇的标准储备液,将其用水稀释成质量浓度为0.2、0.5、1、2、4、5 mg/mL的标准工作液。进行高效液相色谱-蒸发光散射检测器(high performance liquid chromatography-evaporation light scattering detector,HPLC-ELSD)检测,根据样品的保留时间进行定性分析。
2 结果与分析
2.1 测定条件的优化
2.1.1 样品前处理方法的优化
由于肉制品中的基质较为复杂,其中蛋白质和油脂含量较高,在前处理过程中要尽量去除这些杂质,同时也要保证样品中山梨糖醇的提取率。实验比较了3 种前处理方法:方法1为参照GB/T22222—2008《食品中木糖醇、山梨醇、麦芽糖醇的测定 高效液相色谱法》,样品要经石油醚去脂,蒸发净石油醚,加入去离子水超声提取,再加入沉淀剂沉淀蛋白,滤纸过滤,滤液再经0.45 ?m微孔滤膜过滤,待上机检测;方法2参照SN/T 3142—2012《进口食品中D-甘露糖醇、麦芽糖、木糖醇、D-山梨糖醇的检测方法 液相色谱-质谱法》,样品用去离子水超声提取后,将提取液用容量瓶定容,再取出部分提取液经Oasis HLB固相萃取柱净化洗脱,最后经0.22 ?m滤膜过滤,待上机检测;方法3为样品经流动相乙腈-水(7:3,V/V)超声提取,离心后直接经0.22 ?m滤膜过滤,待上机检测。
图1 不同方法的实验结果
Fig. 1 Effect of pretreatments on sorbitol recovery
由图1可知,方法1由于沉淀剂易干扰目标物山梨糖醇的提取,使得其回收率较低;虽然方法2的回收率较方法1高,但步骤繁琐,耗时较长;而方法3的回收率较高,且操作简单,因此,选用方法3作为本实验的前处理方法。
2.1.2 检测器的选择
参照GB/T22222—2008《食品中木糖醇、山梨醇、麦芽糖醇的测定 高效液相色谱法》运用示差折光检测器检测山梨糖醇,该方法仪器系统平衡时间较长、检测过程中基线易飘移、方法检出限较高,实验对检测环境和流速要求较高且方法重现性较差。采用蒸发光散射检测器检测山梨糖醇,检测系统稳定性较好、仪器检出限较低、方法重现性较好。因此本方法选用蒸发光散射检测器检测肉制品中的山梨糖醇。
2.1.3 ELSD参数的优化
ELSD检测主要受到2 个重要参数的影响:漂移管温度和载气(N2)流速。比较漂移管温度分别为80、85、90、95、100 ℃时,载气(N2)流速分别为1.0、1.5、2.0、2.5、3 L/min时对山梨糖醇响应强度的影响。
图2 不同漂移管温度(a)和不同氮气流速(b)条件下山梨糖醇的响应强度
Fig. 2 Response intensity of sorbitol at different drift tube temperatures (a) and different nitrogen flow rates (b)
由图2可知,在一定范围内,漂移管温度越高,山梨糖醇的响应越好,信噪比越大,当漂移管温度过高达到95 ℃以上时,山梨糖醇的响应反而下降,信噪比减小;随着氮气流速的提高,山梨糖醇的响应越好,信噪比也不断增大,在流速达到2.0 L/min以后,山梨糖醇的响应强度变化趋于平衡。因此,最终选择最适用于山梨糖醇检测的ELSD参数设置条件:漂移管温度为90 ℃,载气流速为2.0 L/min。
2.2 方法的验证
2.2.1 最低检出限和定量限
以空白肉制品,经1.3.1节处理后,仪器进样10 μL时,山梨糖醇标准溶液最低检出限为8.0 μg/mL,最低定量限为25 μg/mL。
2.2.2 工作曲线和线性范围
取配制好的山梨糖醇标准工作液,上机检测,以山梨糖醇标准溶液的峰面积计算其对数为纵坐标,以其质量浓度对数为横坐标,绘制标准曲线得到线性回归方程:y=1.25x-7.31,相关系数为0.999 2,线性范围为0.2~5.0 mg/mL。
2.2.3 精密度实验
吸取山梨糖醇标准工作液0.2、1、5 mg/mL,各质量浓度均进样6 次,以峰面积计算精密度。由表1可知,相对标准偏差(relative standard deviation,RSD)介于1.28%~2.02%之间,精密度良好。
2.2.4 回收率
1 mg/mL山梨糖醇标准溶液、空白牛肉干样品、牛肉干样品1mg/mL山梨糖醇加标色谱图如图3所示。取不含有山梨糖醇的空白牛肉干9份,按0.2、1、5 mg/g 3种加标水平加标,经1.3.1节方法处理样品后,按1.3.2节条件用仪器检测,由表2可知,回收率在88.3%~99.0%之间,RSD%均小于5.0%,符合分析要求。
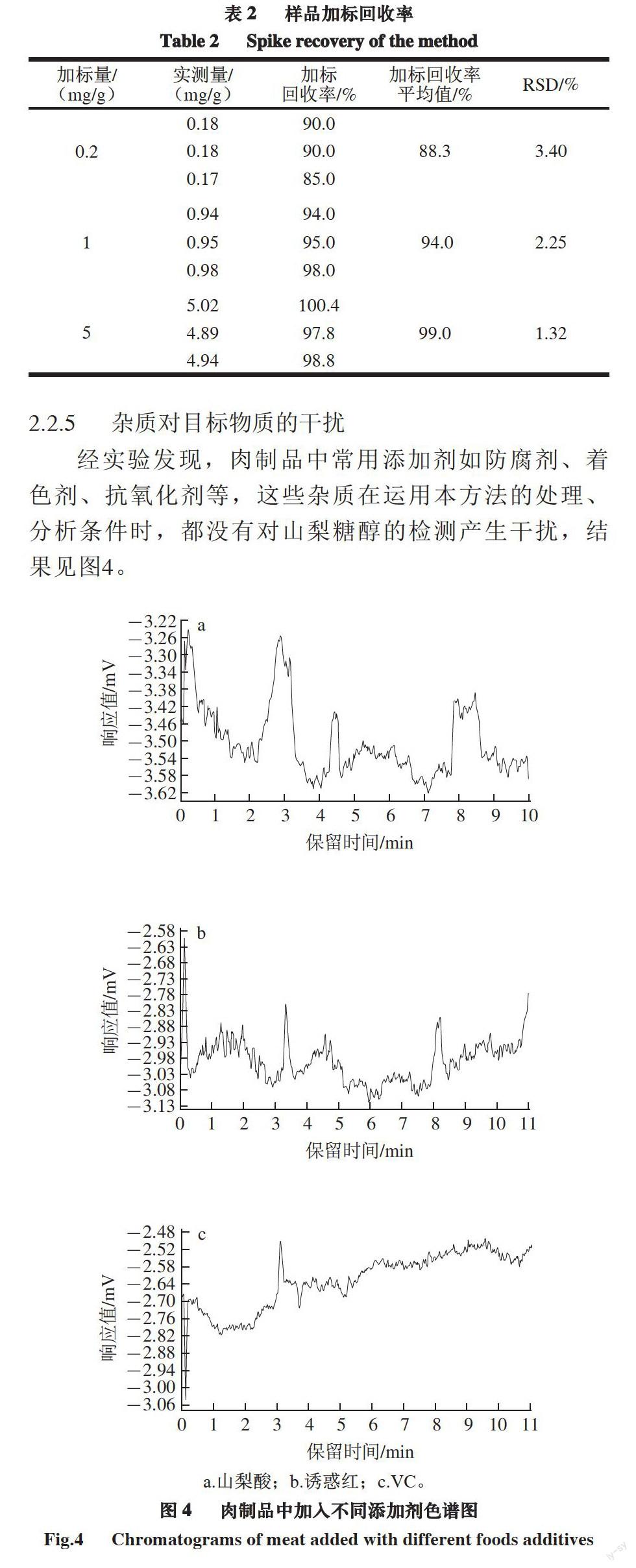
2.2.5 杂质对目标物质的干扰
经实验发现,肉制品中常用添加剂如防腐剂、着色剂、抗氧化剂等,这些杂质在运用本方法的处理、分析条件时,都没有对山梨糖醇的检测产生干扰,结果见图4。
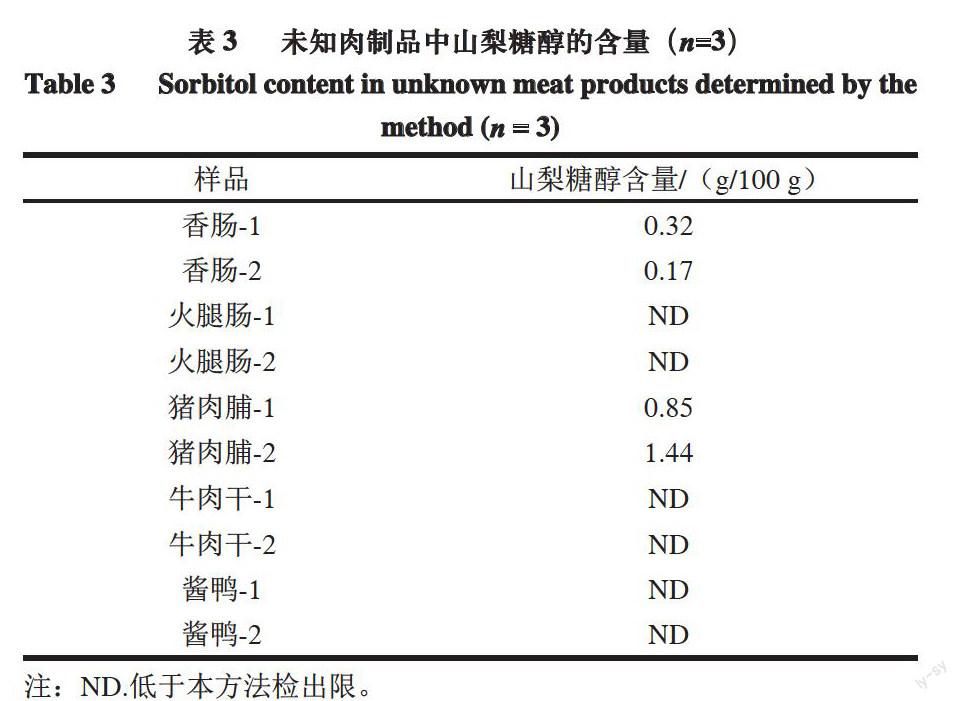
2.3 未知肉制品中山梨糖醇含量的测定
利用本方法对南京各大超市销售的10 批次肉制品(包括香肠制品、火腿肠、猪肉脯、牛肉干、酱卤肉等)进行检测,检测结果见表3。经检测,所检样品中有4 批次产品检出山梨糖醇。
3 结 论
采用高效液相色谱法氨基柱分离、蒸发光散射检测器检测肉制品中的山梨糖醇。结果表明,本方法可以基本排除肉制品中常见添加剂的干扰,若检出阳性样品,可根据检出量的大小来判断:含量不高则因添加调味料而带入的可能性较大;含量过高则生产时人为添加的可能性较大。该方法利用70%乙腈-水提取样品,不仅能沉淀蛋白质而且脂肪提取物和溶出杂质较少,有效缩短了前处理时间,提高了回收率,同时针对山梨糖醇优化了ELSD参数,使得此方法具有前处理简便、检出限低、重现性好、针对性强的特点,可以准确、高效地测定肉制品中的山梨糖醇的含量。
参考文献:
[1] 袁长富, 李仲良, 卢春山, 等. 山梨醇制备及转化催化剂研究进展[J]. 化工生产与技术, 2007, 14(1): 34-37.
[2] 秦树春, 岳大永. 催化剂在山梨醇生产中的应用[J]. 淀粉与淀粉糖, 2007(1): 29-32.
[3] 杨仲春. 山梨醇的国内外产需状况及其应用[J]. 甲醇与甲醛, 2003(6): 18-25.
[4] 王淑霞, 王英秋. 山梨醇的应用及国内市场浅析[J]. 化工设计, 1994(6): 9-12.
[5] 闫晓蕾. 山梨糖醇在香肠制品中的持水作用研究[D]. 无锡: 江南大学, 2012.
[6] 李黎, 刘玉峰. 高效液相色谱法测定食品中的糖醇[J]. 食品科学, 2007, 28(6): 278-280.
[7] 甘宾宾, 马彦, 叶志云. 反相高效液相色谱法测定山梨醇和甘露醇[J]. 化学世界, 1999(2): 99-102.
[8] 于珍, 闫正, 蔡立鹏, 等. 高效液相色谱法-蒸发光散射法测定无糖糕点饼中糖醇含量[J]. 食品工业科技, 2010, 31(3): 362-364.
[9] 马立田, 王式箴. 高效液相色谱法测定低热量食品中的葡萄糖、果糖、蔗糖、麦芽糖和山梨糖醇的研究[J]. 食品与发酵工业, 1990, 24(4):12-17.
[10] 徐绣珠, 徐根良. 糖和糖醇高效液相色谱分析[J]. 分析化学, 1999, 27(5): 547-550.
[11] 辛梅华, 徐金瑞, 方柏山, 等. 蔗糖水解液及发酵液中糖及糖醇的高效液相色谱分析[J]. 分析测试学报, 1997, 16(6): 44-46.
[12] 李传慧, 李淑娟, 安娟, 等. HPLC/MS/MS法同时测定食品中5 种天然甜味剂[J]. 中国医药指南, 2008(19): 161-163.
[13] 马书民, 王明泰, 韩大川, 等. 液相色谱串联质谱法测定食品中甘露糖醇、麦芽糖、木糖醇、山梨糖醇[J]. 中国食品添加剂, 2012(5): 206-210.
[14] LOOS R, GAWLIKBM, BOETTCHERK, etal.Sucralosescreeningin European surface waters using a solid phase extraction liquidchromatography-triple quadrupole mass spectrometry method[J].Journal of Chromatography A, 2009, 1216(7):1126-1130.
[15] 高国琰, 董责章. 气相色谱法尿半乳糖醇及其他糖醇的测定[J]. 中国医科大学学报, 1995, 24(3): 247-249.
[16] 陈晨, 朱建良, 欧阳平凯. 稀水溶液中糖和糖醇的气相色谱分析[J]. 南京化工大学学报, 1997, 19(2): 79-83.
[17] 刘敬兰, 陈连文. 衍生化毛细管GC法分离山梨醇及甘露醇[J]. 分析化学简报, 2001, 29(10): 1185-1187.
[18] 王静, 王晴, 向文胜, 等. 色谱法在糖类化合物分析中的应用[J]. 分析化学, 2001, 29(2): 222-227.
[19] 周洪斌, 熊治渝, 余杨, 等. 醋酸酐衍生-气相色谱-质谱联用测定葡萄酒中的糖醇[J]. 色谱, 2013, 31(11): 1093-1101.
[20] 周洪斌, 熊治渝, 李平, 等. 离子色谱-质谱联用法检测食品中的糖醇[J]. 色谱, 2013, 31(8): 786-790.
[21] 唐坤甜, 林立, 梁麗娜, 等. 无糖和低糖食品中的糖和糖醇同时分析的阴离子交换色谱-脉冲安培检测法研究[J]. 食品科学, 2008, 29(6): 327-331.

