乳清蛋白抗菌薄膜中山梨酸钾的扩散性研究
张玉亭,雷 桥,,*,包建强,潘家祯,黄志英
(1.上海海洋大学食品学院,上海 201306;2.华东理工大学机械与动力工程学院,上海 200237)
乳清蛋白抗菌薄膜中山梨酸钾的扩散性研究
张玉亭1,雷 桥1,2,*,包建强1,潘家祯2,黄志英1
(1.上海海洋大学食品学院,上海 201306;2.华东理工大学机械与动力工程学院,上海 200237)
将山梨酸钾添加至乳清分离蛋白成膜液中制成抗菌包装薄膜,通过扩散实验并结合菲克扩散理论,研究了在不同浓度、温度、pH条件下抗菌蛋白薄膜中山梨酸钾的扩散行为。根据幂律模型的扩散指数,发现pH3.8时山梨酸钾的初期释放动力学属于非菲克扩散,而在其他条件下基本符合菲克第一扩散定律。扩散系数研究表明:抗菌膜中山梨酸钾浓度增加,温度升高,pH降低,扩散系数呈非线性增大;模拟液pH3.8时,由于薄膜溶胀性较大,山梨酸钾的扩散系数在35℃条件下高达5.722×10-12m2/s;通过阿伦尼乌斯公式中活化能比较,发现山梨酸钾的扩散系数在pH为3.8的模拟液中最易受温度影响。
山梨酸钾,乳清蛋白膜,溶胀,菲克定律,扩散性
山梨酸钾作为一种已产业化生产的常用食品防腐剂,可以有效控制食品中霉菌,酵母菌和好氧性细菌的活性,且安全系数高,它可以被人体的代谢系统吸收而迅速分解为二氧化碳和水,在体内无残留,故已成为世界上最主要的防腐剂。目前,食品级山梨酸钾通常直接添加在各类食品中用来保鲜防腐,随着活性包装的发展,将山梨酸钾等抗菌剂加入食品包装中做成抗菌包装材料开始受到人们的广泛关注。天然可食性蛋白薄膜材料既可以保护食品免受机械损伤,又可以作为抗菌剂良好的释放载体,减缓抗菌剂与食品内部的反应,延长食品的保质期,为食品的保鲜和抑菌提供新的方向和思路。
抗菌蛋白薄膜中山梨酸钾的扩散性与食品包装对食品的保鲜效果有着密切的关系。对于抗菌蛋白薄膜来说,抗菌剂会在抗菌膜、食品和两者之间的空隙进行迁移分配,最终达到平衡分布。山梨酸钾通过食品与抗菌膜之间的接触面进行迁移吸附而进入食品[1-2]。Cristiana M.P. Yoshida研究发现山梨酸钾在壳聚糖膜和棕榈酸-壳聚糖膜的扩散机制不符合菲克定律,而且扩散系数不会因为脂质的存在而改变[3]。M. Ozdemir 研究了山梨酸钾在可食性乳清分离蛋白膜中的扩散机制,研究表明其扩散指数介于0.55到0.86之间,扩散模型为不规则的非菲克扩散[4]。J.H. Choi等研究了溶液pH和温度对卡拉胶抗菌膜中山梨酸钾扩散性的影响,结果表明所测范围溶液的pH对山梨酸钾扩散性无明显影响;当pH5.2,温度从40℃降至5℃时,扩散系数从4.23×10-13m2/s降至1.29×10-13m2/s[5]。然而,国内对抗菌蛋白薄膜的抗菌剂迁移研究较少。
本文选用山梨酸钾作为抗菌剂,以乳清分离蛋白和酪蛋白酸钠为成膜基材,探讨温度、模拟液pH及抗菌剂含量对山梨酸钾扩散性的影响,确定乳清分离蛋白-酪蛋白酸钠复合抗菌膜中山梨酸钾的扩散系数和扩散指数,为抗菌膜中抗菌剂的扩散性研究提供数据参考。
1 材料与方法
1.1 材料与仪器
乳清分离蛋白(Hilmar,美国,蛋白>92.0%,脂肪<1.8%,乳糖<1.0%,灰分<3.5%),酪蛋白酸钠(MG,澳大利亚,99.21%蛋白),甘油,山梨酸钾,磷酸二氢钾,磷酸氢二钾,盐酸,氢氧化钾(国药试剂集团,中国,分析纯)。
WFZ UV-2系列紫外分光光度计 北京普析通用;DF-101S集热式恒温加热磁力搅拌器 河南省巩义市科瑞仪器有限公司;雷磁pH S-3C pH计 上海精密科学仪器有限公司;SHB-ⅢA循环水式多用真空泵 郑州长城科工贸有限公司;0~25mm电子数显螺旋测微仪 桂林广陆数字测控有限责任公司;GDS-100L恒温恒湿箱 索亚特实验设备有限公司;GX-ZGF101恒温鼓风干燥箱 上海贺德实验设备有限公司;YP202N电子天平 上海精密科学仪器有限公司。
1.2 抗菌蛋白薄膜的制备
参照文献[6-7]中乳清蛋白-酪蛋白酸钠复合薄膜制备方法,制备含量为0.150%、0.375%、0.750%(w/v)的山梨酸钾抗菌复合蛋白薄膜。
1.3 模拟液的配制
本文选用不同pH的磷酸盐缓冲溶液[5](3.8,5.2,7.0分别代表酵母菌、霉菌、细菌比较容易生长的pH)来模拟抗菌蛋白薄膜中山梨酸钾在pH不同的食品中的扩散性。0.2mol/L的磷酸缓冲液由磷酸二氢钾和磷酸氢二钾配制而成,pH用雷磁pH S-3C pH计通过0.1mol/L的盐酸或氢氧化钾调节。
1.4 薄膜溶胀率的测定
为了研究膜的溶胀与扩散性之间的关系,将膜裁成2cm×2cm的膜放在不同条件下的磷酸缓冲液中,每隔一段时间将膜取出用滤纸除去表面多余液体,用天平称重后再放回[8]。薄膜的溶胀率由式(1)计算:
SR=(Wt-W0)/W0
式(1)
式中:SR为膜的溶胀率;W0为膜初始质量;Wt为溶胀过程中不同时刻薄膜的质量。
1.5 扩散迁移实验
将山梨酸钾含量为0.150%、0.375%、0.750%(w/v)的抗菌膜分别裁成2cm×2cm大小(大约0.2g),采用电子数显螺旋测微仪选取5个点测量膜的厚度,并取平均值。按照表1所示,将裁好的膜片分别置于100mL pH为3.8、5.2、7.0的磷酸缓冲液中,置于15、25、35℃不同温度环境下,每隔2min吸取3mL模拟液,紫外分光光度法254nm处测山梨酸钾吸光值,直至各组均达到平衡为止[9-10]。
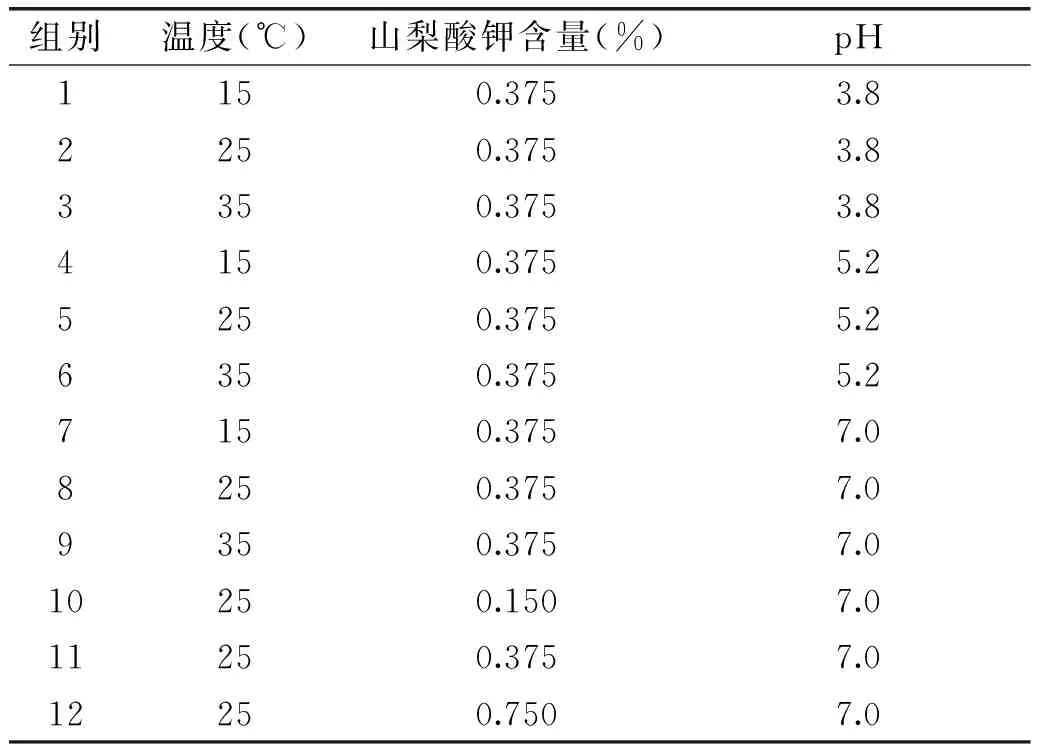
表1 实验分组表Table 1 The experimental group table
2 结果与讨论
2.1 薄膜的溶胀性比较
由图1可知,在模拟液pH为3.8的条件下,所测温度范围内,抗菌膜均表现为有明显的溶胀行为,初始阶段溶胀很快,之后缓慢增加,最后达到平衡,且环境温度越高膜的溶胀率越高。由图2可知,环境温度同为25℃条件下,模拟液pH为3.8时,抗菌膜有明显的溶胀行为,在pH5.2和pH7.0时,抗菌膜溶胀率几乎没有明显变化。由图1、图2可知,pH对乳清蛋白膜的溶胀率影响作用显著,这可能是由于pH较低时,膜的网络结构中氨基质子化,静电斥力和亲水性增加,导致膜结构疏松,孔道变大,故溶胀率变大。

图1 不同温度条件下乳清分离蛋白/山梨酸钾抗菌膜的溶胀率变化(C=0.375%,pH3.8)Fig.1 Swelling behavior of WPI/potassium sorbate films at different temperature(concentration 0.375%,pH3.8)

图2 不同pH下乳清分离蛋白/山梨酸钾抗菌膜的溶胀率变化(C=0.375%,T=25℃)Fig.2 Swelling behavior of WPI/potassium sorbate films at different pH(concentration 0.375%,T=25℃)
2.2 不同薄膜在不同条件下的迁移扩散比率变化

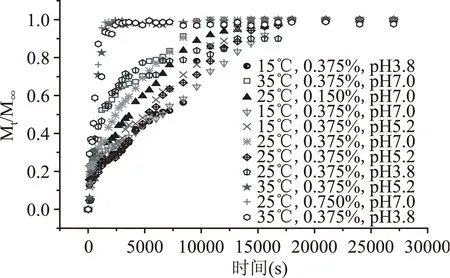
图3 不同条件下山梨酸钾的扩散比率随时间的变化Fig.3 Potassium sorbate diffusion in the different condition
2.3 山梨酸钾释放动力学
根据Fick定律,山梨酸钾的扩散模型可用式(2)二阶偏微分方程来表示[11]:
式(2)
式中:C为山梨酸钾在乳清分离-酪蛋白酸钠膜中的浓度,D(t)为与时间有关的山梨酸钾的扩散系数,X为扩散距离,t为浸泡时间。根据Crank的理论[11],山梨酸钾抗菌薄膜的释放动力学可用式(3)表示:
式中:Mt为t时刻山梨酸钾释放质量,M∞为山梨酸钾的最终释放质量,L为膜的厚度。
短时间内,当Mt/M∞<2/3时,上述方程可用式(4)表示[12-13]:
式(4)
通过求取Mt/M∞对t1/2的斜率,可获得抗菌膜的扩散系数。
式(5)
式中:slope为Mt/M∞对t1/2的斜率。
经拟合,不同条件下山梨酸钾抗菌膜的扩散系数D(当Mt/M∞<2/3时)如表2所示。由表2可知,山梨酸钾在乳清蛋白-酪蛋白酸钠复合膜中的扩散系数的数量级为10-13,表明该乳清分离蛋白膜作为抗菌载体具有良好的缓释作用。
为确定抗菌蛋白膜中山梨酸钾的迁移机制,将迁移曲线的前面部分(当Mt/M∞<2/3时)代入幂律函数[14],
式(6)
式中:k为描述大分子网络结构特征的常数;n为扩散指数,表示迁移机理。根据不同的扩散指数可分为以下三种情况:n≤0.5时,迁移机理为菲克第一定律;0.5
n值和k值可以通过lnMt/M∞对lnt的斜率和截距获得。不同条件下抗菌膜的扩散指数n和k值结果如表2所示,其中相关系数R2代表lnMt/M∞对lnt的线性相关性。由表2可知,抗菌膜在pH5.2和pH7.0的模拟液中n值均较低,基本介于0~0.5之间,迁移机理为菲克第一定律,这与图2中抗菌膜在pH5.2和7.0时无明显溶胀性的结论相符。抗菌膜在pH3.8模拟液中n值较高,介于0.5~1之间,属于非菲克扩散行为,这与抗菌膜在此条件下溶胀性比较明显的结果相一致。
2.4 山梨酸钾浓度对薄膜扩散性的影响
由表2可知,山梨酸钾含量分别为0.150%、0.375%、0.750%(w/v)三种抗菌膜在温度25℃和pH7.0条件下初期扩散系数分别为3.733E-13,4.478E-13、19.420E-13m2/s。高浓度的山梨酸钾抗菌膜,其初期扩散系数最高。这可能是因为山梨酸钾是亲水的,高浓度山梨酸钾抗菌膜可以吸收更多的水,而水作为塑化剂,它能促进膜中山梨酸钾的释放。这种作用类似于乙酸、丙酸从壳聚糖膜的释放。
2.5 温度对扩散系数的影响
由表2中扩散系数D可知,在所有的模拟液中,温度明显影响着山梨酸钾的释放速率,随着温度的升高,薄膜在不同模拟液中山梨酸钾扩散系数也增加。
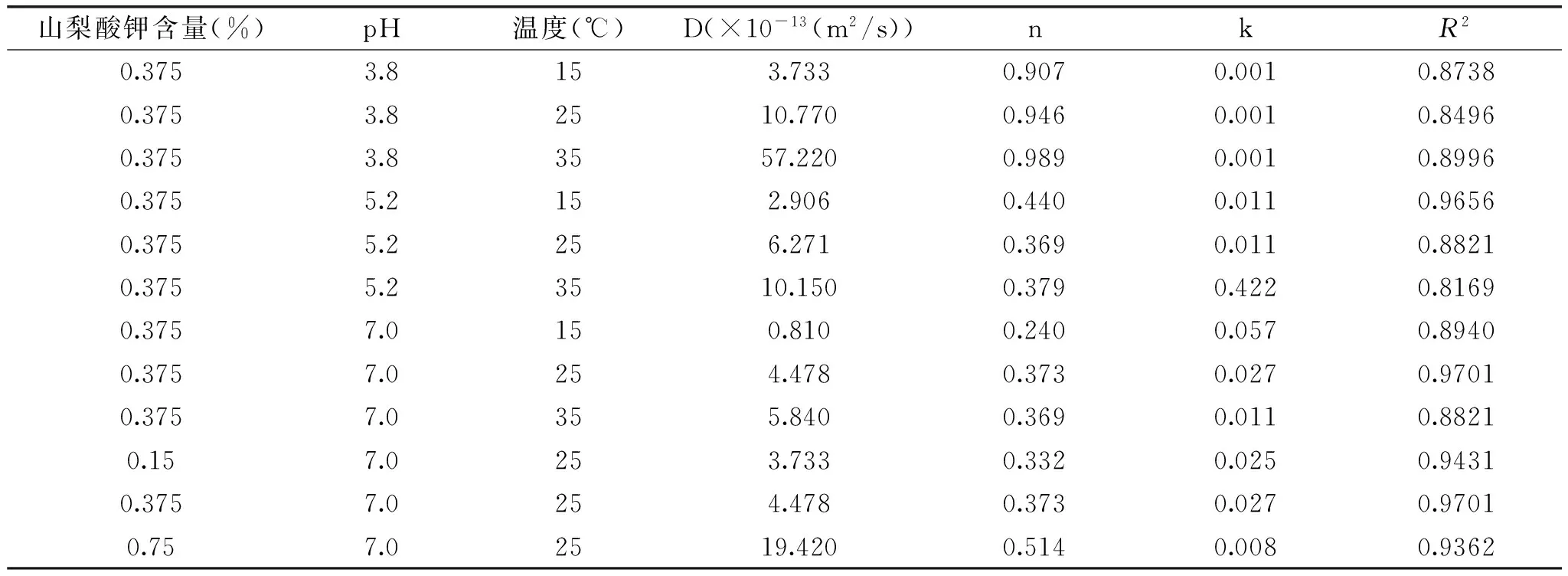
表2 含有不同山梨酸钾的抗菌蛋白薄膜在不同pH溶剂和温度下的扩散指数n,k值及扩散系数DTable 2 Diffusion exponent(n),constant(k)and diffusion coefficient(D)of films containing potassium sorbate in different systems
为了进一步研究抗菌膜中抗菌剂的扩散系数与温度的关系,根据阿伦尼乌斯定律,反应速率常数与温度之间的指数关系可以用式(7)表示:
式(7)
式中:K为反应速率常数,A为常数,Ea为活化能(J/mol),R为通用气体常数(J/(mol·K),T为绝对温度。
阿伦尼乌斯方程可以用来反映化学反应中反应速率和温度变化的关系,而扩散速率可以视为扩散过程中的反应速率,故扩散过程方程也可用式(8)来表示[5]:
式(8)
式中:D为扩散系数,D0为常数,Ea为扩散过程的活化能(J/mol)。
如图4所示,通过阿伦尼乌斯方程可以做lnD对1/T的曲线来计算扩散过程的活化能[16]。活化能Ea用于描述扩散过程对温度变化的敏感性。由式(8)和图5可求得,抗菌膜在pH3.8,pH5.2,pH7.0的食品模拟液中的活化能分别为46.25,73.47,100.44kJ。结果表明山梨酸钾在pH为3.8的磷酸缓冲液的扩散系数最容易受温度影响。这可能是pH3.8时,薄膜内部蛋白质空间结构变得疏松,扩散加快,活化能越低,扩散速率越大。
2.6 pH对薄膜扩散系数的影响
由图5可以看出,山梨酸钾在pH3.8,5.2,7.0的模拟液中其扩散系数随pH降低而升高。pH明显影响了其扩散过程,这与薄膜的溶胀有关,正如图1和图2所示,在pH3.8时,薄膜的溶胀性高,膜易分解,导致了高的迁移率。
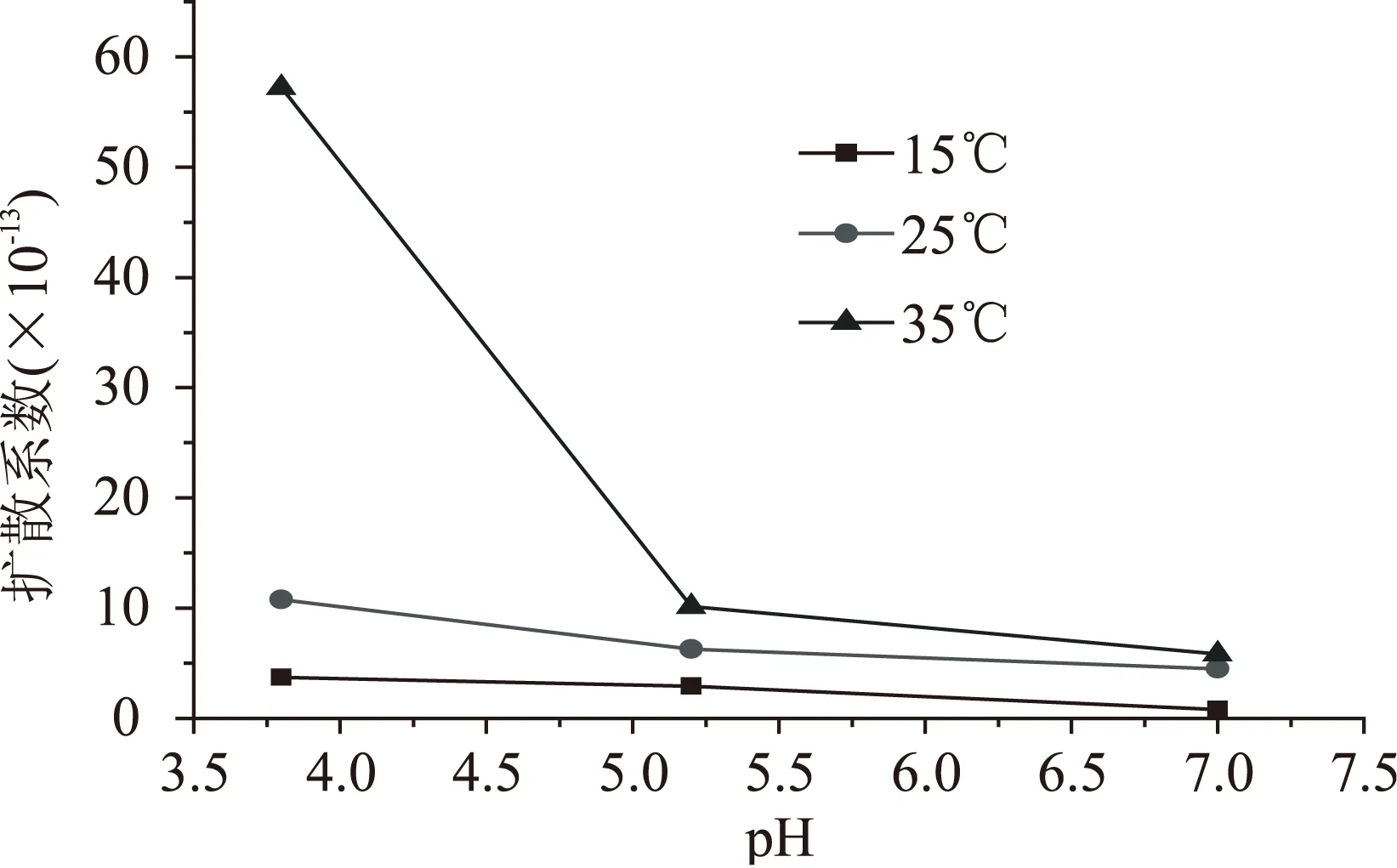
图5 山梨酸钾抗菌膜在pH7.0,5.2,3.8食品模拟液中的扩散系数变化Fig.5 Changes of diffusion coefficient(D) of potassium sorbate in the different pH
3 结论
温度、薄膜中山梨酸钾的浓度、食品模拟液pH是山梨酸钾向食品中迁移扩散的重要影响因素。乳清分离蛋白-酪蛋白复合膜中山梨酸钾初期扩散速率随温度和山梨酸钾初始浓度增加而增加,随pH增加而降低。乳清分离蛋白复合膜作为抗菌载体,其扩散系数为10-13数量级,表示其具有良好的抗菌剂缓释效果。
包装不同的食品,对薄膜中抗菌剂扩散系数的要求不同,保质期短且易感染微生物的产品,在储存过程中需要保持较好的抗菌环境,所以扩散系数以大为好,反之,较小的扩散系数则可以延长抗菌剂释放时间。因为每种食品都有一个内在pH,而且储藏温度因食品种类不同而不同,为了延长食品货架期,要根据情况调整薄膜中山梨酸钾的浓度和薄膜的面积,并且要注意储存条件。
[1]王利娜,冷小京.可食性抗菌膜的研究进展[J].食品科技,2011,36(10):97-101.
[2]赵利,王素雅,谢俊杰.食品抗菌包装技术研究进展[J].食品工业科技,2001,22(5):78-80.
[3]Yoshida C M P,Bastos C E N,Franco T T. Modeling of potassium sorbate diffusion through chitosan films[J]. LWT-Food Science and Technology,2010,43(4):584-589.
[4]Ozdemir M,Floros J D. Analysis and modeling of potassium sorbate diffusion through edible whey protein films[J]. Journal of Food Engineering,2001,47(2):149-155.
[5]Choi J H,Choi W Y,Cha D S,et al. Diffusivity of potassium sorbate in κ-carrageenan based antimicrobial film[J]. LWT-Food Science and Technology,2005,38(4):417-423.
[6]黄志英,雷桥,包建强,等.抗菌蛋白膜的包装性能及抑菌性能研究[J].食品工业科技,2014,35(6):288-291.
[7]陈桂云,雷桥.海藻酸钠对可食性复合膜性能的影响研究[J].食品工业科技,2011,32(12):400-403
[8]Sangsuwan J,Rattanapanone N,Auras R A,et al. Factors affecting migration of vanillin from chitosan/methyl cellulose films[J]. Journal of food science,2009,74(7):C549-C555.
[9]Sfirakis A,Rogers C E. Effects of sorption modes on the transport and physical properties of nylon 6[J]. Polymer Engineering & Science,1980,20(4):294-299.
[10]Mohney S M,Hernandez. Permeability and solubility of D-limonene vapor in cereal package liners[J]. Journal of Food Science,1988,53(1),253-257.
[11]Crank J. The mathematics of diffusion[M]. Oxford,UK:Oxford University Press.1975:47-53.
[12]Franssen L R,Rumsey T R,Krochta J M. Whey protein film composition effects on potassium sorbate and natamycin diffusion[J]. Journal of Food Science,2004,69(5):C347-C350.
[13]王志伟,孙彬青,刘志刚.包装材料化学物迁移研究[J].包装工程,2004,25(5):1-4.
[14]卢鹏,王志耕,梅林,等.壳聚糖抗菌膜中山梨酸钾迁移的数学模型及实验分析[J].食品工业科技,2012(2):112-114.
[15]Bichara A,Fugit J L,Taverdet J L. Modeling of mass transfers between food simulants and treated plasticized PVC[J]. Journal of Applied Polymer Science,1999,72(1):49-58.
[16]Redl A,Gontard N,Guilbert S. Determination of sorbic acid diffusivity in edible wheat gluten and lipid film[J]. Journal of Food Science,1996,61:116-120.
Diffusivity of potassium sorbate inantimicrobial films of whey protein isolate
ZHANG Yu-ting1,LEI Qiao1,2,*,BAO Jian-qiang1,PAN Jia-zhen2,HUANG Zhi-ying1
(1.College of Food Science and Technology,Shanghai Ocean University,Shanghai 201306,China;2.School of Mechanical and Power Engineering,East China University of Science and Technology,Shanghai 200237,China)
The effect of concentration of potassium sorbate,solution pH and temperature on diffusion of potassium sorbate of whey protein composite films were investigated by the measured value and calculated value with Fickian diffusion model. The kinetics of potassium sorbate release followed non-Fickian diffusion(pH 3.8)and Fick’s first law of diffusion as shown by diffusional exponent of power function model. Diffusion coefficient was found to be increased with increased concentration of potassium sorbate and temperature in the range of values tested,but decreased with pH due to swelling behavior in low pH condition. When pH was 3.8 and at 35℃,diffusion coefficient of antibacterial films was up to 5.722×10-12m2/s. According to activation energy(Ea)of the Arrhenius activation energy model,when pH was 3.8,the diffusivity to temperature changes was more sensitive.
potassium sorbate;whey protein isolate;swelling behavior;Fick’s law;diffusivity
2014-11-13
张玉亭(1990-),女,硕士,研究方向:食品工程与包装技术。
*通讯作者:雷桥(1970-),女,博士,副教授,研究方向:食品工程与包装技术。
上海高校知识服务平台上海海洋大学水产动物遗传育种中心(ZF1206)。
TS205.9
A
1002-0306(2015)13-0262-05
10.13386/j.issn1002-0306.2015.13.047

