1-苯基-1′H-螺[吲哚-3,2′-喹唑啉]-2,4′(H)-二酮及其衍生物抗炎活性及分子对接研究
张 金, 王良鹏, 赵佳文, 刘 佳, 任德成, 马养民
(陕西科技大学 化学与化工学院, 陕西 西安 710021)
1-苯基-1′H-螺[吲哚-3,2′-喹唑啉]-2,4′(H)-二酮及其衍生物抗炎活性及分子对接研究
张 金, 王良鹏, 赵佳文, 刘 佳, 任德成, 马养民
(陕西科技大学 化学与化工学院, 陕西 西安 710021)
喹唑啉螺异吲哚二酮及其衍生物是一类重要的含氮螺环化合物,具有良好的抗菌、抗炎等生物活性和药学活性.以本课题组合成的1-苯基-1′H-螺[吲哚-3,2′-喹唑啉]-2,4′(H)-二酮及其衍生物为配体与环氧合抑制酶(COX-2)进行分子对接,从分子层面分析相互作用机理,筛选出高活性的生物功能分子.发现所有的喹唑啉酮衍生物都与COX-2有相互作用,其中3′N上连有苯胺基的喹唑啉螺异吲哚二酮衍生物与COX-2的作用力最强.
喹唑啉螺异吲哚二酮; 分子对接; 抗炎; COX-2
0 引言
炎症是人类疾病中最常见而复杂的病理过程,可以发生于机体的任何部位和任何组织,是机体清除刺激因素、对局部组织损伤进行修复的过程.喹唑啉螺异吲哚二酮类化合物及其衍生物是一类含有喹唑啉酮和螺环吲哚结构的生物功能分子,具有良好生物活性和药学活性,在抗菌[1]、消炎[2]、抗肿瘤[3]、舒张血管[4]、镇痛[5]等方面表现出显著的效果.喹唑啉螺异吲哚二酮类化合物集高活性、芳香性、易修饰性及生物亲和性等特性于一身,通过调控螺环吲哚和喹唑啉酮结构的取代基,使其具有更强的抗菌、抗炎等生理活性[6-8],并采用操作简单,高效环保的方法合成1-苯基-1′H-螺[吲哚-3,2′-喹唑啉]-2,4′(H)-二酮及其衍生物[9].
分子对接方法最初是科学家在分子水平上研究生物体系中的化学问题时提出的.随着计算机技术的发展,分子对接技术也有了很大进步,其在药物设计、药理分析和探测生命体系等方面有较广泛地应用.特别是在酶学研究以及药物设计与筛选中具有十分重要的意义.在药物设计中,分子对接主要用来从小分子数据库中搜寻与受体生物大分子有较好亲和力的小分子,进行药理测试,从中发现新的先导化合物.其优点是小分子配体来自现有的化合物,合成路线成熟;分子对接方法从整体上考虑受体与配体的结合效果,加速先导化合物的发现进程[10-12].
因此,对喹唑啉螺异吲哚二酮这类化合物的分子抗炎机制进行探究,根据分子与环氧合抑制酶 (COX-2)之间的结合效果,筛选出具有优异抗炎活性的生物功能分子.
1 分子对接原理
1.1 定义
分子对接是分子模拟的重要方法之一 ,就是配体与受体通过几何配比和能量配比相互识别形成分子复合物[13],如图1所示.
图1 配体与受体的相互作用
1.2 基本原理
配体与受体的结合是一个十分复杂的过程,涉及到配体和受体的去溶剂化、配体和受体(主要是活性位点处的残基)的构象变化以及配体与受体之间的相互作用.
配体与受体是否能结合以及结合的强弱取决于结合过程中的自由能变化:
△Gbinding=△ Hbinding-T△Sbinding=-RTlnKd
分子对接计算是把配体分子放在受体活性位点的位置,然后按照几何互补、能量互补、化学环境互补的原则来实现评价配体与受体相互作用的好坏,并找到两个分子之间最佳的结合模式.
1.3 分类
分子对接方法根据不同的简化程度可分为以下3类:
(1)刚性对接:研究体系的构型不发生变化;
(2)半柔性对接:研究体系尤其是配体的构象允许在一定范围内变化;
(3)柔性对接:研究体系的构想基本上是可以自由变化的.
1.4 用途
如图2 所示,分别为结构不同的两抗生素TET、SNM 与牛血清白蛋白 (BSA)分子对接的结果[14].图中黑色线条表示氢键,抗生素以球棍模型表示,BSA 以折线模型表示,在图中可清晰看到,抗生素以氢键形式与周围氨基酸残基连接.图中还标明了对应氨基酸残基的名称和准确位置.
通过分子对接确定复合物中两个分子正确的相对位置和取向,研究两个分子的构象,特别是底物构象在形成复合物过程中的变化,是确定酶激动剂、抑制剂作用机制以及药物作用机制,设计新药的基础.
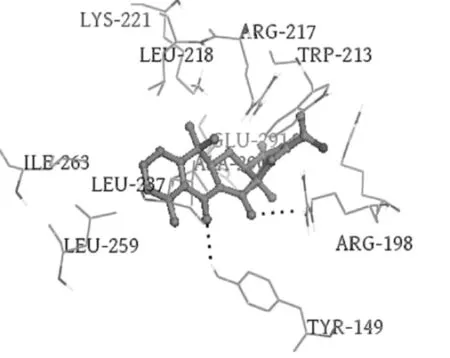
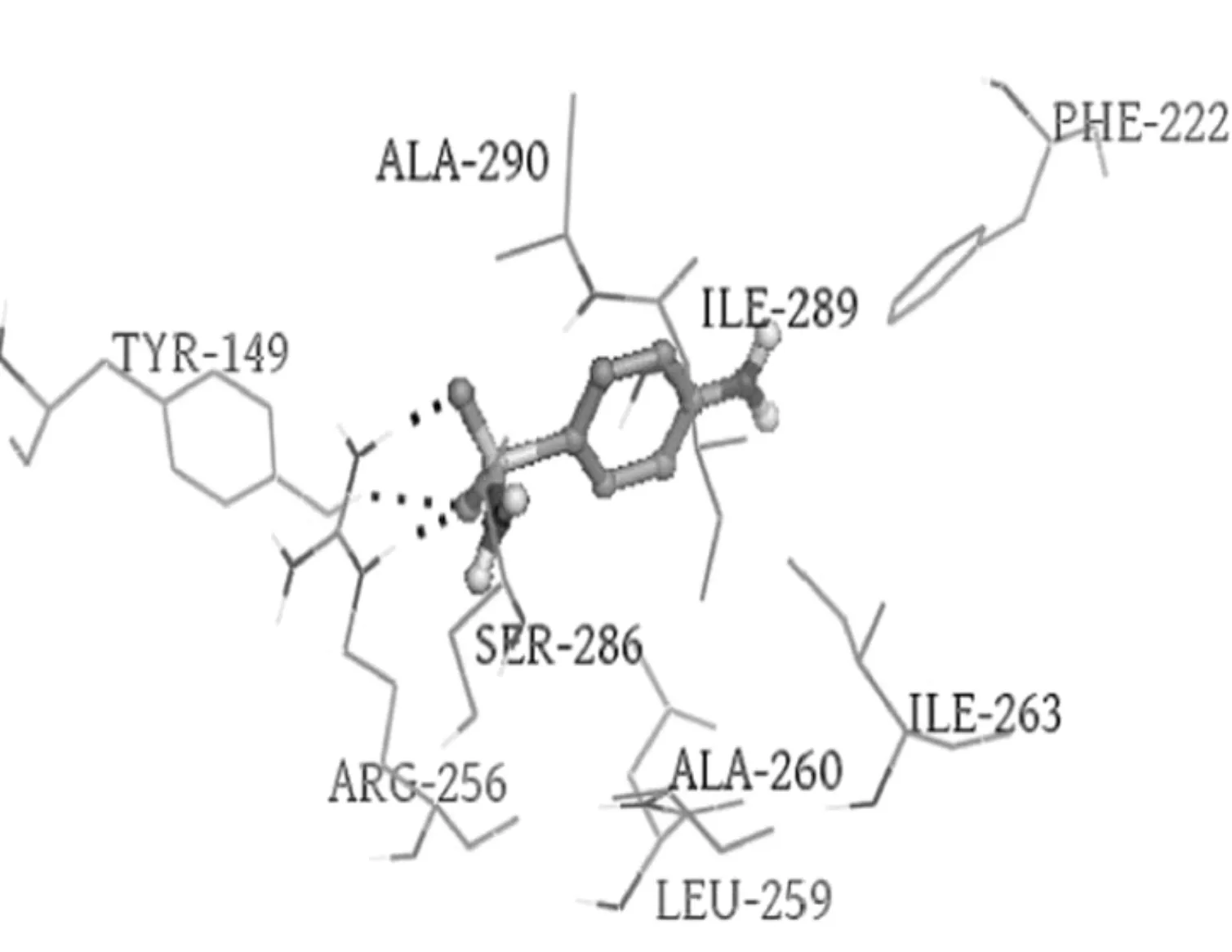
图2 抗生素TET、SNM与牛血清白蛋白 (BSA)分子对接的结果
2 抗炎活性的分子对接
2.1 目的
从已合成的1-苯基-1′H-螺[吲哚-3,2′-喹唑啉]-2,4′(H)-二酮及其衍生物中,选出8 个有代表性的活性功能分子,与COX-2蛋白酶做分子对接计算模拟,从分子层面分析分子与配体的相互作用.
2.2 对接准备
以合成的8个化合物与COX-2蛋白酶做分子对接,探明生物功能分子抗炎作用的机理.COX-2蛋白酶的三维结构从蛋白数据库下载.合成的化合物三维结构用Chem-Bio-Office 2010中的Merk Molecular Force Field 94来进行能量优化,对接软件为AutoDock 4.2,选取的对接活性中心为X:-40.92,Y:44.226,Z:24.276,对接口袋的长宽高各位60 Å,用拉马克基因遗传定律作为计算标准,运算规模和最大评估次数为150和2 500 000次.
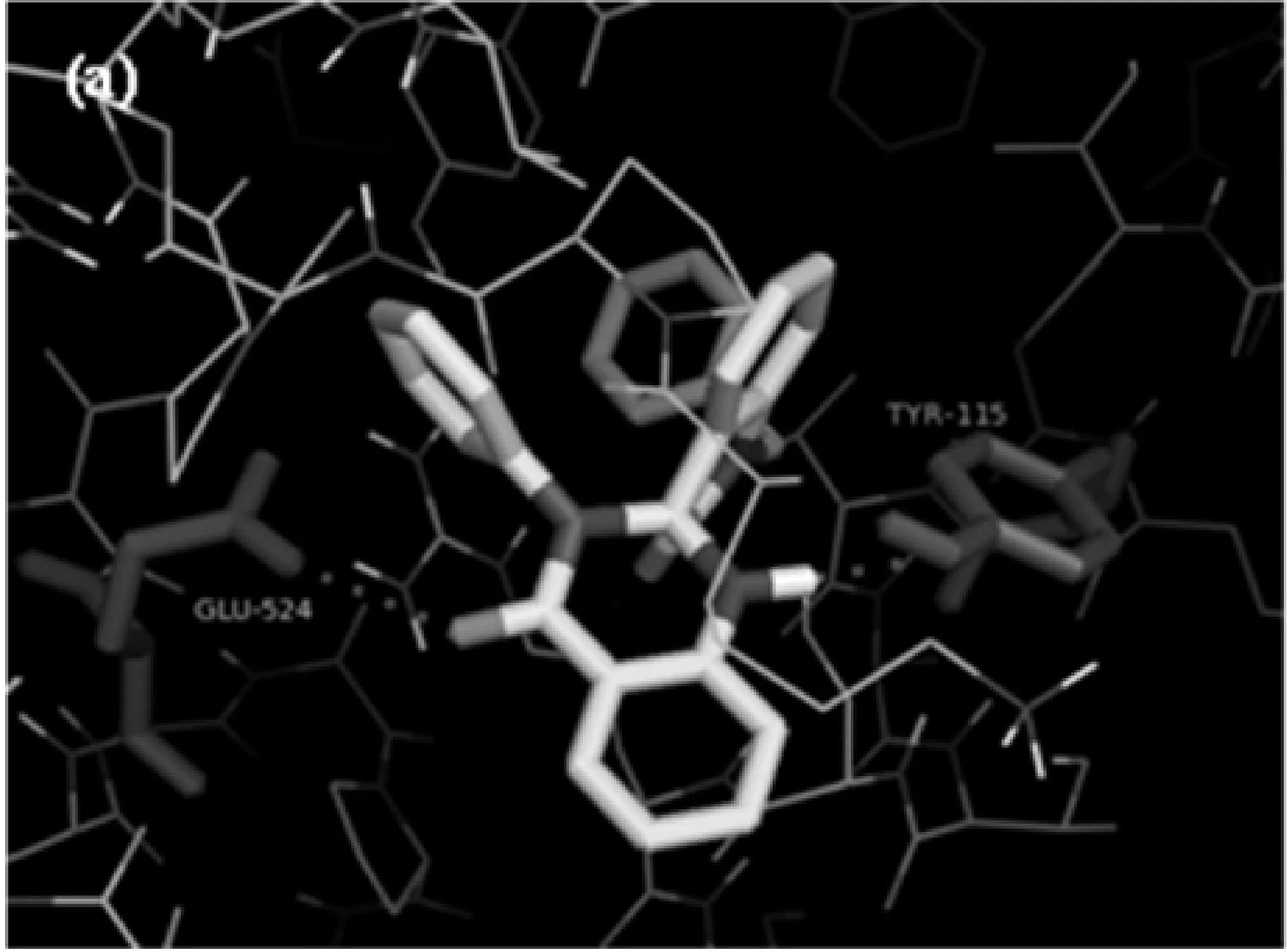
(a)化合物1与COX-2的分子对接示意图
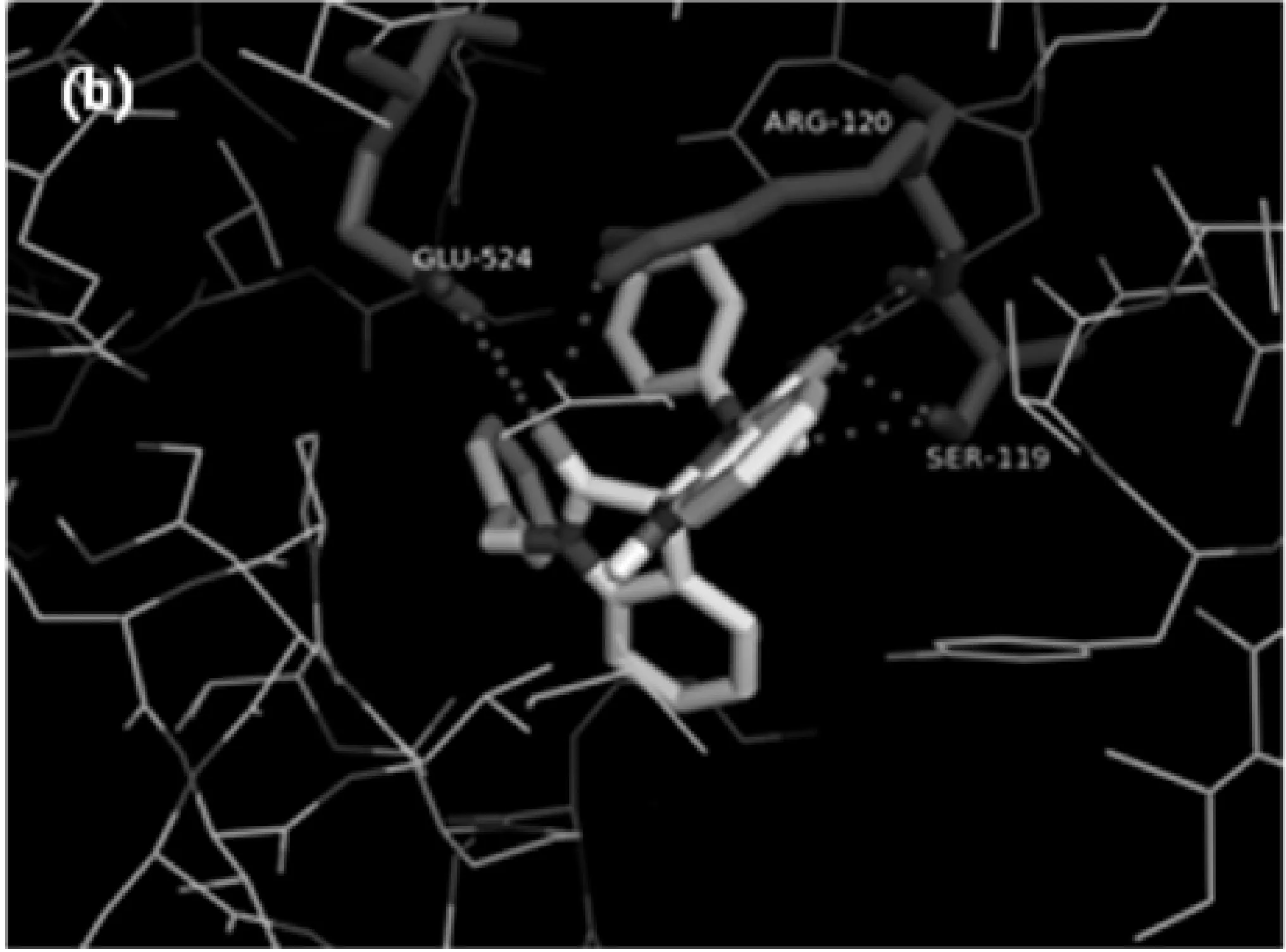
(b)化合物2与COX-2的分子对接示意图
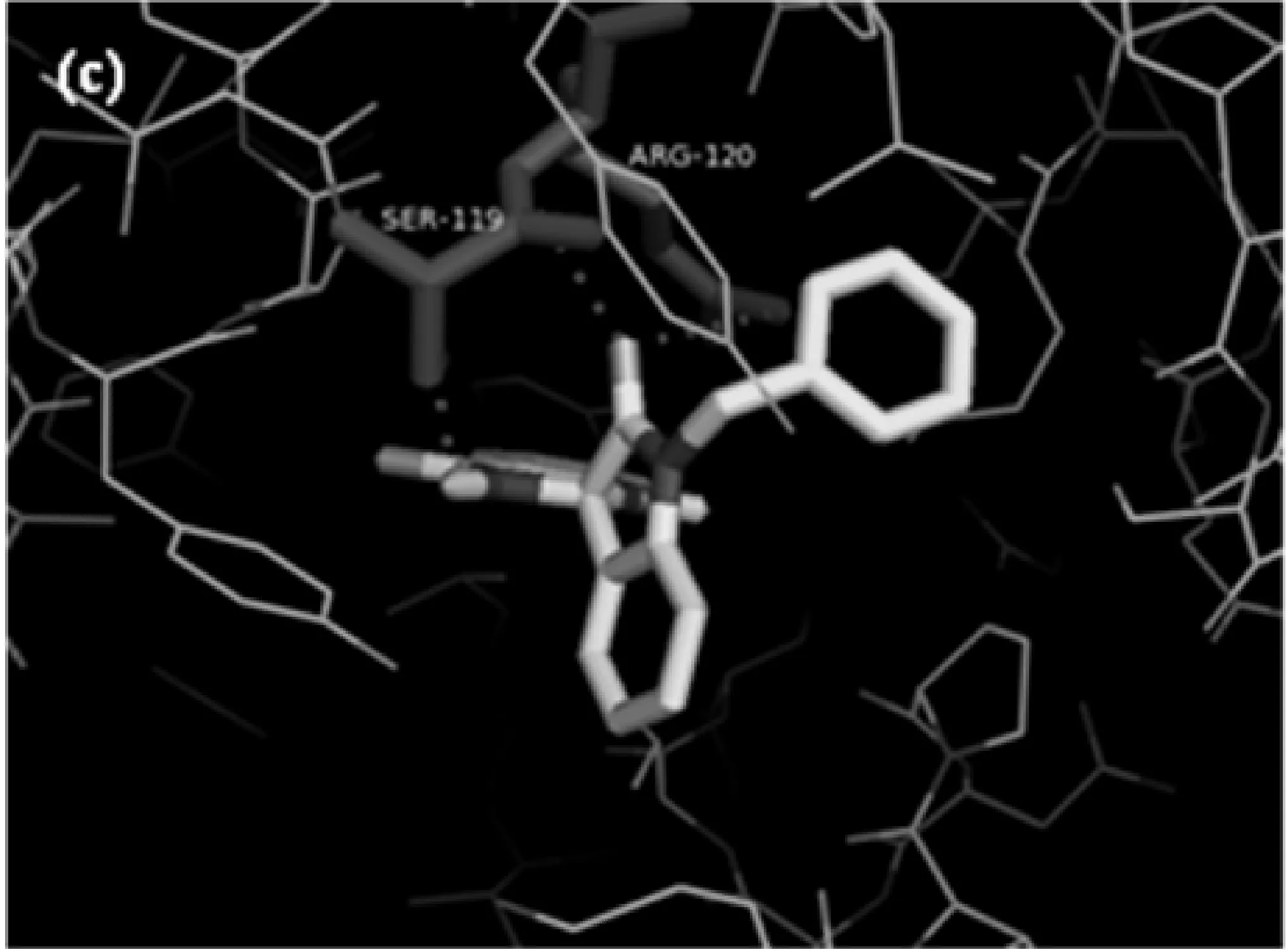
(c)化合物3与COX-2的分子对接示意图
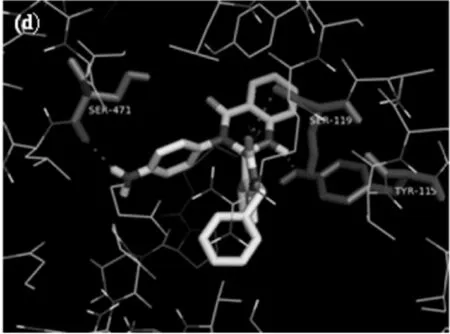
(d)化合物4与COX-2的分子对接示意图
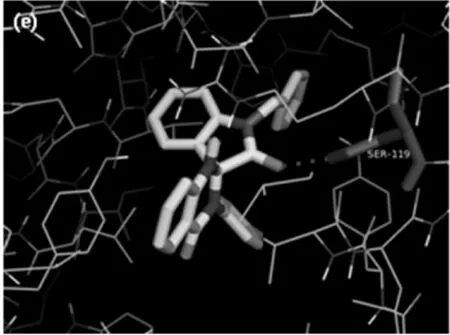
(e)化合物5与COX-2的分子对接示意图
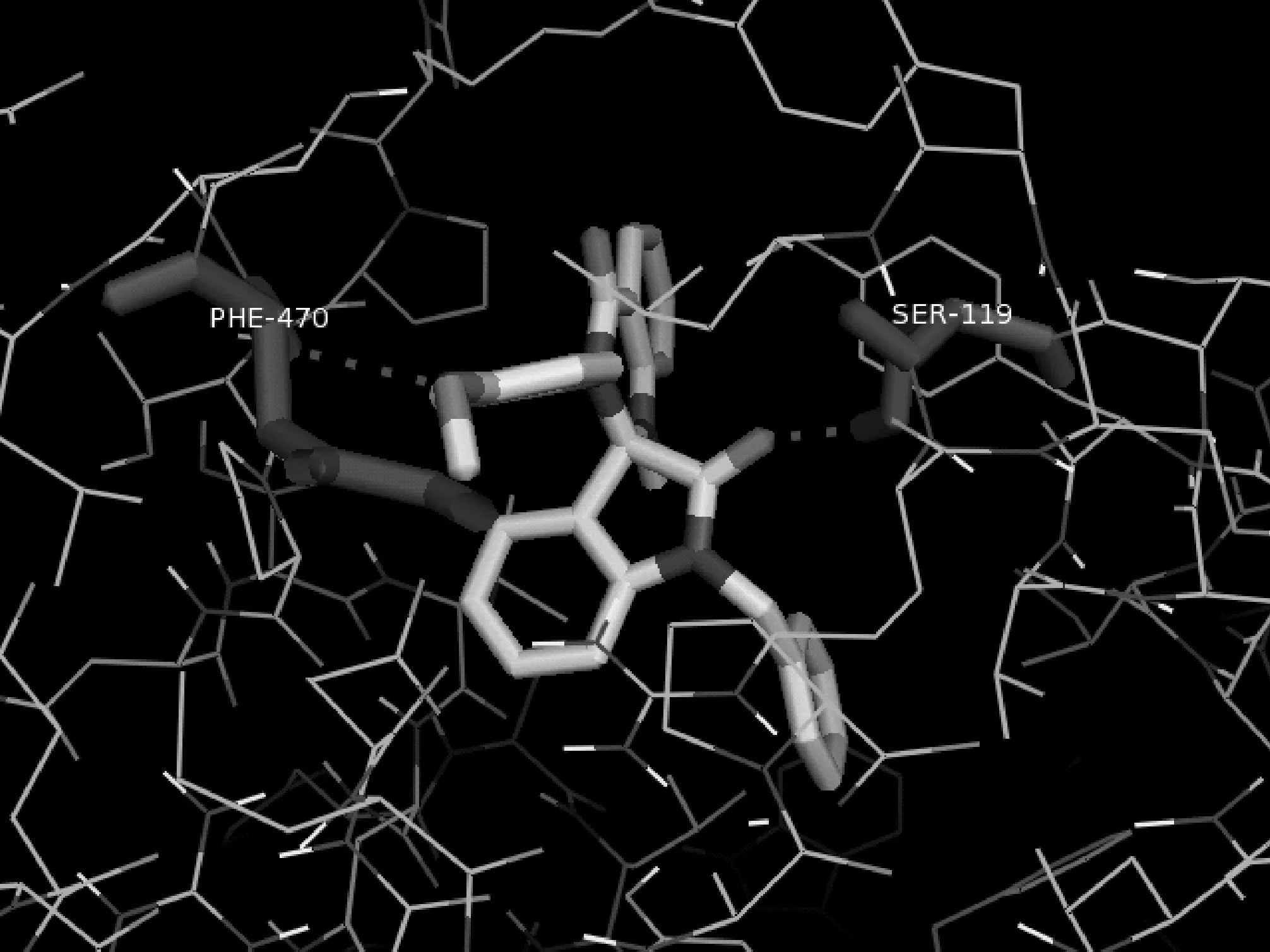
(f)化合物6与COX-2的分子对接示意图
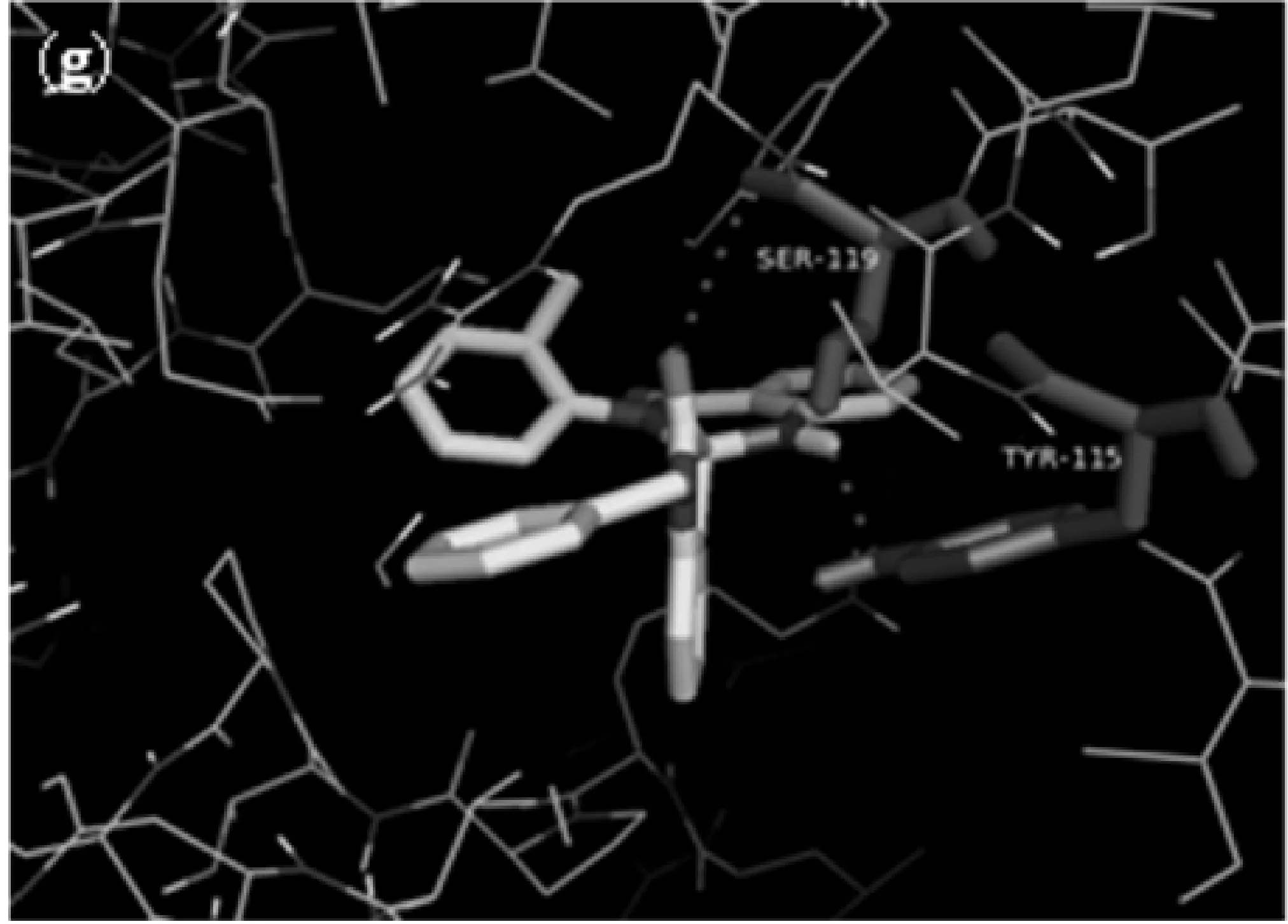
(g)化合物7与COX-2的分子对接示意图
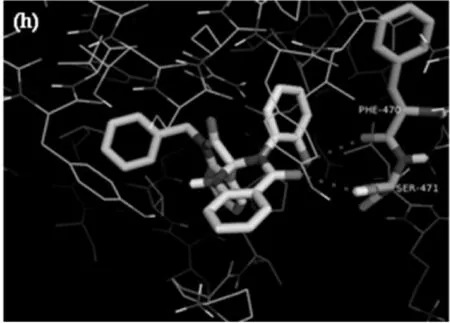
(h)化合物8与COX-2的分子对接示意图
2.3 对接结果与分析
通过8个化合物与COX-2蛋白酶的分子计算模拟,我们发现,这些分子与GLU-524、ARG-120、VAL-89、TYR-115、SER-119等氨基酸残基相互作用.配体小分子通过以氢键与这些氨基酸残基相连与蛋白质大分子紧密结合.具体数据见表1.
化合物1与COX-2蛋白酶对接形成的复合物如图3(a),喹唑啉酮环上的1′NH结构以氢键与TYR-115相连,键长为2.2 Å;羰基碳上的氧原子以键长3.2 Å的氢键与GLU-524相连.
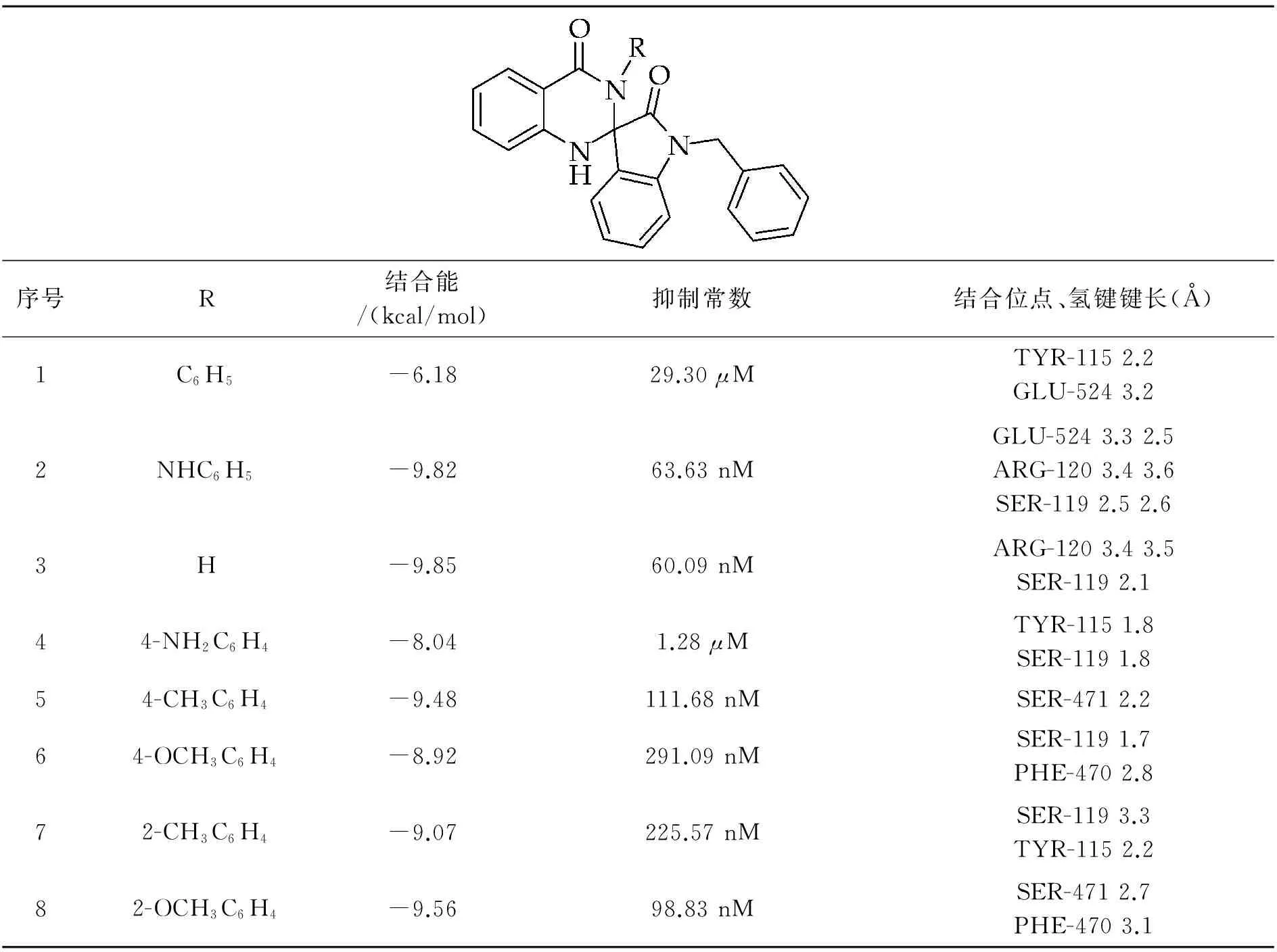
表1 分子对接相关数据
化合物2与COX-2蛋白酶结合较为紧密,其中螺环吲哚结构中羰基氧原子与ARG-120,3′N取代基上NH与SER-119形成两个氢键;吲哚环上羰基氧原子与GLU-514也形成两个氢键,同时还与ARG-120相连,如图3(b).
化合物3是螺环吲哚结构中羰基氧原子与ARG-120相连,形成两个氢键,键长分别为3.4、3.5;3′NH基团以键长2.1 Å的氢键与SER-119相连,如图3(c).
化合物4喹唑啉酮环上的1′NH结构与TYR-115、吲哚环上羰基氧原子与SER-119、氨基与SER-471之间均形成氢键,见图3(d).
化合物5吲哚环上羰基氧原子与SER-119之间形成氢键,如图3(e).
化合物6吲哚环上羰基氧原子与SER-119之间形成氢键,3′N侧链基团上甲氧基上的氧与PHE-470形成氢键,如图3(f).
化合物7吲哚环上羰基氧原子与SER-119之间形成氢键,喹唑啉酮环上的1′NH结构与TYR-115之间形成氢键,如图3(g).
化合物8与COX-2蛋白酶形成的复合物如图3(h),喹唑啉酮环上的羰基碳上的氧原子与SER-471形成氢键,3′N侧链基团上甲氧基上的氧与PHE-470形成氢键.
从以上分子对接结果来看,COX-2蛋白酶活性中心起主要作用的是GLU-524、 SER-119等, VAL-89等氨基酸都是保守的,相互作用的大都是喹唑啉酮和螺环吲哚结构中的氮原子和氧原子与氨基酸之间形成的氢键.其中,化合物2结构中多个氮原子和氧原子,与COX-2蛋白酶结合最为紧密,抗炎效果最佳. 结构相似的化合物抗炎活性也近似,如化合物5、7和化合物6、8,相比较而言,3′N侧链基团上甲氧基要比甲基与蛋白酶结合效果好.因此,含有较多N、O原子的喹唑啉螺异吲哚二酮的化合物对COX-2蛋白酶作用强的可能性较大.
3 结论
以1-苯基-1′H-螺[吲哚-3,2′-喹唑啉]-2,4′(H)-二酮及其衍生物为配体通过与COX-2蛋白酶分子计算模拟,发现化合物2与COX-2的结合最为紧密,抗炎效果较好.并探讨了抗炎药物与蛋白酶的作用机理,明确作用位点,为合成新颖、抗炎作用更强的新型药物提供了理论依据.这种方法的使用,使1-苯基-1′H-螺[吲哚-3,2′-喹唑啉]-2,4′(H)-二酮及其衍生物进入活性化合物组合研究的新层面,不仅对了解药物作用机制有积极的作用,更重要的是,其弥补了传统方法的不足,节省了人力和物力,在药物研究领域建立了全新的研究理念和先进的研究手段.
[1] Alaimo R J,Russell H E.Antibacterial 2,3-dihydro-2-(5-nitro-2-thienyl)-quinazolin-4-(1H)-ones[J].Journal of medicinal chemistry,1972,15(3):335-336.
[2] Hoonur R S,Patil B R,Badiger D S,et al.Transition metal complexes of 3-aryl-2-substituted 1,2-dihydroquinazolin-4(3H)-one derivatives:New class of analgesic and anti-inflammatory agents[J].European Journal of Medicinal Chemistry,2010,45(6):2 277-2 282.
[3] Xia Y,Yang Z Y,Hour M J,et al.Antitumor agents.Part 204:1 synthesis and biological evaluation of substituted 2-aryl quinazolinones[J].Bioorganic & Medicinal Chemistry Letters,2001,11(9):1 193-1 196.
[4] Levin J,Chan P S,Bailey T,et al.The synthesis of 2,3-dihydro-4(1H)-quinazolinone angiotensin II receptor antagonists[J].Bioorganic & Medicinal Chemistry Letters,1994,4(9):1 141-1 146.
[5] Okumura K,Oine T,Yamada Y,et al.4-Oxo-1,2,3,4-tetrahydroquinazolines.I.syntheses and pharmacological properties of 2-methyl-3-aryl-4-oxo-1,2,3,4- tetrahydroquinazolines and their 1-acyl derivatives[J].Journal of Medicinal Chemistry,1968,11(2):348-352.
[6] Helali A Y H,Sarg M T M,Koraa M M S,et al.Utility of 2-methyl-quinazolin-4(3H)-one in the synthesis of heterocyclic compounds with anticancer activity[J].Open Journal of Medicinal Chemistry,2014,4(1):12-37.
[7] Mohammadi A A,Askari S,Rohi H.Design,synthesis and antibacterial evaluation of Same novel 3′-(Phenylamino)-1′H-spiro[indoline-3,2′-quinazoline]-2,4′ -(3′H)-dione derivatives[J].Synthetic Communications,2013,44(4):457-467.
[8] Engen K,Sävmarker J,Rosenström U,et al.Microwave heated flow synthesis of spiro-oxindole dihydroquinazolinone based IRAP inhibitors[J].Organic Process Research & Development,2014,18(11):1 582-1 588.
[9] Mohammadi A A,Dabiri M,Qaraat H.A regioselective three-component reaction for synthesis of novel 1′H-spiro[isoindoline-1,2′-quinazoline]-3,4′(3′H)-dione derivatives[J].Tetrahedron,2009,65(18):3 804-3 808.
[10] Pavan P,Subashini R,Ethiraj K R,et al.Potential anti-bacterial agents:Montmorillonite clay-catalyzed synthesis of novel 2-(3,5-substituted-1H-pyrazol-1-yl)-3- substituted quinolines and their in silico molecular docking studies[J].RSC Advances,2014,101(4):58 011-58 018.
[11] Ashraf Z,Saeed A,Nadeem H.Design, synthesis and docking studies of some novel isocoumarin analogues as antimicrobial agents[J].RSC Advances,2014,96(4):53 842-53 853.
[12] Castro M J,Richmond V,Romero C,et al.Preparation, anticholinesterase activity and molecular docking of new lupine derivatives[J].Bioorganic & Medicinal Chemistry,2014,22(13):3 341-3 350.
[13] 仝建波,钟 黎,赵 翔,等.分子表面随机采样分析用于HIV整合酶抑制剂的QSAR研究[J].计算机与应用化学,2014,31(3):287-292.
[14] Tan X,Song Z.Relationship investigation of molecular structure-binding affinity of antibiotics to bovine serum albumin using flow injection chemiluminescence analysis and molecular docking[J].RSC Advances,2014,4(7):3 263-3 271.
Anti-inflammatory and molecular docking studies of 1-benzyl-1′H-spiro[indoline-3,2′-quinazaline]-2,4′(H)-dione derivatives
ZHANG Jin, WANG Liang-peng, ZHAO Jia-wen,LIU Jia, REN De-cheng, MA Yang-min
(College of Chemistry and Chemical Engineering, Shaanxi University of Science & Technology, Xi′an 710021, China)
Spiroindoline-quinazalinedione and their derivatives are an important class of spirocyclic compounds,and they possess a broad spectrum of biological and pharmaceutical activities,such as anti-bacterial and anti-inflammatory et al.To investigate the antimicrobial data on a structural basis, docking studies of 1-benzyl-1′H-spiro[indoline-3,2′-quinazaline]-2,4′(H)-dione derivatives into the crystal structure of cyclooxygenase-2(COX-2) using the way of molecular docking were performed in order to predict the interactions of the synthesized compounds with COX-2.All of the target compounds exhibited high activities,and the compound with 3′-phenylamino had the highest activity.
spiroindoline-quinazalinedione; molecular docking; anti-inflammatory; cyclooxygenase-2
2015-04-23
陕西省科技厅自然科学基础研究计划项目(2014JQ2064); 陕西省教育厅专项科研计划项目(2013JK0682); 陕西科技大学博士科研启动基金项目(BJ12-26)
张 金(1985-),男,黑龙江北安人,讲师,博士,研究方向:有机合成方法学
1000-5811(2015)03-0094-05
R918
A

