HPLC法测定白背叶中大波斯菊苷含量
谢 巍,蒋受军,2*
(1.广西中医药大学,广西 南宁 530001;2.广西玉林食品药品检验所, 广西 玉林 537000)
HPLC法测定白背叶中大波斯菊苷含量
谢 巍1,蒋受军1,2*
(1.广西中医药大学,广西 南宁 530001;2.广西玉林食品药品检验所, 广西 玉林 537000)
目的:建立高效液相色谱法测定白背叶药材中大波斯菊苷含量的方法。方法:采用Gemini-C18色谱柱(4.6mm×250mm,5μm),以甲醇-0.1%磷酸水溶液(40∶60)为流动相,柱温:25℃,流速:1.0mL·min-1,检测波长:336nm。结果:大波斯菊苷达到基线分离,在0.04486~0.8972μg范围内线性关系良好(r=0.999 3),大波斯菊苷平均加样回收率(n=6)为97.67%(RSD=1.94%)。结论:所建立的含量测定方法操作简单、快速、重复性好,可用于白背叶药材的质量控制。
白背叶;大波斯菊苷;HPLC;含量测定
白背叶为大戟科野桐属植物白背叶(Mallotusapelta(Lour.)Muell. Arg.)的干燥叶,又名野芙蓉、白林树、白面虎等,具有健脾化湿、柔肝活血、收敛固脱、消炎止血等功效。主要用于慢性肝炎、肝脾肿大、脱肛、白带、妊娠水肿、耳炎、外伤出血等[1]疾病。在我国主要分布于河南、广西、海南、陕西、云南等地[2]。王志萍等[3-5]研究表明白背叶有一定的保肝、抗肿瘤、抗菌、止血等药理作用。经查阅有关文献资料, 国内外已有对白背叶中化学成分研究的报道[6-8]。大波斯菊苷具有较强的抑制肿瘤细胞作用[9],提示其可能为白背叶药材所具功效的活性成分。本实验建立了HPLC测定白背叶药材中大波斯菊苷含量的方法,以期为建立全面合理的白背叶药材质量控制标准奠定基础。
1 仪器与试药
UltiMate 3000 高效液相色谱仪(Thermo Scientific);HH-S6数显恒温水浴锅(金坛市医疗仪器厂);AG-204电子分析天平(METTLER TOLEDO);Millipore Simplicity-UV超纯水器(美国密里博)。
白背叶由广西金秀圣堂制药有限公司提供, 经广西食品药品检验所韦家福副主任药师鉴定为大戟科植物白背叶(Mallotusapelta(Lour) Muell-Arg)的干燥叶,标本存放于广西食品药品检验所中药标本室。大波斯菊苷对照品自行从白背叶药材中分离、精制而得, 经MS、H1-NMR和13C-NMR确定结构,HPLC峰面积归一化法测得纯度均大于98% 。
水为超纯水,甲醇、乙腈(美国Fisher公司,色谱纯),其余试剂均为分析纯。
2 方法与结果
2.1 对照品溶液制备
精密称取105℃干燥至恒重的大波斯菊苷22.43mg,置于25mL容量瓶中,加适量70%甲醇水溶液超声使溶解并稀释至刻度,摇匀,制成每1mL含大波斯菊苷0.897 2mg的对照品溶液。
2.2 供试品溶液制备
取白背叶药材粉末(24目)约1.0g,精密称定,精密加入70%甲醇水溶液25mL,称量,加热回流提取1.5h,放冷,用70%甲醇水溶液补足减失的量,滤过,取续滤液经0.45μm微孔滤膜滤过,即得。
2.3 色谱条件
采用Gemini-C18色谱柱(4.6mm×250mm,5μm),以甲醇-0.1%磷酸水溶液(40:60)为流动相,流速为1.0 mL·min-1,检测波长336nm,柱温25℃,进样量10μL。采用外标法计算含量,理论塔板数以大波斯菊苷计算应不低于10 000,分离度为2.21。色谱见图1。
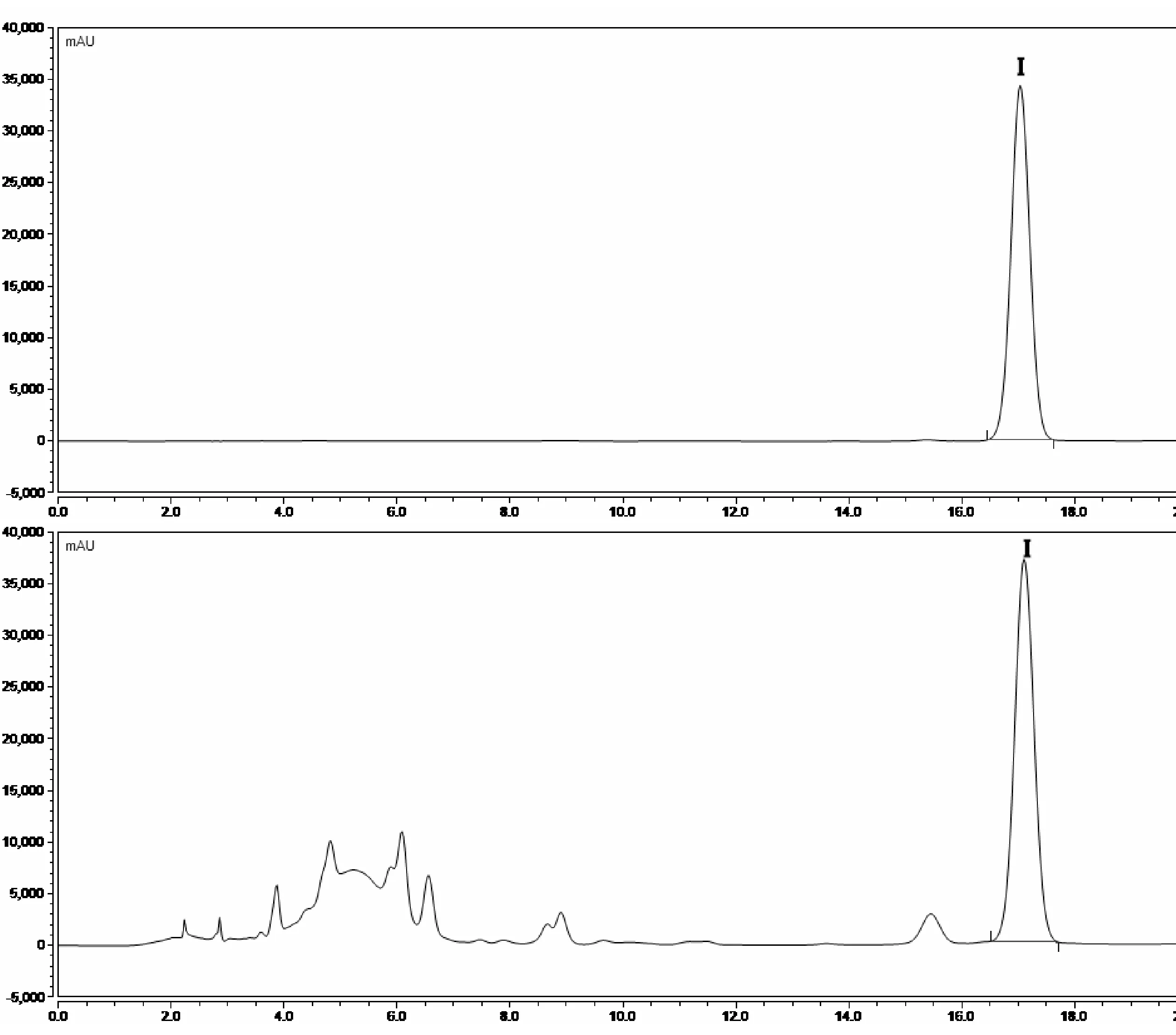
图1 大波斯菊苷对照品(A)和白背叶药材(B)HPLC色谱(I为大波斯菊苷)
2.4 线性关系考察
精密吸取“2.1”项下大波斯菊苷对照品溶液(每1mL中含大波斯菊苷0.897 2mg)0.5、1、2、3、5和10mL,分别置于10mL容量瓶中,用甲醇定容至刻度,摇匀,分别进样10μL,测定峰面积,以大波斯菊苷进样量X(μg)为横坐标,峰面积Y为纵坐标,绘制标准曲线,得回归方程为 Y=1 594.4X-103.75,r=0.999 3,线性范围为0.0448 6~0.897 2μg。
2.5 精密度试验
取白背叶药材粉末(批号011196)约1.0g,精密称定,按“2.2”项下方法制备,进样10μL,连续测定6次,记录峰面积。结果大波斯菊苷峰面积的RSD为0.06%(n=6),表明所用仪器的精密度良好。
2.6 稳定性试验
取同一份白背叶供试品溶液,分别于溶液制备后0、2、4、12、24h进样,测定,记录大波斯菊苷峰面积。结果大波斯菊苷峰面积的RSD分别为0.11%(n=5),表明24h内供试品溶液稳定性良好。
2.7 重复性试验
取同一批白背叶药材粉末6份(批号011196),每份约1.0g,精密称定,按“2.2”项下方法制备,分别进样10μL,记录峰面积,并计算含量。大波斯菊苷的平均含量为24.594 mg/g,RSD为1.46%,表明该方法重现性良好。
2.8 加样回收率试验
精密称定已测定含量(每1g中含大波斯菊苷24.594mg)的白背叶药材粉末6份,每份约0.5g,精密称定,另精密称大波斯菊苷对照品74.55mg置150mL量瓶中,加适量甲醇超声使其溶解,并稀释至刻度,摇匀,即得对照品储备液。分别在上述6份药材中精密加入混合对照品储备液25mL,按“2.2”项下方法制备,分别进样10μL,记录大波斯菊苷的峰面积,计算含量,并计算回收率。结果见表1。

表1 白背叶药材中大波斯菊苷的回收率试验结果 (n=6)
2.9 样品含量测定
取6批不同批号的白背叶药材粉末,每份约1.0g,精密称定,按“2.2”项下方法制备供试品溶液,分别进样10μL测定,记录大波斯菊苷的峰面积,并计算含量。结果见表2。
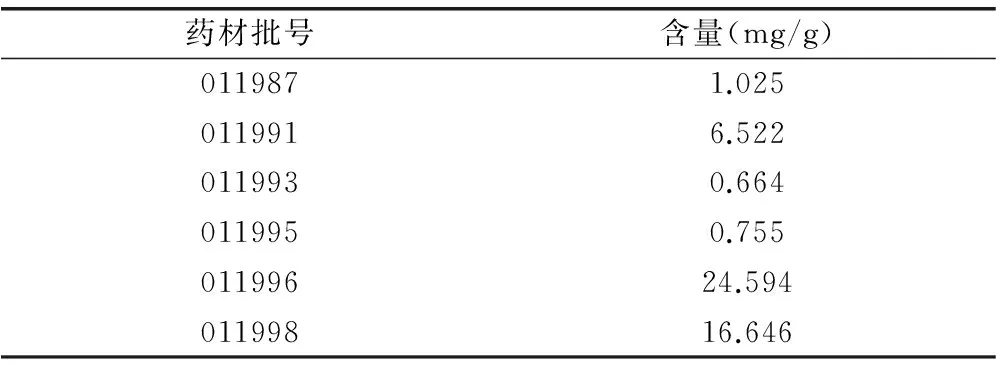
表2 白背叶药材中大波斯菊苷的含量测定结果
3 讨论
3.1 供试品溶液制备方法的选择
本研究优选了不同提取条件制备供试品溶液,考察了不同提取方法(超声提取、回流提取)、提取时间(30、60、90min)、提取溶剂(甲醇、乙醇和70%甲醇水溶液)、溶剂用量(10、25、50mL)和药材粉碎度(10、24、50目)对白背叶药材中大波斯菊苷提取率的影响。结果表明白背叶药材粉末在(24目)1.0g、加70%甲醇25mL、加热回流提取1.5h的条件下,大波斯菊苷提取率最高。
3.2 色谱条件的选择
曾用甲醇∶水(24∶76)梯度洗脱[7],发现大波斯菊苷色谱峰的保留时间较长,经过调整流动相及其比例,大波斯菊苷出峰时间比较适中,且峰分离度较好,因此选择甲醇-0.1%磷酸水溶液(40∶60)作流动相。
3.3 结论
本试验建立了HPLC法测定白背叶药材中大波斯菊苷含量的方法,并测定了6批不同来源白背叶药材中大波斯菊苷的含量,结果表明:不同来源白背叶药材中的含量有一定差异性,提示采用多指标定量方法,能更好地控制白背叶药材质量。
[1] 国家中医药管理局《中华本草》编委会. 中华本草(第四卷) [M].上海: 上海科学技术出版社, 1999: 827.
[2] 单家林.大戟科植物的地理分布和区系特征[J].热带农业科学,1998(4): 231.
[3] 王志萍,冯桥,沈树虎.白背叶根提取物的体外抑菌试验[J].广西中医药,2012,35(3):55.
[4] 赵进军,吕志平, 王晓东,等.白背叶根在肝纤维化动物模型中抗氧化作用的实验研究[J].中药材,2002,25(3):185.
[5] 郑作文,伦玉宁,赵丽丽.白背叶提取物芹菜素对裸鼠人胃癌细胞移植瘤生长及凋亡的影响[J]. 中国实验方剂学杂志,2012,18(23):214.
[6] 韦松,曲磊,郑作文.白背叶黄酮类化学成分研究[J]. 中成药,2012,34(4):69.
[7] 朱斌,白桂昌, 蒋受军,等.白背叶化学成分和含量测定研究[J].中国中药杂志,2007, 32(10): 932.
[8] 朱斌,蒋受军,林瑞超. GC-MS测定白背叶中的挥发油[J].华西药学杂志,2008,23(1):35.
[9] 黄丽贞,郑作文,唐云丽. 白背叶黄酮化合物 QB3对人肿瘤细胞增殖的抑制作用[J].科学技术与工程,2011,11(22):5394.
(责任编辑:宋勇刚)
HPLC Method for Determination of Apigenin-7-O-glucoside inMallotusapelta
Xie Wei1,Jiang Shoujun1,2*
(1.Guangxi University of Chinese medicine, Nanning 530001, China;2.YuLin Institute for Food and Drug Control,Guangxi 537000, China)
Objective:To establish an HPLC method for determination of Apigenin-7-O-glucoside inMallotusapelta. Methods:HPLC was performed on a Gemini-C18analytical column (4.6mm×250 mm, 5μm) at 25 ℃ with methanol and 0.1% Phosphoric acid (40:60) as the mobile phase.Results:The baseline separation of Apigenin-7-O-glucoside was achieved The linear ranges of 0.04486~0.8972μg (r=0.9990). The average recovery(n=6) was 97.67% (RSD=1.94%).Conclusion:The method of determination is proved to be simple, quick, repeatable, and can be used for quality control ofMallotusapelta.
Mallotusapelta;Apigenin-7-O-glucoside;HPLC;Content
2015-02-05
广西科技创新能力与条件建设项目(桂科攻10124008-15);广西自然科学基金项目(2010GXNSFA013233)
谢巍(1989-),男,广西中医药大学硕士研究生,研究方向为食品药品安全性评价。
蒋受军(1969-),男,广西玉林食品药品检验所主任药师,研究方向为中药化学成分及中药质量控制。E-mail:jiangshoujun@sina.com
R284
A
1673-2197(2015)13-0016-03
10.11954/ytctyy.201513007

