高效液相色谱法测定饲料中艾司唑仑的含量
方秋华,肖田安,伍宏凯,胡苑玲
(广东省兽药饲料质量检验所,广州510230)
高效液相色谱法测定饲料中艾司唑仑的含量
方秋华,肖田安∗,伍宏凯,胡苑玲
(广东省兽药饲料质量检验所,广州510230)
建立了高效液相色谱法测定预混合饲料、配合饲料和浓缩饲料中艾司唑仑含量的检测方法。试样用正己烷-二氯甲烷(1∶1,V/V)提取,经MCX固相萃取柱进一步净化,采用反相高效液相色谱-紫外检测法进行定量分析。饲料中艾司唑仑的检测限为0.1 mg/kg,定量限为0.25 mg/kg。在饲料中添加0.25、0.5、2.5 mg/kg水平的药物回收试验中,平均回收率均在82.8%~105.9%之间,相对标准偏差为1.62%~8.40%。该方法灵敏、准确,适用于饲料中艾司唑仑含量的分析检测。
艾司唑仑;饲料;高效液相色谱
艾司唑仑(又称舒乐安定,Estazolam,EZL)属苯二氮卓类抗焦虑镇静催眠药,在人医临床中广泛应用于催眠、镇静、抗惊厥和抗精神失常。该类药物能使动物平静,减轻机体对不良刺激的应激,限制动物的运动,从而减少动物维持体能的营养物质消耗,有益于增重。故有些不法分子在经济利益的驱动下,可能在畜禽养殖中违规添加使用,以提高饲料转化率。在饲料中滥用此类药物将使其原型药物和代谢产物不可避免地残留于动物源性食品中,导致畜产品品质降低,人食用后会造成对中枢神经系统等的不良影响,危害身体健康。农业部176号公告[1]禁止在饲料和动物饮用水中使用包括艾司唑仑在内的精神类药物。已有文献报道用高效液相色谱法测定艾司唑仑的血药浓度[2-8],但前处理方法较简单,无法满足基质较为复杂的饲料样品的测定要求,也有用液相色谱串联质谱法(LC-MS/MS)测定动物组织[9-11]、饲料[12-14]、血液[15-16]及尿液[17]中多种精神类药物,但未有关于饲料中艾司唑仑的高效液相色谱检测方法报道。本研究旨在建立一种高效液相色谱法测定饲料中艾司唑仑,以满足对饲料非法添加的监控要求。
1 材料与方法
1.1 仪器与试剂 Agilent 1260型液相色谱仪,美国安捷伦公司;SUPELCOL Discovery C18色谱柱,美国Supelco公司;Mach 1.6 R冷冻型离心机,美国Thermo公司;MCX固相萃取柱,60 mg/3 mL,美国Waters公司;Millipore纯水机。
艾司唑仑标准品购自日本WAKO公司,乙腈、甲醇、甲酸,均为色谱纯(德国 CNW公司),正己烷、二氯甲烷、氨水、磷酸二氢钾,均为分析纯(广州化学试剂厂),水为超纯水。
1.2 标准储备液的制备 准确称取艾司唑仑标准品约50 mg,于50 mL容量瓶中,用甲醇溶解并定容,配制成浓度为1 mg/mL的标准贮备液,4℃保存,备用。
1.3 样品提取与净化 准确称取试料(2.0±0.02)g,于50 mL离心管中,加入水20 mL,用100 g/L碳酸钠水溶液调pH至8.5~9.0,加入氯化钠约1 g。准确加入正己烷-二氯甲烷(1∶1,V/V)15 mL,中速振荡10 min后,5000 r/min离心5 min,将上清液转入梨形瓶中。残渣再用15 mL正己烷-二氯甲烷(1∶1,V/V)重复提取一次,合并提取液,在(35± 2)℃下旋转蒸发至干。用甲醇5 mL分两次溶解梨形瓶中的残留物,备用。
MCX固相萃取柱用3 mL甲醇、3 mL水活化,取上述备用液过柱,用3 mL 2%甲酸水溶液、3 mL甲醇淋洗,用5%氨水甲醇溶液6 mL洗脱,收集洗脱液,45℃下氮气吹干,加入1 mL甲醇震荡溶解残渣,用0.45 μm的滤膜滤过,滤液供液相色谱测定。
1.4 仪器测定 高效液相色谱系统。色谱柱为SUPELCOL Discovery C18柱(250 mm×4.6 mm,粒径5 μm),或相当者;流动相为乙腈(A),0.4%磷酸二氢钾溶液(B);梯度洗脱程序为:0~10 min,44% A;10~11 min,44%A~75%A;11~15 min,75%A;15~17 min,75%A~44%A;17~20 min,44%A。流速1.0 mL/min;检测波长222 nm;进样量20 μL;柱温30℃。
2 结果
2.1 光谱图及色谱图 在所确定的色谱条件下,艾司唑仑最大吸收波长见光谱图(图1),艾司唑仑标准溶液色谱图见图2,各空白饲料样品添加艾司唑仑(0.5 mg/kg)所获得的色谱图见图3~图5。
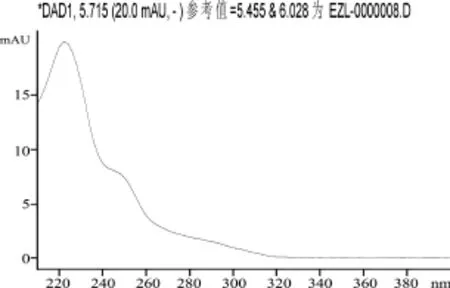
图1 艾司唑仑光谱图

图2 艾司唑仑标准溶液色谱图(1.0 μg/mL)
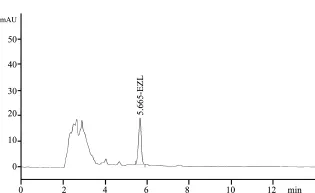
图3 鸡预混料空白添加艾司唑仑色谱图(0.5 mg/kg)

图4 鸡配合料空白添加艾司唑仑色谱图(0.5 mg/kg)
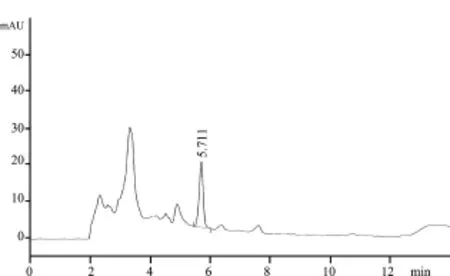
图5 鸡浓缩料空白添加艾司唑仑色谱图(0.5 mg/kg)
2.2 线性范围与检出限 精密吸取艾司唑仑标准液(50 μg/mL)适量,用甲醇稀释成浓度为0.20、0.50、1、2、5、10、20 μg/mL的系列标准工作液,在所确定的色谱条件下,从低浓度到高浓度进样,每一浓度进样三针,将测得的峰面积的平均值(Y)与对应浓度(X)拟合,绘制标准曲线,求回归方程和相关系数(表1)。
采用空白饲料添加低浓度标准品,按1.3项方法进行处理,然后上机检测,以信噪比(S/N)≥3确定检测限,以S/N≥10确定定量限。结果见表1。
2.3 准确度与精密度 对空白饲料分别以0.25、0.5、2.5 mg/kg艾司唑仑3个浓度水平进行添加回收试验,每个浓度平行5份,同日测定,连续做3 d,结果见表2。艾司唑仑在各饲料样品中的平均回收率在82.8%~105.9%之间,批内相对标准偏差为1.01%~7.78%,批间相对标准偏差为1.62%~8.40%。

表1 艾司唑仑在各饲料中的线性方程、检测限和定量限结果表
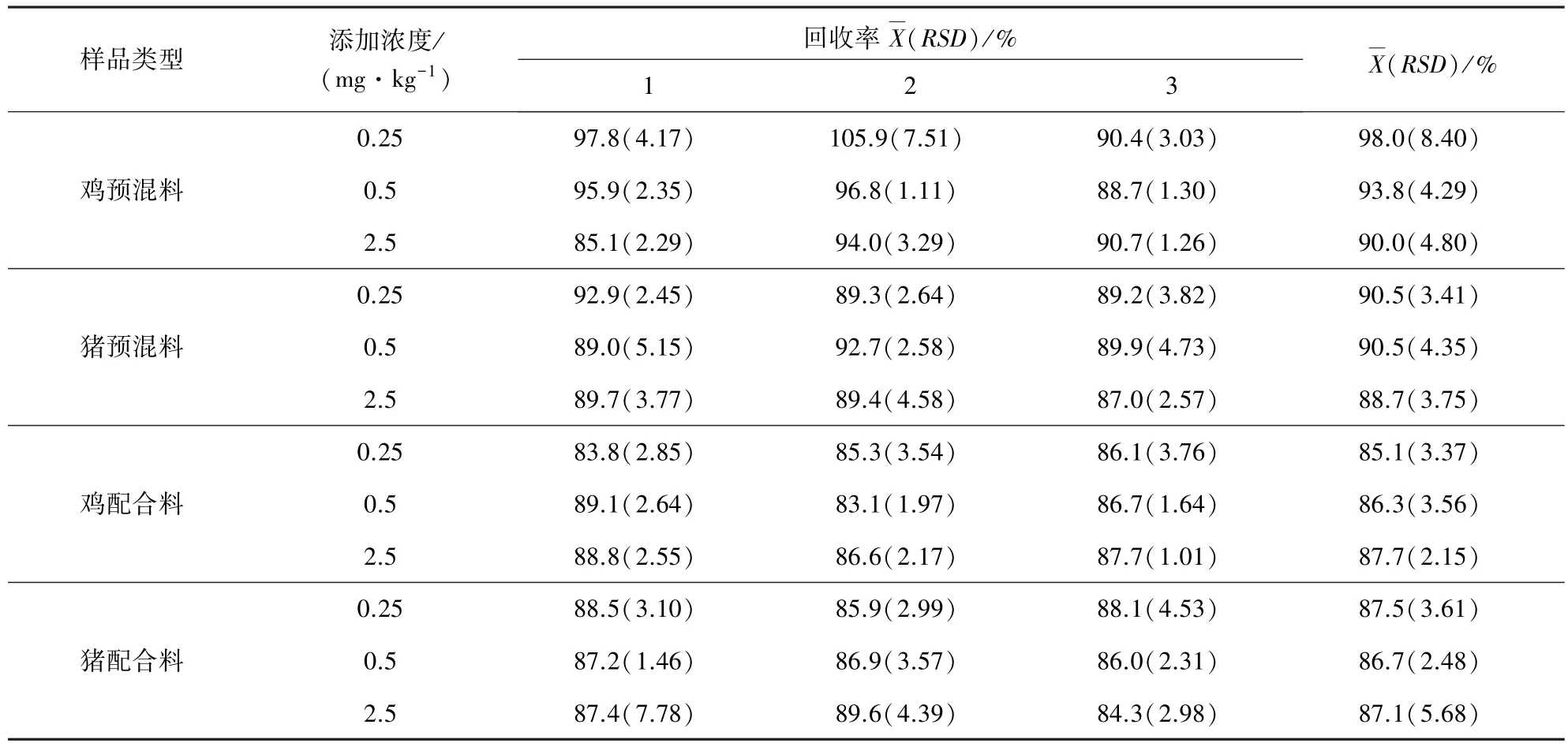
表2 艾司唑仑在各饲料样品中的回收率及相对标准偏差结果表

样品类型 添加浓度/(mg·kg-1)回收率X(RSD)/% 1 2 3X(RSD)/%鸡浓缩料0.25 91.2(3.47) 87.8(3.01) 87.2(1.52) 88.7(3.31)0.5 88.5(4.78) 88.2(6.13) 88.8(1.21) 88.5(4.21)2.5 82.8(3.77) 89.3(7.13) 83.8(3.61) 85.3(5.96)猪浓缩料0.25 91.6(1.38) 86.3(1.04) 87.9(1.40) 88.6(2.84)0.5 88.1(1.15) 90.6(1.29) 89.5(1.02) 89.4(1.62)2.5 93.5(1.89) 90.9(2.53) 90.3(1.56) 91.6(2.47)
3 讨论与小结
3.1 色谱条件的优化 对于色谱柱的选择,已报道的文献资料表明精神类药物在C18色谱柱上有较好的保留性质,所以本研究利用实验室现有的条件,主要比较了 SUPELCOL Discovery C18(150× 4.6 mm,5 μm)、Waters Sunfire C18(150×4.6 mm,5 μm)和SUPELCOL Discovery C18(250×4.6 mm,5 μm)这三种色谱柱。发现艾司唑仑在这三种色谱柱上均具有较好的保留性质,但在Waters C18色谱柱上峰型较宽,在SUPELCOL Discovery C18(150 ×4.6 mm,5 μm)色谱柱上所得峰型虽好,出峰时间太早,容易受杂质峰干扰,所以最后选用SUPELCOL Discovery C18(250×4.6 mm,5 μm)。
对于流动相的优化,本研究主要考察了甲醇或乙腈(有机相)与乙酸铵缓冲溶液、磷酸盐缓冲溶液(不同pH条件下)或超纯水(水相)组成的流动相体系对分析结果的影响。由0.4%KH2PO4(pH 4.5)、KH2PO4/K2HPO4(pH 5.8)、H3PO4/NaH2PO4(pH 6.4)等组成的磷酸盐缓冲溶液、乙酸铵缓冲液(pH 6.84)与甲醇或乙腈组成的一定比例的流动相体系中,能有效地将艾司唑仑与饲料中的其他组分分离。其中以乙腈-0.4%KH2PO4(pH 4.5)流动相体系进行梯度洗脱时能有效地将药物峰与杂质峰分离,且得到最为优异的峰型,对称,不拖尾。
对于波长的选择,本研究在200~400 nm范围内对艾司唑仑标准溶液进行全扫描,在222、225、230、240、254 nm处有5个依次变低的吸收峰,最终选择222 nm进行测定。
3.2 样品前处理方法的研究 对于苯二氮卓类药物的残留检测,已报道的文献常以乙酸乙酯、叔丁基甲醚、乙醚、乙腈、甲醇、正己烷、二氯甲烷、氯仿等为提取溶剂。本研究根据艾司唑仑的理化性质并参考文献主要考察了乙酸乙酯、乙腈、甲醇、正己烷、二氯甲烷等溶剂或其混合物的提取效果,发现以正己烷-二氯甲烷(1∶1,V/V)为提取溶剂时,提取回收效果最好,故以此为提取溶剂。目前对于苯二氮卓类药物的净化主要还是采用固相萃取法,主要考察了MCX、HLB、C18以及硅酸镁小柱等实验室常用小柱的净化效果,发现在相同条件下艾司唑仑在MCX小柱上具有最好的保留效果,回收率可达95%甚至更高,稳定性和重现性也较好,而用其余三种小柱净化后所得回收率不足10%,所以选择MCX小柱对样品进行净化处理。
本文建立的HPLC-紫外检测法,能快速检测预混料、配合料和浓缩料中艾司唑仑含量。该方法前处理简便易行,灵敏度高,精密度好,回收率高,重复性好,可满足饲料中艾司唑仑的分析要求。
[1]中华人民共和国农业部第176号.禁止在饲料和动物饮用水中使用的药物品种[S].
[2]郭胜才,邹晓华,张玉荣,等.高效液相色谱法同时测定血浆中艾司唑仑、三唑仑和阿普唑仑浓度[J].中国医院药学杂志,2003,23(10):599-601.
[3]熊建华,王淑君.高效液相色谱法同时测定人血清中4种苯二氮卓类药物浓度[J].海峡药学,2004,16(1):47-49.
[4]Masatomo MIURA,Tadashi OHKUBO,Kazunobu SUGAWARA,et al.Determination of Estazolam in Plasma by High-Performance Liquid Chromatography with Solid-Phase Extraction[J].Analytical Sciences,2002,18(5):525-528.
[5]侯大平,张志国,国玉芝,等.HPLC法测定艾司唑仑血药浓度的方法验证[J].中国药房,2011,22(14):1280-1282.
[6]刘 福.高效液相色谱法测定艾司唑仑血浓度[J].中国药师,2007,10(11):1152-1153.
[7]叶美娣,滕 彦,汪东海.HPLC法测定地西泮和艾司唑仑的血药浓度[J].中国现代应用药学杂志,2000,17(1):60-62.
[8]李淑芳,安荣姝,马秉智,等.RP-HPLC同时测定人体内盐酸纳洛酮和艾司唑仑血药浓度[J].中国药学杂志,2010,45(5):376-378.
[9]Toshimasa Toyo’oka,Yusuke Kumaki,Masayoshi Kanbori,et al.Determination of hypnotic benzodiazepines(alprazolam,estazolam,and midazolam)and their metabolites in rat hair and plasma by reversed-phase liquid-chromatography with electrospray ionization mass spectrometry[J].Journal of Pharmaceutical and Biomedical Analysis,2003,30(6):1773-1787.
[10]Toshimasa Toyo’oka,Masayoshi Kanbori,Yusuke Kumaki,et al.Detection of Triazolam and Its Hydroxy Metabolites in Rat Hair by Reversed-Phase Liquid Chromatography with Electrospray Ionization Mass Spectrometry[J].Journal of Analytical Toxicology,2000,24(3):194-201.
[11]孙 雷,张 骊,徐 倩,等.超高效液相色谱-串联质谱法检测猪肉和猪肾中残留的10种镇静剂类药物[J].色谱,2010,28(1):38-42.
[12]许成保,锁 然,张 峰,等.超高效液相色谱-四极杆飞行时间质谱快速检测动物饲料中10种违禁精神药物[J].色谱,2012,30(5):457-462.
[13]索德成,赵根龙,李兰,等.液相色谱-串联质谱法同时检测饲料中7种精神类药物[J].分析化学研究简报,2010,38(7):1023-1026.
[14]严丽娟,张 峰,吴 敏,等.UPLC-ESI MS/MS法测定动物饲料中苯二氮卓类药物[J].分析测试学报,2011,30(11):1301-1305.
[15]Dennis J Crouch,Douglas E Rollins,Dennis V Canfield,et al.Quantitation of Alprazolam and cz-Hydroxyalprazolam in Human Plasma Using Liquid Chromatography Electrospray Ionization MS-MS[J].Journal of Analytical Toxicology,1999,23(6):479-485.
[16]陈琴华,罗尚文,陈子林,等.HPLC-MS法同时测定5种抗癫痫药的血药浓度[J].中国科学:化学,2010,40(6):762-767.
[17]顾景凯,夏 荣,钟大放,等.LC/MSn法同时检测人尿液中艾司唑仑、阿普唑仑和三唑仑[J].药学学报,2002,37(2):138-140.
(编 辑:侯向辉)
Determination of Estazolam in Feeds by High Performance Liquid Chromatography
FANG Qiu-hua,XIAO Tian-an∗,WU Hong-kai,HU Yuan-ling
(Guangdong Institute for Veterinary Drugs and Feedstuffs Control,Guangzhou510230,China)
A confirmatory method has been developed and validated for the determination of estazolam(EZL)in premix,compound feed and concentrate feed using high performance liquid chromatography(HPLC).The analyte was extracted from feeds using hexane-dichloromethane(1∶1,V/V),and then the sample extracts were purified by MCX solid-phase extraction.The analyte was analyzed by HPLC-UV.The limit of detection was 0.1 mg/kg for EZL,with quantification limit of 0.25 mg/kg.Recoveries were in the range of from 82.8%to 105.9%from feeds fortified at the 0.25,0.5,2.5 mg/kg levels,and the mean intra-laboratory reproducibility ranged from 1.62%to 8.40%.The developed method was sensitive and specific for the detection of estazolam in feeds.
estazolam;feeds;high performance liquid chromatography(HPLC)
2015-02-02
A
1002-1280(2015)04-0046-05
S859.83
2012农业行业标准制定与修订项目(168)
方秋华,硕士研究生,从事药物残留研究。
肖田安。E-mail:Xiaota@hotmail.com

