酸改性凹凸棒土的制备及其脱汞性能*
施冬雷,乔仁静,许 琦
(1.盐城工学院 化学与生物工程学院,江苏盐城 224051;2.常州大学 石油化工学院,江苏 常州 213164)
汞具有高毒性、易挥发性、生物累积性和持久性等特点[1-3],对环境危害巨大,已引起人们极大的关注。燃煤电厂排放的烟气是大气中元素汞(Hg0)的主要人为来源,我国是全球最大的燃煤国家,对燃煤烟气中汞污染的控制必须实行[4]。美国环保局(EPA)针对燃煤电厂汞排放问题颁布了《清洁空气汞规定》[5]。此外,国家环境保护总局也颁布了《火力发电厂空气污染排放标准》,其中汞排放的限量为 0.03 mg·m-3[6]。
燃煤烟气中的汞主要以氧化汞(Hg2+)、颗粒汞(Hgp)和零价汞(Hg0)三种形式存在[7],Hg2+和Hgp很容易被现有的空气污染控制设备除去。例如,Hg2+可溶于水,能被湿法烟气脱硫设备捕获;Hgp能够附着在飞灰上,能被静电除尘器去除[8]。Hg0可先用催化剂氧化后被空气污染控制设备除去,直接在一个微粒控制系统的上层注射吸附剂是一种潜在的技术。国内外已经报道较多脱汞的吸附剂,例如活性炭、飞灰、钙基吸附剂和石油焦碳等[9]。但是这些吸附剂存在价格贵、吸附性能差和回收率不高等缺点,很难大范围使用。因此,开发新型、高效、廉价的吸附剂成为烟气脱汞的关键。
凹凸棒土(P0)又称坡缕石,是一种层链状富镁硅酸盐粘土矿物,呈针状或纤维状,其理想的化学式为:Si8Mg5O20(OH)2(H2O)4·4H2O,在江苏盱眙县和安徽嘉山县等地有大量储量[10]。在很多研究中,凹凸棒土常用做吸附剂、粘合剂、催化剂及催化剂载体[11-17]。
本文以P0为原料,分别经盐酸、硫酸和硝酸改性处理制得酸改性凹凸棒土(P),其结构经IR,X-射线衍射仪(XRD)和透射电子显微镜(TEM)表征。在模拟烟气条件下考查了其汞脱除能力,并研究了温度、浓度和寿命对脱汞性能的影响。
1 实验部分
1.1 仪器与试剂
烟气模拟系统(6%O2,12%CO2,0.03%NO,0.1%SO2,0.005%Cl2和平衡气 N2;气体总流量为 1 L·min-1,空速 48 000 h-1,氮气分两股:一股和 O2,CO2,NO,SO2和 Cl2混合,另一股通过Hg0蒸气发生装置,最后两股气体混合预热后,进入固定床反应器,Hg0的浓度保持在(20±0.1)μg·m-3;MC-3 000型 Hg0蒸气发生装置;VM-3 000型Hg0在线测量仪。
P0,江苏东大热能机械制造有限公司;盐酸,上海申翔化学试剂有限公司;硝酸,无锡市亚盛化工有限公司;硫酸,上海申翔化学试剂有限公司;六偏磷酸钠,上海山浦化工有限公司;其余所用试剂均为分析纯。
1.2 制备
(1)P0的提纯
称取P010 g,加入200 mL分散剂水溶液(分散剂的用量为凹凸棒土用量的3%),于40℃搅拌1 h;充分搅拌后,于40℃超声震荡2 h;静置30 min后,分离出上部分悬浮液,于80℃干燥,经研磨得纯P0。
(2)P的制备
在反应瓶中依次加入P03 g和2 mol·L-1硫酸,搅拌下于60℃回流反应2 h;过滤,滤饼用蒸馏水洗涤至中性(用BaCl2溶液检测无SO2-4 存在),于80℃干燥;于200℃煅烧2 h。研磨得硫酸改性凹凸棒土
分别改变硫酸浓度为4 mol·L-1和6 mol·L-1,制得
2 结果与讨论
2.1 表征
(1)XRD
图1和表1分别为P的XRD谱图和BET值,由图1和表1可见,经酸改性的凹凸棒土比表面积比 P0明显提高,其中效果最佳;2θ=8.50 °,13.91 °,19.89 °和 28.04 °处的衍射峰分别对应于P0的(110),(200),(040)和(400)位面;与P0相比,的X-射线衍射峰基本无变化,说明P0的结构没有受到破坏。
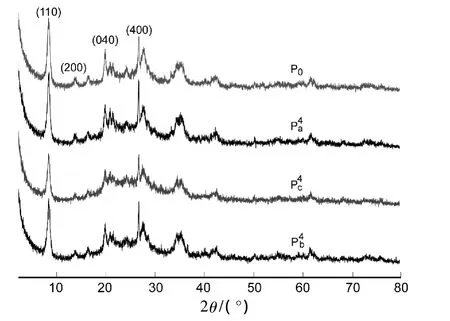
图1 P的XRD图Figure 1 XRD patterns of P
(2)IR
图2为P的IR谱图。P0的主要成分坡缕石的特征峰位于 3 475 cm-1~3 610 cm-1,1 640 cm-1~1 660 cm-1,1 190 cm-1,1 030 cm-1,980 cm-1,510 cm-1和 470 cm-1[18]。由图 2 可见,在P0的IR谱中,1 121 cm-1处的吸收峰为Si-O四面体的伸缩振动峰[19];1 036 cm-1和 981 cm-1处的吸收峰为层内Si-O-Si键的伸缩振动峰;485 cm-1处的吸收峰是 Si-O-Si键的弯曲振动引起;622 cm-1附近的吸收峰为Al-O-Si键的伸缩振动峰。另外,3 415 cm-1和1 617 cm-1附近的吸收峰属于所吸收水分子的伸缩和弯曲振动谱带。经盐酸、硝酸和硫酸改性后,P0的IR谱图中3 415 cm-1,1 617 cm-1,1 526 cm-1和 1 415 cm-1附近的吸收峰分别向 3 431 cm-1,1 634 cm-1,1 576 cm-1和1 426 cm-1靠近。这表明 P0可能存在微量的有机物及碳酸盐,经提纯和酸改性后明显减少。

表1 P的BET值Table 1 BET value of P
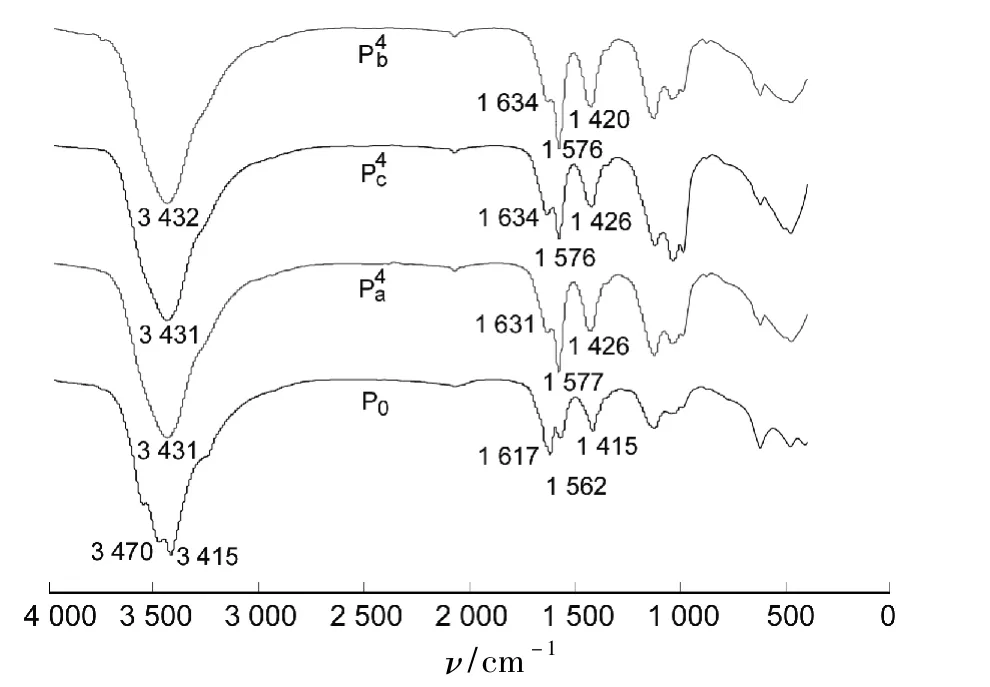
图2 P的IR谱图Figure 2 IR spectra of P
(3)TEM
图3为P的TEM图。由图3可见,P0呈纤维状或棒状结构,且分布较为紧密,部分地方呈现团状,其有效的比表面积和分散性均不理想;分别经盐酸,硝酸和硫酸改性的凹凸棒土呈明显纤维状或棒状结构,整体比较均匀,属于典型的凹凸棒土形貌。凹凸棒土原土中会有许多杂质,主要是碳酸盐及其它粘土。从图3还可以看出,凹凸棒土原土周围有一些圆形及近似圆形的粒状物存在,这些粒状物可能是碳酸盐之类的杂质;而和,杂质粒状物明显减少。这说明采用酸改性凹凸棒土的方法能够提高凹凸棒土的纯度,且可改善凹凸棒土的形貌,提高分散性。
2.2 催化剂活性测试

图3 P0的TEM图Figure 3 TEM images of P0
图4为P0在不同温度下的Hg0脱除效率。P0对模拟烟气中的Hg0不具有催化氧化作用,通过单纯的吸附脱除烟气中的Hg0。P0具有较强的吸附能力,能将Hg0吸附在其表面,通过均相氧化机理,与模拟烟气中的Cl2,NO和O2发生氧化反应,生成汞化合物而被除去。从图4可见,P0的汞脱除效率不高,在180℃时为26.59%。在120℃~180℃,P0的汞脱除效率随温度升高而增大。原因可能是随着温度升高,化学反应速率加大,汞氧化效率变大。在180℃~260℃,P0的汞脱除效率随温度升高而减小。原因可能是随温度升高,物理吸附能力下降,汞吸附效率降低。
为了提高P0的汞脱除能力,本文用不同浓度的硝酸、盐酸和硫酸对其进行改性并研究了其脱汞性能。图5为P在180℃时的Hg0脱除效率。从图5可以看出,经盐酸改性后的凹凸棒土(Pa)脱汞效率明显比经硝酸(Pc)和硫酸(Pb)改性的高,主要是因为Pa比Pb和Pc具有更大的比表面积,能够更多吸附烟气的汞;另外可能的原因是Pa中残余的 Cl-能够促进 Hg0被氧化[20],而和没有促进作用。经4 mol·L-1HCl改性后的凹凸棒土()具有最强的脱汞能力(51.71%),比 P0高约一倍。
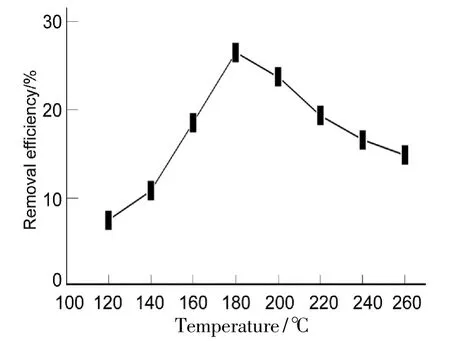
图4 不同温度下P的Hg0脱除效率Figure 4 Hg0removal efficiency of P at different temperature
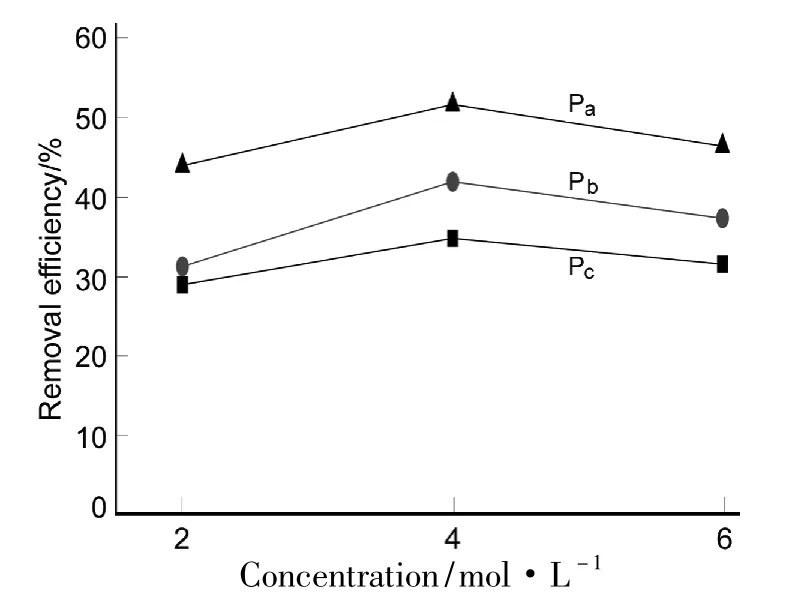
图5 不同酸浓度对P的Hg0脱除效率的影响Figure 5 Effect of concentration of acid on Hg0removal efficiency of P
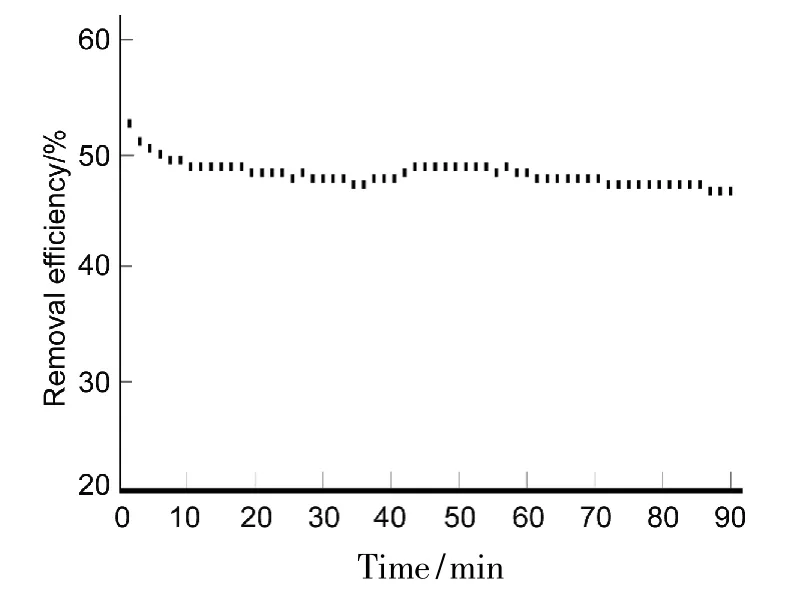
图6 在6 h内的Hg0脱除效率Figure 6 Hg0removal efficiency of in 6 h
与其他吸附剂相比,Cai等[21]考察了 KI和KBr改性粘土的汞脱除性能。结果表明:未经改性的粘土比表面积较小(77.37 m2·g-1),在80℃其汞脱除效率几乎为零;Tao等[22]将CeCl3负载到活性炭上,并测试了其汞脱除性能。结果显示:未经改性的活性炭具有较大的比表面积(395.79 m2·g-1),在 140 ℃其汞脱除效率达到50%以上;Ding等[23]以凹凸棒土、膨润土和发光沸石为吸附剂,对其改性后的汞脱除性能进行了研究。研究发现:未经改性的凹凸棒土、膨润土和发光沸石的比表面积相差很大(分别为153.55 m2·g-1,40.89 m2·g-1和 6.83 m2·g-1),与膨润土和发光沸石相比,改性后的ATP具有较好的汞脱除效率。从以上结果可以得出,汞脱除性能与吸附剂的比表面积有很大的关系,而鉴于P0具有较大的比表面积及其廉价易得,且本文中未改性的P0在180℃有20%以上的汞脱除效率,因此选用P0作为汞脱除的吸附材料是可行的。
3 结论
以凹凸棒土为原料,分别经盐酸、硫酸和硝酸改性处理制得酸改性凹凸棒土,改性后的凹凸棒土的脱汞性能有所提高;经4 mol·L-1盐酸改性的凹凸棒土,在180℃时有最好的脱汞效率(51.71%),且在6 h内保持稳定。该研究为进一步对凹凸棒土改性及其工业化生成提供了参考。
[1] United Nations Environment Programme(UNEP),Global Mercury Assessment,UNEP Chemicals[R].Geneva,Switzerland,December,2002.
[2]Xu W Q,Wang H R,Zhu T Y,et al.Mercury removal from coal combustion flue gas by modified fly ash[J].J Environ Sci,2013,25(2):393 -398.
[3]Presto A A,Granite E J.Survey of catalysts for oxida-tion of mercury in flue gas[J].Environ Sci Technol,2006,40:5601 -5609.
[4]Pacyna E,Pacyna J,Sundseth K,et al.Global emission of mercury to the atmosphere from anthropogenic sources in 2005 and projections to 2020[J].Atmos Environ,2010,44(20):2487 -2499.
[5]US EPA.Final Mercury and Air Toxics Standards(MATS)for Power Plants[EB/OL][2014-02-28]http://www.epa.gov/airquality/powerplanttoxics/actions.html.
[6]State Environmental Protection Administration of China(SEPA),Emission Standard of Air Pollution for Thermal Power Plants,GB 13223-2011,SEPA,Beijing,2011.
[7]Li H L,Wu C Y,Liu L Q,et al.Kinetic modeling of mercury oxidation by chlorine over CeO2-TiO2catalysts[J].Fuel,2013,113:726 -732.
[8]Qu Z,Yan N Q,Liu P,et al.The role of iodine monochloride for the oxidation of elemental mercury[J].J Hazard Mate,2010,183:132 -137.
[9]Cai J,Shen B X,Zhou L,et al.Removal of mercury by clays impregnated with KI and KBr[J].Chem Eng J,2014,241:19 -27.
[10]蔡晋,董如林,何越江,等.凹凸棒土的表面改性及其在不饱和聚酯树脂中的应用[J].常州大学学报,2014,26(2):14 -17.
[11]Chen H,Wang A Q.Kinetic and isothermal studies of lead ion adsorption onto palygorskite clay[J].J Colloid Interface Sci,2007,307:309 -316.
[12]Huang J H,Liu Y F,Liu Y,et al.Effect of attapulgite pore size distribution on soybean oil bleaching[J].J Am Oil Chem Soc,2007,84:687 -692.
[13]Zhao D F,Zhou J,Liu N.Surface characteristics and photoactivity of silver-modified palygorskite clays coated with nanosized titanium dioxide particles[J].Mater Charact,2007,58:249 -255.
[14]Melo D M A,Ruiz J A C,Melo M A F,et al.Preparation and characterization of lanthanum palygorskite clays as acid catalysts[J].J Alloy Compd,2002,344:352-355.
[15]Miao S D,Liu Z M,Zhang Z F,et al.Ionic liquidassisted immobilization of rh on attapulgite and its application in cyclohexene hydrogenation[J].J Phys Chem C,2007,111:2185 -2190.
[16]Zhao D F,Zhou J,Liu N.Characterization of the structure and catalytic activity of copper modified palygorskite/TiO2(Cu2+-PG/TiO2)catalysts[J].Mater Sci Eng A,2006,431:256 -262.
[17]Melo D M A,Ruiz J A C,Melo M A F,et al.Preparation and characterization of terbium palygorskite clay as acid catalyst[J].Microporous Mesoporous Mater,2000,38:345 -349.
[18] 高华,李村,吴振玉,等.酸改性Att/氧化锰复合材料的制备研究[J].非金属矿,2010,33(2):35 -38.
[19]Steudel A,Batenburg L F,Fischer H R,et al.Alteration of swelling clay minerals by acid activation[J].Appl Clay Sci,2009,44(1 -2):105 -115.
[20]Hou W H,Zhou J S,Qi P,et al.Effect of H2S/HCl on the removal of elemental mercury in syngas over CeO2-TiO2[J].Chem Eng J,2014,241:131 -137.
[21]Cai J,Shen B X,Zhou L,et al.Removal of elemental mercury by clays impregnated with KI and KBr[J].Chem Eng J,2014,241:19 -27.
[22]Tao S S,Li C T,Fan X P,et al.Activated coke impregnated with cerium chloride used for elemental mercury removal from simulated flue gas[J].Chem Eng J,2012,210:547 -556.
[23]Ding F,Zhao Y C,Mi L L,et al.Removal of gasphase elemental mercury in flue gas by inorganic chemically promoted natural mineral sorbents[J].Ind Eng Chem Res,2012,51:3039 -3047.

