探讨符合线路SPECT配置针孔准直器进行小动物高能成像的可行性
张秀梅,冯珏,贾红丽
1.河北医科大学第二医院 核医学科,河北 石家庄 050000;2.河北医科大学第一医院 核医学科,河北 石家庄 050031
探讨符合线路SPECT配置针孔准直器进行小动物高能成像的可行性
张秀梅1,冯珏1,贾红丽2
1.河北医科大学第二医院 核医学科,河北 石家庄 050000;2.河北医科大学第一医院 核医学科,河北 石家庄 050031
目的探讨符合线路SPECT配置针孔准直器进行小动物高能成像的可行性。方法① 点源试验。将14.8 MBq的99Tcm、131I和18F三种核素的点源分别置于针孔准直器表面中心轴线不同距离处,采集点源图像并计算分辨率;② 小鼠成像。首先采集小鼠的99Tcm和18F-FDG平面图像,次日采集小鼠的18F-FDG符合线路断层融合影像。结果99Tcm的点源图像清晰、无伪影;131I和18F点源周围均存在少量透射和散射伪影,图像边缘有较明显的环形透射伪影。三种核素点源分辨率均随距离增加而下降,在距离探头30 mm位置,99Tcm、131I和18F的点源分辨率FWHM分别为4.3、5.2、7.4 mm,分辨率FWTM分别为7.1、10.1、14.5 mm。其中,18F分辨率FWHM为7.2 mm,优于SPECT的系统分辨率10 mm。经过模拟放大2.5倍后,小鼠的高、低能影像均较清晰,环形伪影位于有效视野之外。小鼠符合线路18F-FDG的影像不清晰。结论在对分辨率要求不高的场合,符合线路SPECT配置低能针孔准直器进行小动物高能成像是可行的。
符合线路SPECT;针孔准直器;小动物成像;18F-FDG成像
随着新型放射性药物的不断涌现,近几年分子核医学得到了迅猛发展,小动物分子成像研究受到了极大关注[1-4],但是临床上还不具备microSPECT和microPET等先进的专用实验设备。有研究报道,SPECT配置针孔准直器非常适合小动物的低能核素成像,而且通过对针孔准直器的优化设计,可以明显提高成像质量[5-6]。符合线路SPECT在国内已普遍应用,其配置1英寸NaI(TL)晶体后,提高了高能探测的灵敏度。本研究旨在探讨符合线路SPECT配置通用针孔准直器进行小动物高能核素成像的可行性。
1 材料与方法
1.1 仪器与材料
仪器:采用GE Infinia VC Hawkeye型SPECT,配置通用针孔准直器。通用针孔准直器的参数:准直孔的直径3 mm,张角90o,焦距140 mm,物距15 mm,有效视野239 mm。
放射性药物与实验动物:131I、18F-FDG和99Tcm发生器(裂变)均由原子高科股份有限公司提供。清洁级KM小白鼠2只,雌性,购自河北医科大学实验动物中心。
1.2 方法
点源的图像采集与处理:将14.8 MBq 的99Tcm、131I和18F-FDG三个点源分别置于距离针孔准直器表面0、21、42、63、84和105 mm等不同距离处,采集点源的平面影像。采集条件:矩阵256×256,模拟放大因子zoom1.0,总计数500 kc。99Tcm的能峰为140 keV,窗宽为±10%;131I的能峰为364 keV,窗宽为±10%;18F的能峰511 keV,窗宽±10%。像素大小为2.2 mm,共获得18幅点源图像。仔细调整点源图像的灰度,评价点源图像质量。从点源图像的计数剖面曲线上,利用线性插值法获得半高宽(Full Width at Half Maximum,FWHM)和十分之一高宽度(Full Width at Tenth Maximum,FWTM),则点源的分辨率分别为FWHM和FWTM与放大倍数的比值[6]。
小鼠99Tcm和18F-FDG成像:在2只小鼠的尾静脉分别注射7.4 MBq的99Tcm和18F-FDG,并于20 min和1 h后进行平面显像。采集条件:zoom2.5、矩阵256×256,采集计数500 kc,小鼠距准直器表面30 mm。次日相同剂量进行小鼠18F-FDG符合线路断层融合成像。
2 结果

图1 点源图像及对应的归一化计数剖面曲线
2.1 点源图像
在距离准直器42 mm处,99Tcm、131I和18F的点源图像和对应的归一化计数剖面曲线,见图1。99Tcm的点源图像清晰,剖面曲线锐利,131I和18F的点源图像边缘均出现明显的环形伪影。使用多层铅皮进行针孔锥面的部分包绕后,环形伪影被遮挡,表明由于准直器针孔后侧壁较薄,高能射线能够部分穿透,对应的剖面曲线也显示:在视野边缘存在计数突起,18F比131I图像更严重。(见图1)
2.2 SPECT带针孔准直器对不同核素点源的分辨率
点源距准直器不同距离时的分辨率曲线,见图2。由图2可知,三种核素的点源图像分辨率FWHM和FWTM均随探测距离的增加而下降;在相同距离处,核素能量越高,分辨率越差,原因可能是随着射线能量的增高,进入探测视野的散射线也增多,引起图像模糊,尤其是FWTM的下降使图像本底增加,对比度下降。但是从分辨率曲线中可以推出:点源距准直器30 mm时,99Tcm、131I和18F的分辨率FWHM分别为4.3、5.2和7.4 mm,FWTM分别为7.1、10.1和14.5 mm。其中,18F分辨率FWHM为7.4 mm,优于SPECT的系统分辨率10 mm。
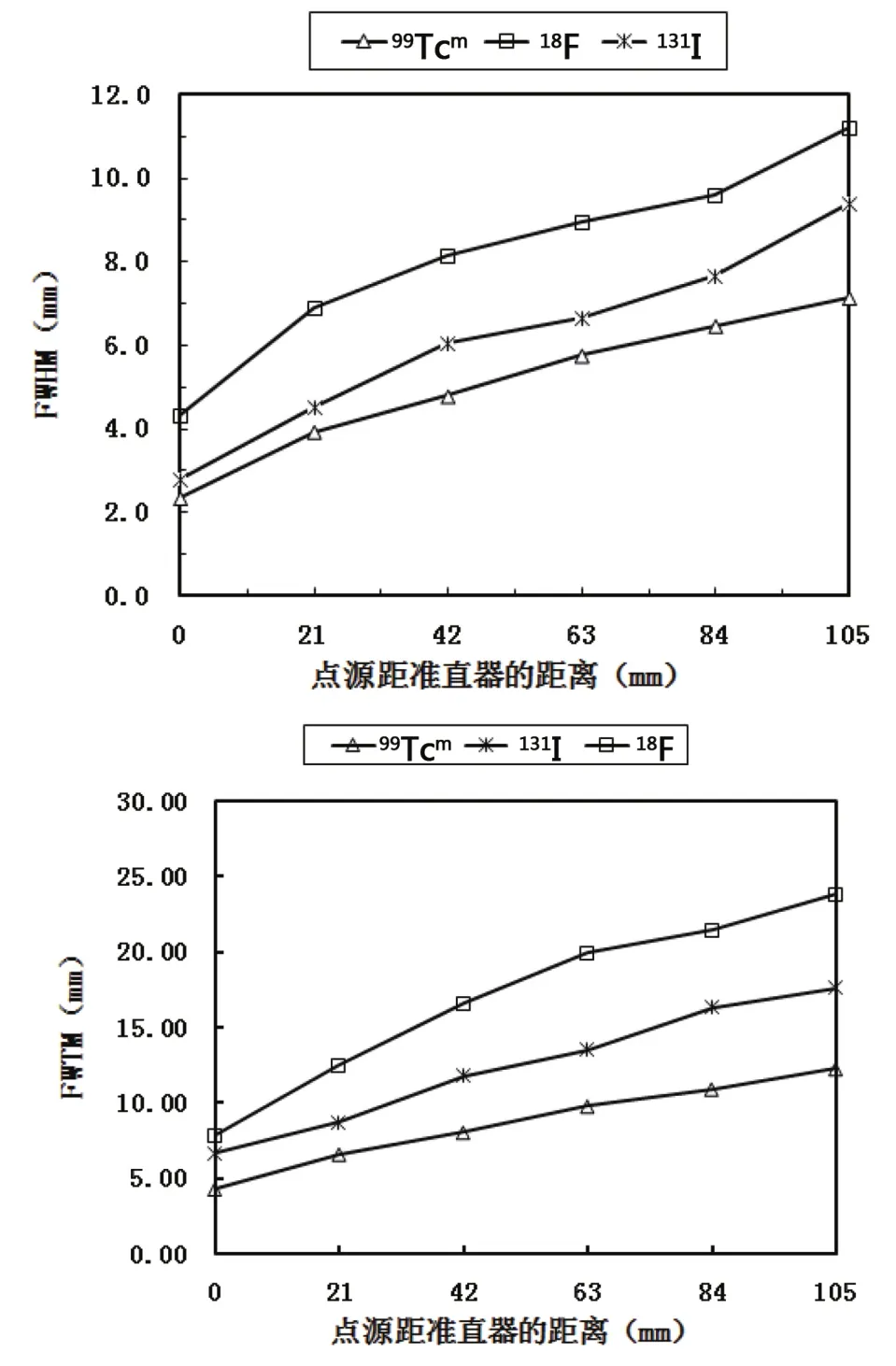
图2 点源距准直器不同距离时的分辨率曲线
2.3 使用针孔准直器获得的小鼠99Tcm和18F-FDG平面图像
小鼠的99Tcm和18F-FDG图像,见图3。由图3可知,在99Tcm图像上,能够清晰地显示小鼠的身体轮廓以及甲状腺、胃、膀胱等。在18F-FDG图像上,小鼠全身轮廓清晰,头、胸部和腹部及膀胱等能均能清晰分辨,腋下和四肢仅有血液本底水平,故有利于这些部位接种肿瘤后的影像学观察。使用zoom2.5倍后,18F-FDG图像上仅在视野边缘四角存在少量伪影,不会对图像造成明显影响。
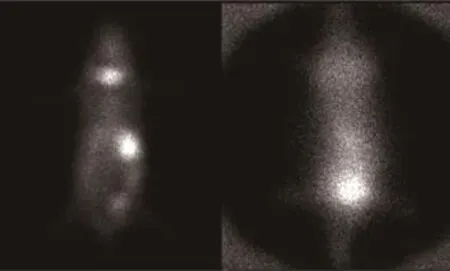
图3 小鼠的99Tcm和18F-FDG平面图像
2.4 小鼠的18F-FDG符合线路断层融合图像
小鼠的18F-FDG符合线路断层融合图像,见图4。由图4可知,在18F-FDG的最大密度投影重建图像上,仅能够显示小鼠的全身轮廓,具体器官不能清晰分辨。在3个方向的断层图像上同样也无法清楚分辨具体脏器的核素分布。
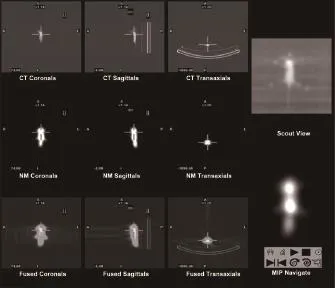
图4 小鼠的18F-FDG符合线路断层融合图像
3 讨论
目前SPECT小动物511 keV高能成像,可能的显像形式有microSPECT、符合线路SPECT和SPECT配置针孔准直器3种方法。microSPECT成像的分辨率和灵敏度可以和microPET相媲美[7],但多数用户没有这种专用设备。SPECT配置通用针孔准直器非常适合于小动物成像,这是因为针孔准直器有两种影像放大方式:① 软件完成的电子放大,即将采集条件中的zoom值加大,采集视野缩小,相当于增大采集矩阵,需要增加采集时间才能获得较好的图像,这种放大方式并不能提高系统的分辨率;② 通过小孔成像原理实现的光学放大,可以有效地克服探测器固有分辨率对系统成像分辨力的制约,取得较好图像。小动物成像时通常是两种方式并用。但是对于常规3/8英寸晶体的SPECT,对高能射线的探测效率仅为9%,能量响应范围<400 keV,不能完成18F 511 keV的高能成像。
符合线路SPECT配置1英寸NaI(Tl)晶体后,对511 keVγ单光子的探测效率提高到37%,而且探头的能量响应范围完全能覆盖到511 keV以上,具有18F显像所必须的各种均匀性、线性和能量等校正功能,具备进行高能显像的基本条件。而采用双探头符合线路SPECT对小鼠进行断层融合成像时,在3个方向的断层图像上无法清楚地分辨具体脏器的核素分布,因此不适合小动物成像。
针孔准直器距点源30 mm时,131I和18F中心点源的分辨率FWHM分别可达到5.2 mm和7.4 mm ,明显优于普通SPECT的系统分辨率。在进行131I和18F显像时,视野边缘会出现伪影环,但使用多层铅皮包绕准直器锥面侧壁后相应的伪影环部分消失,说明高能射线在通用针孔准直器侧壁存在透射和散射[8-9],但是近端侧壁因为有2.5 cm厚的针孔插件,能完全阻挡高能射线穿透,从而在影像与周围伪影环之间形成了有效隔离,小鼠成像时使用2.5倍的zoom值,可以使伪影环远离成像区,有效减少了散射对图像的干扰。
符合线路SPECT配置针孔准直器进行小鼠的高能单光子平面成像,在分辨率上虽然无法和专用的MicroPET和MicroSPECT相比较(1~2 mm),无法清晰地显示小鼠组织器官的结构,但是1英寸NaI(Tl)的应用,明显提高了对高能射线的探测效率。在分辨率要求不高的场合,如对于腋下或大腿根接种荷瘤(瘤体>1 cm)的小鼠,观察其体内不同核素标记的放射性药物的分布、排泄途径等,均可满足显像要求。
[1] Mitchell GS,Cherry SR.A high sensitivity small animal SPECT system[J].Phys Med Biol,2009,54(5):1291-1305.
[2] Kim JS,Lee JS,Im KC,et al.Performance measurement of the microPET focus 120 scanner[J].J Nucl Med,2007,48(9):1527-1535.
[3] 黄勇,孙明山,安里奎·伊萨吉尔雷,等.小动物SPECT-CT装置的研发[J].医疗设备信息,2007,22(9):4-6.
[4] 陈绍亮,赵军,石洪成,等.第51届美国核医学年会概况[J].中华核医学杂志,2004,24(6):382-383.
[5] 孟庆乐,杨瑞,曹艳,等.SPECT/CT融合显像在99Tcm-MIBI甲状腺亲肿瘤显像中的应用[J].中国医疗设备,2014,(2):121-122,151.
[6] 马天予,周荣,吴朝霞,等.基于Monte Carlo模拟设计MicroSPECT针孔准直器[J].清华大学学报(自然科学版),2007,47(s1):933-936.
[7] Rowland DJ,Cherry SR.Small-animal preclinical nuclear medicine instrumentation and methodology[J].Semin Nucl Med,2008,38(3):209-222.
[8] Tenney CR,Tornai MP,Smith MF,et al.Uranium pinhole collimators for 511-keV photon SPECT imaging of small volumes[J].IEEE Transactions on Nuclear Science,2001,48(4):1483-1489.
[9] Zeniya T,Watabe H,Aoi T,et al.Use of a compact pixellated gamma camera for small animal pinhole SPECT imaging[J].Ann Nucl Med,2006,20(6):409–416.
Discussion on the Feasibility of Small Animal High-Energy Imaging Using Coincidence SPECT with a Pinhole Collimator
ZHANG Xiu-mei1, FENG Jue1, JIA Hong-li2
1. Department of Nuclear Medicine, the Second Hospital of Hebei Medical University, Shijiazhuang Hebei 050000, China; 2. Department of Nuclear Medicine, the First Hospital of Hebei Medical University, Shijiazhuang Hebei 050031, China
ObjectiveThis study was aimed to explore the feasibility of small animal high-energy imaging using coincidence SPECT (Single-Photon Emission Computerized Tomography) with a pinhole collimator.MethodsFirst, the point sources of 14.8MBq’s three radionuclides (99Tcm,131I and18F) were placed at di ff erent distances from the central axis of the pinhole collimator respectively. Images of point sources were acquired to calculate their resolutions. Then,99Tcmand18F-FDG images of mice were acquired respectively. The coincidence images of the mouse were acquired on the second day.ResultsThe images of99Tcmpoint source were clear without artifacts; however, there were minor penetration and scattered artifacts in131I and18F images. Additionally, both images had signi fi cant circular penetration artifacts in their edges. Resolutions of99Tcm,131I and18F were declined with the distance increased. At the distance of 30 mm from the pinhole collimator, their FWHM (Full-Widths-at-Half-Maximum) and FWTM (Full-Widths-at-Tenth-Maximum) resolutions were 4.3, 5.2, 7.4 mm and 7.1, 10.1, 14.5 mm respectively. The FWHM resolution of18F showed advantages over the resolution of the images acquired by SPECT. After being zoomed in 2.5 times, both the high-energy and low-energy mice images were clear with the ring artifacts outside the e ff ective fi eld of view. Coincidence18F-FDG images of the mouse were not clear.ConclusionThe coincidence SPECT with the lowenergy pinhole collimator can be used for small animal high-energy imaging if there was no restriction on the resolution of images.
coincidence single-photon emission-computerized tomography; pinhole collimator; small animal imaging;18F-FDG imaging
R814.42
B
10.3969/j.issn.1674-1633.2015.03.010
1674-1633(2015)03-0038-04
2014-07-22
2014-11-02
作者邮箱:zhangxm-65@163.com

