长江口刀鲚幼鱼耳石碳、氧同位素特征初报
姜 涛, 刘洪波, 杨 健,
(1.南京农业大学 无锡渔业学院, 江苏 无锡 214081; 2.中国水产科学研究院 淡水渔业研究中心, 中国水产科学研究院长江中下游渔业生态环境和资源养护重点实验室, 江苏 无锡 214081)
刀鲚(Coilia nasus)作为著名的“长江三鲜”之一,是长江的一种重要的渔获种类。每年三、四月份亲鱼会在长江口区集结并上溯从而形成“鱼汛”。然而,近年来由于水利工程、酷渔滥捕、环境污染等原因,其资源量下降严重并已岌岌可危[1]。如何利用各种新兴技术来客观获取保护这种重要渔业资源的基础信息已经成为目前亟待解决的难题之一。
迄今, 刀鲚的研究主要集中在分子生物学[2-5]、形态学[6-9]等方面, 但近年基于耳石进行刀鲚生活史、群体组成及动态的研究也逐渐增多[10-14]。鱼类耳石具有一些特殊性, 如耳石形成后结构非常稳定、不会被代谢, 其上会形成可以直接读取的年轮; 耳石中积累的元素组成与其生活过的外界水体生境密切相关。这些特殊性被广泛应用鱼类的生境履历反演和群体动态的重建等研究中[15-19]。针对耳石中元素和稳定同位素的分析研究常被统称为耳石微化学研究[20]。前者中的一些元素(如锶、钙)由于在自然界不同水体中的差异分布, 通过分析它们在耳石轴上的含量变化, 可以推测鱼体在生活史过程中所经历的水体元素情况, 继而反演出该鱼的生境履历。除此之外, 耳石核心部位的元素组成, 也常被用于作为源自不同孵化场群体的判别依据[21]。与元素分析相比较, 耳石中稳定同位素的研究多数集中在耳石中碳、氧同位素方面。这其中δ13C被证实与饵料的关系较为密切(如高营养状态下的δ13C要显著高于低营养状态下的值[22]), 而δ18O则被证实为与水温关系十分密切, 且在正常盐度条件下, 1‰的δ18O变化应该对应于约5℃的水温变化[23]。这些特点使得耳石稳定同位素分析除了能像元素分析一样, 作为群体识别或者生境履历的标志外, 还能反映出鱼体的生理状况和环境水温等的情况。Tomida 等[24]利用细鳞大马哈鱼(Oncorhynchus gorbuscha)幼鱼耳石中 δ13C 和 δ18O,发现了自然与人工饲养条件下两者的差异, 并证实了幼鱼的饵料水平以及所经历的环境温度分别对耳石中δ13C和δ18O的影响, 从而为研究成鱼的起源以及评价孵化场对种群资源补充的能力提供了有力的研究手段。Geffen[25]在对自然条件和实验室条件下的鲽鱼(Pleuronectes platessa)幼鱼研究发现 δ18O 显著地受到温度的影响, 而与饵料无关, 同时通过与相关文献作比较发现利用鱼耳石δ18O水平反演的估测水温与真实水温间存在种间差异; 而 δ13C则更多的和生长速度相关。利用耳石中δ13C和δ18O, Gao等[26]发现美国奥泽特湖中的红大马哈鱼(Oncorhynchus nerka)种群存在起源自不同湖岸产卵场的群体。与国外大量的耳石同位素研究报道相比, 中国相关的研究报道较少, 仅 Shen 等[27]曾利用鲢鱼(Hypophthalmichthysmolitrix)耳石中δ18O和δ13C发现赣江、鄱阳湖的鲢鱼种群与长江种群并不相同。
鉴于刀鲚相关研究尚未见任何报道, 本研究尝试对刀鲚幼鱼耳石中碳、氧稳定同位素的特征情况进行了探索, 并讨论其可能反映出的生态学意义,以期从新角度为刀鲚资源保护和群体判别提供理论依据, 也期为今后更深入地研究积累技术基础。
1 材料与方法
1.1 实验材料
本研究选取采自长江口崇明岛水域的刀鲚当年幼鱼7尾。待测量完全长(109.4 mm±1.7 mm)和体质量(2.8 g± 1.2 g)后, 统一摘取右矢耳石用作分析对象样品。
耳石先在去离子水中去除外套膜和有机质, 然后在酒精中清洗。随后, 所有耳石样品使用超声清洗机清洗3 min后, 使用MQ水清洗3遍。清洗完成的耳石样品室温下自然晾干24 h。
1.2 实验方法
以酒精清洁过表面的铝箔纸包裹晾干后的耳石样品, 使用碾钵轻击、磨碎耳石, 再将粉末状耳石样品混匀后留待分析。
耳石同位素分析使用日本东京大学大气海洋研究所配备 Gas Bench Ⅱ气体发生装置的 Delta V Advantage稳定同位素质谱分析仪(ThemoFisher Scientific, Co., Waltham, USA)进行。分析前, 称取约200μg耳石粉末, 并置于试管底部。测定结果 δ18O和δ13C用以下公式计算, 即:

其中“standard”为国际标准物质 VPDB(Vienna Peedee Belemnite),“otolith”为耳石样品。使用NBS18(National Bureau of Standards)作为分析标样。测试精度<0.09‰。
1.3 统计方法
本研究统计分析使用美国微软公司 Excel 2007软件和 IBM公司SPSS 19.0 软件来进行。
2 结果与分析
所有耳石样品δ13C和δ18O结果如表1所示, 其中 δ13C 为 –12.1±1.8(‰VPDB), δ18O 为 –7.9±1.2(‰VPDB)。从表中可以发现, 所有样品的δ13C波动较大, 从最低–14.4 ‰VPDB(CMJ09)到最高–9.8‰VPDB(CMJ15)。与之相比, δ18O 则波动较小, 从–10.1‰VPDB(CMJ15)到–7.0‰VPDB(CMJ11)。
通过表1不难发现, 相对于δ13C的波动, 部分刀鲚幼鱼耳石的 δ18O结果有一定的趋同, 其中CMJ08、–09、–11、–12、–14 的结果均在–7‰VPDB左右波动, 而CMJ13和–15则分别为–9.2‰VPDB和–10.1‰VPDB。有鉴于此, 参考 Gao等[26]将 δ13C和δ18O做散点图, 以分析这些刀鲚个体可能起源的群体情况(图1)。结果显示, 本研究中的 7尾刀鲚幼鱼个体应该可以分为两个组, 其中组一为 CMJ13和–15(全长为 94.5 mm±4.95 mm)组二为 CMJ08、–09、–11、–12、–14(全长为 115.6 mm±16.3mm)。

表1 长江口刀鲚幼鱼耳石δ13C和δ18O的结果Tab.1 δ13C and δ18O values in the otoliths of the juveniles Coilia nasus from the Changjiang River Estuary
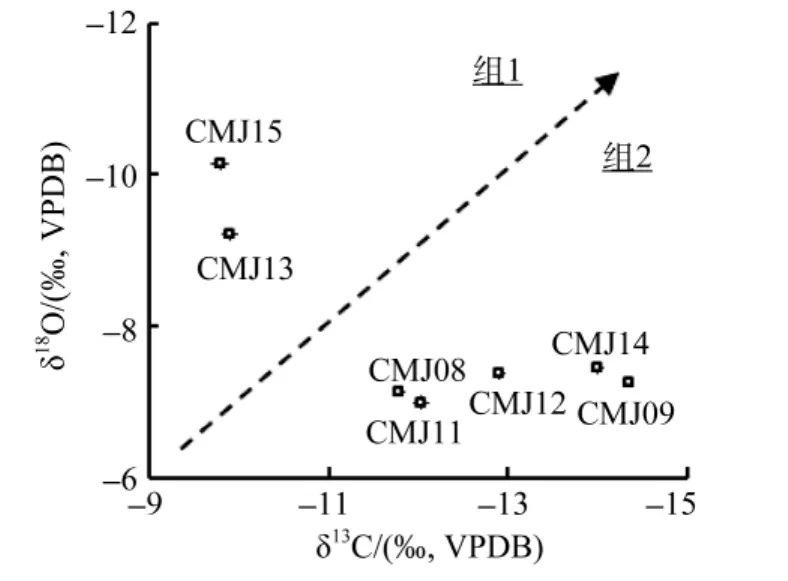
图1 长江口刀鲚幼鱼耳石δ18O和δ13C分布变化Fig.1 Variations of δ13C and δ18O distribution in the otoliths of the juveniles Coilia nasus from the Changjiang River Estuary
3 讨论与结论
尽管国际上利用耳石中的碳、氧稳定同位素作为鱼类群体起源和判别已经有很多成功的例子[26-28],但在国内相关研究尚很缺乏。除去一些耳石同位素研究的综述报道外[23,29], 仅Shen等[27]对中国赣江、鄱阳湖、长江中的淡水鱼类的鲢鱼(Hypophthalmichthys molitrix)群体进行耳石 δ13C和 δ18O分析。因此, 本研究应该是有关刀鲚耳石碳、氧稳定同位素方面的首次探索。
历史上刀鲚溯河后会在长江不同江段或者湖泊内产卵[30]; 然而近年来, 由于水利工程、水质污染、酷渔滥捕等原因, 其产卵场发生了改变[31]。目前对于长江内刀鲚产卵场的位置以及不同产卵场/孵化地资源群体的组成尚很难研究。考虑到耳石稳定同位素对于鱼类群体区分的高精确性, 甚至对于源自相邻水域的群体亦能有很好地区分[26-27], 因此作者尝试将相关的方法引入到长江刀鲚群体的起源探索之中。
本研究中所选用的刀鲚均为不到 1龄的幼鱼。通过Jiang等[11]的结果可以推知, 本研究中刀鲚个体发育过程中的大部分时间应该在自长江内孵化场到长江口间的淡水环境中度过。考虑到淡水环境不会像海水一样受到诸如洋流等因素的影响, δ18O在一定程度上反映了生活史过程中平均水温情况的同时[32-34],也反映了其不同的生境履历过程。通过分析比较δ18O的含量, 可以很明显地发现所研究的刀鲚可能存在2个不同来源的组别(图1), 其中组一为CMJ13和–15; 而组二为 CMJ08、–09、–11、–12、–14。两组刀鲚耳石样品在 δ18O上的不同, 可能反映了其在所经历水体温度条件的不一样。由于所有实验鱼为同一时间长江口崇明水域的刀鲚幼鱼, 其所经历的水体温度的差异可能反映的是不同孵化场水域间的差异。这个现象显示出该两组刀鲚幼鱼个体极有可能起源自长江中不同的孵化场(亦可对应于亲鱼产卵场)水域。
通过上述 δ18O的结果, 推测所研究的刀鲚可能存在起源自不同孵化场的两组。比较所有耳石样品δ13C的情况, 虽然组内不同个体之间存在波动, 但组间的差异更为明显, 即总体上组一个体的 δ13C要高于组二(图1)。考虑到其与营养代谢之间的关系[35-36],以及所有个体均为发育阶段较一致的幼鱼个体, 不难发现两组个体间δ13C的差异很有可能与相应的饵料水平有关。Gao等[37]在研究美国太平洋沿岸黄眼石斑鱼耳石δ18O和δ13C的时候发现: 相对于较为稳定的δ18O, δ13C却在递增, 说明其在生活史过程中栖息地没有变化, 而食物发生了从低级向相对高级营养水平的改变。相似的结果在大西洋鳕鱼中也被发现[38]。由此推测, 本研究中两组样品 δ13C的差异可能是源自两个组别个体之间生活史过程中不同营养水平饵料组成的差异。这也支持基于上述δ18O结果将所有个体归为不同2组的推论。
由于本研究中所有刀鲚的耳石都被均一化成粉末样品来进行分析, 故所有数据反映的是所分析标本的整个生活史过程中的情况。造成本研究中刀鲚幼鱼耳石样品δ13C两组差异进一步的原因可以分为两种情况: 首先是不同孵化场饵料组成和丰度的差异。历史上在长江不同江段、通江湖泊均分布有刀鲚的产卵场[30]。虽然对其产卵场目前具体的分布现状不甚清晰, 但是根据本研究中关于耳石中 δ18O的结果依旧可以发现长江内尚存在有刀鲚的多个产卵场。而这些水域饵料丰度水平的差异势必也会影响到仔稚鱼的摄食从而导致耳石中δ13C的富集情况。如鄱阳湖年平均浮游动物密度 0.449 mg/L[39], 而长江镇江江段江豚保护区水域内最高浮游动物密度也仅 0.115 mg/L[40]。其次是不同孵化场所在长江江段地理位置上的不同, 从而导致两组个体到达长江口水域时间上的差异。随着刀鲚鱼苗的发育, 其需要离开孵化场沿长江进入河口水域, 这期间所需饵料也逐渐从最小的轮虫过渡到枝角类直至体积较大的桡足类[41]。由于幼鱼到达河口水域时发育阶段较其在孵化场要靠后, 也就意味着需要更高营养等级的饵料。这个过程中, 长江口水域营养盐和饵料生物最为丰富, 同时也是多种水生动物的仔稚鱼的栖息场所[42];特别是该水域的沿岸碎波带被证实为刀鲚仔稚鱼聚集的一个重要水域[43]。比较长江中下游的鄱阳湖、巢湖、太湖, 其浮游动物年平均密度最高的属太湖约2.14mg/L, 而最低为鄱阳湖约0.449mg/L[39]。与之相比, 长江口区浮游动物密度要高的多; 尤其在5月和8月, 浮游动物总生物量可分别达到 482.64mg/L和1002.65mg/L[42], 仔稚鱼在该水域能更加容易地获得所需要的更高营养水平的饵料。由此可见与孵化场饵料组成和丰度水平的不同对本研究中耳石样品δ13C的影响相比, 个体由于产卵场/孵化场距河口之间的距离差异而导致的进入长江口水域生活的时间差异对 δ13C的影响可能更为重要, 即距离河口较近的个体从孵化场出来后能够更早地到达河口附近的饵料生物丰富的水域。这一点也能说明为何δ13C较高的个体, 其全长却相对较短的原因。这些个体(组一)可能要比 δ13C 较低的个体(组二)孵化时间要晚,但是由于其孵化场较后者离开河口较近, 所以这些个体能够更早的到达河口水域。同时, 这种情况的存在也说明了不同产卵场刀鲚亲鱼在上溯时, 可能会由于产卵场的不同而存在分批上溯的现象。
综上所述, 本研究中长江口刀鲚幼鱼耳石 δ13C和 δ18O 个体间存在差异, 可以分为两个组, 可能起源自两个不同孵化场水域的群体。其中δ18O反映了两组个体之间生活史过程中所经历的环境积温的不同, 也即孵化场水温条件存在差异。而 δ13C则反映了两组个体在生活史过程中饵料组成条件上有所不同, 这一方面可能由于其孵化场水体饵料组成和丰度的差异, 另一个更重要的原因应该是由于孵化场地理位置的不同, 从而导致的幼鱼到达长江口时间上的差异。
本研究对刀鲚幼鱼耳石中δ13C和δ18O成分特征的探索, 不仅显示出了其在刀鲚起源水域和群体判别上的应用潜力, 也可为今后的深入研究打下了技术基础。在进一步的工作中有必要增加长江刀鲚标本数量, 以便为更详细地探寻资源群体中个体的起源情况。考虑到本研究的对象均为发育阶段较晚的幼鱼耳石, 其中除了有孵化场的信息(如水温和饵料)外, 还包含随后自孵化场到长江口移动过程的信息;故在今后进一步调查不同起源刀鲚群体孵化场水温、营养条件时, 需要优先选取发育阶段更早的仔稚鱼耳石或针对成鱼耳石核心区域(对应于孵化场)进行分析, 并采集长江刀鲚可能的产卵场(如鄱阳湖水域)、不同江段水样标本进行稳定同位素成分的同步测定。这将有可能较为准确地定位不同群体的起源地及了解各起源地个体对长江刀鲚资源群体的补充效应, 以便为更合理地保护长江刀鲚资源提供新依据。
致谢:感谢东京大学大气海洋研究所国际沿岸海洋研究中心的大竹二雄教授以及天野洋典博士在本研究中所提供的帮助和指导。
[1] 田思泉, 田芝清, 高春霞, 等.长江口刀鲚汛期特征及其资源状况的年际变化分析[J].上海海洋大学学报, 2014, 23(2): 245-250.
[2] 徐钢春, 魏广莲, 李建林, 等.基于线粒体 DNA D-loop 序列分析养殖刀鲚与湖鲚的遗传多样性[J].大连海洋大学学报, 2012, 27(5): 448-452.
[3] 徐钢春, 董晶晶, 聂志娟, 等.刀鲚不同组织的乳酸脱氢酶同工酶及 DNA 含量研究[J].上海海洋大学学报, 2012, 21(4): 481-488.
[4] Ma C Y, Cheng Q Q, Zhang Q Y.Genetic diversity and demographical history ofCoilia ectenes(Clupeiformes:Engraulidae) inferred from the complete control region sequences of mitochondrial DNA [J].Mitochondrial DNA, 2012, 23(5): 396-404.
[5] 周晓犊, 杨金权, 唐文乔, 等.基于线粒体 COI基因DNA条形码的中国鲚属物种有效性分析[J].动物分类学报, 2010, 35(4): 819-826.
[6] 王丹婷, 杨健, 姜涛, 等.不同水域刀鲚形态的分析比较[J].水产学报, 2012, 36(1): 78-90.
[7] 聂志娟, 徐钢春, 顾若波, 等.刀鲚幼鱼消化系统的组织形态学结构[J].动物学杂志, 2012, 47(4): 104-113.
[8] 姜涛, 杨健, 刘洪波, 等.刀鲚、凤鲚和湖鲚矢耳石的形态学比较研究[J].海洋科学, 2011, 35(3): 23-31.
[9] 程万秀, 唐文乔.长江刀鲚不同生态型间的某些形态差异[J].动物学杂志, 2011, 46(5): 33-40.
[10] 姜涛, 周昕期, 刘洪波, 等.鄱阳湖刀鲚耳石的两种微化学特征[J].水产学报, 2013, 37(2): 239-244.
[11] Jiang T, Yang J, Liu H B, et al.Life history ofCoilia nasusfrom the Yellow Sea inferred from otolith Sr: Ca ratios[J].Environ Biol Fish, 2012, 95(4): 503-508.
[12] Dou S Z, Amano Y, Yu X, et al.Elemental signature in otolith nuclei for stock discrimination of anadromous tapertail anchovy (Coilia nasus) using laser ablation ICPMS[J].Environ Biol Fish, 2012, 95(4): 431-443.
[13] Dou S Z, Yokouchi K, Yu X, et al.The migratory history of anadromous and non-anadromous tapertail anchovyCoilia nasusin the Yangtze River Estuary revealed by the otolith Sr: Ca ratio[J].Environ Biol Fish, 2012, 95(4): 481-490.
[14] Yang J, Arai T, Liu H B, et al.Reconstructing habitat use ofCoilia mystusandCoilia ectenesof the Yangtze River estuary, and ofCoilia ectenesof Taihu Lake,based on otolith strontium and calcium[J].J Fish Biol,2006, 69(4): 1120-1135.
[15] Brown R J, Severin K P.Otolith chemistry analyses indicate that water Sr: Ca is the primary factor influencing otolith Sr: Ca for freshwater and diadromous fish but not for marine fish[J].Can J Agr Sci, 2009, 66(10): 1790-1808.
[16] Arai T, Goto A, Miyazaki N.Migratory history of the threespine sticklebackGasterosteus aculeatus[J].Ichthyol Res, 2003, 50(1): 9-14.
[17] Arai T, Tsukamoto K.Application of otolith Sr : Ca ratios to estimate the migratory history of masu salmon,Oncorhynchus masou[J].Ichthyol Res, 1998, 45(3):309-313.
[18] Lamson H M , Shiao J C , Iizuka Y, et al.Movement patterns of American eels (Anguilla rostrata) between salt- and freshwater in a coastal watershed, based on otolith microchemistry[J].Mar Biol, 2006, 149(6):1567-1576.
[19] 熊瑛, 刘洪波, 刘培廷, 等.基于耳石元素微化学的江苏吕泗近岸小黄鱼生境履历重建[J].应用生态学报, 2014, 25(3): 836-842.
[20] Campana S E.Otolith science entering the 21st century[J].Mar Freshwater Res, 2005, 56: 485-495.
[21] Thorrold S R, Latkoczy C, Swart P K, et al.Natal homing in a marine fish metapopulation[J].Science,2001, 291(5502): 297-299.
[22] Schwarcz H P, Gao Y W, Campana S E, et al.Stable carbon isotope variations in otoliths of Atlantic cod(Gadus morhua) [J].Can J Fish Aquat Sci, 1998, 55(8):1798-1806.
[23] 高永文, 鲁安怀, 王清印, 等.鱼群识别的氧、碳稳定同位素方法[J].矿物岩石地球化学通报, 2011,30(3): 270-276.
[24] Tomida Y, Suzuki T, Yamada T, et al.Differences in oxygen and carbon stable isotope ratios between hatchery and wild pink salmon fry [J].Fish Sci, 2014,80: 273-280.
[25] Geffen A J.Otolith oxygen and carbon stable isotopes in wild and laboratory reared plaice (Pleuronectes platessa) [J].Environ Biol Fish, 2012, 95: 419-430.
[26] Gao Y W, Sones D B, Svec R A.The hatchery and native origin of lake ozette sockeye salmon from stable isotopic records of otoliths [J].Am Fish Soc Symp,2007, 54: 105-115.
[27] Shen J Z, Gao Y W.Stable isotope analyses in otoliths of silver carp: a pilot study in identification of natal sources and stock differences [J].Environ Biol Fish,2012, 95(4): 445-453.
[28] Schloesser R W, Neilson J D, Secor D H, et al.Natal origin of Atlantic bluefin tuna (Thunnus thynnus) from Canadian waters based on otolith δ13C and δ18O [J].Can J Fish Aquat Sci, 2010, 67(3): 563-569.
[29] 高永文, 鲁安怀, 宋玉国.鱼耳石的碳、氧稳定同位素成分研究[J].自然科学进展, 2004, 14(3): 268-272.
[30] 袁传宓, 秦安舲, 刘仁华, 等.关于长江中下游及东南沿海各省的鲚属鱼类种下分类的探讨[J].南京大学学报(自然科学版), 1980, 3: 67-77.
[31] 张敏莹, 徐东坡, 刘凯, 等.长江下游刀鲚生物学及最大持续产量研究[J].长江流域资源与环境, 2005,14(6): 694-698.
[32] Matta M E, Orland I J, Ushikubo T, et al.Otolith oxygen isotopes measured by high-precision secondary ion mass spectrometry reflect life history of a yellowfin sole (Limanda aspera) [J].Rapid Commun Mass Spectrom, 2013, 27(6): 691-699.
[33] Javor B, Dorval E.Geography and ontogeny influence the stable oxygen and carbon isotopes of otoliths of Pacific sardine in the California Current [J].Fish Res,2014, 154: 1-10.
[34] Kitagawa T, Ishimura T, Uozato R, et al.Otolith δ18O of Pacific bluefin tunaThunnus orientalisas an indicator of ambient water temperature [J].Mar Ecol Prog Ser, 2013, 481: 199-209.
[35] Nelson J, Hanson C W, Koenig C, et al.Infulence of diet on stable carbon isotope composition in otoliths of juvenile red drumSciaenops ocellatus[J].Aquat Biol,2011, 13(1): 89-95.
[36] Gronkijaer P, Pedersen J B, Ankjaero T T, et al.Srable N and C isotopes in the organic matrix of fish otoliths:validation of a new approach for studying spatial and temporal changes in the trophic structure of aquatic ecosytems [J].Can J Fish Aquat Sci, 2013, 70(2): 143-146.
[37] Gao Y W, Dettman D L, Piner K R, et al.Isotopic correlation (δ18O versus δ13C) of otoliths in identification of groundfish stocks[J].T Am Fish Soc,2010, 139: 491-501.
[38] Schwarcz H P, Gao Y W, Campana S E, et al.Stable carbon isotope variations in otoliths of cod (Gadusmorhua) [J].Can J Fish Aquat Sci, 1998, 55: 1798-1806.
[39] 杨富亿, 刘兴土, 赵魁义, 等.鄱阳湖的自然渔业功能[J].湿地科学, 2011, 9(1): 82-89.
[40] 代梨梨, 龚迎春, 冯伟松, 等.江苏镇江长江豚类保护区浮游动物群落结构特征及江豚生存状况评估[J].水生态学杂志, 2011, 32(5): 30-36.
[41] Xu G C, Tang X, Zhang C X, et al.First studies of embryonbic and larval development ofCoilia nasus(Engraulidae) under controlled conditions[J].Aquac Res, 2010, 42(4): 593-601.
[42] 徐兆礼, 沈新强.长江口水域浮游动物生物量及其年间变化[J].长江流域资源与环境, 2005, 14(3):282-286.
[43] 蒋日进, 钟俊生, 张冬良, 等.长江口沿岸随波带仔稚鱼的种类组成及其多样性特征[J].动物学研究,2009, 29(3): 297-304.
——以泉吉河为例

