早期食管癌内镜下手术后接受食管切除的比较分析
张杰 陈海泉,3 相加庆 张亚伟 黄洋乐 陈苏峰 王胜飞王瑞 James Luketich
早期食管癌内镜下手术后接受食管切除的比较分析
张杰1,2陈海泉1,2,3相加庆1,2张亚伟1,2黄洋乐1,2陈苏峰1,2王胜飞1,2王瑞1,2James Luketich4
目的 探讨早期食管癌患者行内镜下切除术(ER)后是否需要二次行食管癌根治术的影响因素。方法 选择2011年6月至2014年3月在复旦大学附属肿瘤医院胸外科收治的经ER手术治疗的早期食管癌患者,根据是否继续行食管癌根治术分组并随访,对食管癌根治术后未见癌残留的病例进行包括浸润深度(T分期)、病灶长度(<3 cm或≥3 cm)、病灶位置(上、中、下段)、分化程度以及有无淋巴管脉管侵犯的相关性统计分析,统计学方法采用χ2检验。结果 共有88例患者术前检查和分期提示为早期食管癌患者接受ER术,再次行食管癌根治术有22例(25.0%),其中7例(31.8%)最终病理未见肿瘤残留。统计学分析显示:ER病灶浸润深度(T0-1a期或T1b期以上)对于是否需行二次根治术具有预测作用(χ2=8.56,P=0.005),而病灶长度、位置、分化程度以及有无淋巴管脉管侵犯未见明显影响(χ2=1.89,P=0.361;χ2=3.01,P=0.165;χ2=3.85,P=0.121;χ2=1.02,P=1.000)。结论根据ER术后的病理结果:T0-1a且切缘为阴性的患者,食管切除多能避免;而T1a以上,特别是内镜黏膜下剥离术(ESD)中黏膜下注射亚甲蓝抬举不满意或内镜下黏膜切除术(EMR)圈套不满意者,推荐行食管癌根治术。对于贲门处的早期癌,ER手术的选择要慎重。
内镜下手术; 早期食管癌; 食管癌根治术
内镜治疗技术近十年来发展迅速[1]。在我国,食管内镜下切除术(endoscopic resection,ER)包括内镜下黏膜切除术(endoscopic mucosal resection,EMR)和内镜黏膜下剥离术(endoscopic submucosal dissection,ESD),多由消化内科医师或内镜室医师开展,如出现穿孔等并发症,则需要胸外科医师参与。而在西方国家,这一技术多由胸外科医师开展。ER由胸外科医师开展具有以下优势:第一,对于已经明确诊断为食管恶性肿瘤的患者,胸外科医师熟悉食管切除术和内镜治疗两者的优缺点,能够根据患者的具体情况(如肿瘤的大小、位置、浸润深度,以及患者的一般情况和主观意愿等),选择个体化符合肿瘤治疗原则的治疗方案,严格把握内镜下治疗的指证[2];第二,对于临床上高度怀疑食管癌的患者,但普通消化内镜检查由于活检大小的束缚不能提供明确病理学证据的,胸外科医师可通过EMR取得大块组织明确病理,从而可以行食管癌根治术或放疗和化疗,如术中冰冻能够明确,还可以选择一期手术[3];第三,最为重要的是,若分期发现肿瘤是T1b期以上,或一旦内镜治疗术中或术后出现食管穿孔或消化道瘘,外科医师可以及时更改治疗策略,进行外科干预[4]。
胸外科医师同时开展ER和食管切除,具有“头对头”的比较资料,本文探讨ER术根治早期食管恶性肿瘤的可能性,分析哪些患者可以避免食管切除,并寻找必要行二次食管根治术的相关因素。目前国内外文献还未见相关报道。
资料与方法
一、临床资料
选择2011年6月至2014年3月,复旦大学附属肿瘤医院胸外科收治的食管早期病变患者,术前检查和分期采用的手段包括消化内镜检查并活检、超声内镜(endoscopic ultrasonography,EUS)、胸部CT、超声和食管造影等。患者术前均行常规消化内镜检查并活检,若为外院消化内镜活检病理切片,则均要求至复旦大学附属肿瘤医院病理科行病理会诊,以会诊报告为最终消化内镜活检病理报告。随访采用电话、门诊复查等方式进行,随访时间截止至2014年7月。随访采用胸部CT、超声和胃镜,内容包括ER术后复发的情况、接受进一步治疗的情况(是否接受二次食管癌根治术)等。
二、ER手术
ER手术包括新型EMR和ESD,本研究使用Olympus 180型号的高清内镜和窄带成像术(narrow band imaging,NBI)。新型EMR使用新型多环黏膜切除器 DT-6(Duette Multiband Mucosectomy kit,Cook Medical,Bloomington,IN),需重叠切除,以保证切除的完整性。ESD使用T型刀或VS刀,爱尔博海博刀系统,内镜下专用切割模式即内镜下电切/电凝(ENDO CUT IQ)[5-6]。切除病灶前,先用NBI观察病灶,在ER手术的创面上做上下内外活检作为外周切缘,当标本和创面切缘均为阴性时定义为R0切除。内镜切除标本至少需要两名不同的病理科医师(其中一位为专科病理医师)按照WHO标准进行组织学评估,内容包括浸润深度、分化程度、有无淋巴管脉管侵犯等。
三、食管切除方式
食管切除的方式包括开放Ivor-lewis两切口两野、左胸一切口、食管拔脱术和微创食管切除术,其中微创食管切除术又包括腹腔镜联合胸腔镜下Ivor-Lewis食管癌根治术、腹腔镜联合胸腔镜+左颈吻合以及Hybrid手术(单纯胸腔镜+开腹或单纯腹腔镜+开胸)。
四、统计学处理
采用统计学软件SPSS 16.0对数据进行分析处理。分类资料包括病灶浸润深度(T分期)、长度(<3 cm或≥3 cm)、位置(上、中、下段)、分化程度以及有无淋巴管脉管侵犯,组间比较采用χ2检验。P<0.05表示差异有统计学意义。
结果
一、ER术后再次行食管癌根治术患者一般资料
本研究中共有88例术前检查和分期提示为早期食管癌的患者接受了ER术,图1为NBI观察到的早期食管癌,与周围病灶具有明显分界。再次行食管癌根治术22例(25.0%),其中7例(31.8%)最终病理未见肿瘤残留。22例患者中10例选择了腔镜微创手术(图2),另外12例选择了常规的开放手术(图3)。11例患者进行食管癌根治术时,发现部分胸腔粘连,可能系ER手术后的反应,用超声刀较容易分离。平均清扫淋巴结数目15枚,22例中2例(9.1%)患者有淋巴结转移。最终病理结果显示:2例为低分化,3例为中低分化,14例为中分化,3例为中高分化。有4例患者接受贲门癌根治术后都有肿瘤残留。未发生由于ER手术的严重并发症(如穿孔等)而需要切除食管的病例。
二、ER诊断为早期食管癌未行根治术患者随访资料
同期未行食管癌根治术的66例早期食管癌患者(包括高级别上皮内瘤变和T1期患者)行ER手术(均为R0切除,切缘为阴性)后进行随访(图4,5),有2例患者(3.0%)出现了局部复发,其中1例在外院行食管切除术,另1例选择放疗,未出现远处转移和死亡病例。
三、二次食管癌根治术的影响因素
对本组研究中行二次食管癌根治术的22例患者ER病灶的浸润深度、长度、位置、分化程度以及有无淋巴管脉管侵犯进行统计学分析,结果显示: ER病灶的浸润深度(T0-1a或T1b以上)对于是否需行二次根治术具有预测作用(χ2=8.56,P= 0.005),而病灶长度、病灶位置、分化程度以及有无淋巴管脉管侵犯未见明显影响(χ2=1.89,P= 0.361;χ2=3.01,P=0.165;χ2=3.85,P=0.121;χ2=1.02,P>1.000,表1)。
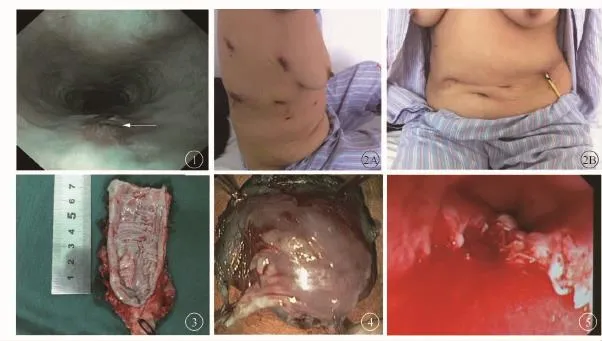
图1 NBI模式下观察食管早期癌,箭头示病灶部位呈现“褐色”表现,与周围正常黏膜具有明显分界,深层血管不能显示图2 早期食管癌患者ER术后行全腔镜食管癌根治术。2A为胸部切口;2B为腹部切口 图3 内镜下切除后早期食管癌患者接受食管癌根治术(箭头所指为ER后的创面) 图4 早期食管癌患者ESD切除后的标本 图5 早期食管癌患者ER切除后的创面,可见食管肌层显露
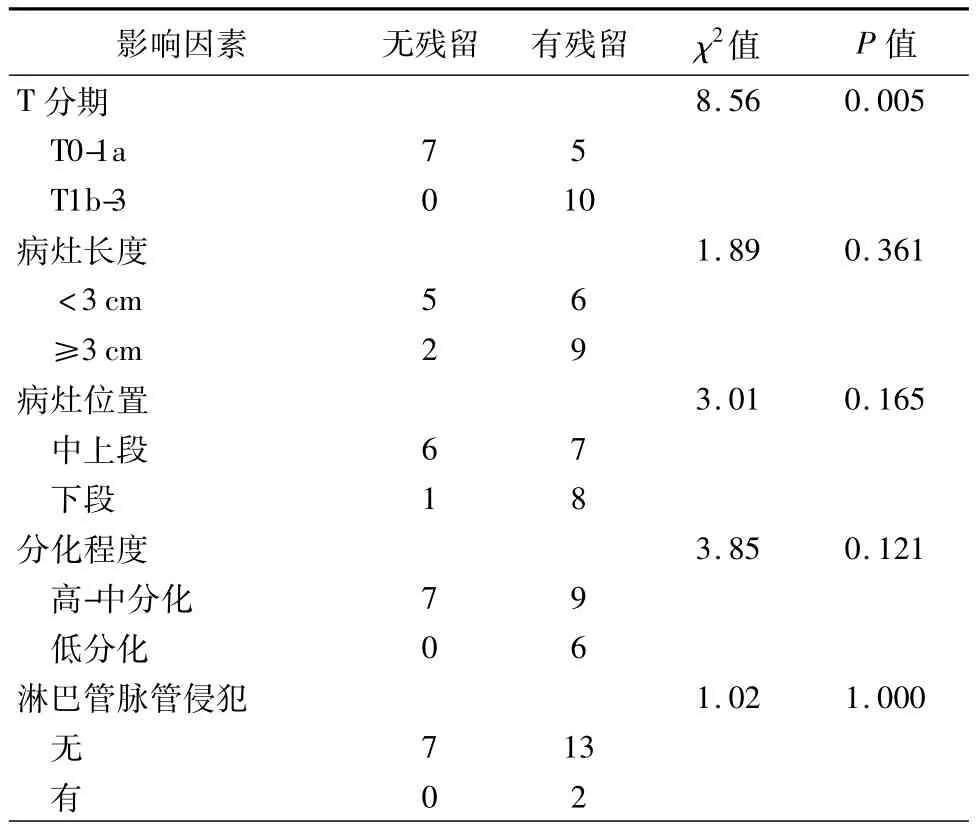
表1 行ER术早期食管癌患者二次根治术的影响因素(例)
讨论
近些年,肿瘤治疗的最新理念是在注重疗效的同时,更加注重患者的生存质量。因此,各种小切口和无切口的手术越来越受到肿瘤外科医师的青睐。随着消化内镜的普及和各种染色放大内镜的应用,消化道肿瘤尤其是早期癌肿瘤的发现迅速增多。对于食管癌前期病变、早期癌和黏膜下肿瘤,传统的治疗方法是外科手术切除,疗效确切但手术创伤大,患者恢复慢、住院时间长、治疗费用高、术后生活质量也大为降低。随着内镜治疗器械的不断开发和新技术的逐步开展,近年来食管镜下外科手术得到了飞速发展[7-9]。在美国,来自流行病学随访和最终结果数据库(Surveillance,Epidemiology and End Results,SEER)的资料显示,T1N0食管癌的内镜下治疗从1998年的8.1%上升到2008年的24.1%(P<0.001),内镜下治疗与食管切除的5年生存率是相似的,而内镜下治疗的癌症相关生存率甚至高于食管切除组[10]。
复旦大学附属肿瘤医院胸外科率先在国内胸外科领域开展内镜下切除术,胸外科医师既能开展内镜手术,也能进行食管切除手术,在选择治疗模式时就能避免偏移,使患者利益最大化。目前已经积累了一定数量的病例,并根据这些资料对内镜下切除术和食管切除术进行“头对头”的比较研究。
最近Bergeron等[11]报道,与食管切除术相比较,EUS对于早期食管癌的准确分期还存在明显的缺陷与不足,敏感度与特异度都不高,准确的病理分期还有赖于食管切除术。根据我们在临床实践中的体会,EUS对于食管癌的分期准确性依赖于操作者的经验。而本研究提示:ER手术对于高级别上皮内瘤变和T1a患者的分期是准确的;而对于存在危险因子的内镜手术后患者,食管癌根治术才能达到最精确的病理分期。
本研究中,接受ER术后有22例(25.0%)患者又进一步接受了食管癌根治术。分析其原因: (1)存在危险因子,包括肿瘤长度≥3 cm,分期为T1b以上,周径超过1/2圈,分化差,有淋巴管脉管侵犯(lymphocytes vascular invasion,LVI)阳性,四周切缘阳性。(2)根据病灶浸润深度诊断分期为T1a,肿瘤长径<3 cm,但患者强烈希望切除食管。(3) ER术后随访过程中出现复发,患者拒绝再次行ER治疗。本研究中没有因为ER术后严重并发症而进行的食管切除术,说明采用ER对术前诊断为早期食管癌的治疗还是非常安全的。
早期食管癌行ER术后,有的患者由于自身担心或存在高危因素,最终选择了食管切除。对于ER术后哪些患者可以免除食管切除,我们的经验是: (1)ER手术提示食管癌T分期诊断为T0-1a、切缘为阴性的患者,多不必进行食管切除术。(2)食管癌T分期诊断为T1b以上,特别是ESD术中食管黏膜下注射亚甲蓝后黏膜抬举不满意,或EMR圈套不满意的患者,临床上判断在T1b期以上,推荐其进行食管癌根治术。(3)贲门处的早期癌由于病变范围较难判断或ER手术容易出血等原因,选择进行ER手术时要谨慎,往往需要进行食管癌根治术,以防止ER术后的肿瘤残留。
未来,我们还要比较食管切除与非手术治疗哪一种处理方式更能使ER术后提示T1b期的患者获益。另外,近几年,特别在美国,发现食管射频消融和冷冻治疗结合内镜下的切除获得了比单纯内镜下切除更好的效果,我们将进一步研究这种联合治疗的模式是否能提高中国早期食管鳞癌患者内镜下手术治疗的效果[12]。
1 Pech O,May A,Manner H,et al.Long-term efficacy and safety of endoscopic resection for patients with mucosal adenocarcinoma of theesophagus[J].Gastroenterology,2014,146(3):652-660.
2 Tian J,Prasad GA,Lutzke LS,et al.Outcomes of T1b esophageal adenocarcinoma patients[J].Gastrointest Endosc,2011,74(6): 1201-1206.
3 dTae HJ,Lee HL,Lee KN,et al.Deep biopsy via endoscopic submucosal dissection in upper gastrointestinal subepithelial tumors: a prospective study[J].Endoscopy,2014,46(10):845-850.
4 张裔良,张杰,陈海泉,等.新型多环黏膜切除器在食管内镜下手术的初步应用[J].中国癌症杂志,2013,(7):530-534.
5 Homma K,Otaki Y,Sugawara M,et al.Efficacy of novel SB knife Jr examined in amulticenterstudyon colorectalendoscopic submucosal dissection[J].Dig Endosc,2012,24(s1):117-120.
6 Monnier P,Jaquet Y,Radu A,et al.Extensive(8 to 12 cm2) noncircumferential endoscopic mucosal resection for early esophageal cancer[J].Ann Thorac Surg,2010,89(6):S2151-S2155.
7 Higuchi K,Tanabe S,Azuma M,et al.A phase II study of endoscopic submucosal dissection for superficial esophageal neoplasms(KDOG 0901)[J].Gastrointest Endosc,2013,78(5): 704-710.
8 Watson TJ.Endoscopic therapies for Barrett’s neoplasia[J].J Thorac Dis,2014,6(Suppl 3):S298.
9 Lewis JJ,Rubenstein JH,Singal AG,et al.Factors associated with esophageal stricture formation after endoscopic mucosal resection for neoplastic Barrett’s esophagus[J].Gastrointest Endosc,2011,74 (4):753-760.
10 Berry MF,Zeyer-Brunner J,Castleberry AW,et al.Treatment modalities for T1N0 esophageal cancers:a comparative analysis of local therapy versus surgical resection[J].J Thorac Oncol,2013,8 (6):796-802.
11 Bergeron EJ,Lin J,Chang AC,et al.Endoscopic ultrasound is inadequate todeterminewhich T1/T2 esophagealtumorsare candidates for endoluminal therapies[J].J Thorac Cardiovasc Surg,2014,147(2):765-773.
12 Gosain S,Mercer K,Twaddell WS,et al.Liquid nitrogen spray cryotherapy in Barrett’s esophagus with high-grade dysplasia:longterm results[J].Gastrointest Endosc,2013,78(2):260-265.
Comparative analysis of esophagectomy after endoscopic resection in early stage esophageal cancer
Zhang Jie1,2,Chen Haiquan1,2,3,Xiang Jiaqing1,2,Zhang Yawei1,2,Huang Yangle1,2,Chen Sufeng1,Wang Shengfei1,2,Wang Rui1,2,James Luketic43.1Department of Thoracic Surgery,Shanghai Cancer Hospital,Fudan University,Shanghai 200032,China;2Department of Oncology,Shanghai Medical College,Shanghai 200032,China;3Department of Thoracic Surgery,Shanghai Chest Hospital,Shanghai Jiao Tong University,Shanghai 200030,China;4Department of Cardiothoracic Surgery,University of Pittsburgh Medical Center,Pittsburgh,15213,USA
Chen Haiquan,Email:hqchen1@yahoo.com
Objective The aim of this study is to investigate the related factors indicating necessarily second esophagectomy after the treatment of endoscopic resection(ER)in early stage of esophageal cancer.Methods From June 2011 to March 2014,the data of patients with early stage esophageal cancer treated with ER were prospectively collected from the Department of Thoracic Surgery of Shanghai Cancer Hospital.Patients with or without further esophagectomy were followed up,and statistical analysis was carried out based on the factors including the depth of invasion(T grade),the depth of invasion of ER lesion(T0-1a or beyond T1a),the length of lesion(<3 cm or≥3 cm),the location of tumor(upper,middle or lower),the degree of differentiation,and with or without lymph vascular invasion among patients without tumor residual after esophagectomy.Results Eighty-eight patients with early stage esophageal cancer indicated by preoperative examination and staging underwent ER surgery,and 22(25.0%)of them received further esophagectomy,among whom 7(31.8%)had notumor residual according to the final pathological reports.Statistical analysis showed that the invasive depth of ER lesion(T0-1a or above T1b)was a predicting factor which could indicate whether the patient need further radical surgery or not(χ2=8.56,P=0.005),while that had no significant effect on the length of lesion,location of lesion,differentiation degree and lymphatic vessel invasion(χ2=1.89,P=0.361;χ2=3.01,P=0.165;χ2=3.85,P=0.121;χ2=1.02,P=1.000).Conclusions Patients with lesions at stage T0-1a and negative surgical margin based on the pathological results can probably avoid esophagectomy after ER.While those beyond T1a stage,especially those with dissatisfaction about ESD mucosal protrusion after submucous injection with Methylene blue or endoscopic mucosal resection(EMR)mucosal trap,were recommended for esophagectomy.As for early stage cardia cancer,it should be very cautious when choosing to perform ER surgery.
Endoscopic resection; Early stage esophageal cancer; Esophagectomy
2015-01-13)
(本文编辑:周珠凤)
10.3877/cma.j.issn.2095-8773.2015.01.007
200032 上海,复旦大学附属肿瘤医院胸外科1,复旦大学上海医学院肿瘤学系2;200030 上海交通大学附属胸科医院胸外科3;15213 美国匹兹堡大学胸心外科4
陈海泉,hqchen1@yahoo.com
张杰,陈海泉,相加庆,等.早期食管癌内镜下手术后接受食管切除的比较分析[J/CD].中华胸部外科电子杂志,2015,1 (1):35-39.

