纳米(Er3+-Gd3+)/TiO2光催化性能的研究
刘丽静
(包头师范学院 化学学院,内蒙古 包头 014030)
随着工业的快速发展,伴随而来的是日益严重的污染问题,可持续发展的绿色、环保、低碳生活成为人类追求和向往的目标。在各种环境问题中,大多与水污染问题息息相关,且印染废水占很大比重。半导体光催化技术因其快速性、稳定性、无二次污染等优点有很大的发展前景。TiO2因其独特的物理化学性能,在催化、光催化、电催化和太阳能电池方面有很高的应用价值[1]。针对TiO2光催化材料量子效率低和光响应范围窄等缺陷,人们研究出很多种改性方法来提高TiO2的光催化性能。离子掺杂是提高TiO2光催化活性、拓展其光响应范围的一种有效手段[2],将稀土离子引入到TiO2晶格中,因其具有独特的4f电子构型在其晶格中引入新电荷、形成缺陷或改变晶格类型,调整其分布状态,影响光生电子和空穴的运动状况、调整其分布状态或者改变TiO2的能带结构,最终导致TiO2的光催化活性发生改变。文献[3]研究了镧系掺杂对TiO2的微结构和光催化活性的影响,证明稀土掺杂能够提高活性,但有关稀土共掺杂的研究较少。
TiO2光催化采用紫外光照射[4],操作复杂,成本高。本实验将稀土Er3+、Gd3+共掺杂对纳米TiO2催化剂进行改性,通过降解孔雀石绿有机染料来测试样品的催化性能,加入助催化剂双氧水,降低基元反应的活化能,使反应更易进行,使催化剂在无光源照射、不需通入氧气条件下,常温常压下就能降解有机染料,且时间短见效快。
1 实验
1.1 超声波法制备纳米(Er3+-Gd3+)/TiO2
用浓硝酸溶解氧化铒、氧化钆,配制成0.1mol/L稀土硝酸盐溶液,其中Er3+、Gd3+摩尔分数各占50%。取适量该溶液和TiO2粉体(AR)混合,使(Er3+-Gd3+)在TiO2中的摩尔分数分别为0%、0.1%、0.2%、0.5%、1.0%、2.0%、5.0%,将其放入锥形瓶中加入适量蒸馏水,在KQ-250B超声波清洗器中连续震荡40min,促进非均相界面的扰动和相界面更新,从而加速界面间的传质和传热过程进行充分混合。然后将其转移至烧杯中,放入208电热恒温干燥箱中,将温度调到100℃烘干,用研钵将其研成细碎的粉末,装入坩埚中。将样品放入型号5RJX4-13马弗炉中进行烧结,500℃煅烧2h,待样品降至室温后取出,再次研磨。按照上述方法配制(Er3+-Gd3+)摩尔分数为5.0%的样品等量,干燥研磨后分成4等份,分别在450、550、600、650℃下煅烧,到达目标温度后恒温2h,再次研磨。由此制出500℃不同稀土掺杂量的催化剂和450、500、550、600、650℃不同温度煅烧的催化剂,以考察稀土掺杂量和温度对催化剂性能的影响。
1.2 纳米(Er3+-Gd3+)/TiO2催化剂的表征
采用XD-3全自动多晶X-Ray衍射仪表征样品的组成、结构、晶体的物相;利用傅里叶红外分析仪IR PRESTIGE-21(CE),将样品与标准品进行光谱比较,2个光谱中的峰与峰的相互对照可以为结构鉴定提供依据,进而判断出特征官能团,测定粉末样品表面的成键及表面吸附情况;采用S-3400N扫描电子显微镜(SEM)测试样品的粒径大小。
1.3 纳米(Er3+-Gd3+)/TiO2光催化活性的测定
配制10mg/L孔雀石绿溶液,取100mL,加入(Er3+-Gd3+)/TiO2催化剂0.1g,再加入0.5mL30%H2O2,实验室中无灯源照射,常温常压不需通氧条件下,把溶液放在90-2型恒温磁力搅拌器上,以一定的速度进行搅拌。每20min取反应液8mL放入TD5Z型台式低速离心机,以3 500r/min分离10min,然后用YIS-7220型分光光度计测定孔雀石绿溶液在最大吸收波长616nm处的吸光度,取上清液测定其吸光度,用蒸馏水做参比液,溶液降解率的计算公式为:

其中,η为溶液降解率;A0、A分别为孔雀石绿溶液在初始和t时刻的吸光度。
以降解率为依据,对不同稀土掺杂量、不同煅烧温度的(Er3+-Gd3+)/TiO2进行光催化性能测试。
2 结果与分析
2.1 纳米(Er3+-Gd3+)/TiO2的结构表征
2.1.1 SEM表征
不同摩尔分数下(Er3+-Gd3+)/TiO2的SEM如图1所示。

图1 不同摩尔分数下样品的SEM照片
从图1可以看出,样品以颗粒状堆积在一起,当(Er3+-Gd3+)的摩尔分数为0时,样品平均粒径为 100nm,当(Er3+-Gd3+)的摩尔分数为5.0%时,样品平均粒径为60nm,因此稀土Er3+-Gd3+的掺杂能够明显细化晶粒,增大催化剂的表面积,提高催化活性;有少量片状物出现,是样品煅烧时出现的团聚现象,符合锐钛矿是层状晶体的理论。当催化剂粒子尺寸下降到和载流子德布罗意波长相当时,费米能级附近电子能级变得离散或能隙会变宽,从而会出现量子尺寸效应[5],引发的光生电子和空穴分别具有更高的负电势和正电势,将会导致光生电子和空穴的氧化还原能力增强,谱带蓝移,从而提高催化剂的氧化还原能力[6]。
2.1.2 XRD的表征
煅烧温度为500℃,不同摩尔分数的(Er3+-Gd3+)/TiO2粉体样品的XRD图谱如图2所示。

图2 不同摩尔分数下样品的XRD图
由图2可看出,波峰尖锐,说明结晶完好。在2θ为 25.289°、36.865°、37.862°、38.629°、48.134°、53.859°、55.158°、62.802°、68.782°、70.315°、74.940°处有较为明显的特征吸收峰,与标准卡片JCPDS NO.21-1271锐钛矿型 TiO2的特征吸收峰基本一致,说明该样品的晶型为锐钛矿[7]。随着稀土掺杂量的增多,波峰强度降低且宽化,说明晶粒尺寸减小,稀土掺杂能抑制晶粒长大,与SEM 分析一致。随着稀土(Er3+-Gd3+)掺杂量的增大,当x=5.0% 时,在2θ为28.441°、33.812°时出现了氧化稀土的波峰,说明稀土以氧化物的形式掺杂在 TiO2中,而稀土(Er3+-Gd3+)掺杂量较少时未能检测出。当(Er3+-Gd3+)摩尔分数增加时,晶粒减小,(Er3+-Gd3+)的掺杂对纳米TiO2在高温下发生的烧结(颗粒增大)有强烈的抑制作用。主要是因为掺入的(Er3+-Gd3+)部分阻隔了TiO2颗粒间的界面,提高了TiO2颗粒相互间扩散的势垒,从而有效抑制了在高温条件下纳米TiO2晶粒的增长。纳米微粒尺寸小、表面能高,位于表面的原子占相当大的比例。稀土(Er3+-Gd3+)掺杂能够细化晶粒,催化剂的粒径越小,单位质量催化剂的表面原子数越多,反应活性中心数越多,有利于光催化反应在表面上进行,因而光催化反应速率和效率都相应地有所提高。
2.1.3 FT-IR的表征
不同摩尔分数下(Er3+-Gd3+)/TiO2的红外图谱如图3所示。由图3可知,3 761.49cm-1处的吸收峰为TiO2表面吸附的—OH的伸缩振动峰,2 358.27cm-1处为 TiO2的特征吸收峰[8],1 090.40cm-1是晶体的Ti—O键的伸缩振动和变角振动峰,则690.21cm-1的吸收峰为TiO2晶体表面的Ti—O键的伸缩振动;在x=0.1%和x=5.0%的图上3 428.61cm-1处出现一个由O—H伸缩振动引起的吸收峰,说明稀土掺杂后样品能够更好地吸附O—H,强氧化性的羟基自由基可以降解的目标物质至完全分解生成CO2、H2O等小分子,所以稀土Er、Gd掺杂能提高样品的催化活性[9]。在x=5.0%的图谱中583.26cm-1和 478.99cm-1处出现了微弱的Er—O和Gd—O稀土氧化物吸收峰,与XRD分析一致。

图3 不同摩尔分数下(Er3+-Gd3+)/TiO2的红外图谱
2.2 纳米(Er3+-Gd3+)/TiO2光催化性能
2.2.1 Er3+、Gd3+掺杂量对光催化性能的影响
质量浓度为10mg/L孔雀石绿溶液最大波长为616nm,测得其吸光度为1.121,依据(1)式,由吸光度可得降解率。不同摩尔分数下(Er3+-Gd3+)/TiO2降解孔雀石绿的降解率如图4所示,由图4可知,随着稀土掺杂量的增加,制备出的催化剂的催化活性越强,孔雀石绿的降解速率越大。本实验中,在500℃ 煅烧x=5.0%的催化剂的催化性能最佳。实验室中无灯源照射、常温常压、不需通氧条件下,每100mL孔雀石溶液中催化剂用量为0.1g,加入0.5mL 30%H2O2,降解时间为80min时,其降解率已达100%,而无稀土掺杂的催化剂其降解率仅为40%。这是由于稀土Er3+、Gd3+离子掺杂后,更容易与羟基自由基键合[10],使TiO2表面能量壁垒提高,从而抑制催化剂表面电子-空穴对的复合,使其光催化活性增大[11];另一方面是由于稀土掺杂的样品粒径减小,表面面积增大,提供更多的活性位,提高催化性能,与SEM和红外分析结果一致。

图4 不同摩尔分数下样品降解孔雀石绿的降解率
2.2.2 煅烧温度对光催化性能的影响
Er3+-Gd3+的摩尔分数为5.0%,在450、500、600、650℃煅烧温度下样品降解孔雀石绿的降解曲线如图5所示。
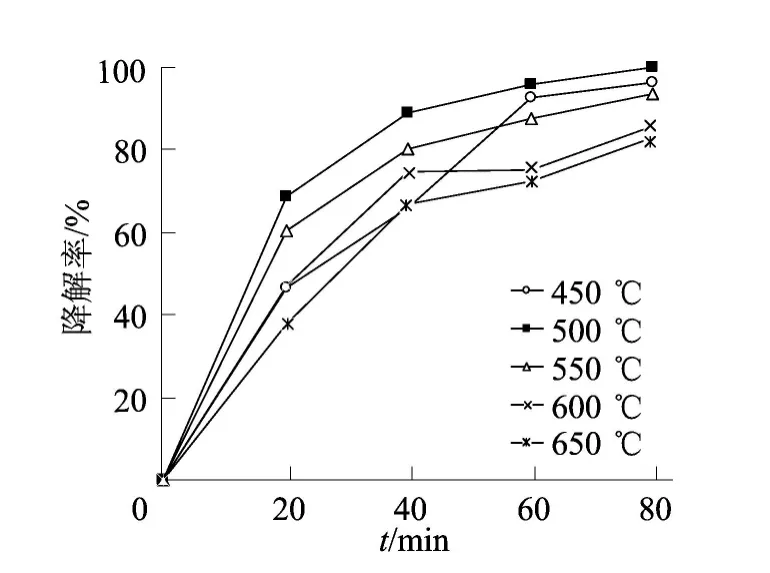
图5 不同煅烧温度下样品降解孔雀石绿的降解率
从图5可见,在500℃煅烧2h的样品催化活性明显高于600℃ 和650℃ 煅烧的催化剂,略高于450℃和550℃煅烧的催化剂。煅烧的作用是使样品由无定型态转化到晶型态,晶型的TiO2比无定型的TiO2活性高,不同温度煅烧催化性能不同,这是因为晶粒大小和结晶度与热处理温度有关,在400℃ 煅烧时,样品晶化还不完全,但当温度过高时,有烧结团聚现象,减少催化剂表面积,从而导致光催化活性反而降低,与SEM分析结果一致。稀土掺杂对TiO2晶型转变温度有很大的影响[12],温度升高有利于金红石相的形成[13],一般情况下纯的TiO2在550℃ 时开始出现锐钛矿相,当温度升高至750℃ 时完全转变为金红石型,锐钛矿比金红石相催化效果更好。
3 结论
本文采用超声波法制备稀土Er3+、Gd3+的共掺杂纳米TiO2的方法操作简单,工艺周期短,生产成本低;稀土 Er3+、Gd3+的共掺杂能细化晶粒,吸附更多的羟基,从而提高催化活性;加入助催化剂H2O2,使催化反应在无灯源照射下就能进行,因为TiO2在光催化过程,基元反应中有H2O2的生成,所以H2O2能够降低基元反应的活化能[14-16]。H2O2是强氧化剂,具有捕获电子的能力,能有效抑制电子-空穴的复合,使反应更易进行,实现无灯源照射就能进行催化反应;Er3+-Gd3+摩尔分数为5.0% 的催化剂,在煅烧温度为500℃时催化性能最佳。无灯源照射条件下降解孔雀石绿80min时,其降解率可达到100%。
[1]Yu J G,Su Y R,Cheng B.Template-free fabrication and enhanced photocatalytic activity of hierarchical macro-mesoporous titania[J].Advanced Functional Materials,2007,17(2):1984-1990.
[2]Dai K,Peng T,Chen H,et al.Photocatalytic degradation of commercial phoxim over La-doped TiO2nanoparticles in aqueous suspension[J].Environmental Science & Technology,2009,43(5):1540-1545.
[3]Zhang Y H,Zhang H X,Xu Y X,et al.Significant effect of lanthanide doping on the texture and properties of nanocrystal line mesoporous TiO2[J].Solid State Chem,2004,177(10):3490-3498.
[4]Guo Y W,Cheng C P,Wang J,et al.Detection and analysis of reactive oxygenspecies(ROS)generated by nano-sized TiO2powder under ultra-sonic irradiation and application in sonocatalytic degradation of organic dyes[J].Hazard Mater,2011,192:786.
[5]Mahalakshmi M.,Arabindoo B,Palanichamy M,et al.Preparation,characterization,and photocatalytic activity of Gd3+doped TiO2nanoparticles[J].Journal of Nanoscience and Nanotechnology,2007,7(9):3277-3285.
[6]Sakai N,Ebina Y,Takada K,et al.Electronic band structure of titania semiconductor nanosheets revenled by electrochemical and photo electrochemcal studies[J].J Am Chem Soc,2004,126(18):5851-5858.
[7]Kandiel T A,Fedhoff A,Robben L,et al.Tailored titanium dioxide nanomaterials:anatase nanoparticles and brookite nanorods as highly active photocatalysts[J].Chem Mater,2010,22:2050-2060.
[8]燕宁宁,张 莹,龚昌杰,等.Ce-TiO2光催化剂的制备与性能研究[J].功能材料,2012,43(1):92-95.
[9]胡江海,刘雪霆,崔 鹏.碳、铈掺杂改性纳米TiO2及其光催化性能研究[J].合肥工业大学学报:自然科学版,2009,32(3):392-395.
[10]Furube A,Asahi T,Masuhara H,et al.Charge carrier dynamics of standard TiO2catalysts revealed by femtosecond diffluse reflectance spectroscopy[J].Phys Chem B,1999,103(16):3120-3127.
[11]戴冬梅,鲁 冰,刘园园,等.N,Cd-TiO2光催化活性的实验与理论研究[J].中山大学学报:自然科学版,2011,50(4):74-78.
[12]侯廷红,毛 健,杨 玲,等.稀土离子掺杂纳米TiO2的谱学特性研究[J].四川大学学报:工程科学版,2006,38(5):117-121.
[13]张 慧,陈建华,陈鸿博,等.纳米TiO2混晶的形成及其对光催化性能的影响[J].分子催化,2006,20(3):249-253.
[14]Anpo M,Shima T,Kodama S,et al.Photocatalytic hydrogenation of propyne with water on small-particle titania:size quantization effects and reaction intermediates[J].Journal of Physical Chemistry,1987,91(2):4305-4310.
[15]Shalil N B,Sugunan S.Photoinduced oxidation of benzhydrol over lanthana modified sol-gel titania[J].Journal of Sol-Gel Science and Technology,2007,42(3):101-105.
[16]Yu J C,Lin J,Lo D,et al.Influence of thermal treatment on the adsorption of oxygen and photocatalytic activity of TiO2[J].Langmuir,2000,16(18):7304-7308.

