β-谷甾醇的结构修饰研究进展
袁金伟,王 帆,买文鹏,杨亮茹,肖咏梅,毛 璞,屈凌波
(河南工业大学 化学化工学院,河南 郑州 450001)
0 引言
β-谷甾醇(β-sitosterol)是以环戊烷全氢菲为骨架(又称甾核)的一种化合物,在它的C—3 位和C—5 位分别有一个羟基(—OH)和一个双键,在C—17 位侧链上连接有10 个碳的烷基(图1).β-谷甾醇广泛存在于各种植物油、坚果等植物种子中,是植物甾醇中含量较多的一种[1].药理研究表明:β-谷甾醇具有降低血清胆固醇、消炎解热、抗氧化、抗肿瘤等药理作用.另外,β-谷甾醇对结肠癌、乳腺癌、白血病等均具有较好的防治作用[2].自20 世纪50 年代发现植物甾醇具有降低血浆胆固醇的作用以来,人们主要将其作为降胆固醇药物和功能性食品添加剂使用.随着对β-谷甾醇等植物甾醇的深入研究和广泛应用,β-谷甾醇的价值不仅体现在医药方面,而且在食品、保健品和化妆品等行业也得到广泛的使用[3].2000 年9 月,美国FDA 批准添加植物甾醇酯或甾烷醇酯的食品可使用“ 有益健康”标签.
目前,对β-谷甾醇衍生物的合成、生物活性、产品开发和利用等方面已有许多的研究和报道,并成为近年来植物甾醇研究与开发的热点.为了对该领域有更深入的了解,笔者从β-谷甾醇修饰结构位点和产物类型出发,对近年来β-谷甾醇结构修饰的研究进展进行了综述,希望对β-谷甾醇的开发和利用起到一定的借鉴和推动作用.

图1 β-谷甾醇的结构Fig.1 Structure of β-sitosterol
1 β-谷甾醇的结构修饰
β-谷甾醇的分子结构中,甾体的多元环及C-17 位上的链烃导致了它在水中的溶解度极小,而C-3 位极性羟基又限制了它在脂中的溶解度.因此,β-谷甾醇在人体中的吸收利用度差,从而限制了其在临床或其他产品开发中的应用.为了提高β-谷甾醇的生物利用度、增强其药理活性,近年来通过结构修饰和改造,已经合成出系列的β-谷甾醇衍生物,有效地改善了其生物利用度,部分化合物的生物活性明显提高.
1.1 β-谷甾醇3 位羟基的酯化
1.1.1 化学合成法
植物甾醇既具有疏水性,又具有亲水性,因此该物质具有一定的乳化特性以及调节和控制反向流动膜流动性的能力.琥珀酸单酯含有羧基,有良好的水溶性,与甾醇形成单酯后,能够提高甾醇的溶解性,增强甾醇的药理效果.为了改善β-谷甾醇的乳化性能和提高其生物活性,陈静波等[4-6]将β-谷甾醇与琥珀酸酐反应,得到了β-谷甾醇琥珀酸单酯,产率达到98%以上,并对该化合物的IR、NMR 和MS 裂解规律进行了分析.
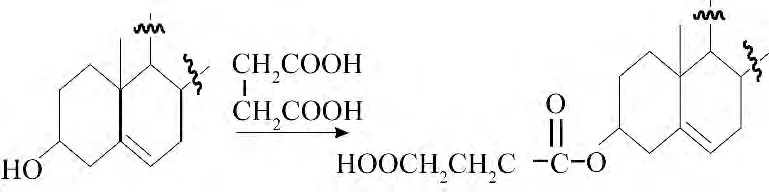
β-谷甾醇能降低血清总胆固醇水平和低密度脂蛋白胆固醇,而烟酸具有较强的降低甘油三酯的作用.β-谷甾醇烟酸酯结合了β-谷甾醇和烟酸的降血脂特点,可作为一种新型的降血脂药物,发挥其协同作用.2007 年黄琴等[7]通过烟酰氯和β-谷甾醇在有机溶剂中合成了β-谷甾醇烟酸酯,通过IR、MS 对其结构进行了表征,并对反应条件进行了优化.
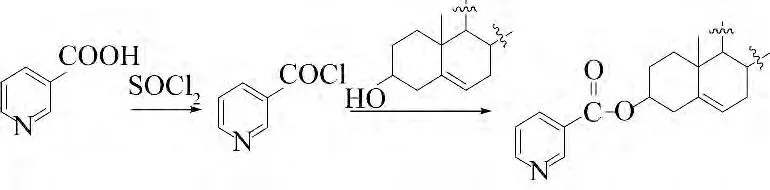
DMF-POCl3(Vilsmeier 试剂)是一种有效的甲酰化试剂,通常用于酚羟基的甲酰化.对于醇羟基的甲酰化往往通过多步反应来实现.2006 年Negi等[8]利用Vilsmeier 试剂DMF-POCl3对β-谷甾醇等植物甾醇中的二级醇进行了甲酰化反应,得到了甲酰化产物,这个反应具有操作简单、条件温和、化学选择性高、产率高等优点,为二级醇甲酰化提供了一种有效的方法.
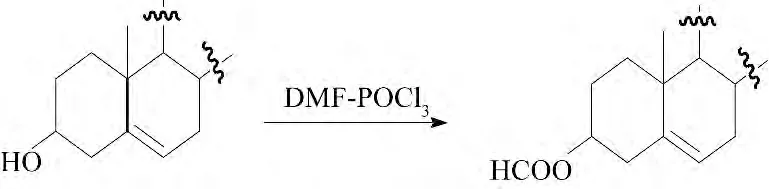
为了进一步研究植物甾醇酯对人体肿瘤细胞的抗恶性细胞增生和凋亡的影响,2008 年Julien-David 等[9]以β-谷甾醇等植物甾醇为原料,在不同催化剂催化下分别与油酸和9,10-二羟基十八酸等反应,得到了β-谷甾醇油酸酯、β-谷甾醇-9,10-二羟基十八酸酯等衍生物,为进一步开展其活性研究奠定了基础.
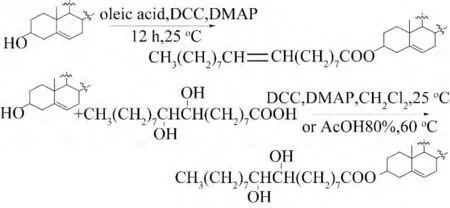
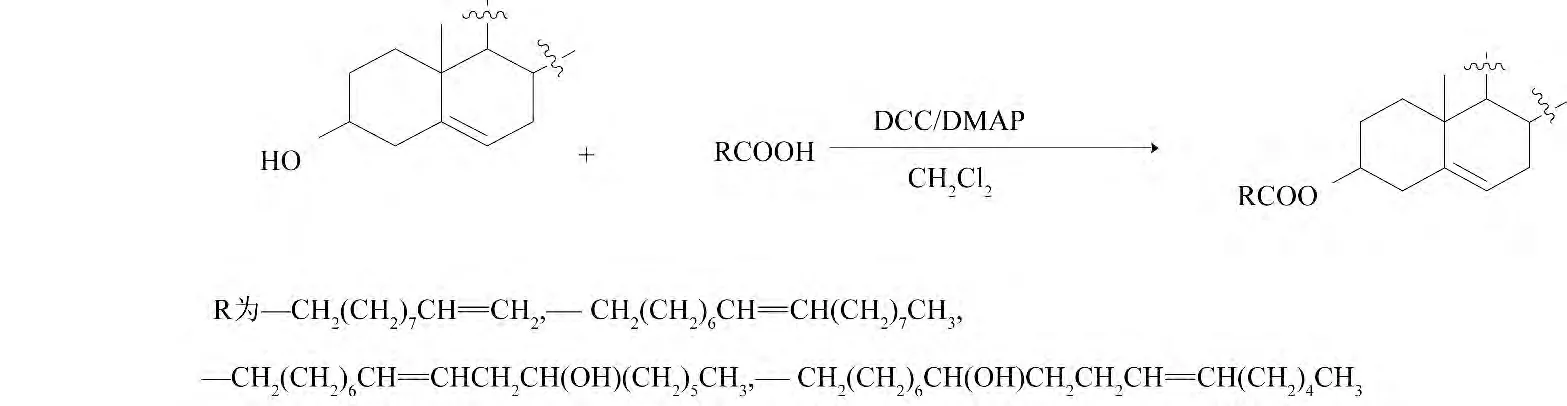
2010 年Farshori 等[10]以β-谷甾醇为原料,DCC/DMAP 为催化剂,与不同链长的不饱和脂肪酸反应,得到β-谷甾醇的不饱和高级脂肪酸酯,其结构经过NMR、IR 等确证.抗菌活性实验表明,在β-谷甾醇的不饱和高级脂肪酸酯衍生物结构中,脂肪酸碳链上有羟基取代的衍生物具有较强的抗菌活性.
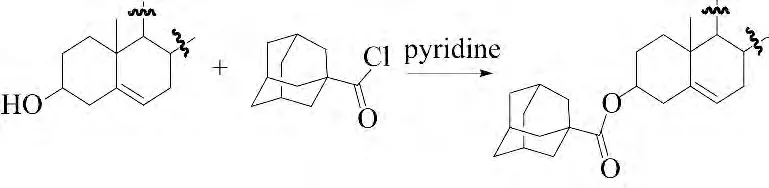
金刚烷衍生物具有广泛的生理活性,如抗病毒、抗胆碱酯酶、抗肌肉松弛和局部麻醉等作用,结构中含有金刚烷基团的药物已经被设计并合成.2003 年Dikusar 等[11]为了提高植物甾醇等醇类和酚类的生物活性,将β-谷甾醇等醇类(或酚类)化合物与1-金刚烷酰氯在吡啶存在的条件下反应,得到含有金刚烷药效基团的β-谷甾醇酯衍生物,其结构经过IR、UV 和NMR 等鉴定.1.1.2 酶催化合成法
为了提高β-谷甾醇的乳化分散能力和生物利用度,2013 年Panpipat 等[12]以β-谷甾醇为原料,以Candida antarctica lipase A 为催化剂,通过脂肪酶催化的生物合成方法,与不同链长和不同饱和度的脂肪酸反应,制备了系列的β-谷甾醇脂肪酸酯以及这些化合物的纳米分散体,并对其热力学特性、分散度和稳定性进行了研究,促进了β-谷甾醇脂肪酸酯衍生物在食物中的应用.
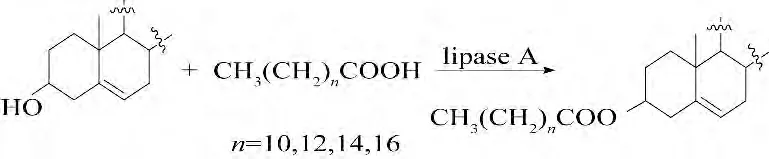
共轭亚油酸具有提高免疫功能、抑制癌细胞形成、减少心脏病发病率、抗糖尿病、促进生长等多种生物活性.为了改善甾醇的油溶性,方便食品加工应用,同时提高其生物活性,2006 年李瑞等[13]以共轭亚油酸与β-谷甾醇为原料,开展了有机相脂肪酶催化下合成共轭亚油酸β-谷甾醇酯的工艺研究,对工艺条件进行了优化,反应产率可达72%,且对甾醇酯的分离纯化方法进行了研究.
2004 年Vu 等[14]以β-谷甾醇为原料,lipase AK、AS、AYS 和TL IM 等脂肪酶为催化剂,分别与共轭亚油酸和中等长度的脂肪酸(C6-C12)等反应,结果表明,脂肪酶AYS 是最有效的酶催化剂.所得产物β-谷甾醇脂肪酸酯经过NMR 表征,熔点和凝固点通过DSC 进行了研究.
多重不饱和脂肪酸(PUFA)在医药材料、化妆品、健康食品和食品辅料等领域得到广泛的应用,如二十碳五烯酸乙酯已经被用来治疗动脉硬化症和高血脂.1999 年Shimada 等[15]利用Pseudomonas sp.酶催化的方法,使二十碳五烯酸、二十五碳六烯酸、γ-亚麻酸和亚油酸等多重不饱和脂肪酸(PUFA)与β-谷甾醇等植物甾醇反应,在温和的条件下得到高产率(>85%)β-谷甾醇不饱和脂肪酸酯.
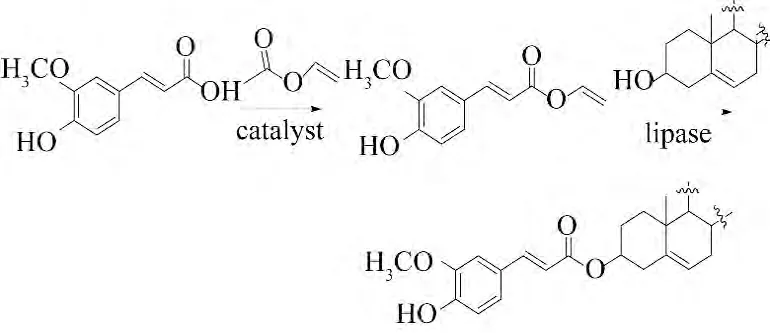
阿魏酸普遍存在于植物叶和种子中,其具有抗癌、治疗糖尿病、心血管疾病和神经性疾病等广泛的生理活性.2011 年Tan 等[16]通过化学酶合成法,通过二步反应方便地合成了植物甾醇阿魏酸酯衍生物.阿魏酸首先与醋酸乙烯酯发生酯交换反应生成阿魏酸乙烯酯,然后与β-谷甾醇在Candida rugosam 酶催化下发生醇解得到β-谷甾醇阿魏酸酯衍生物,其结构经过IR、HPLC-MS/MS 确证.抗氧化活性试验表明,该化合物具有较高的抗氧化活性.
1.1.3 固相催化合成法
2003 年Pouilloux Y 等[17]以MgO 为固相催化剂,2011 年Robles-Manuel S 等[18]以氧化铝负载的MgO 为固体催化剂,通过酯交换的方法,将β-谷甾醇与高级脂肪酸甲酯反应,得到了系列的β-谷甾醇高级脂肪酸酯.该催化剂具有稳定性好、重复利用次数多等优点.

1.2 β-谷甾醇3 位羟基桥连高分子聚合物的合成
为了克服β-谷甾醇水溶性和脂溶性差的缺点,Lim 等[19]以β-谷甾醇为原料,首先与丁二酰酐反应生成β-谷甾醇的单酯化产物CES,然后与不同相对分子质量的多聚乙二醇PEG 反应得到由丁二酰酐桥连β-谷甾醇和PEG 的衍生物HPS,其结构经过NMR、MS 等鉴定.溶解度测定显示,HPS 的水溶性比β-谷甾醇有明显提高.

1.3 甾体酮肟类化合物的合成
近年来,从海洋生物中分离出大量具有生理活性的甾体类化合物,该类化合物具有较强的抗肿瘤、抗病毒活性.其中甾核部分含有肟基与烯酮共轭的甾体化合物是芳香酶抑制剂,而芳香酶是雌激素生物合成中的关键中间体,因此,甾体酮肟化合物的合成引起了化学家的重视.2007 年崔建国等[20]以β-谷甾醇、胆甾醇等为原料,经氯铬酸吡啶氧化生成β-谷甾(胆甾)-4-烯-3,6-二酮,然后与盐酸羟胺反应合成了(3E)-β-谷甾(胆甾)-4-烯-3,6-二酮-3-肟,总收率达60%以上,并对其结构进行了表征.2009 年Cui 等[21]以β-谷甾醇等植物甾醇为原料,通过多步反应合成了系列的植物甾醇肟类化合物,构效关系研究表明:羟亚胺基处于A 环和B 环上的甾体肟类化合物对癌细胞具有明显的细胞毒性,且当一个肟基团处于B 环上,同时A 环或B 环上有一个羟基时,比其他的甾体肟类化合物具有较高的细胞毒性.
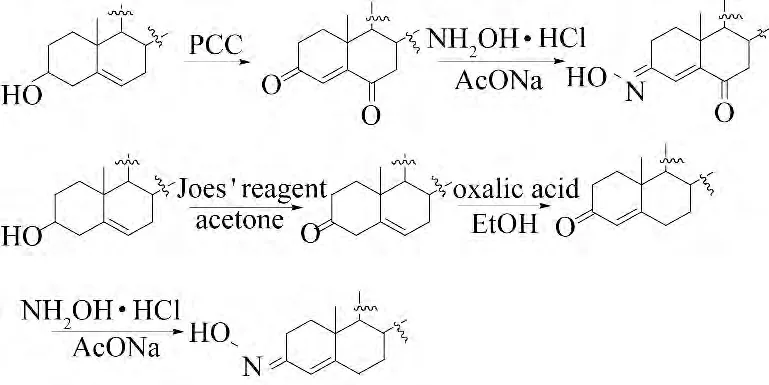
1.4 β-谷甾醇氧化产物的合成
2010 年Carvalho 等[22]以β-谷甾醇等植物甾醇为原料,首先采用金属镁试剂作为氧的供体,将β-谷甾醇等植物甾醇中的双键氧化为环氧化物,然后用无毒的Bi(OTf)3处理后,环氧化物开环得到一个反式的邻二醇.该方法具有氧化剂稳定、低毒、开环试剂无毒、产率高等优点.
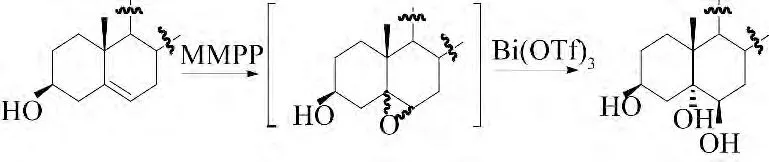
2012 年Ghosh P 等[23]以β-谷甾醇等甾醇为原料,SeO2为氧化剂,通过一锅煮的方法,合成了甾醇的3 种衍生物,即甾醇的芳香化产物4β,7α-二羟基甾醇和3β,4β-二羟基甾醇衍生物,该合成方法对反应溶剂具有一定的选择性,且反应产物种类多,是合成甾醇衍生物的一种有效方法.

2006 年Sripalakit P 等[24]选择标准菌株和真菌株研究了对β-谷甾醇等植物甾醇17 位侧链的代谢清除试验.结果表明,菌株Mycobacterium sp.NRRL R-3683 和NRRL B-3805 等能够有效地将β-谷甾醇转化为AD 和ADD.植物甾醇的结构影响17 位侧链的代谢清除,结果表明β-谷甾醇转化为AD 和ADD 具有最高的转化率.
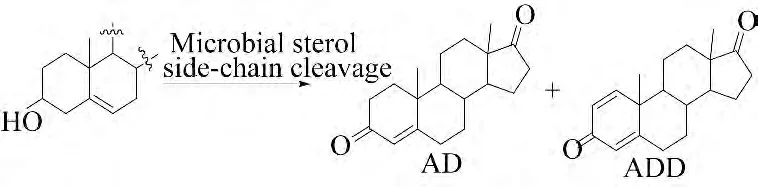
1.5 β-谷甾醇还原产物的合成
研究发现,作为功能性食品添加剂,β-谷甾醇及其饱和形式甾烷醇能有效降低人体的胆固醇水平.饱和形式β-谷甾烷醇具有较好的抗氧化性能,不易转化为对人体有害的固醇物质,因此在抑制胆固醇吸收方面更加有效.2011 年陈慧等[25]采用液相还原法制备的介孔碳(CMC)负载的Pd 催化剂,将β-谷甾醇通过催化加氢制备了β-谷甾烷醇.

1.6 β-谷甾醇醚化产物的合成
β-谷甾醇是芫花中具有强烈杀虫活性的成分之一,为了筛选高效的甾醇类杀虫剂,研究β-谷甾醇衍生物的分子结构与生物活性之间的关系,2004年孙汉洲等[26]以β-谷甾醇为原料,通过卤代、酯化和醚化等反应合成了系列的β-谷甾醇卤代产物、酯化产物和醚化产物,并利用IR、MS 和元素分析等对其结构进行了表征.
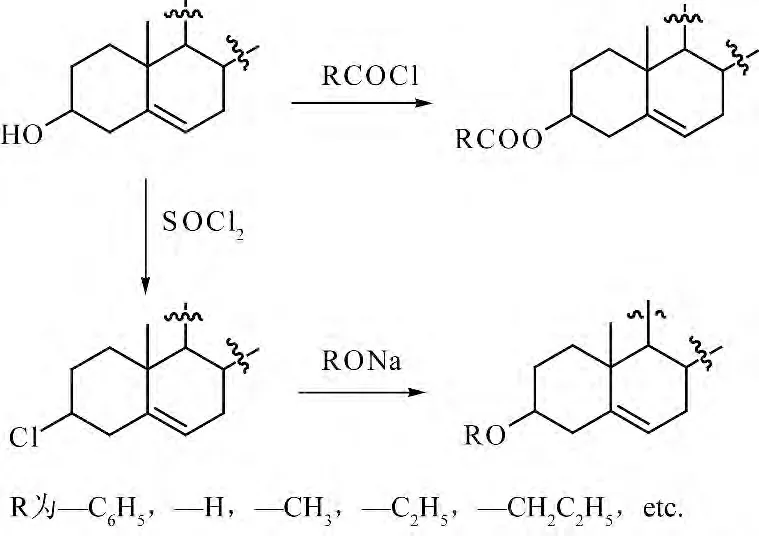
1.7 β-谷甾醇-磺酸盐衍生物的合成
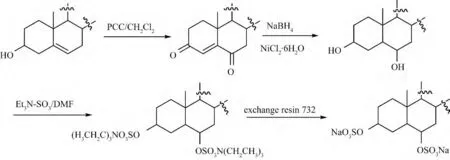
从海洋生物中分离得到的多羟基甾醇的硫酸化钠盐显示出广泛的生物活性,如抑制HIV 复制、抑制蛋白酪氨酸酶和抗肿瘤等活性.为了进一步研究此类化合物的结构与活性,2009 年Cui[27]以β-谷甾醇等植物甾醇为原料,首先通过PCC 氧化得到共轭烯二酮,然后使用NaBH4和NiCl2还原得到二醇,再与Et3N-SO3的复合物反应得到二硫酸铵盐,最后通过交换树脂合成系列的甾醇的硫酸化钠盐衍生物.活性研究表明:这些化合物对人的肝癌Sk-Hep-1、肺癌H-292 和前列腺癌PC-3 具有一定的抑制作用,且这些甾醇硫酸化钠盐衍生物17 位取代基对其生物活性有重要的影响.
1.8 β-谷甾醇-磷脂衍生物的合成
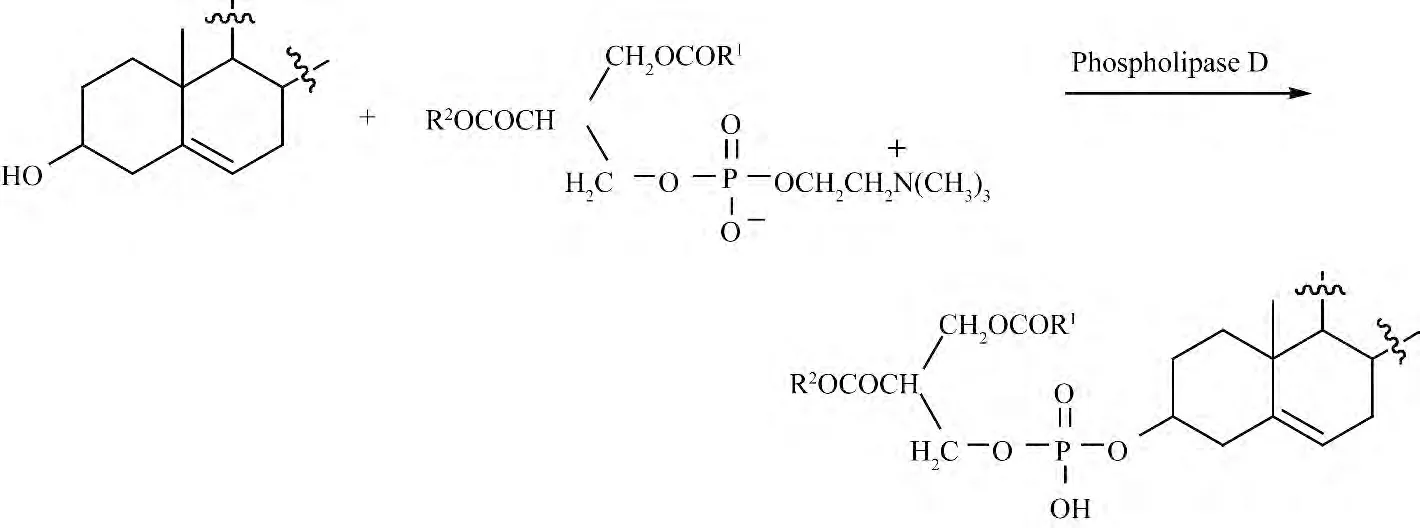
为了提高植物甾醇的利用度,提高其在食物或药物中的应用效果,2004 年Hernandez Ernesto 等[28]将磷脂引入β-谷甾醇等植物甾醇的结构修饰中,通过磷脂酶D 作用,使β-谷甾醇与磷脂反应得到了β-谷甾醇-磷脂衍生物.
2 结论与展望
β-谷甾醇作为一种天然活性物质,是一种天然的营养强化剂,已通过临床实验证实了其安全性.国外已将其作为食品添加剂应用于奶油和面包等食品中,我国也将其应用到食用油的生产中.但是,游离的植物甾醇在水与油脂中的溶解性都较低,在人体内的生物利用度也较差,因此,利用前药等分子设计理论对β-谷甾醇进行化学结构修饰,必将使β-谷甾醇及其衍生物在医药、食品、化妆品等行业获得更广泛的应用.
[1]李庆勇,姜春菲,张黎,等.β-谷甾醇、豆甾醇诱导人肝癌细胞SMMC-7721 凋亡[J].时珍国医国药,2012,23(5):1173-1175.
[2]张忠泉,邢煜君,胡国强,等.β-谷甾醇诱导人肝癌HepG2细胞凋亡机制研究[J].中国中药杂志,2011,36(15):2145-2148.
[3]Moghadasian M H.Pharmacological properties of plant sterols in vivo and in vitro observations[J].Life Sciences,2000,67(6):605-615.
[4]陈静波,古昆,施南华,等.羟基甾醇类化合物的琥珀酸单酯化研究[J].合成化学,2000,8(5):466-468.
[5]沙鸥,钱保华,许文林.β-谷甾醇琥珀酸酯的合成表征及质谱碎裂机理研究[J].食品研究与开发,2006,27(6):125-126.
[6]沙鸥,邵强,黄一波,等.植物甾醇琥珀酸酐酯化产物的分析表征[J].中国油脂,2004,29(10):34-37.
[7]黄琴,陈茂彬.β-谷甾醇烟酸酯的制备[J].化学与生物工程,2007,24(9):62-64.
[8]Srivastava V,Negi A S,Kumar J K,et al.A simple,convenient and chemoselective formylation of sterols by Vilsmeier reagent[J].Steroids,2006,71(7):632-638.
[9]Julien-David D,Geoffroy P,Marchioni E,et al.Synthesis of highly pure oxyphytosterols and(oxy)phytosterol esters:Part II.(Oxy)-sitosterol esters derived from oleic acid and from 9,10-dihydroxystearic acid[J].Steroids,2008,73(11):1098-1109.
[10]Farshori N N,Banday M R,Zahoor Z,et al.DCC/DMAP mediated esterification of hydroxy and non-hydroxy olefinic fatty acids with βsitosterol:In vitro antimicrobial activity [J].Chinese Chemical Letters,2010,21(6):646-650.
[11]Dikusar E A,Kozlov N G,Potkin V L,et al.1-Adamantanecarboxylic acid esters of certain terpenols,sterols,and plant phenols [J].Chemistry of Natural Compound,2003,39(3):276-279.
[12]Panpipat W,Dong M D,Xu X B,et al.Thermal properties and nanodispersion behavior of synthesized β -sitosteryl acyl esters:A structure-activity relationship study[J].Journal of Colloid and Interface Science,2013,407:177-186.
[13]李瑞,张晓鸣.有机相脂肪酶催化合成共轭亚油酸β-谷甾醇酯的研究[J].中国油脂,2006,31(2):56-59.
[14]Vu P L,Shin J A,Lim C H,et al.Lipasecatalyzed production of phytosteryl esters and their crystallization behavior in corn oil [J].Food Research International,2004,37(2):175-180.
[15]Shimada Y,Hirota Y,Baba T,et al.Enzymatic synthesis of steryl esters of polyunsaturated fatty acids [J].Journal of the American Oil Chemists Society,1999,76(6):713-716.
[16]Tan Z L,Shahidi F.Chemoenzymatic synthesis of phytosteryl ferulates and evaluation of their antioxidant activity[J].Journal of Agricultural and Food Chemistry,2011,59(23):12375-12383.
[17]Pouilloux Y,Courtois G,Boisseau M,et al.Solid base catalysts for the synthesis of phytosterol esters[J].Green Chemistry,2003,5(1):89-91.
[18]Robles -Manuel S,Barrault J,Valange S.Selective synthesis of phytosterol esters from natural sterols and fatty methyl esters over Mgcontaining solid catalysts[J].Comptes Rendus Chimie,2011,14(7-8):656-662.
[19]Lim J C,Chung D W.Study on the synthesis and characterization of surface activities of hydrophilic derivatives of β -sitosterol[J].Journal of Applied Polymer Science,2012,125(2):888-895.
[20]崔建国,范磊,黄立梁,等.(3E)-胆甾-4-烯-3,6-二酮-3-肟及其类似物的合成[J].合成化学,2007,15(6):689-692.
[21]Cui J G,Fan L,Huang L L,et al.Synthesis and evaluation of some steroidal oximes as cytotoxic agents:Structure/activity studies(I)[J].Steroids,2009,74(1):62-72.
[22]Carvalho J F S,Cruz Silva M M,Melo M L S.Efficient trans-diaxial hydroxylation of Δ5-steroids[J].Tetrahedron,2010,66(13):2455-2462.
[23]Ghosh P,Das J,Sarkar A,et al.Oxidation with selenium dioxide:the first report of solvent-selective steroidal aromatization,efficient access to 4β,7α -dihydroxy steroids,and syntheses of natural diaromatic ergosterols[J].Tetrahedron,2012,68(32):6485-6491.
[24]Sripalakit P,Wichai U,Saraphanchotiwitthaya A.Biotransformation of various natural sterols to androstenones by Mycobacterium sp.and some steroid-converting microbial strains[J].Journal of Molecular Catalysis B:Enzymatic,2006,41(1-2):49-54.
[25]陈慧,戴乐,谢建新,等.介孔碳负载的Pd催化剂催化β-谷甾醇加氢制备β-谷甾烷醇[J].催化学报,2011,32(12):1777-1781.
[26]孙汉洲,李忠海,赵芳,等.系列β-谷甾醇衍生物合成与结构表征[J].吉林化工学院学报,2004,21(3):10-12.
[27]Cui J G,Wang H,Huang Y M,et al.Synthesis and cytotoxic analysis of some disodium 3 β,6 β-dihydroxysteriol disulfates [J].Steroids,2009,74(13-14):1057-1060.
[28]Hossen M,Hernandez E.Phospholipase Dcatalyzed synthesis of novel phospholipid -phytosterol conjugates[J].Lipids,2004,39(8):777-782.

