主-髂-股动脉多发病变腔内治疗策略及临床意义
李明军, 戚春厚, 黄兆栋, 李 俊
随着CTA、MRA、DSA血管成像技术的发展与提高,主-髂-股动脉多发病变的检出率逐年增加。因其导致下肢缺血甚至引起足趾坏死,致残率高,已引起临床高度重视。目前,采用的外科血管转流术创伤大,并发症多,且病变涉及范围广泛,治疗受到限制,随着PTA技术逐步成熟,腔内治疗取得显著疗效。本文回顾性分析我院2010年1月—2014年8月8例主-髂-股动脉多发病变患者经腔内治疗的策略及临床意义。
1 材料与方法
1.1 临床资料
本组8例患者均为男性,年龄42~71岁,平均年龄56.1岁,其中1例45岁患者于就诊前3年已行左下肢高位截肢;8例患者均有不同程度的跛行,下肢麻木、发凉。术前均行CTA或MRA。病变累及肾动脉水平以下腹主动脉狭窄1例、闭塞7例,双侧髂总动脉狭窄1例、闭塞6例,1例累及到股腘动脉;5例股动脉、足背动脉搏动未触及,3例触及较弱。8例患者病变部位见表1。
1.2 治疗方法
根据术前下肢CTA或MRA的影像资料,选择穿刺点及贯通路径,4例行左肱、双侧股动脉穿刺,1例行左肱、右股深动脉穿刺,1例行左肱、右股浅动脉穿刺,1例行双侧股浅动脉穿刺,1例行左股动脉穿刺,依据病变部位采用逆行、顺行、对穿贯通技术开通闭塞段。根据DSA影像分析,决定是否留置导管溶栓,球囊扩张或支架植入等治疗。

表1 8例患者CTA显示病变分布
2 结果
治疗后8例患者肾动脉开口以下腹主动脉全部开通,12条髂总动脉除3条未处理外9条全部贯通,髂外动脉均贯通,4例术后1个月彩色多普勒超声(彩超)检查示腔内及血流正常。随访1~12个月,5例患者下肢缺血症状消失,2例明显改善;1例患者1年后支架内血栓形成再次闭塞,插管溶栓48 h后支架内再通,1个月后来院复诊,无临床症状。8例患者腔内治疗方法及随访结果见表2。图1~3为3例患者治疗过程CTA图像。
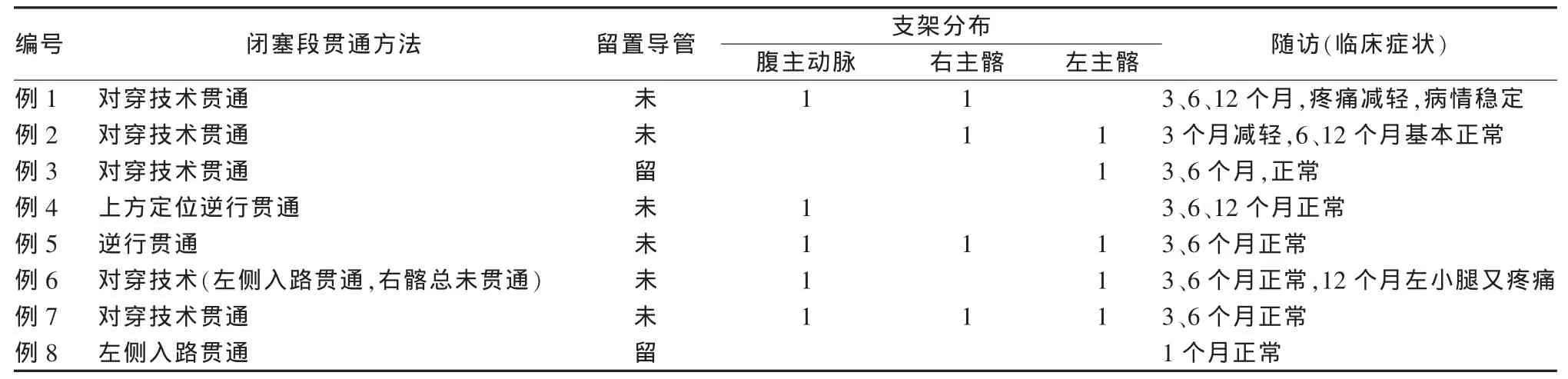
表2 8例患者腔内治疗方法及随访结果
3 讨论
主-髂-股动脉多发病变的发病原因尚不清楚,多数认为与动脉粥样硬化、血栓形成和多发性大动脉炎有关。病变的基础是动脉硬化、血栓形成,致主-髂-股动脉多发狭窄闭塞(三岔口),导致远端缺血、坏死。经典治疗是经腹主动脉至一侧或双侧股腘动脉人工血管旁路移植术,但创伤大,围手术期病死率达3.9%。随着血管腔内治疗技术的发展,血管腔内贯通、溶栓、球囊扩张、支架植入治疗主-髂-股动脉多发病变,以其成功率及远期通畅率高、并发症低而逐步被接受和采用,特别是为高龄不能耐受外科手术的患者带来希望。杨燎等[1]报道成功率为 97.1%;Sharafuddin 等[2]报道成功率为 94%;沈晨阳等[3]报道,髂动脉支架介入治疗术后1~3年通畅率与腹主-股动脉人工血管旁路移植术后通畅率无明显差异。
术前检查及检查方式在主-髂-股动脉多发病变整个诊疗过程中非常重要。首先注意双侧股动脉搏动,本组8例患者,5例股动脉、足背动脉搏动未触及,3例触及较弱;其次通过CTA、MRA全面了解
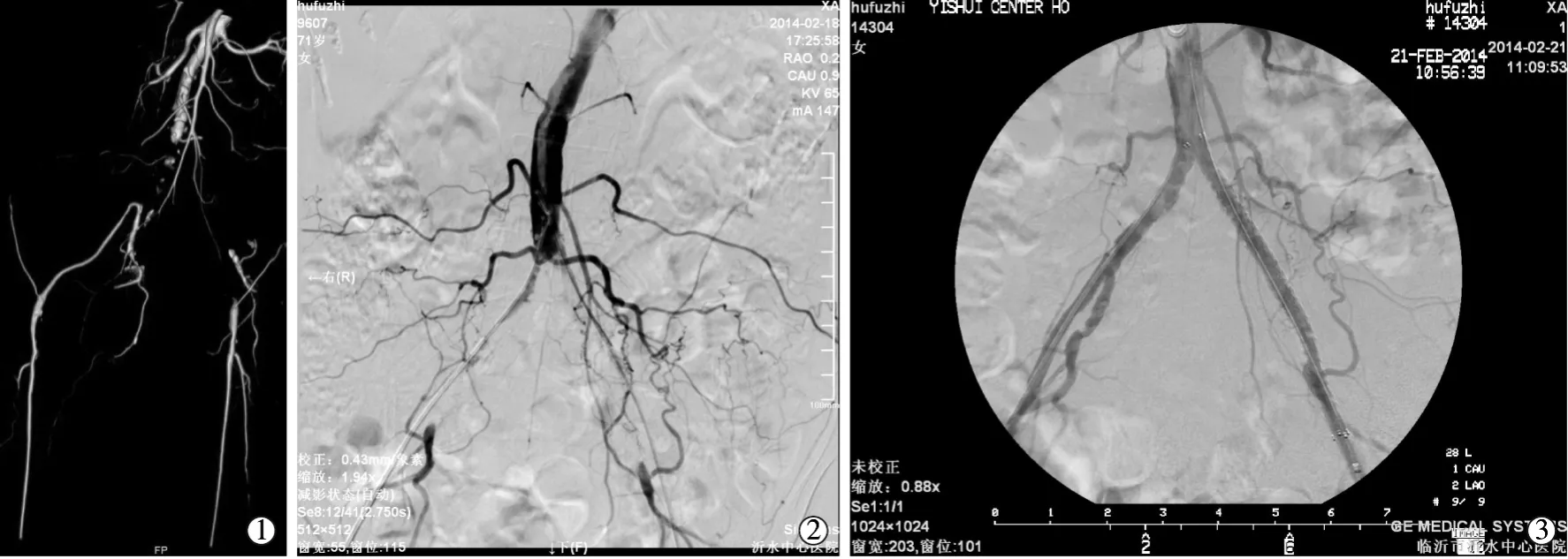
图1 右骼总动脉,左骼总、骼外动脉闭塞开通前后
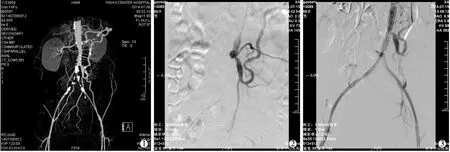
①CTA:腹主动脉远段、双侧髂总动脉闭塞;②DSA示腹主动脉远段未显示;③闭塞段贯通后,双球囊扩张,支架置入后造影,血管显示好血管情况,明确显示血管的走行,血管壁钙化,狭窄、闭塞的程度、范围。根据CTA或MRA资料,进行术前风险评估,选择、制定治疗方案以及手术效果的预测等。CTA或MRA的扫描范围均要包括肾动脉以上的腹主动脉、主髂动脉、股部动脉、腘动脉、膝下动脉及足部,防止漏诊、误诊。本组8例患者,常规下肢动脉CTA或MRA血管成像,漏诊3例,均再次行腹主动脉成像,明确诊断。
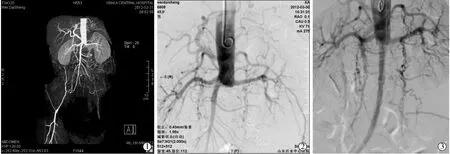
图3 腹主动脉,右骼总、骼外动脉闭塞开通前后(左下肢3年前高位截肢)
主-髂-股动脉完全闭塞入路选择是决定腔内治疗成功关键,病变范围广泛,肾动脉水平以下的腹主、髂总、髂外动脉狭窄闭塞且部分患者伴有广泛股、腘动脉病变,不论外科旁路移植手术还是血管腔内治疗,技术难度非常大,因其是慢性过程,侧支循环丰富。本组1例选择股深动脉穿刺贯通,通过股深动脉与膝下动脉侧支循环,增加下肢远端血供,达到满意临床效果[4-5]。在实际操作中,由于动脉闭塞,穿刺点搏动难以触及,为了提高穿刺成功率,经左肱动脉入路置猪尾巴导管于肾动脉水平以上腹主动脉内行DSA造影,应用路图功能,定位穿刺靶血管。对于病变范围广泛,侧支循环丰富,一侧肢体无明显临床症状的患者,可不予处理;双下肢均有临床症状,在选择治疗方案时,先贯通症状明显侧,再贯通对侧,尽可能保留侧支,维持远端血供。
本病治疗的难点是开通闭塞段,主-髂-股动脉多发病变属于三岔口,由于病变范围广泛,走行迂曲,动脉硬化等因素,贯通过程中很容易进入血管内膜下,也可能贯通血管壁。为了有效开通闭塞段,最大程度降低并发症的发生,最好选用3 F以下直头导管配合微导丝,不宜使用普通导管、导丝,利于提高成功率,减少进入血管内膜下的概率;试用对穿技术,经左肱动脉入路,用deep球囊配合微导丝,顺行贯通腹主动脉闭塞段,造影证实后,撤换进入交换导丝固定,起到定位作用,再经股动脉逆行贯通髂外、髂总动脉;对穿成功造影证实后,分别使用deep球囊预扩张,根据血管走行,将微导丝远端塑型进入腹主动脉或主髂动脉血管腔内,反复造影观察,判断是否在真腔。双向贯通造影确认后,交换导丝交汇进入,不可盲目球扩及支架植入,造影观察是否有腔隙及新鲜血栓。临床上许多主-髂动脉全程闭塞者是在局限性重度狭窄或闭塞的基础上继发形成长段血栓而成,通过留管溶栓,部分病例可将TASC分级D级病变转化为C级、B级甚至A级病变,然后根据情况行腹主动脉、髂动脉球囊扩张或支架植入术,本组1例D型病变,经留置导管溶栓72 h后,腹主动脉远段、右主髂动脉开通,左髂总动脉狭窄,转变为A型,植入支架1枚,治疗成功。对于无腔隙动脉硬化病变,用deep球囊预扩张,选用自小到达的球囊逐步扩张,再支架置入,手术即可成功。
支架内血栓形成再闭塞,直接插管溶栓,效果很好,不可盲目行支架再植入。本组1例患者术后1年,又出现原有症状,来院CTA复查,腹主动脉、左髂总动脉闭塞,经贯通插管溶栓72 h,血管再通,不需球囊扩张及支架植入。
主-髂-股动脉(三岔口)多发病变的基础是动脉硬化、血栓形成导致管腔狭窄闭塞,由于是慢性、渐进性过程,患者逐步适应肾血流量改变,主-髂-股动脉多发病变狭窄闭塞贯通后,血流动力学瞬间改变,易导致肾脏灌注不足,从而引起一系列临床症状,甚至出现肾衰竭死亡。Moise等[6]治疗31例,肾功能不全发生率为5例,2例患者需要永久性透析。所以治疗过程中维持肾脏血供,降低致死性肾衰竭并发症发生是重点关注的问题。本组病例在选择球囊、支架时,宜小不宜大,支架的直径较腹主动脉正常血管腔小2 mm,既保证肾脏血供,又达到满足下肢血供。对于肾动脉开口水平以下腹主动脉全程闭塞的病变,球囊扩张及支架植入过程中密切注意斑块脱落栓塞肾动脉。为了有效预防,选用直径4~5 mm球囊预扩张,支架植入过程中支架近心端越过肾动脉开口水平以上,释放5~10 mm停止,观察支架自膨情况,达到圆锥形为目的,固定外管回抽支架推送器内芯,固定支架,透视监视下缓慢回拉整个释放系统,当支架近心端标记位于肾动脉水平以下时停止回拉,造影确认无误后再缓慢释放支架。目的是以支架近心端圆锥形下拉,可有效防止斑块脱落。禁止支架近心端覆盖肾动脉,影响肾血流。本组手术的8例患者无一例发生肾功能不全。
总之,腔内治疗创伤小,风险小,并发症率低,可重复治疗,是治疗主-髂-股动脉多发病变的有效方法。但是受到病例数量及远期随访的限制,对远期通畅率的估计缺乏循证医学统计数据支持。
[1]杨 燎,吴庆华,陈 忠,等.腔内技术与主股动脉转流治疗TASC C D型主髂动脉病变的远期通畅率结果[J].心肺血管病杂志,2013,32:10-12.
[2]Sharafuddin MJ, Hoballah JJ, Kresowik TF, et al.Long-term outcome following stent Reconstruction of the aortic bifurcation and the role of geometric determinants[J].Ann Vasc Surg, 2008,22:346-357.
[3]沈晨阳,赵克强,李 伟,等.358例下肢动脉硬化闭塞症外科治疗效果分析[J].中华普通外科杂志,2008,23:197-199.
[4]吴安乐,黄求理,宋侃侃,等.动脉粥样硬化所致髂-股动脉狭窄或闭塞的血管腔内介入治疗[J].介入放射学杂志,2009,18: 819-822.
[5]顾建平,楼文胜,徐 克.加强下肢动脉硬化闭塞症介入治疗的研究[J].介入放射学杂志, 2011, 20: 757-759.
[6]Moise MA,Alvarez-Tostado JA,Clair DG,et al.Endovascular management of chronic infrarenal aortic occlusion[J].JEndovasc Ther, 2009, 16: 84-92.

