健脾生血颗粒对大鼠胚胎-胎仔发育毒性研究
赵 刚 夏 莹 黄志军 裴学军 唐惠丹
(1 健民集团儿童药物研究院,武汉,430052; 2 湖北省食品药品安全评价中心,武汉,430073)
健脾生血颗粒对大鼠胚胎-胎仔发育毒性研究
赵 刚1夏 莹2黄志军1裴学军1唐惠丹1
(1 健民集团儿童药物研究院,武汉,430052; 2 湖北省食品药品安全评价中心,武汉,430073)
目的:评价灌胃给予健脾生血颗粒对大鼠胚胎-胎仔发毒性作用。方法:孕鼠随机分为阴性对照、阳性对照和低、中、高剂量试验组,分别于孕期第6至第15天连续灌胃给药。其中,低、中、高剂量试验组分别灌胃健脾生血颗粒浸膏1.16、3.48、10.44 g/kg/d,阳性对照组灌胃维生素A醋酸酯0.08 g/kg/d,阴性对照组给予同样体积的纯净水。记录孕鼠的体重、身长、摄食量及临床表现。于妊娠第20天剖检孕鼠,观察胎盘和胎鼠外观形态,记录黄体数、活胎数、死胎数、吸收胎、着床数及胎盘质量,制作骨骼和内脏标本,以作进一步检查。结果:阳性对照组出现了明显的致畸作用,证明本试验系统结果可靠。试验组大鼠经给药后,均未见明显异常临床症状,各剂量组对胚胎的形成均无明显影响,且黄体数、植入数、死胎、活胎以及吸收胎与阴性对照组比较差异均无统计学意义。此外,低、中剂量的浸膏对亲代大鼠未见明显一般毒性,但高剂量浸膏可致亲代大鼠体重和摄食量下降,影响部分胎鼠的发育,主要表现为体重减轻,少数动物关节畸形等。结论:在本试验条件下,健脾生血颗粒浸膏对大鼠胚胎-胎仔发育毒性的无不良反应剂量为3.48 g/kg,相当于成人临床最大用量的42倍。
健脾生血颗粒;大鼠;胚胎-胎仔发育毒性
安全性研究是新药开发和老产品二次开发的重点内容。由于历史等原因,国内较多上市产品并未严格按照GLP的规范对药物安全性进行全面研究,尤其是10年前批准生产的药品,即使进行了相关安全性评价研究,当时的评价基础和研究技术也难以满足当今的技术要求[1]。随着药品进入市场后大规模的应用检验,上市产品的安全性问题逐渐暴露[2]。因此,国家鼓励药企对已批准生产的药品进行上市后再评价研究,尤其是安全性评价研究[3]。同时,可靠的安全性再评价研究数据也能为上市产品提供学术推广资料。让医疗工作者对产品的认识更加深入,更加放心地去选择产品。
健脾生血颗粒和健脾生血片是健民药业集团股份有限公司独家生产的中西复方制剂,二者仅有剂型差别,处方一致,主要成分为党参、茯苓、黄芪、山药、鸡内金、龟甲、大枣等中药成分及硫酸亚铁,功能主治为健脾和胃,养血安神,用于小儿脾胃虚弱及心脾两虚型缺铁性贫血,以及成人气血两虚型缺铁性贫血。该产品以中医经典方“参苓白术散”“生脉饮”及“龙骨牡蛎汤”为基础化裁而得,可显著改善缺铁性贫血患者脾胃运化功能,并具益气养血之功[4-5]。目前,该产品在临床上主要用于妊娠期妇女和小儿缺铁性贫血的治疗与预防,以及改善体弱成人的气虚、脾虚等症状。由于该产品在妊娠期妇女患者中应用较为广泛[6-8],所以为了更进一步明确该产品的不良反应,保证孕妇和胎儿安全,本研究拟采用SPF级SD大鼠,探讨健脾生血颗粒浸膏对胚胎-胎仔发育的毒性作用。
1 材料与方法
1.1 药品 健脾生血颗粒浸膏,由健民药业集团股份有限公司提供(批号:140111-18),每克浸膏相当于生药材3.3 g,含七水硫酸亚铁0.154 g。维生素A醋酸酯,购于国药控股星鲨制药(厦门)有限公司(批号:10132001)。溶剂对照为饮用纯净水,由武汉神阳饮品有限公司提供。
1.2 动物及分组 SD大鼠,SPF级,购于湖北省实验动物研究中心,生产许可证号:SCXK(鄂)2008-0005,实验动物质量合格证号:42000600002944。交配开始前,所有动物均适应性饲养10 d,动物年龄为10~11周龄,雌鼠体重200~270 g,雄鼠体重310~400 g。动物饲养于屏障系统的IVC笼具中,动物房实行压差及温湿度监控和自动控制。相对湿度控制范围为39%至55%,温度控制范围为20.1 ℃至23.7 ℃。IVC笼内每小时换气次数40次以上,光照明10 h/暗14 h,循环交替至实验结束。动物饲料由武汉市万千佳兴生物科技有限公司提供。动物饮用水为经高压灭菌消毒的瓶装水。将雌鼠、雄鼠1∶1合笼,次日检查阴栓及阴道涂片,精子与阴栓同存者即被判断为交配成立,当日记为妊娠0日。将交配成功的孕鼠随机分为5组,即溶剂对照组、阳性对照组和低、中、高剂量试验组,每组20~22只。其中,溶剂对照组灌胃纯净水,阳性对照组灌胃0.08 g/kg/d维生素A醋酸酯,低、中、高剂量试验组分别灌胃健脾生血颗粒浸膏1.16、3.48、10.44 g/kg/d。给药体积均为10 mL/kg。每组均从妊娠第6天给药至妊娠第15天,给药1次/d。
1.3 观察指标
1.3.1 存活期检查从动物到达至动物解剖当日,每天进行2次存活性观察及笼边观察,观察动物存活情况、体征变化、行为等。体重称量从试验前即开始,称重1次/3 d。孕鼠分别在妊娠第0、7、14、20天测定摄食量。
1.3.2 终点检查剖检前,采用2%戊巴比妥钠麻醉实施安乐死,所有动物均对体表、天然孔道和脑外表面进行检查。孕鼠于妊娠第20天处死。观察胎盘,称取卵巢、子宫及所有附着的胎仔总重,计数黄体数,活胎、死胎、吸收胎并计算着床数。胎仔剖检前,以戊巴比妥钠(5~20 mg/胎仔)腹腔注射安乐死。测量活胎胎仔体重、顶臀长,并通过内外生殖器辨别胎仔性别。部分胎仔经Bouin氏液固定[9],以作内脏检查,部分胎仔经剥皮后用茜素红染色[10],以作骨骼检查。
1.4 统计学方法 所有定量数据均采用均数和标准差表示,应用SPSS 18.0软件进行统计分析,计量资料采用t检验分析,计数资料采用秩和检验。
2 结果
2.1 不良反应 动物死亡及临床情况本实验中未观察到因供试品引起的临床症状或死亡。
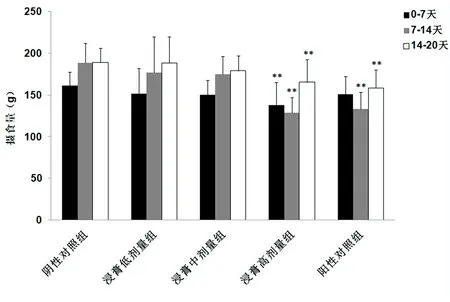
图1 健脾生血颗粒浸膏对孕鼠摄食量的影响
注:与同类阴性对照组相比,**P<0.01。
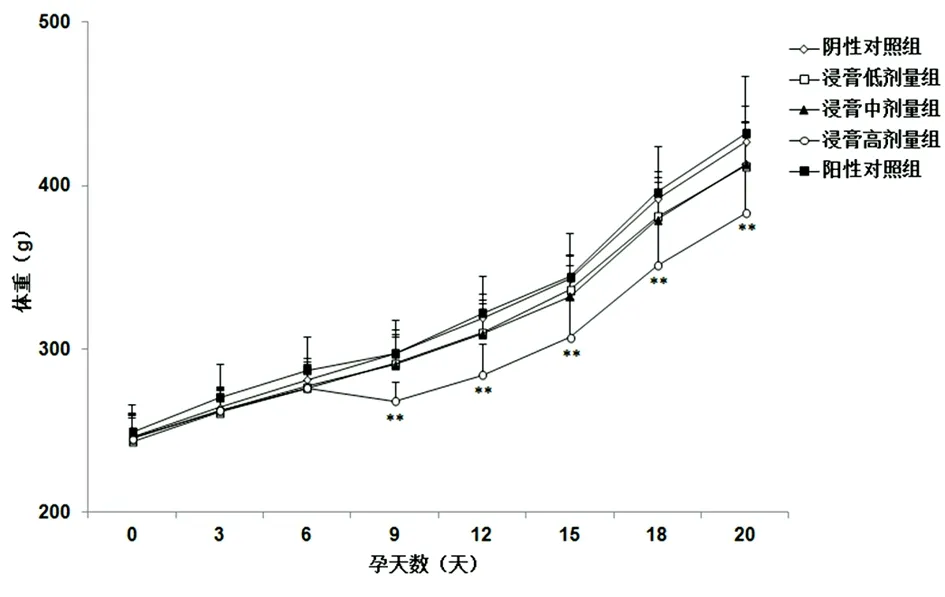
图2 健脾生血颗粒浸膏对孕鼠体量的影响
注:与同孕天数的阴性对照组相比,**P<0.01。
2.2 孕鼠摄食量和体重健脾生血颗粒浸膏对孕鼠摄食量的影响 见图1。由图可见,健脾生血颗粒浸膏低、中剂量组摄食量相对于阴性对照组差异无统计学意义(P>0.05),高剂量组摄食量显著低于阴性对照组,阳性对照组给药后孕7 d至孕20 d的摄食量显著低于阴性对照组。
大鼠随孕天数增加的体重情况见图2。由图可见,低、中剂量的健脾生血颗粒浸膏对孕鼠体重无明显影响。健脾生血颗粒浸膏高剂量组给药后于孕9 d至孕20 d孕鼠体重显著低于阴性对照组。
2.3 胚胎毒性 通过对孕鼠黄体数、植入数、着床率、死胎率等指标观察可见,健脾生血颗粒浸膏各剂量组对胚胎形成无明显影响,各组黄体数、植入数、死胎、活胎、吸收胎等差异均无统计学意义。健脾生血颗粒浸膏对胎鼠外观的影响见表1。由表可见,健脾生血颗粒浸膏各给药组胎鼠身长、尾长及低、中剂量组胎鼠平均体重、身长与阴性对照组相比差异均无统计学意义(P>0.05),高剂量组胎鼠平均体重显著低于阴性对照组。包括阴性对照组在内各组可见1~3例皮下出血,健脾生血颗粒浸膏各给药组胎鼠外观均无畸形。
通过对胎鼠骨骼的检查发现,高剂量的健脾生血颗粒浸膏可导致胎鼠骨骼发育延迟,主要表现为囟门闭合不全,枕骨、胸骨、四肢骨骨化不全、脊椎骨弯曲等。结果见表2。经头部徒手切片及其他新鲜内脏检查,评价健脾生血颗粒浸膏对胎鼠内脏的影响,结果表明,各试验组均可见少数胎鼠内脏异常。与阴性对照组相比,低、中、高剂量的健脾生血颗粒浸膏组差异有统计学意义,而阳性对照组明显影响胎鼠内脏发育,主要表现为眼缺失、肾积水、脑室萎缩等。
3 讨论
本研究为健脾生血颗粒(片)二次开发研究内容的一部分,严格按照GLP操作规范对产品的生殖毒性进行评价。结果显示,阳性对照品维生素A醋酸酯0.08 g/kg经口灌胃给药后出现明显致畸作用,表现为骨化不全、骨缺失、内脏积水、眼缺失等,说明本实验系统结果可靠。综合评价各试验结果可见,低、中剂量的健脾生血颗粒浸膏对亲代大鼠和子代胎鼠均无明显毒性;高剂量的健脾生血颗粒浸膏可导致亲代大鼠体重和摄食量下降,影响部分胎鼠的发育,主要表现为体重减轻,少数动物关节畸形等。因此,在本实验条件下,健脾生血颗粒浸膏未见毒性作用剂量为3.48 g/kg。以人体质量60 kg计算,约相当于人临床最大用量的42倍、12岁以下儿童临床最大用量的30倍。
健脾生血颗粒是由13味中药和西药硫酸亚铁组成的复方制剂,通过文献查阅,中药部分并无毒性药材[11-15]。分析处方,硫酸亚铁成分可能在高剂量组产生毒性作用中占主导角色。但健脾生血颗粒浸膏剂量在3.48 g/kg以下时,对孕鼠亲、子代均无不良反应。提示患者按正常剂量服用本品时,对妊娠期妇女和胎儿是安全的,尤其是对于铁缺乏的缺铁性贫血患者,吸收的铁经血红蛋白利用后,循环铁和结合铁相对更少。但为保证安全,不应额外再服用其他铁制剂。本研究结果作为生殖毒性试验研究的一部分,结合生育力与早期胚胎发育毒性试验和围产期毒性试验研究,将对产品在妊娠期妇女缺铁性贫血治疗中的安全性提供重要参考。同时,本研究模式也可为其他品种的上市后再评价提供借鉴。
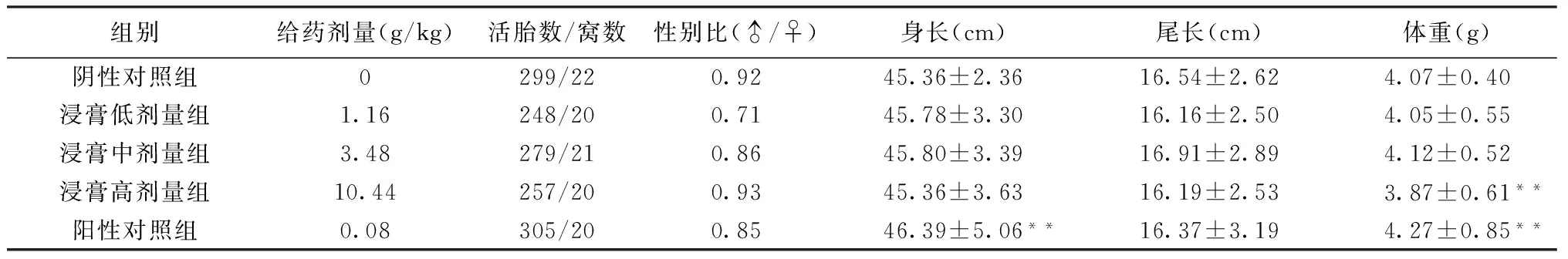
表1 健脾生血颗粒浸膏对胎鼠外观的影响(Mean±SD)
注:与同类阴性对照组相比,**P<0.01。
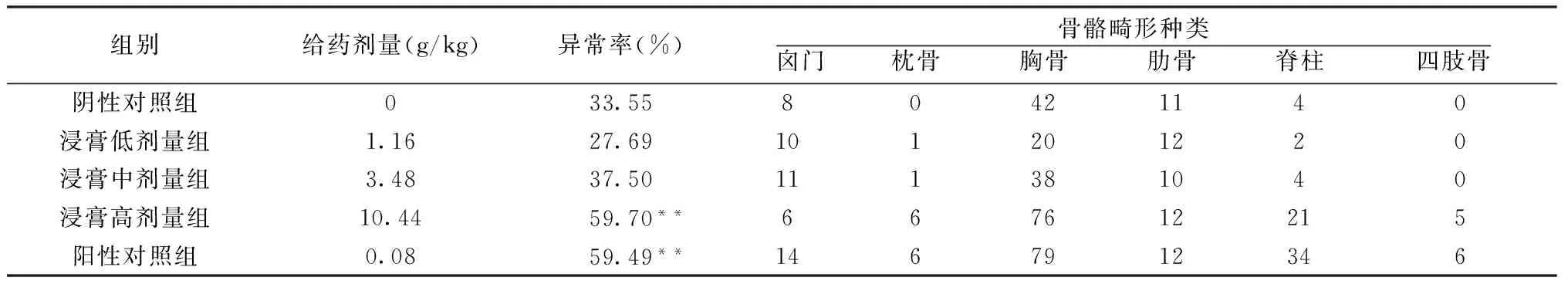
表2 健脾生血颗粒浸膏对胎鼠骨骼的影响
注:与同类阴性对照组相比,**P<0.01。
[1]艾青华,黎元元,谢雁鸣.参芪扶正注射液上市后安全性再评价研究[J].中国中药杂志,2014,39(18):3633-3636.
[2]叶祖光,张广平.中药安全性评价的发展、现状及其对策[J].中国实验方剂学杂志,2014,10(16):1-6.
[3]王志飞,谢雁鸣.中药上市后再评价发展概述[J].世界中医药,2014,9(9):1113-1116.
[4]孙艳.健脾生血颗粒治疗婴幼儿缺铁性贫血50例临床观察[J].中国现代医生,2015,53(3):127-129.
[5]赖鹏程,沈朝霞.健脾生血颗粒治疗小儿缺铁性贫血临床研究[J].儿科药学杂志,2014,20(4):36-38.
[6]白婧.妊娠合并贫血64例临床诊治分析[J].中国实用医药,2014,9(2):137-138.
[7]何群双.健脾生血颗粒治疗孕妇缺铁性贫血的疗效观察[J].湖北中医杂志,2006,28(8):14-15.
[8]黄逸玲.健脾生血颗粒治疗妊娠合并贫血48例观察[J].实用中医药杂志,2006,22(2):103.
[9]Liang A,Li C,Liu T,et al.Study on embryo toxicity of Cinnabaris[J].China Journal of Chinese Materia Medica,2009,34(21):2794-2798.
[10]Chen XD,Deng M,Zhou JS,et al.Bone Morphogenetic Protein-2 regulates in vitro osteogenic differentiation of mouse adipose derived stem cells[J].European Review for Medical and Pharmacological Sciences,2015,19(11):2048-2053.
[11]成金乐,邓雯,黄萍,等.党参破壁粉粒的抗溃疡作用与急性毒性实验研究[J].西北药学杂志,2011,26(2):120-122.
[12]凌宗全.白术化学成分及药理作用研究进展[J].内蒙古中医药,2013,32(35):105-106.
[13]王东升,李锦宇,罗超应,等.白术提取液急性毒性试验[J].西北农业学报,2011,20(5):40-43.
[14]李林燕,柳燕,曹小帅,等.南五味子软胶囊对大鼠长期毒性的实验研究[J].安徽医药,2012,16(5):586-588.
[15]张永娜.五味子影响黄药子肝肾毒性的试验观察[J].泰山医学院学报,2014,35(8):794-796.
(2015-08-26收稿 责任编辑:王明)
Effect of Invigorating Spleen-Generating Blood Granule on Embryo-fetal Development of Rats
Zhao Gang1, Xia Ying2, Huang Zhijun1, Pei Xuejun1, Tang Huidan1
(1AcademyofPediatricDrugs,JianminPharmaceuticalGroup,Wuhan430052,China; 2CenterofFoodandDrugSafetyEvaluationinHubei,Wuhan430073,China)
Objective: To investigate the effects of Invigorating Spleen-Generating Blood Granule on embryo-fetal development of rats after intragastric administration. Methods: Pregnant rats were randomly divided into five groups: negative control, positive control, treatment groups with low, medium, or high dosage. The control groups were given oral administration with extract of the granule at 1.16、3.48、10.44 g/kg/d respectively for 10 days after six days' pregnancy. The positive control group were given Vitamin A acetate at 0.08 g/kg/d;the negative group were given pure water with same volume. Then the weight, body length, food consumption, and clinical features of pregnant rats were recorded. Pregnant rats were dissected at their 20 days' pregnancy. Then placentas, fetal rat appearances, skeleton, viscera, and numbers of corpus luteum, live fetus, dying fetus, absorbed fetus, implantation and other factors were recorded. Results: Obvious teratogenesis appeared in positive control rats, showed the reliability of the experiment. No abnormal clinical symptoms were observed in the rats of all treatment groups. There were no statistical differences of numbers of corpus luteum, live fetus, dying fetus, absorbed fetus, and implantation among the rats of all treatment groups and negative control. No general toxicity was found from rats with low or medium dosage. But high dosage of extract may result in a decline of weight, and food consumption. Furthermore, the development of fetal rats was also affected. Conclusion: The safe dosage of Invigorating Spleen-Generating Blood Granule on embryo-fetal development of rats was under 3.48 g/kg, 42 times of clinical dosage on human.
Invigorating Spleen-Generating Blood Granule; Rat; Toxicity on embryo-fetal development
武汉市科技攻关计划项目(编号:2013070204020053)
赵刚(1983.10—),男,博士,高级工程师,从事儿童药物新药开发与药理毒理研究,E-mail:zhaogangsna@126.com
R285.5
A
10.3969/j.issn.1673-7202.2015.10.034

