乙基纤维素对油脂流变性质和凝胶特性的影响
罗淑玲 傅 红 张 虹 郑丽婷 林炎娟 胡 鹏 叶秀云,3
(福州大学生物科学与工程学院1,福州 350108)(丰益(上海)生物技术研发中心有限公司2,上海 200137)(福州大学酶工程研究所3,福州 350108)
有机凝胶剂可以为液体油提供类似于固体流变学特性的功能。因此,近年来凝胶剂在食用油脂的结构化中得到广泛应用,可作为替代特种油脂产品如冰激凌、人造奶油、起酥油和奶酪等的饱和脂肪酸或反式脂肪酸的手段,降低心血管疾病的风险[1-2]。
2011 年,Dey 等[3]和 Laredo等[4]发现了高聚物乙基纤维素(ethyl cellulose,EC)能够有效地用于油脂凝胶化,当添加量为2%时即可形成凝胶网络结构[5-6],并具有长期的物理稳定性[7]。乙基纤维素是纤维素的一种重要的衍生物,无毒[8]、可降解,在医药领域应用广泛,可以用作片剂粘合剂和薄膜包衣等材料,也可用作混合材料制备包衣缓释制剂,是一种良好的药物辅助材料[9]。而EC在油脂领域的研究,主要集中于在油相体系中添加特定相对分子质量的EC,观察油相宏观性质(即硬度、稳定、弹性等)的变化特征,以及EC形成高分子网络结构防止油脂结构坍塌的性能[10]。一般来说,网络结构对液态油的截留能力直接影响到塑性脂肪的质构、外观及物理稳定性等[11-12]。而高分子溶液的许多重要性质例如力学性能、溶解性能以及流动性能等[13]均和高聚物相对分子质量有关,而高聚物的相对分子质量又与其特性黏度之间存在依赖关系,即高聚物的特性黏度越大,其相对分子质量也越大[14]。但是到目前为止,对于不同相对分子质量的EC及其所具有的不同特性黏度对油脂流变性能及凝胶特性的影响,文献中尚未有具体报道。因此,本研究探讨了一系列不同特性黏度(相对分子质量)的EC在构建液态油脂网络结构时,对油脂流变性质、凝胶特性的影响以及它截留液态油脂的能力,为进一步探究EC在脂肪产品中的应用提供基础数据。
1 材料与方法
1.1 原料与试剂
5种不同特性黏度等级的乙基纤维素(EC):EC7(特性黏度值6~9 mPa·s),EC20(特性黏度值18~22 mPa·s),EC50(特性黏度值 45 ~55 mPa·s),EC100(特性黏度值90~110 mPa·s),EC200(特性黏度值180~220 mPa·s),其中乙氧基含量为47.5% ~49.5%:阿拉丁试剂有限公司;根据高聚物在溶液中的特性黏度[η]与其相对分子质量M的相关关系Market-Houwink方程即[η]=KMα(K和 α分别为2个参数)可知[14],5种不同黏度的EC按照相对分子质量从小到大依次为EC7,EC20,EC50,EC100和EC200。
大豆油:嘉里特种油脂(上海)有限公司。
1.2 仪器与设备
MCR301流变仪:奥地利安东帕有限公司;Nikon ECLIPSE E100生物显微镜:上海泽仕光电科技有限公司;TA-XT2质构仪:英国 Stable Micro System公司。
1.3 试验方法
1.3.1 EC 溶液的制备
称取一定质量的乙基纤维素于大豆油中,加热搅拌直至溶胀溶解,按此方法分别配置不同质量分数的溶液。
1.3.2 显微镜观察
取适量EC油相溶液于载玻片上,盖上盖玻片,轻压成透明薄片,用光学显微镜低倍镜(40×)观察样品形貌。
1.3.3 静态流变性质测定
平行板(PP50-SN18341;gap=1 mm),剪切速率范围:10-4~103s-1,温度:25 ℃,取22 个数据点。测定质量分数为2%的不同黏度等级EC溶液表观黏度随剪切速率的变化。
1.3.4 动态流变性质测定
1.3.4.1 应变扫描(线性黏弹区的确定)
平行板(PP50-SN18341;gap=1 mm),测定复合模量G*随振荡应变的变化,复合模量G*恒定的振荡应变区为线性黏弹区。
1.3.4.2 频率扫描
平行板(PP50-SN18341;gap=1mm),在线性黏弹区固定一振荡应变,测定不同质量分数不同黏度等级EC溶液的储能模量G’随振荡频率f的变化。
1.3.5 质构分析
质构仪TPA2测试模式,以直径为5 mm的探头(P/5)测样品硬度值[15]:测试前速度1.0 mm/s;测试速度3.0 mm/s;测试后速度3.0 mm/s;1次距离10.0 mm;2 次距离 10.0 mm;间隔时间5.00 s。
1.3.6 油迁移测定
称取一定质量的EC油凝胶样品置于双圈牌中速定量滤纸(直径18 cm)的中心位置,放置2 h后移开样品并对滤纸进行称量[16]。通过下式计算油凝胶的油脂损失率。

式中:m为滤纸和油脂迁移的质量/g;m0为空白滤纸的质量/g;M为凝胶样品的质量/g。
2 结果与讨论
2.1 EC溶液的静态流变性质
2.1.1 EC黏度对油相溶液表观黏度的影响
图1为不同黏度等级EC溶液的表观黏度随剪切速率的变化曲线。数据显示,EC溶液的表观黏度随剪切速率增大而减小,属于“剪切变稀”的假塑性流体。通常认为,“剪切变稀”现象与溶液中的高分子链缠结有关,而缠结点处于不断形成和拆散的动态平衡中,当体系所受外力增大时,体系的缠结点被拆散的速度远大于形成速度,导致溶液中缠结点浓度下降,故在宏观上表现为溶液黏度减小。
从图1中可以看出,在剪切速率为10-4~100 s-1的低剪切速率区,EC黏度大小对油相溶液的表观黏度有较大影响。当EC黏度等级为 EC7,EC20,EC50,EC100时,溶液的表观黏度随EC黏度增加而增大,这是因为EC黏度越大,相对分子质量越大,高分子链也越长,所以分子链的缠结作用更明显;而且EC分子链中含有大量的-OH,可形成分子内或分子间氢键,故EC黏度越大导致分子链间的相互作用更强。
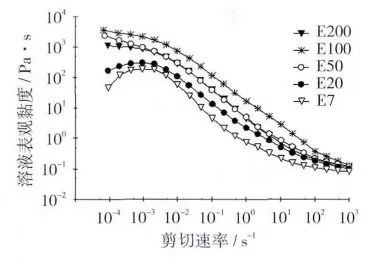
图1 不同黏度等级EC油相溶液的表观黏度随剪切速率变化曲线
但是,当EC黏度等级为EC200时,溶液的表观黏度反而降低,这可能是因为随着EC黏度增加,分子链间的氢键作用增强,导致其玻璃化转变温度也相应升高[12],需要更大的外界作用力才能破坏分子链间的氢键。因此,在相同条件下,与EC7~EC100相比,EC200更难完全溶解于油相体系中而导致溶液的表观黏度降低。图2为EC100和EC200的油相溶液显微镜图像,从图2中可看出,a为均一的油相溶液,表明EC100高分子链在油相中已完全溶解;b为不均一的油相溶液,溶液中还悬浮着未完全溶解的EC200小颗粒。不同黏度等级EC在油相中的溶解情况可通过图3形象地表现出来,图3中显示,与EC7~EC100相比,由于EC200分子链较长,分子链间的氢键作用增强,使得油脂分子不能完全地进入EC200分子链间,导致EC200在油脂中的溶解能力降低,故溶液表观黏度减小。

图2 EC100和EC200油相溶液的显微镜图像

图3 不同黏度等级EC在大豆油中的溶解示意图
图1 还显示,在剪切速率为100~1 000 s-1的高剪切速率区,剪切速率对溶液表观黏度的影响作用远大于EC黏度,可能因为在强外力作用下,溶液中EC分子链的缠结点受到严重破坏,缠结点的形成速度远远小于拆散速度。当剪切速率增加为1 000 s-1时,不同黏度等级EC溶液的表观黏度接近,均在0.1 Pa·s左右。
2.1.2 EC质量分数对溶液表观黏度的影响
图4为不同质量分数EC100油相溶液的表观黏度随剪切速率变化曲线,结果显示,在一定剪切速率下,溶液表观黏度随着EC质量分数增加而增加。因为EC质量分数增加使得油相体系内高分子链数目增多,促使溶液内部形成更强的缠结网络结构,表现出更大的表观黏度。
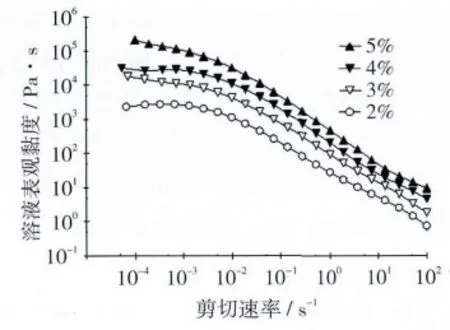
图4 不同质量分数EC100油相溶液的表观黏度随剪切速率变化曲线
2.2 EC油相溶液的动态流变学性质
2.2.1 线性黏弹区的确定

图5 不同黏度EC油凝胶的线性粘弹性区域
溶液粘弹性质测定需要在线性黏弹区内进行[17]。线性黏弹区指复合模量G*(G*=G'+iG″)不随振荡应力或应变变化的区域。由图5可知,质量分数为8%的EC油凝胶在线性黏弹区所对应的振荡应变范围分别是:EC7为0.01% ~0.68%,EC20为 0.01% ~0.99%,EC50 为 0.01% ~0.99%,EC100为 0.01% ~1.47%,EC200 为 0.01% ~0.15%。因此,本研究选取振荡应变值为0.1%时测定不同黏度等级EC油凝胶的动态流变性质。
2.2.2 EC油相溶液的动态流变学性质
在不同质量分数和不同黏度等级EC条件下,溶液的储能模量G'与振荡频率f的关系如图6所示,当G'曲线表现出与振荡频率无关性的平台趋势时,表明此时已形成稳定的凝胶网络结构[18]。结果可以看出,当溶液质量分数增加时G'曲线平台逐渐变宽,而且平台的高度明显增加,表明EC质量分数对溶液中凝胶网络结构的形成有显著影响,并且随着质量分数的增加凝胶网络结构越稳定。
另一方面,各图质量分数为8%的不同黏度等级EC油溶液的流变特性显示,当EC黏度较低(EC7)时,溶液的G'曲线在低频区出现一个平台,但在高频区仍表现出一定的频率相关性,说明EC7在该浓度下未能形成稳定的凝胶网络结构。随着EC黏度的增加,G'曲线的频率无关性范围增大,平台高度增加。对EC50和EC100来说,G'曲线完全显示出频率无关性,说明此时溶液已形成稳定的凝胶网络结构,而且EC100的G'值更高,表示其凝胶网络强度更大。但是,EC200油凝胶的凝胶网络稳定性降低,G'值下降,这可能是因为其分子链过长导致在油相中不能完全溶胀所造成的凝胶结构不完整。

图6 不同质量分数和不同黏度等级EC油相溶液的G'~f流变特性
2.3 EC油凝胶的质构分析
当EC质量分数为8%时,研究不同黏度等级EC油凝胶的质构特性,结果如图7所示。由以上结论可知,在EC7~EC100范围内,油凝胶的硬度随着EC黏度等级的增加而增加,在EC100时达到最大硬度值,为175.94 g。但是EC200的凝胶硬度显著降低,仅达到13.35 g。这一结果和前面的流变特性结果分析相一致,与低黏度等级 EC油凝胶相比,由于EC200不具备凝胶网络结构形成的完整性,导致其凝胶硬度相应减小。
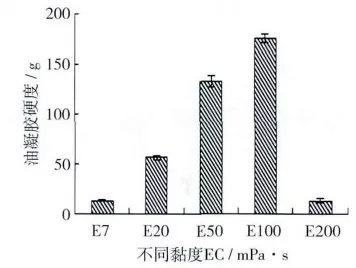
图7 质量分数为8%的不同黏度等级EC对油凝胶硬度的影响

图8 不同质量分数EC100油凝胶的硬度
EC质量分数对油凝胶硬度的影响如图8所示,当质量分数为4%~14%时,油凝胶硬度随着EC100质量分数增加呈现幂函数型增长趋势。因此,可认为质量分数对油凝胶硬度的影响效果非常显著。
2.4 EC油凝胶的油脂损失率
EC通过高分子链相互缠结及氢键等相互作用力构成凝胶网络结构,将油脂截留。通过测定凝胶的油脂损失率可以反映凝胶网络的稳定性。
图9显示,在EC7~EC100范围内时,当EC黏度增加时凝胶的油脂损失率减少,其中EC100最小,其凝胶油脂损失率仅为凝胶中液态油的3.14%,由上可知EC100凝胶的网络结构最为稳定。而EC200油凝胶的油脂损失率最高,达到15.43%,这与前面所研究得到的流变和质构的结论相一致。
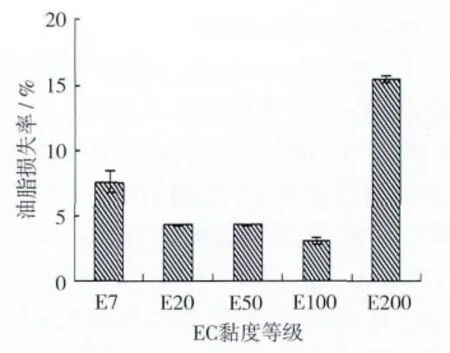
图9 质量分数为8%的不同黏度等级EC对凝胶油脂损失率的影响

图10 EC100质量分数对凝胶油脂损失率的影响
溶液质量分数对凝胶油脂损失率的影响结果示于图10,随EC质量分数增加,凝胶的油脂损失率逐渐减少。表明凝胶的网络结构越稳定,其截留液态油脂的能力越强。
3 结论
试验研究表明EC油相溶液为牛顿型流体,溶液的表观黏度随剪切速率增大而减小。在一定剪切速率下,当EC黏度等级为EC7~EC100时,溶液表观黏度随EC黏度增加而增大,而EC200溶液的表观黏度下降。并且EC质量分数增加,溶液的表观黏度也增大。
EC油相溶液在低浓度时主要表现出黏性行为,当质量分数增大时溶液开始出现凝胶化,且随着溶液质量分数增加,凝胶的网络结构稳定性、硬度以及对液态油脂的截留能力均增强,在8%时,EC100油凝胶的物理性质最佳。
[1]Blanco Muoz M A.Olive oil in food spreads[J].Grasasy Aceites,2004,55:92-94
[2]Marangoni AG,Idziak SH J,Vega C,et al.Encapsulation-structuring of edible oil attenuates acute elevation of blood lipids and insulin in humans[J].Soft Matter,2007(3):183-187
[3]Dey T,Kim DA,Marangoni A G.Ethylcellulose oleogels.In:Marangoni AG,Garti N(eds)Edible oleogels:structure and health implications[M].Urbana:AOCS Press,2011:295-311
[4]Laredo T,Barbut S,Marangoni A G.Molecular interactions of polymer oleogelation[J].Soft Matter,2011(7):2734 -2743
[5]Aiache J.M,Gauthier P,Aiache S.New gelification method for vegetable oils I:Cosmetic application[J].International Journal of Cosmetic Science,1992,14(5):228-234
[6]Gauthier P,Aiache S,Aiache JM.Novel glyceride gels II.Viscosity characteristics[J].International Journal of Cosmetic Science,1996,18(5):229-235
[7]Sánchez R,Franco JM,Delgado M A,et al.Development of new green lubricating grease formulations based on cellulosic derivatives and castor oil[J].Green Chemistry,2009(11):686-693
[8]张扬,扬子明,邓思贤,等.乙基纤维素——艾叶粉溶液微胶囊的制备及缓释性能研究[J].广东化工,2009,36(5):6-8
[9]吴晓辉,王林格,黄勇.电场纺丝法制备药物缓释乙基纤维素纤维的研究[J].高分子学报,2006(7):264-268
[10]Laredo T,Barbut S,Marangoni A.G.Molecular interactions of polymer oleogelation[J].Soft Matter,2011,7(6):2734-2743
[11]Firouz Jahaniaval,Yukio Kakuda,Varghese Abraham.Oil-binding capacity of plastic fats:effects of intermediate melting point TAG[J].Journal of American oil and Chemistries Society,2002,79(4):389 -394
[12]Nuria C,Acevedo,Fernanda Peyronel,et al.Marangoni.Nanoscale structure intercrystalline interactions in fat crystal networks[J].Current Opinion in Colloid & Interface Science,2011,16:374-383
[13]中国科学技术大学高分子物理教研室.高聚物的结构与性能[M].北京:科学出版社,1981
[14]郑昌仁.高聚物分子量及其分布[M].北京:化学工业出版社,1986
[15]池建伟,李阳,张虹,等.β-谷甾醇与γ-谷维素键合特征的红外光谱分析[J].中国粮油学报,2013,28(8):97-101
[16]Tolibjon SOmonov,Laziz Bouzidi,Suresh S.Quantification of oil binding capacity of structuring fats:A novel method and its application[J].Chemistry and Physics of Lipids,2010,163:728-740
[17]罗昌荣.高质量番茄粉的研制及其贮藏稳定性的研究[D].无锡:江南大学,2001
[18]张俐娜.天然高分子科学与材料[M].北京:科学出版社,2007:260-264.

