非晶态磷酸铁的沉淀反应机理及性能
严 鹏,谢 刚,张春明,何丹农,3
(1.纳米技术及应用国家工程研究中心,上海 200241; 2.福建省建筑科学研究院,福建 福州 350000; 3.上海交通大学材料科学与工程学院,上海 200240)
非晶态磷酸铁的沉淀反应机理及性能
严 鹏1,谢 刚2,张春明1,何丹农1,3
(1.纳米技术及应用国家工程研究中心,上海 200241; 2.福建省建筑科学研究院,福建 福州 350000; 3.上海交通大学材料科学与工程学院,上海 200240)
采用微反应器合成正极材料纳米磷酸铁(FePO4),对样品进行分析,并研究沉淀反应的机理。微反应器能将FePO4的颗粒尺寸控制在20~30 nm,同时非晶态FePO4的电化学性能较好。以0.1C的电流在4.2~2.5 V充放电,前驱体以及在350 ℃、400 ℃、450 ℃、500 ℃焙烧样品的首次放电比容量分别为115.0 mAh/g、99.5 mAh/g、82.5 mAh/g、63.5 mAh/g和41.0 mAh/g;以科琴黑作为导电剂,采用400 ℃下焙烧制备的FePO4组装电池,首次放电比容量达140.0 mAh/g,循环30次的容量保持率为78.2%。
微反应器; 非晶型; 磷酸铁(FePO4); 导电剂
磷酸铁(FePO4)不仅可以作为合成高性能磷酸铁锂(LiFePO4)的原料,还可直接作为电极材料,进行尝试性基础研究,且只需在较低温度条件下合成、成本低廉,并拥有较高的放电容量[1]。
本文作者在前期研究的基础上[2],通过微通道反应器一步法快速合成纳米FePO4,着重对纳米FePO4沉淀反应机理进行摸索,控制反应过程,探索纳米FePO4沉淀反应的规律,建立理论模型;考察焙烧温度对纯FePO4电化学性能的影响,研究导电剂对纯FePO4电化学性能的影响。
1 实验
1.1 FePO4的制备
称取Fe(NO3)3·9H2O(汕头产,98.5%)和(NH4)2HPO4(汕头产,99%),分别配制成0.3 mol/L的溶液。用注射器分别抽取100 ml,通过精密注射泵以100 ml/min的速度注入到微通道反应器中,两股液体混合,反应生成FePO4·xH2O沉淀。将得到的样品放入离心机中,以3 500 r/min的转速离心5 min,进行固液分离,重复离心操作3次。将样品放在玻璃皿上,置于鼓风干燥箱中,于120 ℃下干燥数小时,得到干燥的FePO4·xH2O,将烘干后的样品分别在350 ℃、400 ℃、450 ℃、500 ℃及550 ℃下焙烧,得到FePO4。
量取100 ml Fe(NO3)3溶液,置于烧杯中,边搅拌,边滴加100 ml(NH4)2HPO4溶液,反应生成FePO4·xH2O沉淀,再用相同的步骤,制备共沉淀法FePO4。
1.2 材料的分析
用JEM-1010型透射电镜(TEM,日本产)观察制备粉体的颗粒形貌与团聚状况。
1.3 电池的组装、测试
将制得的FePO4粉体、导电剂科琴黑(日本产,电池级)或乙炔黑(日本产,电池级)和粘结剂聚偏氟乙烯(成都产,电池级)按质量比8∶1∶1混匀,以N-甲基吡咯烷酮(上海产,AR)为溶剂调成浆料,均匀涂覆于0.01 mm厚的铝箔(江苏产,99.99%)上,在100 ℃下真空(-0.1 MPa)干燥10 h,制成正极。
以金属锂片(成都产,电池级)为负极,Celgard 3501膜(美国产)为隔膜,1 mol/L LiPF6/EC+DEC(体积比1∶1,江苏产)为电解液,在手套箱中组装成CR2025型扣式电池。
在室温下,用BTS-5V1A电池测试系统(深圳产)进行循环性能测试,电压为2.5~4.2 V,电流为0.1C,循环30次。
2 结果与讨论
2.1 FePO4的形貌分析
分别用共沉淀法与与微反应器制备FePO4样品,探讨微反应器在制备纳米颗粒方面的优势。
FePO4的沉淀反应是一个快速的化学反应过程,成核生长都在瞬间完成,因此需要良好的微观混合来提供均一的反应环境,才能制得粒径均一的FePO4。在烧杯中,混合效果有限,尽管有搅拌,但不同区域的反应环境会有差别,特别是当一滴反应溶液滴入到另一种反应溶液中时,瞬间导致局部FePO4浓度过大。由于沉淀反应非常迅速,在混合未完全的情况下已经发生了一部分反应,导致烧杯中局部区域的pH值、反应物过饱和度等偏差较大,生成其他的杂质沉淀。

图1 共沉淀法和微反应器制备的FePO4的TEM图
从图1a可知,共沉淀法制备的FePO4形貌不规整,尺寸不均一,且颗粒团聚明显,与烧杯内微观混合效果不佳有直接联系;从图1b可知,微反应器法制备的FePO4颗粒分散性相对较好,粒径分布较窄。在微反应器中,由于反应器体积微小,达到均匀混合的时间极短(一般为毫秒级别),包含的反应液始终处在较均匀的混合状态,因此产物的纯度较高,颗粒的特性,如大小、形状和化学组成更均匀。
2.2 FePO4沉淀的反应机制
一般认为:成核前的化学反应是Fe3+与PO43-的简单反应,但由于三价铁离子是弱碱阳离子,存在多步水解反应。
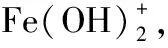
运用Matlab软件进行计算,可得到在不同pH值时,Fe3+、Fe(OH)2+和Fe(OH)2+的相对含量。当溶液pH值为1时,Fe(OH)2+占铁离子物质的量的98.7%,Fe(OH)2+占1.3%,溶液中几乎没有Fe3+;当溶液pH值小于1时,溶液中的铁离子主要以Fe(OH)2+的形式存在。
磷酸根PO43-也存在多步水解反应。设定溶液的pH值为0~14,根据水解平衡常数得知:溶液中磷酸根的存在形式为H3PO4、H2PO4-、HPO42-和PO43-,建立式(2)的磷酸根浓度平衡公式。
运用Matlab软件进行计算,可得到在不同pH值时,H3PO4、H2PO4-、HPO42-和PO43-的相对含量。在pH值为8~10时,溶液中的磷酸根主要以H2PO4-、HPO42-的形式存在;随着pH值不断升高,H2PO4-呈减少的趋势,直到PO43-的产生;当溶液的pH值为9.5时,溶液中的磷酸根主要以HPO42-的形式存在,占磷酸根物质的量的99.3%。
调节两种反应溶液的pH值分别为1、9.5,使得参与反应形成FePO4的反应离子为Fe(OH)2+、Fe(OH)2+和HPO42-,它们之间的反应见式(3)、(4)。
Fe(OH)2++HPO42-+(1-x)H2O→FePO4·xH2O↓
(3)
Fe(OH)2++HPO42-+H++(2-x)H2O
→FePO4·xH2O↓ (4)
当(NH4)2HPO4溶液的pH值过高时,Fe(OH)2+与OH-反应形成红褐色沉淀Fe(OH)3,或两种反应溶液不在特定的pH值范围内,溶液中存在其他离子(如H2PO4-等),导致其他的副反应产生,生成Fe(H2PO4)(HPO4)·xH2O(Ksp=3.9×10-20)[3]、Fe2(HPO4)3(Ksp=8.6×10-41)和Fe(PO4)x(H2PO4)y·nH2O等杂质,势必将影响FePO4的品质[理论n(Fe)∶n(P)=1∶1]。
2.3 不同温度焙烧的FePO4的电化学性能
前驱体和不同温度焙烧的FePO4的0.1C循环性能见图2。

1 前驱体 2 350 ℃ 3 400 ℃ 4 450 ℃ 5 500 ℃
从图2可知,前驱体和在350 ℃、400 ℃、450 ℃、500 ℃下焙烧的样品,0.1C首次放电比容量分别为115.0 mAh/g、99.5 mAh/g、82.5 mAh/g、63.5 mAh/g和41.0 mAh/g,其中前驱体的首次放电比容量最高,但随后衰减明显,第30次循环的放电比容量仅为40.0 mAh/g,容量保持率仅为34.8%,主要是因为未经焙烧的前驱体中含有过多的结晶水和NH4+化合物等杂质,会与电解液中的锂盐发生反应;在350 ℃、400 ℃下焙烧的FePO4,第30次循环的放电比容量分别为73.1 mAh/g、73.0 mAh/g,容量保持率分别为73.5%、88.5%;在450 ℃、500 ℃下焙烧的样品,第30次循环的放电比容量分别为52.5 mAh/g和51.5 mAh/g,容量保持率分别为82.7%、125.6%。
随着焙烧温度的升高,FePO4样品的放电比容量呈下降的趋势,原因是样品会由无定相逐渐转变成晶体相,并伴随着颗粒的长大,阻碍Li+与电子的传输;同时,结晶型FePO4虽然热力学稳定,但电化学性能不活泼,处于电化学惰性状态。FePO4电极材料首次与第2次循环的放电比容量相差较大,主要原因是固体电解质相界面(SEI)膜的生成,对电极材料的电化学性能有一个负面效应,如消耗部分Li+等,导致出现不可逆容量损失。
2.4 导电剂对FePO4电化学性能的影响
在400 ℃下焙烧制备的FePO4与导电剂乙炔黑、科琴黑机械混合后的0.1C循环性能见图3。
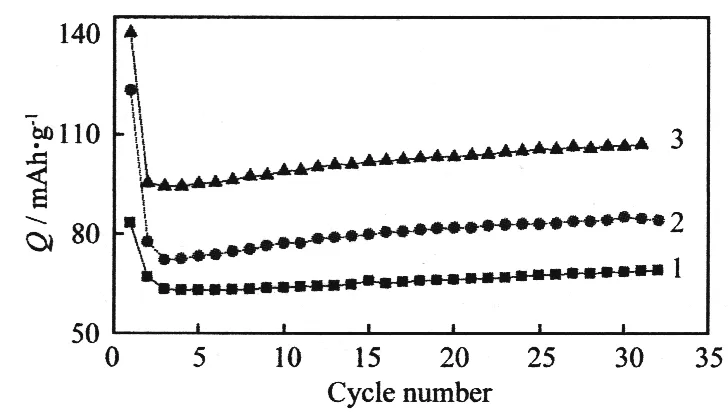
1 无导电剂 2 乙炔黑 3 科琴黑
从图3可知,未添加导电剂的FePO4,首次和第30次循环的放电比容量分别为85.0 mAh/g、73.0 mAh/g;用乙炔黑作为导电剂后,首次放电比容量提高到125.0 mAh/g,第30次循环的容量保持率为67.6%;用科琴黑作为导电剂后,首次放电比容量为140.0 mAh/g,第30次循环的容量保持率为78.2%。科琴黑比乙炔黑具有更高的导电性,可提高FePO4颗粒之间的电子传导能力。
3 结论
采用微通道反应器制备的FePO4颗粒分散性相对较好,颗粒的粒径分布也较窄;
FePO4沉淀反应机理进行探讨,参与反应形成FePO4的反应离子为Fe(OH)2+、Fe(OH)2+和HPO42-。
非晶态的FePO4电化学性能最佳,结晶态的FePO4虽然热力学稳定,但电化学性能不活泼,处于电化学惰性状态;以科琴黑为导电剂的效果最佳,首次放电比容量可达到140.0 mAh/g,第30次循环的容量保持率为78.2%。
[1] YANG Xu-lai(杨续来),LIU Cheng-shi(刘成士),XIE Jia(谢佳),etal.磷酸铁锂磁性杂质对电池自放电的影响[J].Battery Bimonthly(电池),2013,42(6):314-317.
[2] Yan P,Lu L,Liu X,etal.An economic and scalable approach to synthesize high power LiFePO4/C nanocomposites from nano-FePO4precipitated from an impinging jet reactor[J].J Mater Chem A,2013,1(35):10 429-10 435.
[3] Pierri E,Tsamouras D,Dalas E.Ferric phosphate precipitation in aqueous media[J].J Cryst Growth,2000,213(1):93-98.
Precipitation reaction mechanism and performance of amorphous ferric phosphate
YAN Peng1,XIE Gang2,ZHANG Chun-ming1,HE Dan-nong1,3
(1.NationalEngineeringResearchCenterforNanotechnology,Shanghai200241,China;2.FujianAcademyofBuildingResearch,Fuzhou,Fujian350000,China;3.SchoolofMaterialScienceandEngineering,ShanghaiJiaotongUniversity,Shanghai200240,China)
Cathode material nano ferric phosphate(FePO4)was synthesized by micro-reactor and the precipitation reaction mechanism was studied.The prepared samples were characterized.The amorphous FePO4was controlled in a narrow particle size distribution of 20~30 nm and the amorphous FePO4showed better electrochemical performance.When charged-discharged in 4.2~2.5 V with the current of 0.1C,the specific discharge capacity of precursor and the samples sintered at 350 ℃, 400 ℃, 450 ℃, 500 ℃ was 115.0 mAh/g,99.5 mAh/g,82.5 mAh/g,63.5 mAh/g and 41.0mAh/g,respectively.The cell using Ketjen black as conductive agent and assembled with FePO4prepared by sintered at 400 ℃ had the initial specific discharge capacity of 140.0 mAh/g,the capacity retention was 78.2% after 30 cycles.
micro-reactor; amorphous; ferric phosphate(FePO4); conductive agent
严 鹏(1987-),男,江苏人,纳米技术及应用国家工程研究中心工程师,硕士,研究方向:新能源材料,本文联系人;
国家自然科学基金(21171116),国家国际科技合作项目(2012DFG11660),上海启明星计划(B类)(14QB1402900),上海市自然科学基金(14ZR1429500)
TM912.9
A
1001-1579(2015)05-0241-03
2015-01-15
谢 刚(1987-),男,江西人,福建省建筑科学研究院工程师,硕士,研究方向:功能材料制备及分析;
张春明(1983-),男,江苏人,纳米技术及应用国家工程研究中心副研究员,博士,研究方向:新能源材料;
何丹农(1956-),男,上海人,纳米技术及应用国家工程研究中心主任,上海交通大学材料科学与工程学院,教授,博士,研究方向:纳米材料及器件。

