盐酸头孢他美酯干混悬剂微生物限度检查方法的建立
甘永琦,朱 斌(广西食品药品检验所,南宁 530021)
盐酸头孢他美酯是第三代口服广谱头孢菌素类抗生素。其通过抑制细菌细胞壁合成过程中黏肽链的交叉连结,使细菌不能形成完整的细胞壁,从而发挥抗菌作用,且其活性不受细菌产生的β-内酰胺酶的影响。其对链球菌属、肺炎链球菌等革兰阳性菌及大肠埃希菌、流感嗜血杆菌、克雷伯菌属、沙门菌属、志贺菌属、淋病奈瑟氏球菌等革兰阴性菌都有很强的抗菌活性,尤其对第一、二代头孢菌素敏感性低的沙雷菌属、吲哚阳性变形杆菌、肠杆菌属及柠檬酸菌属的抗菌活性较为显著,但其对假单胞菌、支原体、衣原体、肠球菌等耐药性微生物无效[1-5]。自1992年上市以来,盐酸头孢他美酯得到了广泛地应用,目前国内生产的剂型有干混悬剂、胶囊和片剂3种。2010年版《中国药典》(二部)规定干混悬剂需进行微生物限度检查。为此,笔者根据2010年版《中国药典》(二部)附录ⅪJ“微生物限度检查法”口服制剂的规定,对盐酸头孢他美酯干混悬剂的微生物限度检查方法进行研究和敏感菌株验证,并用建立的方法对该品种进行细菌、霉菌及酵母菌计数和控制菌检查,以分析其微生物污染状况。
1 材料
1.1 仪器
WGP-500型电热恒温培养箱(上海安亭科学仪器厂);LRH-250A型生化培养箱(广东省医疗器械厂);生物安全柜(新加坡ESCO公司);MSL3768型高压灭菌锅(日本三洋公司)等。
1.2 药品与试剂
盐酸头孢他美酯干混悬剂(浙江普洛康裕制药有限公司,批号:130603、120104、120604、120601、130502、120802、130502、130403;浙江震元制药有限公司,批号:20130103、20121102、20130102、20130102、20130103、20130501、20130503、20120409、20121002、20130502、20121003);pH为7.0的氯化钠-蛋白胨缓冲液(北京三药科技开发公司,批号:120331);氯化钠(国药集团化学试剂有限公司,批号:10019318)。
1.3 菌种
大肠埃希菌(Escherichia coli)[CMCC(B)44102]、金黄色葡萄球菌(Staphylococcus aureus)[CMCC(B)26003]、枯草芽胞杆 菌(Bacillus subtilis)[CMCC(B)63501]、白色念珠菌(Candida albicans)[CMCC(B)98001]、黑 曲 霉[CMCC(F)98003]均由中国医学微生物菌种保藏管理中心提供。
1.4 培养基
营养琼脂培养基(批号:110105)、改良马丁培养基(批号:1202022)、玫瑰红钠琼脂培养基(批号:1204102)、营养肉汤培养基(批号:130311)、胆盐乳糖培养基(BL,批号:121127)等均购自北京三药科技开发公司;4-甲基伞形酮葡糖苷酸培养基(MUG,批号:1304172)和靛基质(批号:130305)均购自北京陆桥技术部有限责任公司。
2 方法与结果
2.1 细菌、霉菌和酵母菌计数方法的建立及验证
2.1.1 菌液的制备 接种大肠埃希菌、金黄色葡萄球菌与枯草芽胞杆菌的新鲜培养物至营养肉汤培养基或营养琼脂培养基中,33 ℃下培养18~24 h;接种白色念珠菌的新鲜培养物至改良马丁培养基或改良马丁琼脂培养基中,25 ℃下培养24~28 h。上述培养物以0.9%无菌氯化钠溶液制成每1 ml含菌数为50~100 CFU的菌悬液(菌悬液制备后应在2 h内使用,保存在2~8 ℃的菌悬液可在24 h内使用)。
2.1.2 供试液的制备 取本品10 g,加pH为7.0的无菌氯化钠-蛋白胨缓冲液至100 ml,用匀浆仪以1 000 r/min匀浆30 s,混匀,静置5~10 min,取上清液作为供试液。
2.1.3 回收率试验(1)试验组:取供试液1 ml,另分别取各试验菌50~100 CFU,分别注入同一平皿中,立即倾注琼脂培养基,待凝固后,置于规定温度下,细菌培养3 d,白色念珠菌和黑曲霉培养5 d,分别平行制备2个平皿,平板计数。(2)菌液组:取试验菌50~100 CFU注入平皿中,立即倾注琼脂培养基,待凝固后,置于规定温度下,细菌培养3 d,白色念珠菌和黑曲霉培养5 d,分别平行制备2个平皿,测定所加入的试验菌数。(3)供试品对照组:取供试液1 ml注入平皿中,立即倾注琼脂培养基,待凝固后,置于37 ℃培养24~48 h,测定供试品的本底菌数。
对照组各试验菌的回收菌应不低于70%。回收率=(试验组平均菌落数-供试品对照组平均菌落数)/菌液组的平均菌落数×100%。
2.1.4 细菌计数方法预试验 根据文献报道[6],选取大肠埃希菌作为敏感菌株,分别采用常规法和薄膜过滤法(冲洗量为100 ml)对2个厂家各1批样品进行方法筛选,结果见表1。
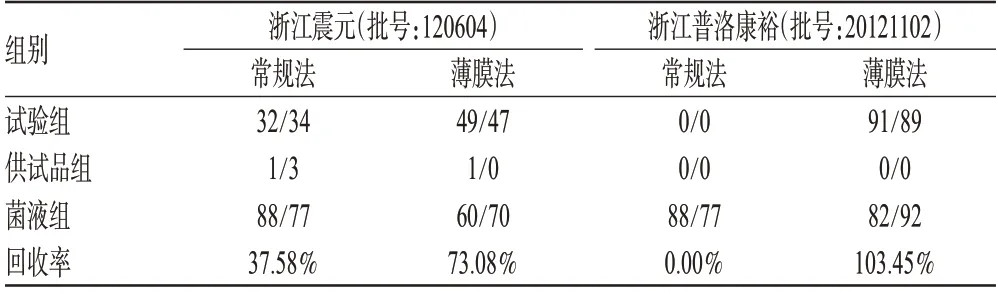
表1 大肠埃希氏菌验证试验结果(CFU/平皿)Tab 1 Verification results ofEscherichia coli(CFU/plate)
由表1可见,采用常规法试验,2个厂家生产的盐酸头孢他美酯的大肠埃希菌回收率均未达到70%,不能有效消除盐酸头孢他美酯对细菌的抑制作用,因此采用常规法进行细菌计数不可行;而采用薄膜过滤法试验结果显示,冲洗量为100 ml时,大肠埃希菌的回收率>70%,符合要求,因此初步确定采用冲洗量为100 ml的薄膜过滤法进行细菌计数。
2.1.5 计数方法的验证 分别对3批样品进行计数方法验证,细菌采用薄膜过滤法,用0.9%无菌氯化钠溶液冲洗100 ml,其他菌种采用常规法进行加菌回收率试验,结果见表2。
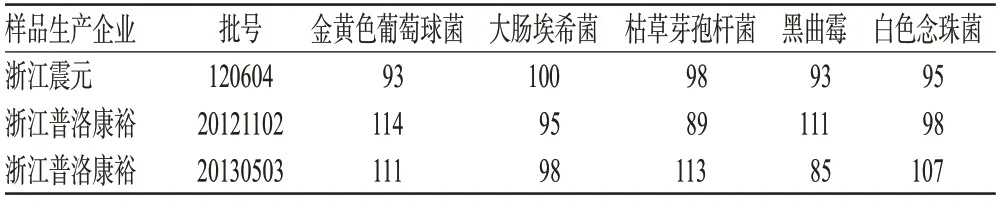
表2 计数方法验证试验回收率结果(%)Tab 2 Recovery results of count verification test
由表2可见,5种规定试验菌的回收率均>70%,符合2010年版《中国药典》(二部)的规定,方法成立。
2.2 控制菌检查方法的建立与验证
2.2.1 菌液的制备 接种大肠埃希菌的新鲜培养物至营养肉汤培养基中,培养18~24 h,用0.9%无菌氯化钠溶液制成每1 ml含菌数为10~100 CFU的菌悬液(菌悬液在室温下放置应在2 h内使用,若保存在2~8 ℃可在24 h内使用)。
2.2.2 控制菌检查方法(1)培养基稀释法:供试品对照组取“2.1.2”项下的供试液10 ml,阳性对照组取供试液10 ml及大肠埃希菌10~100 CFU,阴性对照组取10 ml 0.9%无菌氯化钠溶液,均接种至500 ml的BL培养基中,培养18~24 h。(2)薄膜过滤法:取上述培养基稀释法中各组的试液加入滤膜中,用0.9%无菌氯化钠溶液冲洗100 ml,取出膜接种至100 ml的BL培养基中,培养18~24 h。
取上述培养物0.2 ml,接种至含5 ml MUG培养基的试管内培养,分别于培养5、24 h时置紫外光灯(366 nm)下观察,同时用未接种的MUG培养基作本底对照。若管内培养物呈现荧光,为MUG阳性;不呈现荧光,则为MUG阴性。观察后,沿培养管的管壁加入数滴靛基质试液,若液面呈玫瑰红色,为靛基质阳性;呈试剂本色,则为靛基质阴性。本底对照应为MUG阴性和靛基质阴性。
2.2.3 检查方法的验证 大肠埃希菌检查方法验证试验结果见表3(表中“+”表示MUG阳性,“-”表示MUG阴性)。由表3可见,培养基稀释法中,有1批样品的阳性对照组结果呈阴性,表明该方法不能有效消除盐酸头孢他美酯对大肠埃希菌的抑制作用;而薄膜过滤法中,阴性对照及供试组的MUG和靛基质均呈阴性,阳性对照中2批样品的MUG和靛基质均呈阳性,表明采用薄膜过滤法进行大肠埃希菌检查的方法成立。

表3 大肠埃希菌检查方法验证试验结果Tab 3 Verification results ofEscherichia coli test
上述结果显示,盐酸头孢他美酯干混悬剂对细菌有一定抑制作用,采用薄膜过滤法,加入100 ml的冲洗液可以消除其抑制作用。这表明,采用薄膜过滤法可进行细菌计数及大肠埃希菌检查,采用常规法可进行霉菌和酵母菌计数。
2.4 样品检查
根据微生物限度检查法口服制剂规定,采用建立的微生物限度检验方法对2013年国内共19批盐酸头孢他美酯干混悬剂进行检验,结果均未检出大肠埃希菌,部分样品存在少量细菌污染,但未超出限度,且未检出霉菌和酵母菌,合格率为100%。
3 讨论
头孢他美酯是通过口服吸收的有生物活性的头孢他美的酯类前药[7],其进入肠壁和肝脏中被酯酶水解成头孢他美后发挥其抗菌活性[8]。头孢他美酯干混悬剂不溶于水,而采用离心沉淀法对供试品进行前处理则对样品本身所含的微生物有一定影响[9]。因此,本研究采用静置取上清液的方法制备供试液,以避免药渣对薄膜过滤的干扰。在细菌计数和控制菌检查试验中,本品显示了对大肠埃希菌的抗菌活性。该药物本身仅具有较弱的抗菌活性[10],由于体外缺乏酯酶,在溶液中不能完全水解成头孢他美,导致活性受限。因此,可通过薄膜过滤加入100 ml的冲洗液进行细菌计数和控制菌检查。
本研究发现,不同厂家的样品对大肠埃希菌的体外抗菌活性存在差异,说明企业的生产工艺不同,导致产品在水溶液中的稳定性也不同。本研究为国内首个全面报道头孢他美酯干混悬剂微生物限度检查方法学的研究,并对国内2个厂家生产的样品进行了检验,建立了可行、有效、统一的方法,可为该品种微生物限度检查方法的收载提供借鉴。
[1]张淑华,欧真蓉,陈蜀,等.国产头孢他美酯、头孢他美酯体内外抗菌作用研究[J].中国抗生素杂志,2001,26(2):144.
[2]傅颖君.盐酸头孢他美酯体外抗菌作用[J].江西医学院学报,2002,42(3):30.
[3]阮邹荣,袁虹,孙凌,王选锭.盐酸头孢他美酯的药代动力学研究[J].中国临床药理学杂志,2000,16(4):301.
[4]周大伟,武海霞.盐酸头孢他美酯的药理和临床应用[J].张家口医学院学报,2003,20(6):46.
[5]余泽波,向小琴,王其南,等.国产头孢他美酯片临床观察[J].重庆医学,2000,29(5):458.
[6]彭晓姗,唐映红.盐酸头孢他美酯体内和体外抗菌作用研究[J].中国医药科学,2014,4(1):33.
[7]俞绍鑫,吴朝倩.盐酸头孢他美酯的药理与临床应用[J].中国抗生素杂志,2001,26(2):153.
[8]刘家健,刘敦茀,曾晓辉,等.国产盐酸头孢他美酯的制备[J].中国抗生素杂志,2001,26(2):151.
[9]周剑,李霞.药品微生物限度检查法中几种样品前处理方法的可行性研究[J].中国药房,2012,23(33):3 136.
[10]高丽佳,杨俊卿,刘全,等.头孢他美酯的体内抗菌作用研究[J].儿科药学杂志,2001,7(2):7.

