双环醇片治疗药物性肝损伤疗效与安全性的系统评价Δ
王爱华,张 宁,冯 欣(首都医科大学附属北京妇产医院药剂科,北京 100006)
药物性肝损伤,又称药物性肝炎(Drug-induced liver injury,DILI),是指在药物使用过程中,因药物本身或/及其代谢产物或由于特殊体质对药物的超敏感性或耐受性降低所导致的肝脏损伤[1]。据世界卫生组织统计,DILI已上升至全球死亡原因的第5位[2]。在美国,50%以上的急性肝功能衰竭是由药物引起的[3]。在我国,DILI的发生率较高,仅次于病毒性肝炎及脂肪性肝病(包括酒精性及非酒精性)[4]。此外,有研究发现,成人中丙氨酸氨基转移酶(ALT)的升高有10%~50%是由药物引起的[5]。因此,临床应加强重视并警惕DILI的风险。
目前多种药物均可能引起DILI,如抗肿瘤的化疗药、抗结核药等[6]。在我国,越来越多的研究发现中药也是导致DILI的主要原因[7],可占到临床DILI的4.8%~32.6%[8]。通常,轻度DILI患者在停药后会自行好转,然而对于重度患者或者仍需进行药物治疗的患者,则需要采取保肝治疗。双环醇片主要用于治疗慢性肝炎导致的氨基转移酶升高,然而有研究显示,在改善DILI方面,双环醇片也起到了良好的作用[9]。除双环醇片外,目前在我国通常作为保肝的药物还包括甘草酸二铵、硫普罗宁、还原型谷胱甘肽和葡醛内酯等[10]。多项研究评价了双环醇片对比其他药物治疗DILI的疗效,但这些研究样本量较小、参考价值有限,目前尚无系统的有效性和安全性研究和评价。为此,本研究采用Meta分析的方法系统评价了双环醇片对比其他药物治疗DILI的疗效和安全性,以为临床治疗提供循证参考。
1 资料与方法
1.1 纳入与排除标准
1.1.1 研究类型 国内外公开发表的随机对照试验(RCT)。
1.1.2 研究对象 各种药物导致肝损伤的患者,性别、年龄不限。排除酒精性肝损害、病毒性肝炎和其他非酒精性脂肪性肝炎患者。
1.1.3 干预措施 试验组患者给予双环醇片治疗,对照组患者给予其他阳性药物治疗。
1.1.4 结局指标 主要疗效指标包括总有效率,次要结局指标包括ALT、天冬氨酸氨基转移酶(AST)和总胆红素(TBIL)。疗效判定标准:显效,临床症状和体征消失,肝功能恢复正常;有效,临床症状和体征好转,肝功能下降幅度超过50%;无效,未能达到上述标准。总有效率=(显效例数+有效例数)/总例数×100%[11]。安全性指标为不良反应(ADR)发生率。
1.2 文献检索
计算机检索PubMed、Cochrane图书馆临床试验数据库、中国生物医学文献数据库(CBM)、中文科技期刊数据库(VIP)及中国期刊全文数据库(CNKI)。检索时限从建库起至2013年9月。使用“双环醇(Bicyclol)”和“肝炎(Hepatitis)”或“药物性肝损伤(Drug-induced liver injury,DILI)”等相关中英文主题词进行检索,同时手工检索纳入研究的参考文献。
1.3 质量评价
按照Cochrane系统评价员手册5.0.1版推荐的质量评价标准评价纳入研究的质量[12]:①随机方法是否正确;②是否采用隐藏分组;③是否采用盲法;④失访及其处理是否恰当。将研究的风险偏倚分为“低风险”“不清楚”“高风险”。如果完全满足以上4条质量标准,则发生各种偏倚的可能性最小,视为低风险研究;如果其中1条或1条以上的标准被判定为不清楚,则发生各种偏倚的可能性中等,视为中等风险研究;如果其中1条或1条以上的标准被判定为高风险,则该研究的偏倚风险高,视为高风险研究。质量评价由两位研究者独立进行,若遇分歧,则通过讨论最终达成一致。
1.4 资料提取
主要提取以下资料:第一作者、发表年份、试验组和对照组总例数、患者基本情况(导致DILI药物)、药物治疗方案(剂量及疗程)及结局指标。先由一位研究者进行资料提取,再由另一位研究者重新阅读文献进行核对,有分歧的数据经讨论达成一致。
1.5 统计学方法
采用Rev Man 5.2统计软件进行Meta分析。采用比值比(Odds ratio,OR)或均数差(Mean difference,MD)及其95%可信区间(Confidence interval,CI)作为研究的效应指标,P<0.05为差异有统计学意义。使用χ2进行异质性检验,若P>0.05且I2<50%,则采用固定效应模型进行合并分析;反之,则采用随机效应模型进行合并分析。
2 结果
2.1 纳入研究基本信息与质量评价结果
按“1.2”项下的检索策略共找到774篇摘要,阅读题目和摘要并剔除重复文献后剩余30篇文献,通过获取全文对其进一步评价,最终纳入11篇(项)研究,合计1 183例患者[11,13-22],所有文献均为中文。纳入研究基本信息详见表1。按照Cochrane手册的文献质量评价标准[10],11项研究的偏倚风险均为高风险,详见表2。
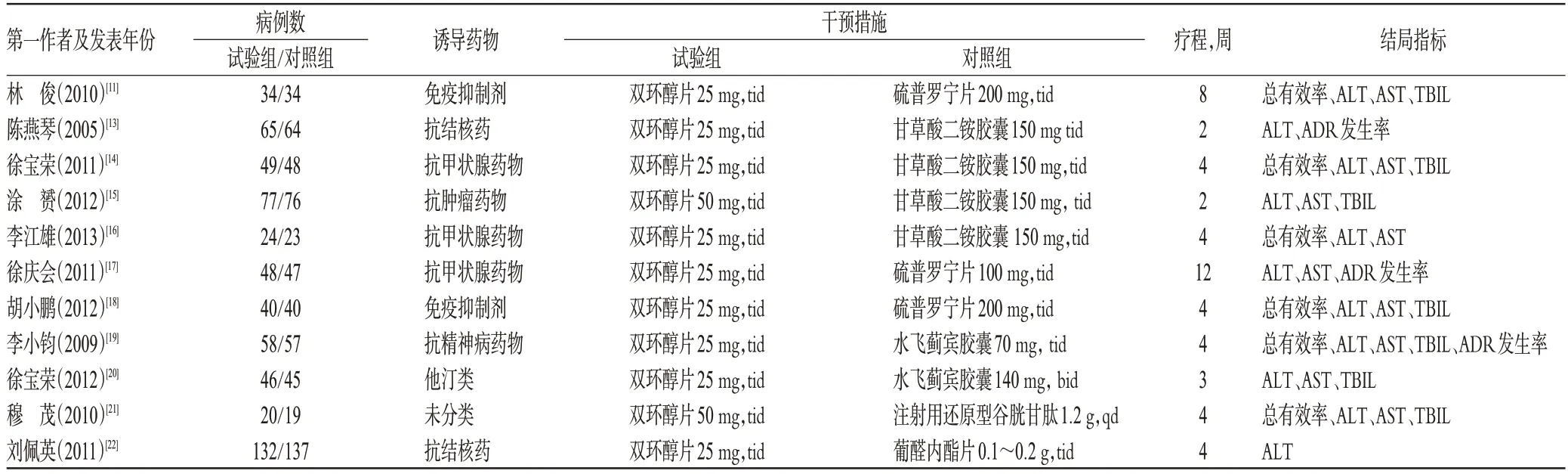
表1 纳入研究基本信息Tab 1 Basic characteristic of included studies
2.2 Meta分析结果
2.2.1 总有效率 6项研究报道了总有效率[11,15,17-19,21],各研究间无统计学异质性(P=0.67,I2=0),采用固定效应模型分析,Meta分析结果见图1。由图1可见,试验组患者总有效率显著高于对照组,两组比较差异有统计学意义[OR=2.83,95%CI(1.59,5.03),P<0.001]。按照不同阳性对照药物进一步行亚组分析。结果发现,双环醇片治疗DILI的总有效率均显著高于甘草酸二胺胶囊[OR=4.83,95%CI(1.61,14.47),P<0.000]和硫普罗宁片[OR=2.56,95%CI(1.06,6.18),P=0.04];但与水飞蓟宾胶囊[OR=1.76,95%CI(0.40,7.75),P=0.45]和注射用还原型谷胱甘肽比较,差异无统计学意义[OR=2.02,95%CI(0.41,9.99),P=0.39]。
2.2.2 ALT 11项研究报道了ALT[11,13-22],各研究间无统计学异质性(P=0.73,I2=0),采用固定效应模型分析,Meta分析结果见图2。由图2可见,试验组患者ALT指标显著优于对照组,两组比较差异有统计学意义[MD=-28.10,95%CI(-34.42,-21.78),P<0.001]。按照不同阳性对照药物进一步行亚组分析。结果发现,双环醇片在改善患者ALT方面显著均优于甘草酸二铵胶囊[MD=-27.03,95%CI(-39.32,-14.75),P<0.000]、硫普罗宁片[MD=-30.19,95%CI(-41.27,-19.11),P<0.000]、水飞蓟宾胶囊[MD=-16.41,95%CI(-31.06,-1.76),P=0.03]、葡醛内酯片[MD=-30.39,95%CI(-49.15,-11.63),P=0.001]和注射用还原型谷胱甘肽[MD=-41.90,95%CI(-60.98,-22.82),P<0.001]。
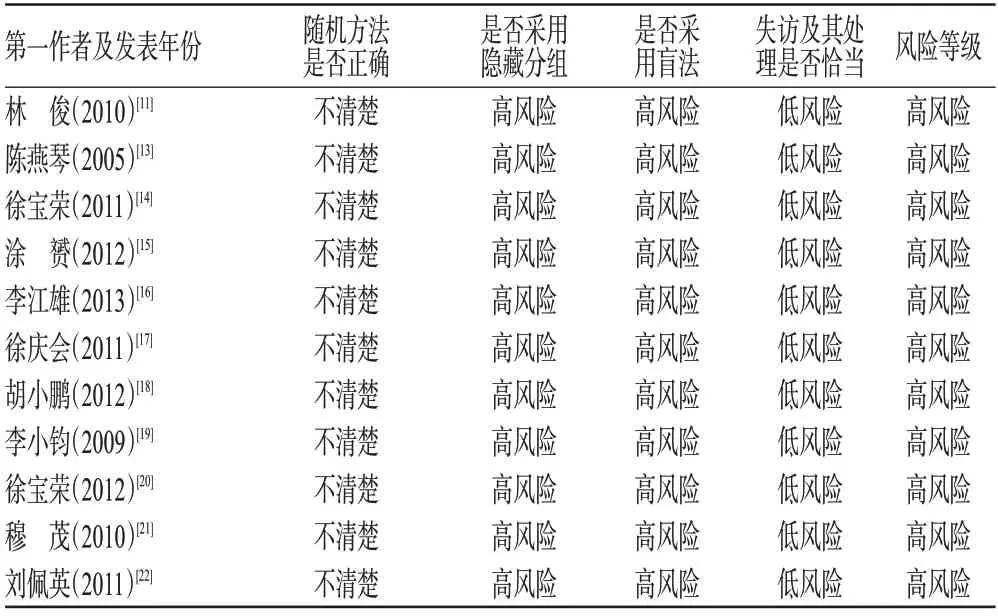
表2 纳入研究质量评价结果Tab 2 Quality evaluation of included studies
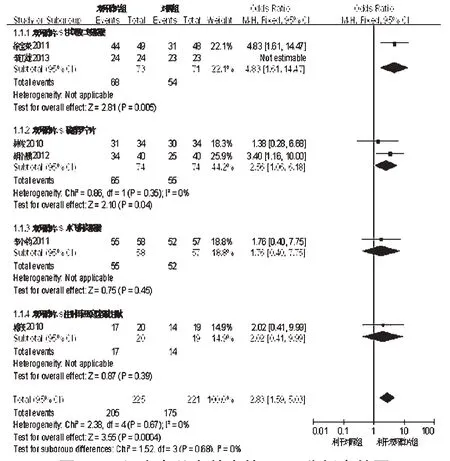
图1 两组患者总有效率的Meta分析森林图Fig 1 Forest plot of Meta-analysis of total efficacy rate in 2 groups
2.2.3 AST 9项研究报道了AST[11,14-21],各研究间无统计学异质性(P=0.43,I2=0),采用固定效应模型分析,Meta分析结果见图3。由图3可见,试验组患者AST指标显著高于对照组,两组比较差异有统计学意义[MD=-15.30,95%CI(-20.77,-9.83),P<0.001]。按照不同阳性对照药物进一步行亚组分析。结果发现,双环醇片在改善患者ALT方面均显著优于甘草酸二铵胶囊[MD=-23.05,95%CI(-33.17,-12.92),P<0.000]、水飞蓟宾胶囊[MD=-13.17,95%CI(-25.55,-0.78),P=0.04]和注射用还原型谷胱甘肽[MD=-22.40,95%CI(-38.35,-6.45),P=0.006];但与硫普罗宁片比较,差异无统计学意义[MD=-8.51,95%CI(-17.22,0.20),P=0.06]。
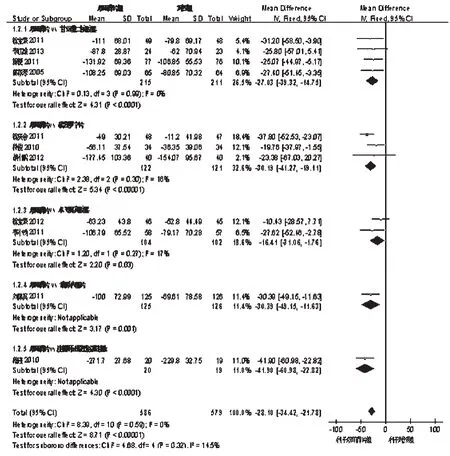
图2 两组患者ALT的Meta分析森林图Fig 2 Forest plot of Meta-analysis of ALT in 2 groups
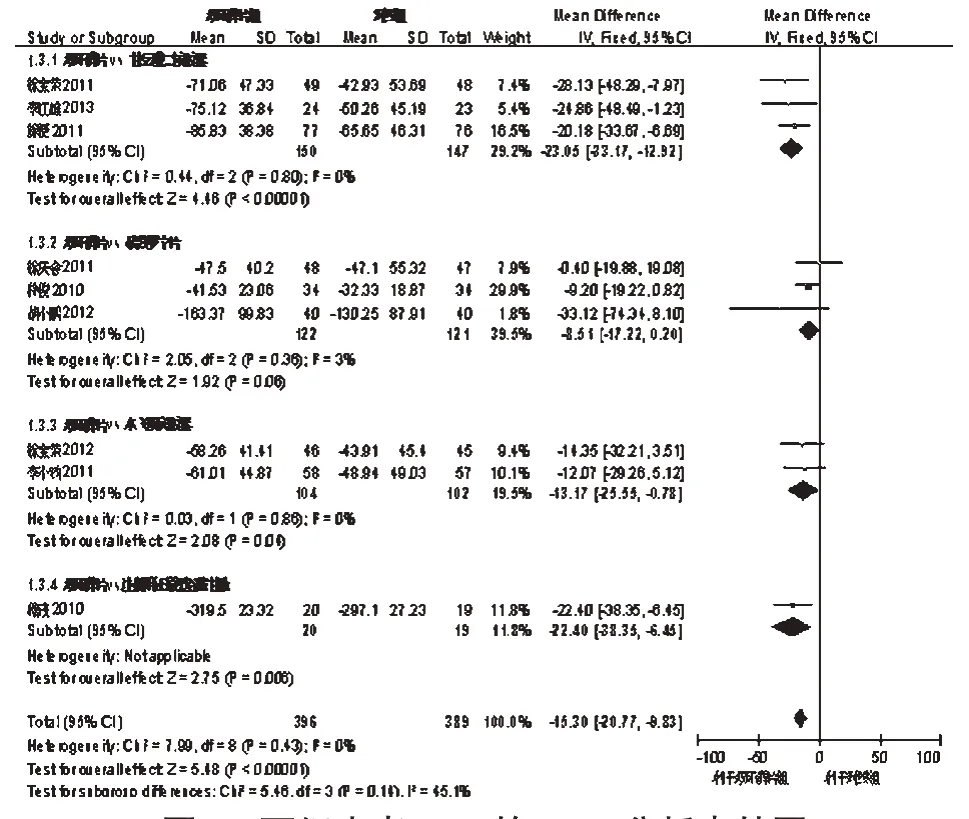
图3 两组患者AST的Meta分析森林图Fig 3 Forest plot of Meta-analysis of AST in 2 groups
2.2.4 TBIL 6项研究报道了TBIL[11,14-15,18,20-21],各研究间无统计学异质性(P=0.25,I2=24%),采用固定效应模型分析,Meta分析结果见图4。由图4可见,试验组患者TBIL水平显著高于对照组,两组比较差异有统计学意义[MD=-1.91,95%CI(-3.36,-0.46),P=0.01]。按照不同阳性对照药物进一步行亚组分析。结果发现,双环醇片在改善患者ALT方面显著优于甘草酸二铵胶囊[MD=-2.51,95%CI(-4.48,-0.53),P=0.01];但与水飞蓟宾胶囊[MD=-3.28,95%CI(-6.97,0.41),P=0.08]、硫普罗宁片[MD=0.15,95%CI(-2.52,2.83),P=0.91]和注射用还原型谷胱甘肽[MD=-7.20,95%CI(-19.51,5.11),P=0.25]比较,差异无统计学意义。
2.2.5 ADR发生率 3项研究报道了ADR发生率[13,17,19],各研究间无统计学异质性(P=0.15,I2=46%),采用固定效应模型分析,Meta分析结果见图5。由图5可见,试验组患者ADR发生率与对照组比较,差异无统计学意义[OR=0.45,95%CI(0.20,1.01),P=0.05]。按照不同阳性对照药物进一步行亚组分析。结果发现,双环醇片的ADR发生率显著低于硫普罗宁片[OR=0.05,95%CI(0.00,0.86),P=0.04],但与甘草酸二铵胶囊[OR=0.77,95%CI(0.20,3.02),P=0.71]和水飞蓟宾胶囊[OR=0.80,95%CI(0.23,2.79),P=0.73]比较,差异无统计学意义。
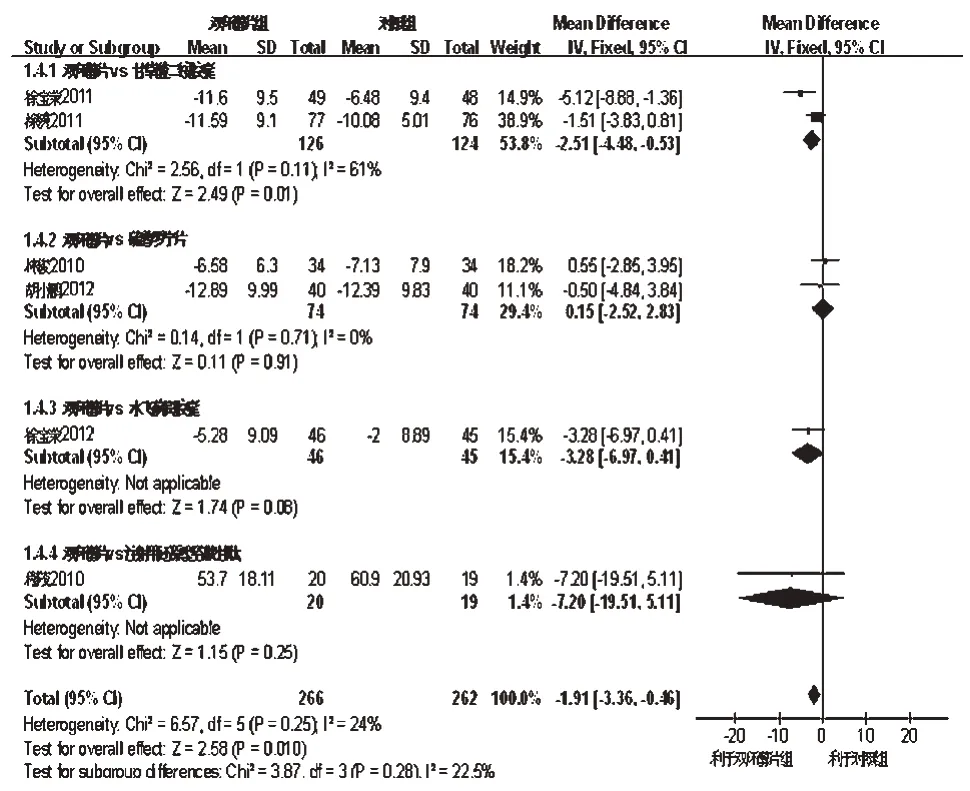
图4 两组患者TBIL的Meta分析森林图Fig 4 Forest plot of Meta-analysis of TBIL in 2 groups
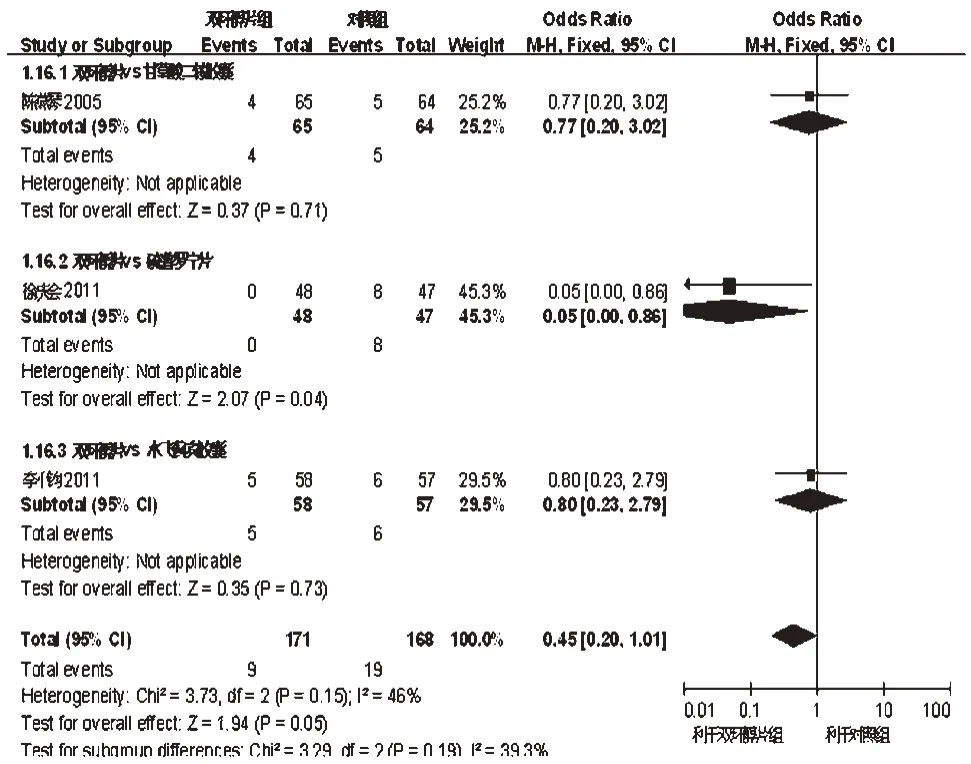
图5 两组患者ADR发生率的Meta分析森林图Fig 5 Forest plot of Meta-analysis of rate of adverse drug reaction in 2 groups
3 讨论
本研究首次对双环醇片治疗DILI的有效性和安全性进行了系统评价。结果显示,双环醇片治疗DILI的疗效显著优于对照组,可以显著改善患者的ALT、AST及TBIL水平;安全性方面,双环醇片的ADR发生率与对照组比较差异无统计学意义,表明双环醇片的安全性较好。
双环醇片是中国医学科学院药物研究所研制的具有国际自主知识产权的国家一类新药,具有保肝降酶的作用,被批准用于治疗慢性肝炎所致的氨基转移酶升高。在先前的基础研究中,双环醇片就显示出对顺铂、四环素等引起的实验性肝损伤有明显保护作用[23]。近期研究也显示,双环醇片可减轻肝脏炎症,保护肝脏细胞免受损伤而使胶原合成和分泌减少,并通过促进胶原降解和吸收来抑制肝纤维化的形成和发展。
本研究也存在一定的局限性:首先,纳入研究全为中文文献,且研究的风险偏倚较高,这些因素影响了本研究证据的强度;其次,在药物治疗的疗程和有效性的定义方面,各研究均存在差异,这些都导致本研究结论有一定的偏倚风险。
综上所述,双环醇片治疗DILI疗效优于其他阳性药物,且安全性相似。但由于纳入研究存在高偏倚风险,该结论尚需高质量的RCT进一步验证。
[1]刘思纯,马博.药物性肝损害的诊断和治疗现状[J].新医学,2007,38(9):564.
[2]肝博士杂志编辑部.药物性肝损害病死率位居全球第五[J].肝博士,2006(5):68.
[3]Andrade RJ,Lucfna MI.Drug-induced hepatotoxicity[J].N Engl J Med,2003,349(20):1 974.
[4]Li L,Wang JY.Advances in the pathogenesis of drug-induced hepatic injury[J].J Fudan Univ Med Sci,2007,34(2):313.
[5]Sierra F,Torres D.A concise and structured review of drug-induced toxic hepatic disease[J].Ann Hepatol,2004,3(1):18.
[6]王媛,刘岩,袁娟丽,等.DILI研究进展[J].中国药物经济学,2013,8(5):52.
[7]Ni H,Simile C,Hardy AM.Utilization of complementary and alternative medicine by United States adults:results from the 1999 national health interview survey[J].Med Care,2002,40(4):353.
[8]邢卉春,段英,程丹颖.药物性肝损伤[EB/OL].[2014-07-24].http://baike.baidu.com/view/566801.htm.
[9]任东东,邓存良.药物性肝损伤的研究进展[J].西南军医,2014,16(6):670.
[10]杨佼,吕文良.药物性肝损伤临床研究及治疗进展[J].现代中西医结合杂志,2012,21(12):1 359.
[11]林俊,郭洪波,解泽林,等.肾移植术后早期肝损伤的预防和治疗效果分析[J].肝脏,2010,15(5):335.
[12]Higgins JPT,Green S.Cochrane handbook for systematic reviews of interventions version5.1.0[EB/OL].[2014-07-24].htttp://www.cochrane-handbook.org.2011.
[13]陈燕琴,高同军,迟俭,等.双环醇片治疗抗结核药物性肝损害临床疗效和安全性分析[J].传染病信息,2005,18(4):188.
[14]徐宝荣.双环醇片治疗甲亢性肝损害临床疗效分析[J].中国肝脏病杂志:电子版,2011,3(3):5.
[15]涂赘,万以叶.双环醇片对肺癌患者DILI的防治研究[J].医学研究杂志,2012,41(7):156.
[16]李江雄.双环醇治疗甲亢性肝损害疗效观察[J].首都医药,2013,20(8):46.
[17]徐庆会,白玉,仲云.双环醇治疗甲亢及抗甲状腺药物治疗后致肝功能损害疗效观察[J].胃肠病学和肝病学杂志,2011,20(7):666.
[18]胡小鹏,尹航,王玮,等.双环醇片治疗肾移植术后DILI的疗效观察[J].胃肠病学和肝病学杂志,2012,21(4):342.
[19]李小钧,刘琳,王向群.双环醇片治疗氯丙嗪、氯氮平所致肝损害临床疗效和安全性分析[J].中国民康医学,2011,23(11):1 314.
[20]徐宝荣.双环醇片治疗他汀类降脂药所致肝损害的临床疗效分析[J].首都医药,2012,19(16):42.
[21]穆茂,程明亮,祝娟娟,等.双环醇治疗药物性肝病的临床研究[J].首都医药,2010,17(12):53.
[22]刘佩英.双环醇治疗抗结核药所致肝损害269例临床疗效观察[J].中国社区医师,2011,13(22):67.
[23]Yu YN,Chen H,Li Y.Effect of bicyclol on cisplatin-induced hepatotoxicity in the hepatocarcinoma 22 tumour-bearing mice[J].Basic Clin Pharmacol Toxicol,2009,104(4):300.

