阿奇霉素对比阿莫西林/克拉维酸治疗下呼吸道感染的药物经济学评价
贾立华,牛文敬,尹 月,马 吉,张婉璐,任文静(解放军307医院药学部,北京 100071)
下呼吸道感染(LRTI)是一种急性疾病,发病时间通常不超过21 d;其以咳嗽为主要症状,伴随至少1 种不能用哮喘和窦腔感染解释的诸如咳痰、喘息、呼吸困难等临床表现,包括急性支气管炎、流感、社区获得性肺炎(CAP)、慢性阻塞性肺疾病(COPD)急性加重和支气管炎急性加重[1]。在我国,社区呼吸道感染是最常见的感染性疾病,具有较高的发病率和病死率[2]。感染初始治疗通常是经验性选择抗生素,经验选择要依赖患者的病史、相关实验室检查、体格检查和当地细菌敏感性和流行病学特点,同时还应兼顾药物的安全性和经济性,才能制订出最合理的个体化治疗方案。
阿奇霉素于2002 年在我国上市,被广泛应用于成人与儿童的呼吸道感染,其对流感嗜血杆菌具有很强的抑菌活性,最小抑菌浓度为0.25~4 mg/L,比红霉素低4~8 倍。该药首选用于流感社区暴发流行期间出现持续性咳嗽、不发热的儿童和成人患者。由于细菌的外排泵机制和结合靶位的改变,近年来细菌对阿奇霉素的耐药现象日益增加[3]。因此,从疗效、安全性和药物经济性因素综合评价该药临床应用的效益和风险是正确用药的关键,经研究报道如下。
1 资料与方法
1.1 试验设计
1.1.1 研究设计 计算机检索Cochrane 图书馆、EMBase、Medline、PubMed、中国期刊全文数据库、中文科技期刊数据库和万方数据库,纳入18 项采用随机、盲法、平行对照或多中心大规模的临床试验作为评价阿奇霉素与阿莫西林/克拉维酸两种药物治疗方案的基础信息,同时检索现有药物经济学文献研究方法,确定经济学分析模型。
1.1.2 样本纳入标准 ①诊断为急性支气管炎、慢性支气管炎急性加重、CAP的门诊或住院患者;②患者年龄、性别不限,试验组患者给予阿奇霉素治疗,对照组患者给予阿莫西林/克拉维酸治疗。
1.1.3 样本排除标准 ①明确为囊性纤维化、传染性单核细胞增多症或无急性感染的COPD患者;②入组前48 h给予抗菌药物的患者;③对大环内酯类药物具有超敏性者;④药物或酒精滥用者;⑤妊娠期妇女;⑥同时使用华法林、卡马西平和/或麦角胺者,凝血或其他血液疾病者;⑦需要进行血液透析、腹膜透析、血浆置换、血液灌流者;⑧血清转氨酶、碱性磷酸酶或胆红素值大于正常值上限的2 倍者;⑨确定或怀疑中、重度肾功能不全者;⑩艾滋病或已知的艾滋病毒抗原或抗体的血清阳性者。
1.1.4 样本例数 纳入18 篇研究,共3 365 例患者,其中试验组有1 906例,对照组有1 459例。
1.1.5 给药方案和日治疗费用 试验组患者给药方案为单剂量500 mg,应用3 d,或者首剂量500 mg,维持250 mg,应用5 d;对照组患者给药方案为0.875 g/0.125 g,治疗周期为7 d。依据北京市物价局的最高限定零售价,试验组的单疗程治疗费用为57.04元,对照组的单疗程治疗费用为71.19元。
1.1.6 疗效结果评价指标 ①临床治愈或症状好转;②细菌清除率;③药品不良反应。
1.2 药物经济学分析设计
1.2.1 经济学分析类型 按照受试对象、干预措施、重要结局和设计方案(PICO原则)将问题转化为P:LRTI患者;I:阿奇霉素;C:阿莫西林/克拉维酸;O:临床疗效和不良反应的Meta分析结果。同时,通过检索Proquest、Springer Link 和Wiley Online Library数据库,参照筛选文献结果,确定效果评价指标为治疗有效率,经济学评价模型为决策树模型[4-6]。
1.2.2 治疗效果赋值 疗效指标选用治疗有效率:对治愈或好转,没有发生药品不良反应的疗效赋值为4;对治愈或好转,发生药品不良反应的疗效赋值为3.5;对治疗无效或失败,未发生药品不良反应的赋值为1;对治疗无效或失败,发生药品不良反应的赋值为0.5。
1.2.3 评价角度 卫生服务提供者。
1.2.4 数据来源 临床疗效数据和药品不良反应结果数据来源于18项RCT对于疗效与安全性评价的Meta分析,详见图1、图2。结果,两组患者治疗有效率[RR=0.93,95%CI(0.55,1.55),P=0.77]和不良反应发生率[RR=0.79,95%CI(0.62,1.0),P=0.05]比较差异无统计学意义。
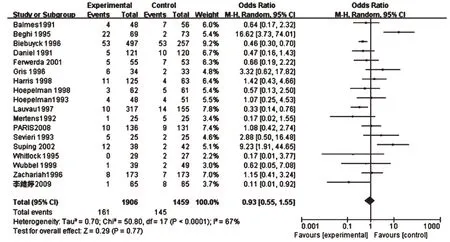
图1 两组患者治疗有效率的Meta分析森林图Fig 1 Forest plot of Meta-analysis of efficiency rate in 2 groups
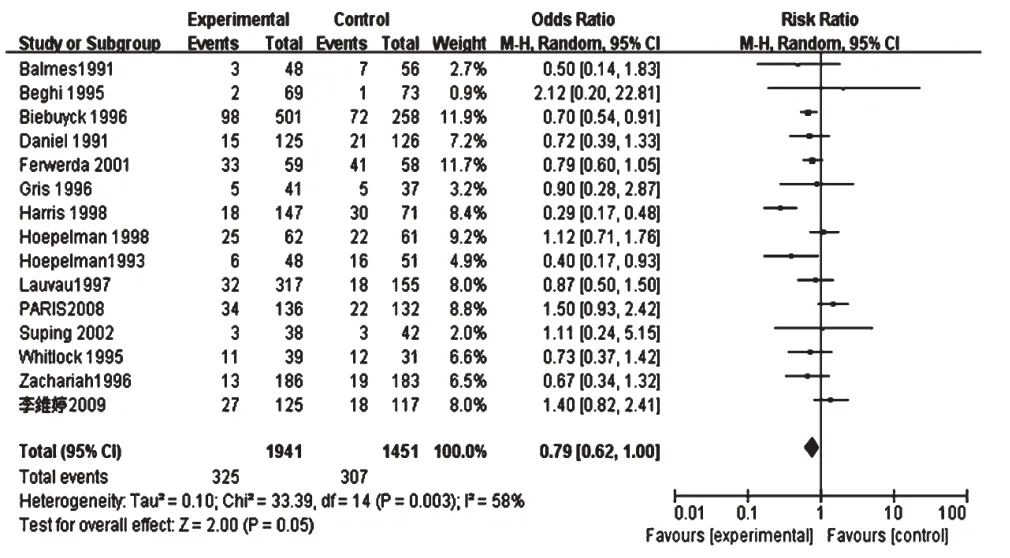
图2 两组患者不良反应发生率的Meta分析森林图Fig 2 Forest plot of Meta-analysis of adverse reaction rate in 2 groups
1.2.5 成本确定 研究中涉及的成本,在直接医疗成本方面包括用药成本和相关卫生服务成本:药品的单位成本信息以北京市物价部门定价为准,卫生服务项目单位成本以国家发改委和北京市物价局公开的定价信息进行测算。参照中国《社区获得性肺炎临床路径(2012 年版)》的要求,将治疗检查必需项目和用药费用、药品不良反应处置费用纳入卫生服务成本。
1.2.6 成本-效果分析 采用Treeage Pro 2011 版软件将结果赋值进行统计分析。
1.2.7 敏感度分析 根据成本-效果分析结果,对药品成本、检查成本及结果赋值因素分别进行单因素敏感性分析。
2 研究结果
2.1 决策树模型参数及赋值
选择决策树模型对阿奇霉素和阿莫西林/克拉维酸治疗LRTI 进行成本-效果分析,决策节点定义为药物治疗方案,决策分支定义为药物治疗结果及概率,通过图1和图2的Meta分析结果,将各参数赋值,结果详见表1。

表1 决策树模型参数及赋值Tab 1 Model parameter and valuation in decision tree model
2.2 成本-效果分析结果
采用Treeage Pro 2011 版软件将表2 参数赋值,运用软件统计分析,回推结果详见图3、表2。
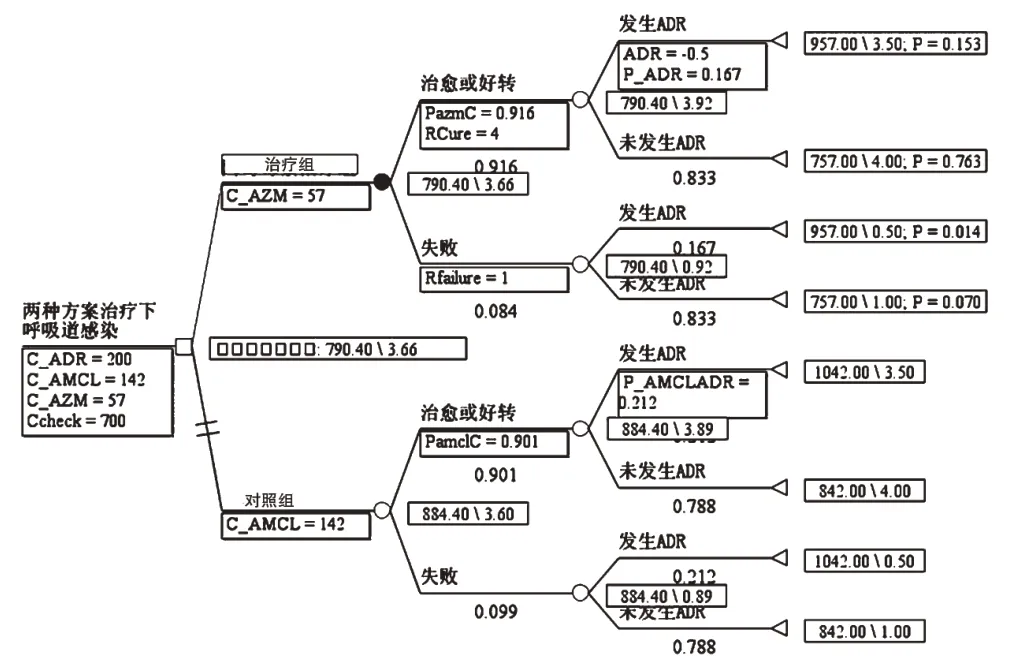
图3 Treeage软件进行成本-效果评价的决策树模型Fig 3 Decision tree model of evaluation of cost-effectiveness by Treeage software
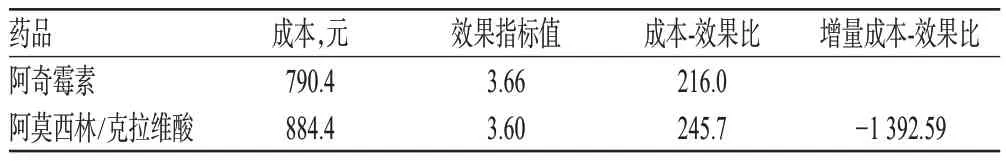
表2 决策树模型成本-效果分析结果Tab 2 Results of cost-effectiveness analysis in decision tree model
2.3 单因素敏感性分析结果
考虑到分析结果局限性,分别对价格因素、成本因素和疗效赋值进行替代假设,采用Treeage Pro 2011 版软件分别进行单因素敏感性分析,其结果均保持稳定,详见表3。
3 讨论
依据原卫生部发布的临床路径要求,阿奇霉素用于CAP和慢性支气管炎治疗的标准住院日为7~14 d,故为急性症状,研究随访时间均在1 个月内,因此选择决策树模型进行分析。模型参数可以来源于各种资料,如Meta 分析结果、RCT、观察性研究、数据库、病例资料、专家意见、医疗服务项目单价以及研究者假设或者指南中的规定等。数据应当与模型设计的特征一致,并且与干预措施作用的人群相关,模型中所有的数据应当明确报告来源和选择理由[7]。本文选择了18项RCT的系统评价结果,采用这些数据提高了经济学评价的可靠性。

表3 单因素敏感性分析结果Tab 3 Results of single factor sensitivity analysis
从卫生服务提供者角度出发,考虑患者均接受门诊治疗,治疗成本主要包括药品费用、检查费用、药品不良反应处理成本和其他费用,经过Treeage Pro 2011版软件对成本-效果赋值结果回推。结果表明,阿奇霉素的成本-效果比为216.0,阿莫西林/克拉维酸为245.7,阿奇霉素治疗成本-效果比低于阿莫西林/克拉维酸。考虑到成本和效果因素的不确定性,分别通过下调药品价格、提高检查费用或药品不良反应处置成本、改变疗效赋值等单因素变量进行单因素敏感性分析,其结果均保持稳定。
目前,大环内酯类药物包括阿奇霉素的耐药性在世界上许多国家呈现一个显著的上升趋势。但基于阿奇霉素较广的抗菌谱和独特的免疫调节机制,2007 年美国感染病学会和美国胸科学会联合委员会(IDSA/ATS)在成人CAP 治疗指南中仍然推荐,对于门诊患者中没有肺炎链球菌耐药风险的感染中,大环内酯类药物依然是治疗CAP的首选药物,文献证据等级为Ⅰ级[8]。从本次检索的18篇文献看,单药口服阿奇霉素在门诊治疗LRTI,无论疗效、安全性和药物经济性均不亚于阿莫西林/克拉维酸,特别是对急性支气管炎的儿童患者,口服阿奇霉素的疗效显著优于阿莫西林/克拉维酸。
2013年美国食品药品管理局(FDA)在药物安全公告中指出,静脉使用阿奇霉素有可能导致致命的心律失常[9]。这再次提醒临床,在能够选择口服制剂的情况下,其药物成本和安全性均远远高于静脉给药。
由于本文纳入研究的文献分别来源于荷兰、比利时、意大利、中国、美国、法国、爱尔兰及其他欧洲国家,各地阿奇霉素耐药性各异,资源利用情况各异,势必带来较大偏倚。因此,为使患者获得最佳的治疗效果,还应综合患者实际和经济状况,修正和调整治疗方案。
[1]Woodhead M,Blasi F,Ewig S,et al.Guidelines for the management of adult lower respiratory tract infections:full version[J].Clin Microbiol Infect,2011,17(Suppl 6):1.
[2]胡成平,林江涛.呼吸系统疾病专辑[M].北京:人民卫生出版社,2013:34-35.
[3]Syrogiannopoulos GA,Grivea IN,Tait-Kamradt A,et al.Identification of an erm(A)erythromycin resistance methylase gene in Streptococcus pneumoniae isolated in Greece[J].Antimicrob Agents Chemother,2001,45(1):342.
[4]De Cock E,Krueger WA,Sorensen S,et al.Cost-effectiveness of linezolid vs vancomycin in suspected methicillin-resistant staphylococcus aureus nosocomial pneumonia in Germany[J].Infection,2009,37(2):123.
[5]Paladino JA,Gudgel LD,Forrest A.Azithromycin vs cefuroxime with or without erythromycin for the treatment of community-acquired pneumonia[J].Chest,2002,122(4):1 272.
[6]van Valkengoed IG,Postma MJ,Morré SA,et al.Costeffective anlalysis of a population based screening programme for asymptomatic chlamydia trachomatis infections in women by means of home obtained urine specimens[J].Sex Transm Infect,2001,77(4):276.
[7]Dresser LD,Niederman MS,Paladino JA.Cost-effectiveness of gatifloxacin vs ceftriaxone with a macrolide for the treatment of community-acquired pneumonia[J].Chest,2001,119(5):1 439.
[8]Mandell LA,Wunderink RG,Anzueto A,et al.Infectious diseases society of America/American thoracic society consensus guidelines on the management of community-acquired pneumonia in adults[J].Clin Infect Dis,2007,44(Suppl 2):27.
[9]Ray WA,Murray KT,Hall K,et al.Azithromycin and the risk of cardiovascular death [J].N Engl J Med,2012,366(20):1 881.

