HPLC法测定人血浆中克林霉素含量及其药动学研究
作者单位:650032 昆明,成都军区昆明总医院药剂科(唐 冰,周娅琳),肾病内科(韩 敬)
唐 冰,周娅琳,韩 敬
HPLC法测定人血浆中克林霉素含量及其药动学研究
作者单位:650032 昆明,成都军区昆明总医院药剂科(唐冰,周娅琳),肾病内科(韩敬)
唐冰,周娅琳,韩敬
[摘要]目的建立人血浆中克林霉素的HPLC检测方法。方法采用HPLC法检测人血浆中克林霉素含量,检测条件为:色谱柱:Inertsil® DOS-3 C185 μm硅胶柱(250 mm×4.6 mm);流动相:乙腈/0.05 M KH2PO4=30/70(v/v),流速:1 ml/min;柱温:35 ℃,检测波长:204 nm,进样量为100 μl。结果血浆中克林霉素浓度在0.20~16.0 μg/ml范围内线性关系良好(r=0.9992~0.9998),最低检测浓度为0.20 μg/ml,方法学回收率为82.42%~89.37%,日内及日间精密度RSD<15%。结论此方法专属、准确、灵敏度高,样品处理过程简便,适合克林霉素临床药代动力学研究。
[关键词]克林霉素;检测;HPLC;血浆;药代动力学
目前检测人血浆中克林霉素含量的常用方法有HPLCS法和LC/MS/M法。所报道的HPLC法,需要经过固相萃取这一步骤[1-3],检测操作较为繁琐,保留时间较长;而LC/MS/MS法检测结果准确[4-5]、重现性好、精密度高,但其由于检测仪器的价格较高,难以推广应用。本研究探讨了直接采用HPLC-UV法检测人血浆中的克林霉素,以适合克林霉素临床样本检测的需求。
1仪器与材料
1.1仪器Waters 2690型高效液相色谱仪:包括2695溶剂输送系统、在线脱气机、自动进样器、2487双通道紫外检测器、柱温箱、Empower数据系统(Waters公司);BP121S电子天平(德国赛多利斯);LDZ-5-2型自动平衡离心机(北京离心机厂);AS2060B型超声波清洗仪(美国AUTOSCIENCE);XW-80A型漩涡混合器Vortex(上海精科);Texas 75062高速离心机(美国雅培)。
1.2试剂盐酸克林霉素胶囊(上海新亚药业);盐酸克林霉素对照品(含量>99.5%,上海新亚药业);奈韦拉平对照品(内标,纯度99.5%,苏州百拓);空白血浆(本院输血科提供);乙腈(色谱纯,美国默克);二氯甲烷(色谱纯,美国TEDIA,批号:504071);甲醇(色谱纯,美国默克);超纯水(Milli-Q)。
2方法和结果
2.1色谱条件色谱柱:Inertsil DOS-3 C185 μm柱(250 mm×4.6 mm);流动相:乙腈/0.05 M KH2PO4,流速:1 ml/min;柱温:35 ℃,检测波长:204 nm,进样量为100 μl。
2.2贮备液及工作液配制
2.2.1盐酸克林霉素储备液精密称取盐酸克林霉素对照品10.0 mg于10 ml量瓶中,用水溶解并定容配成浓度为1.0 mg/ml的储备液,置4 ℃冰箱贮存备用。
2.2.2内标奈韦拉平储备液精密称取奈韦拉平对照品10 mg于10 ml量瓶中,用水溶解并定容配成浓度为1.0 mg/ml的储备液,置4 ℃冰箱贮存备用。
2.3血浆样本的处理于0.5 ml血浆中分别加入50 μl内标溶液(10 μg/ml奈韦拉平储备液),100 μl氢氧化钠溶液(0.4 mol/L),涡流混合0.5 min,定量加入二氯甲烷3.5 ml,涡流混合1 min,离心(5000 r/min)5 min后,弃上层,留下层40 ℃水浴氮气吹干;用流动相200 μl溶解残渣,涡流混合1 min离心(10 000 r/min)5 min,取上清液150 μl置于进样小瓶内,进样50 μl进行分析,记录色谱图。
2.4特异性采用2.3处理步骤分别处理空白血浆、空白血浆+克林霉素对照品、给药后1 h的受试者的血浆样品、以及配制的最低检测浓度血浆样品,以2.1色谱条件分别进样检测,其色谱图见图1。盐酸克林霉素和内标的保留时间分别约为6.1 min和8.5 min。结果表明,空白血浆中的内源性物质不干扰盐酸克林霉素和内标奈韦拉平的测定。


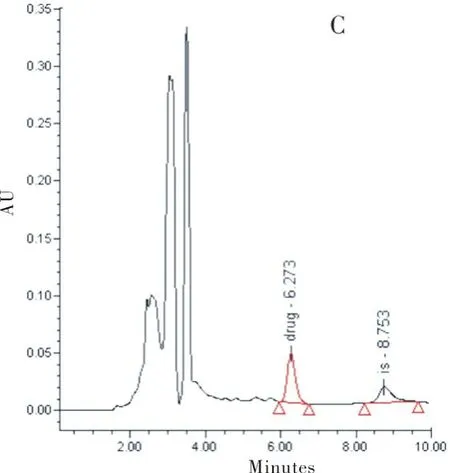


图1 测定血浆中盐酸克林霉素及内标奈韦拉平色谱图
A:空白血清色谱图;B:空白血清加10 μg/ml标准品色谱图;C:空白血清加40 μg/ml标准品和内标色谱图;D:最低检测限0.25 μg/ml色谱图(drug:克林霉素;is:内标);E:给药血浆样品色谱图(受试者用药后1 h血样,左边峰为克林霉素,右边为内标)
2.5标准曲线在健康人空白血清中精密加入不同量的盐酸克林霉素标准溶液,使其浓度分别为0.2、0.5、1、2、4、8、16 μg/ml。按样品处理与测定方法进行测定,以样品浓度(X)与盐酸克林霉素峰面积和内标峰面积的比值(Y)进行回归,得回归方程:Y=0.5980X+0.0140,R=0.9992,表明盐酸克林霉素在0.2~16 μg/ml范围内呈良好线性关系(图2)。

图2 HPLC法测定人血浆中克林霉素含量标准曲线
2.6最低定量限检测限按基线噪音3倍计算,并符合精密度和准确度的要求,本方法的最低检测浓度为0.20 μg/ml,RSD<10%。
2.7精密度在空白人血清中加入不同量的盐酸克林霉素配制成低、中、高(0.5、2、16 μg/ml)不同浓度的质控血样,每个浓度各6个样品,按上述条件分别测定日内、日间变异,结果见表1。其RSD<15%,符合检测要求。
2.8方法学回收率在空白血浆中加入克林霉素储备液,配制成高、中、低3个浓度点(0.5、2.0、16.0 g/ml)的质控样品,按2.3“血浆样品处理”项下的方法处理,每个浓度平行分析6个样本。以实际测得的峰面积与储备液配制的相同浓度测得的峰面积的比计算回收率,结果见表1。
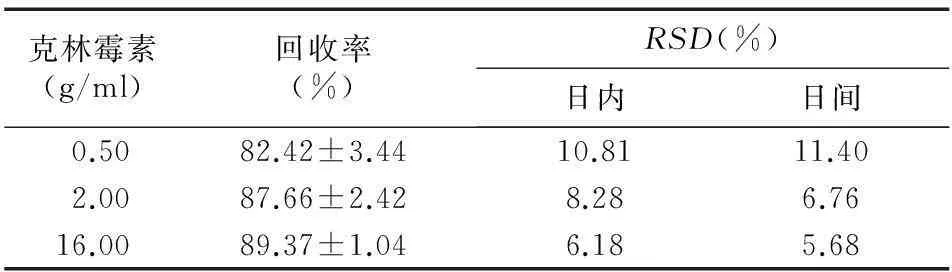
表1 血浆中盐酸克林霉素HPLC测定方法的精密度与
2.9样品稳定性考察
2.9.1血样保存稳定性配制成高、中、低3个浓度点(0.5、2.0、16.0 g/ml)的血浆质控样品,在-80 ℃冰箱贮存,分别于0、30、60及90 d检测血药浓度,结果表明,血样中克林霉素含量变化RSD<15%。
2.9.2血样放置稳定性配制成高、中、低3个浓度点(0.5、2.0、16.0 g/ml)的血浆质控样品,分别存放于-4 ℃和室温条件,分别于0、2、4、6和8 h检测血药浓度,结果表明,血样中克林霉素含量变化RSD<15%。
2.9.3血样冻融稳定性将高、中、低3个浓度点(0.5、2.0、16.0 g/ml)的血浆质控样品分别冻融6次(-80 ℃冷冻,室温下融化)后检测其浓度,含量变化RSD<15%,结果表明反复冻融对检测结果无显著影响。
2.10药动学研究经医院伦理委员会批准,筛选20名健康志愿受试者口服盐酸克林霉素胶囊300 mg,测定其主要药动学参数为:平均t1/2为(2.26±0.55)h,平均Cmax为(3.24±1.26)μg/ml,平均达峰时间Tmax为(1.09±0.42)h,平均AUC(0-t)和AUC(0-∞)分别为(11.86±5.56)和(12.18±5.64)μg/(ml·h),平均血药浓度-时间曲线见图3。
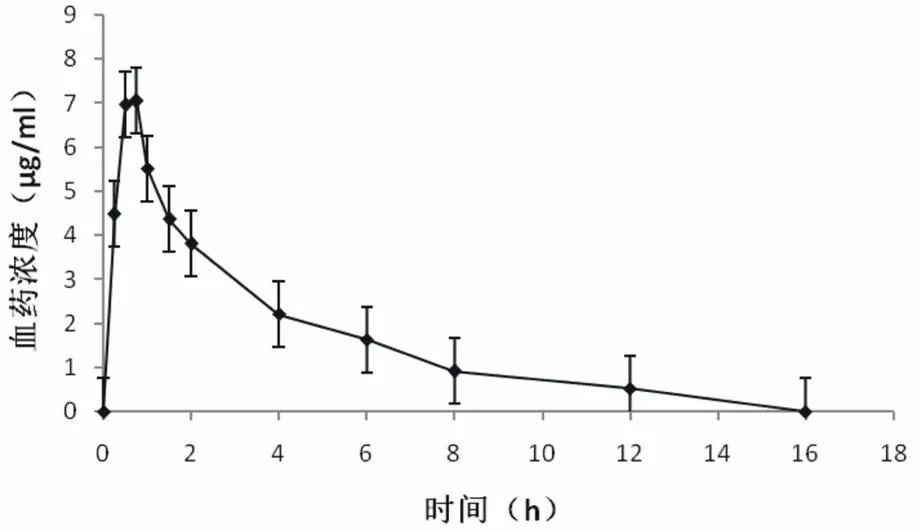
图320名受试者单次口服克林霉素300 mg后平均血药浓度-时间曲线
3讨论
本研究从特异性、精密度、准确度、稳定性及方法学回收率等方面进行了较为全面的方法学确证,所有检测RSD均低于15%,符合人体血浆检测方法学的要求[6]。将其用于人体药代动力学研究,取得了较为理想的结果,所得到的药代动力学参数与国内外报道一致。研究中发现,如果当流动相pH值在6.5~6.8范围内,克林霉素的出峰时间比较稳定。
研究结果证实,本研究所建立的HPLC-UV法检测人血浆中的克林霉素含量方法,专属性、准确性、灵敏度高,重现性好,样品处理过程简便,适合克林霉素临床检测需求。
【参考文献】
[1]Hiltrud Fieger-Büschges,Gabriele Schüβler,Véronique Larsimont,et al.Determination of clindamycin in human plasma by high-performance liquid chromatography using coupled columns[J].Journal of Chromatography B,1999,724:281-286.
[2]Chu-Min Llu,Yi-Kai Chen,Tsung-Hsien Yang,et al.High-perfor-mance liquid chromatographic determination of clindamycin in human plasma or serum:application to the bioequivalency study of clindamycin phosphate injections[J].Journal of Chromatography B,1997,696:298-302.
[3]龚海明,秦群,闵慧,等.反相高效液相法测定人血浆中克林霉素浓度[J].中南药学,2008,6:536-538.
[4]张丹,韩静,王涛,等.液相色谱-串联质谱法测定人血浆中克林霉素[J].质谱学报,2009,30:346-351.
[5]王英峰,董颖,申严,等.HPLC-MS测定人血浆中的盐酸克林霉素[J].药物分析杂志,2006,26:749-751.
[6]《化学药物临床药代动力学研究技术指导原则》课题研究组.《化学药物临床药代动力学研究技术指导原则》[M/OL].2005,国家食品药品监督管理总局药品审评中心网站颁布,http://www.cde.org.cn/zdyz.do?method=largePage&id=2070
(收稿日期:2014-11-03)
文章编号1004-0188(2015)03-0299-03
doi:10.3969/j.issn.1004-0188.2015.03.026
中图分类号R 927.11
文献标识码A

