盐酸埃克替尼治疗晚期非小细胞肺癌的临床疗效观察
梁绍平,王华庆
(天津医科大学肿瘤医院淋巴瘤科,国家肿瘤临床医学研究中心,天津市肿瘤防治重点实验室,天津300060)
论著
盐酸埃克替尼治疗晚期非小细胞肺癌的临床疗效观察
梁绍平,王华庆
(天津医科大学肿瘤医院淋巴瘤科,国家肿瘤临床医学研究中心,天津市肿瘤防治重点实验室,天津300060)
目的:观察盐酸埃克替尼治疗晚期非小细胞肺癌的临床疗效及安全性。方法:回顾分析埃克替尼治疗30例晚期非小细胞肺癌的临床效果,采用口服治疗,125mg/次,3次/d,评价其近期疗效、无病进展生存期及不良反应。结果:30例患者在接受埃克替尼1个月治疗后,完全缓解(CR)0例,部分缓解(PR)10例,疾病稳定(SD)14例,疾病进展(PD)6例,客观有效率(ORR)为33.3%,疾病控制率(DCR)为80%。在各临床因素中,ECOG评分及是否伴有脑转移与近期疗效具有相关性(P<0.05)。截至随访结束,24例(80%)出现无进展生存期(PFS)终点事件,全组中位PFS为8.0个月。患者的PFS主要与患者年龄、吸烟与否、ECOG评分以及是否伴有其他部位的转移有关(P<0.05)。全组不良反应发生率为43.3%,主要为皮疹5例(16.7%),皮肤瘙痒2例(6.7%),腹泻1例(3.3%),胃部不适1例(3.3%),肝功能轻度损害6例(20.0%)。结论:盐酸埃克替尼治疗晚期非小细胞肺癌疗效肯定,耐受性好。
盐酸埃克替尼;非小细胞肺癌;表皮生长因子受体;分子靶向治疗
肺癌作为全球发病率及死亡率位居前列的肿瘤,严重威胁到人类的健康及生活。由于肺癌发病的隐匿性,70%的患者在发现时已丧失手术机会,而传统以铂类为主的两药联合化疗虽然一定程度上降低了死亡率,但毒副反应较大,晚期患者因体质较差不能耐受化疗。近年来,靶向作用的表皮生长因子酪氨酸激酶抑制剂通过选择性抑制表皮生长因子受体(EGFR)酪氨酸激酶的活性,阻断EGFR的信号传导而起到抗肿瘤的疗效,尤其对于EGFR突变型的肺癌患者疗效更好,成为晚期非小细胞肺癌(NSCLC)患者的一线治疗方案。其代表药物吉非替尼及厄洛替尼以其优越的Ⅲ期临床试验结果广泛应用于临床治疗,而基于同样原理由我国自主研发的EGFR-TKI小分子抑制剂埃克替尼在ICOGENⅢ期临床试验中,显示出与吉非替尼疗效相当但安全性更高的治疗价值。本研究通过入组30例采用埃克替尼治疗的晚期NSCLC患者,分析其临床疗效及不良反应。
1 资料和方法
1.1 临床资料 2011年9月-2013年6月天津医科大学肿瘤医院收治的经组织学或细胞学证实并服用埃克替尼治疗的晚期非小细胞肺癌患者30例。男性9例,女性21例;中位年龄55岁(41~72岁);26例为腺癌患者,4例为非腺癌的非小细胞肺癌患者。7例有长期吸烟史。ECOG评分0~1分者20例,≥2分者10例。共有12例进行了EGFR检测,10例出现19或21外显子的突变,其余2例为野生型。5例患者接受过手术治疗。埃克替尼一线治疗3例;二线治疗21例,其中19例只进行单独靶向治疗,2例联合化疗;三线治疗6例,4例为单独靶向治疗,2例联合化疗。12例患者出现脑转移,其中10例接受过全脑的放疗或γ刀治疗,1例接受过颅内转移瘤的切除手术。20例患者出现脑转移之外的其他部位的转移,主要包括纵隔、骨、肾上腺、肝脏等。每例患者临床资料完整,并至少具有一个可评价病灶。所有患者在治疗前血常规及肝肾功能正常。
1.2 治疗方法 所有患者均接受盐酸埃克替尼口服治疗,125mg/次,3次/d,持续用药直至出现肿瘤进展或不可耐受的不良反应。治疗2个月后进行近期疗效及不良反应评价。所有患者在接受埃克替尼治疗前进行血常规、肝肾功能,肺部肿瘤标志物、胸部CT、腹部彩超、头部CT或MRI及骨扫描检查,全面评估病情及ECOG评分。用药期间定期复查上述指标,服药后每2个月进行影像学检查,评价疗效,直至出现疾病进展或不可耐受的毒副反应。
1.3 评价标准 根据RECIST实体肿瘤标准评价近期疗效,分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD)。以CR和PR计算客观缓解率(ORR),以CR、PR和SD计算疾病控制率(DCR)。无进展生存期(PFS)是指患者接受该方案治疗时至疾病进展、任何原因导致死亡或随访终点的间隔时间。毒性反应根据常见的不良反应事件评价(CTC)进行分级。
1.4 统计学方法 采用SPSS 15.0统计软件进行统计分析,采用Fishers精确法检验进行亚组变量分析比较,定义P<0.05为差异有统计学意义。生存情况分析采用Kaplan-Meier法进行描述,差异性检验采用Log-Rank法,检验水准α=0.05。
2 结果
2.1 近期疗效 所有患者服用埃克替尼1个月后进行首次疗效评价,CR 0例,PR 10例(33.3%),SD14例(46.7%),PD6例(20%)。ORR(CR+PR)10例(33.3%),DCR(CR+PR+SD)24例(80%)。对各基本变量的近期疗效进行统计学分析,其中ECOG评分、是否伴有脑转移与近期疗效具有相关性(P<0.05)(表1)。
2.2 无进展生存期(PFS) 截至2014年2月随访结束,24例患者出现PFS终点事件,其中4例患者在使用埃克替尼1~2个月后发生进展,全组中位PFS为8.0(1~22)个月(图1)。由于随访时间较短,仅有3例患者发生死亡,无法评价总生存情况OS。
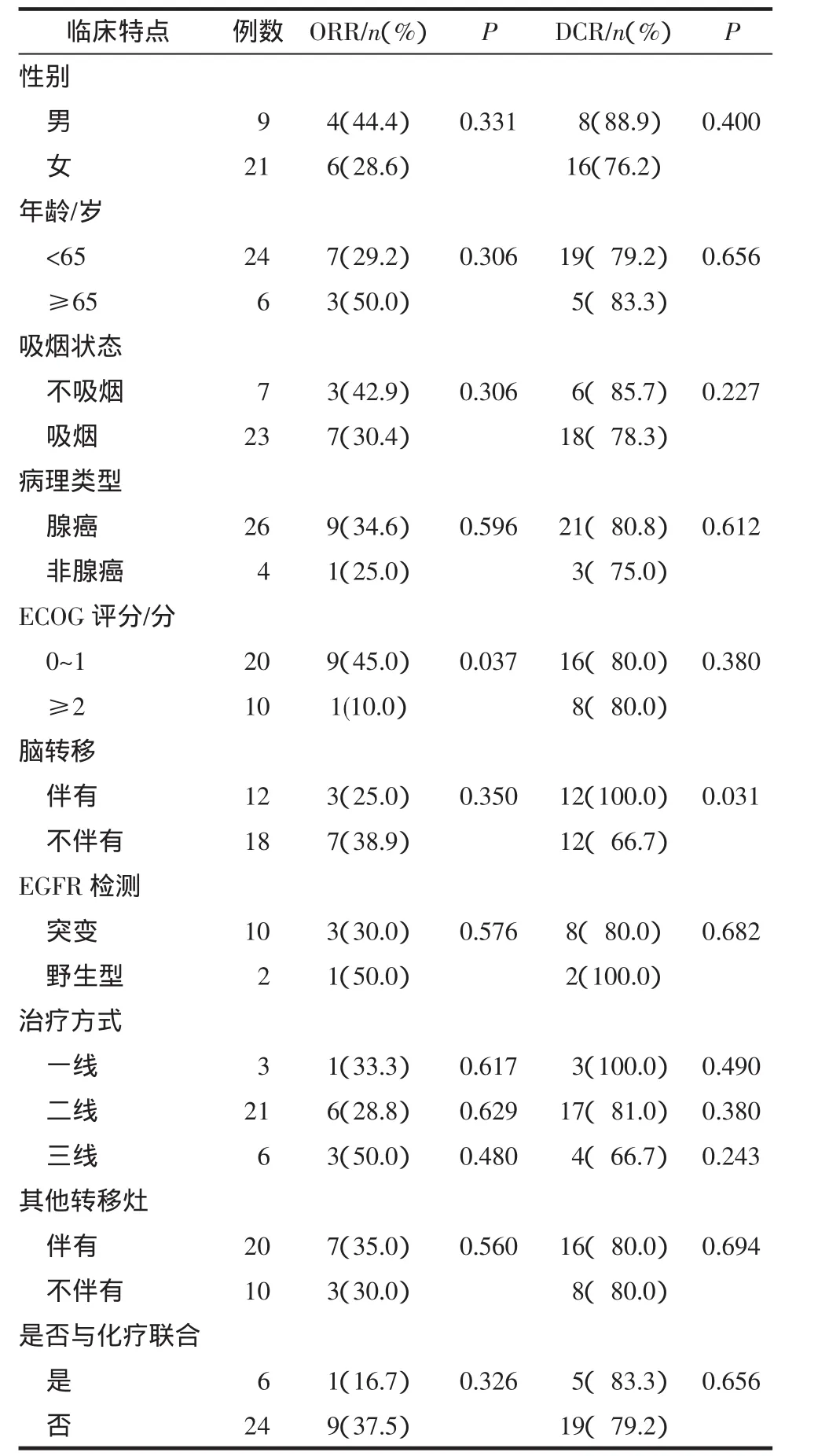
表1 30例晚期NSCLC患者临床特征与近期疗效相关性分析Tab 1 Analysisof the relationship between clinical characteristics and short-term response in 30 patients w ith advanced NSCLC

图1 30例晚期NSCLC患者无病进展生存期情况Fig 1 Analysisof progression free survival in 30 patientsw ith advanced NSCLC
进行亚组间变量分析发现,患者的PFS主要与患者年龄、吸烟与否、ECOG评分以及是否伴有其他部位的转移有关(P<0.05)。年龄小于65岁,无吸烟史及ECOG评分较低的患者具有较长的疾病无进展生存期。
2.3 症状缓解情况 全组30例患者中有16例出现肿瘤相关症状的缓解(53.3%),一般在治疗后1~12 d内出现。主要包括咳嗽憋气、咳痰带血及骨痛等症状,2例患者饮食睡眠情况好转。
2.4 不良反应 全组30例患者中共有13例(43.3%)出现药物相关不良反应,主要不良反应包括皮疹5例(16.7%),皮肤瘙痒2例(6.7%),腹泻1例(3.3%),胃部不适1例(3.3%),肝功能轻度损害6例(20.0%),主要为Ⅰ~Ⅱ度反应,给予对症处理后好转。其中1例患者出现Ⅲ度的皮疹反应,无一例患者因不良反应无法耐受而退出治疗。
3 讨论
EGFR是一类与细胞增殖、分化、黏附、迁移、侵袭等生命过程相关的多功能跨膜糖蛋白,其异常激活与肿瘤的发生发展密切相关。EGFR-TKI通过选择性抑制ATP与EGFR酪氨酸激酶结合,从而抑制EGFR-TKI的活性,阻止肿瘤细胞的增殖、侵袭转移,促进肿瘤细胞凋亡[1]。基于这一理论基础的EGFR-TKI在大量Ⅲ期临床试验中表现出良好的临床疗效及安全性。
2009年开展的IPASSⅢ期临床试验,进行了吉非替尼与TP(紫杉醇联合卡铂)化疗方案一线治疗晚期NSCLC的疗效比较。吉非替尼的ORR达到43%,明显高于同期化疗组(32.2%),中位PFS为5.7个月,中位生存期达到18.6个月[2]。一项厄洛替尼治疗复发患者的Ⅱ期临床试验,客观缓解率达到12.3%,中位OS 8.4个月,中位PFS 2.2个月,1年生存率为40%,有效延长了晚期NSCLC患者的生存时间[3]。吉非替尼与厄洛替尼也分别于2003、2004年被美国FDA批准用于晚期NSCLC的治疗。临床研究还发现,在NSCLC患者中,女性、腺癌、不吸烟、亚洲人及EGFR激酶结构域外显子18-21突变的患者对EGFR-TKI的治疗反应较好。
盐酸埃克替尼是在化学结构、分子作用机制、疗效方面与吉非替尼相似的一类EGFR-TKI。药代动力学分析发现,盐酸埃克替尼在体内达到峰值的时间最短,消除半衰期为2.1~5.6 h[4]。在ICOGEN的Ⅲ期临床试验中,埃克替尼组获得27.6%的ORR及75.4%的DCR,与吉非替尼组的OR R(27.2%)及DC R(74.9%)相当,但其临床安全性优于吉非替尼[5]。本研究30例患者客观有效率为33.3%,疾病控制率为80%,比ICOGEN中的结果稍高,可能与样本量较小有关。在对ICOGEN的亚组变量分析中,盐酸埃克替尼治疗晚期NSCLC的疗效与临床分期、性别、病理类型、ECOG评分及吸烟史有关。在本研究中,只有ECOG评分、是否伴有脑转移对近期疗效有明显影响(P<0.05)。本研究的PFS明显优于ICOGEN试验的PFS(137 d),分析原因主要是因为本组以腺癌患者为主、且部分患者同时接受放疗、化疗等其他方面的治疗,病例数较少,存在主观选择偏倚。年龄小于65岁,长期吸烟史及ECOG评分较低的患者具有较长的PFS。在不良反应方面,本组患者发生率为13/30(43.3%),主要为Ⅰ~Ⅱ级皮疹、腹泻及肝功能检查异常等,耐受性良好。
对于EGFR突变的患者,EGFR-TKI表现出绝对的治疗优势。在IPASS研究中,261例EGFR突变患者中,吉非替尼组的缓解率达到71.2%,明显高于化疗组47.3%(P<0.001),PFS也较化疗组的6.3个月增长到9.5个月[2]。之后相关研究如WJTOG3405、OPTIMAL、EURTAC等临床试验均证实了这一治疗优势,也奠定了对于EGFR突变的NSCLC患者临床治疗采用一线TKI治疗的地位[6-8]。本研究中EGFR突变的患者中位PFS为11.0个月,明显高于全组中位PFS,再次验证了EGFR-TKI对突变型EGFR患者的治疗优势。但目前TKI一线治疗的研究多集中于吉非替尼及厄洛替尼,缺乏系统多中心的埃克替尼的临床试验,在王雷等[9]进行的66例晚期NSCLC研究中,盐酸埃克替尼一线、二线、三线及以上治疗的患者中位PFS分别为11(1~16.3)、6(0.3~11.5)、5(1~14.7)个月,具有统计学差异。初步证实了盐酸埃克替尼也可以作为晚期NSCLC患者的一线治疗。
随着EGFR-TKI对晚期NSCLC尤其是突变型NSCLC临床价值的肯定,除了一线用于EGFR突变的NSCLC治疗外,TKI与化疗的各种联合模式也得到了尝试。(1)EGFR-TKI与化疗同步联合。一项II期的随机对照研究比较厄洛替尼单药及与化疗联合治疗182例晚期腺癌患者,两种治疗方案在近期疗效及生存上均未表现出统计学差异[10]。多项研究结果也均未显示出联合化疗的疗效更优,因而范云等人提出对于非选择人群的NSCLC患者,不推荐化疗与EGFR-TKI的同步联合模式。但对于EGFR突变的患者尚缺乏试验分析比较,且在对于TKI耐药的患者,采用同步联合模式ORR更高,但PFS及OS无差异[11]。所以针对同步联合模式的研究仍需深入。(2)EGFR-TKI与化疗序贯治疗。这一治疗模式得到了FAST-ACT研究组验证,II期以及Ⅲ期临床试验证明化疗序贯厄洛替尼较化疗序贯安慰剂PFS、OS明显延长。但对于EGFR野生型患者两组未表现出统计学差异[12]。在IPASS的野生型亚组分析中,TP方案作为一线治疗比吉非替尼治疗更能提高PFS。FASTACT-II研究对于突变状态未知的亚组分析显示,TKI联合化疗的PFS为7.1个月,优于对照组的6.1个月,且OS也得到延长(18.1个月:16.2个月)。同时患者的生活质量也更高。因此,2013年的CSCO大会上,张力等提出对于EGFR野生型患者,建议仍然首选化疗。对于未进行检测的NSCLC患者,序贯治疗的模式仍然推荐[2,12]。在本研究中,大部分患者采取数周期化疗,待病情有所好转或稳定后,序贯EGFR-TKI治疗模式。
EGFR-TKI对于NSCLC脑转移的患者治疗价值也得到了大量研究。EGFR-TKI作为小分子抑制剂,能一定比例透过血脑屏障,增加中枢神经的血药浓度。丹麦学者Weber等[13]采用核素C11标记厄洛替尼,PET-CT显像表明厄洛替尼能在NSCLC颅内转移灶中聚集。在采用TKI治疗后,脑转移病灶也出现明显的缩小。多项临床研究显示,TKI联合放疗是伴有脑转移的NSCLC患者的有效治疗手段。在一项II期临床试验中,采用全脑放疗(40Gy/20 f)联合吉非替尼治疗,PFS为10.0个月,OS为13.0个月,表现出了较好的初步疗效[14]。而这一联合治疗对于EGFR突变的患者更有治疗价值。同时一项纳入155例EGFR敏感突变的晚期NSCLC患者的回顾性研究显示,具有相似比例脑转移的两组患者,分别接受TKI及化疗,中位随访25个月后,分别有33%和48%出现颅内病灶进展,显示了TKI对于预防脑转移发生的潜在价值[15]。本组研究中共有12例脑转移患者,其中10例接受放疗或γ刀治疗联合靶向治疗,仅有3例出现颅内病灶的进展,12例中位无进展生存期为6.5(4~12)个月。
综上,埃克替尼是治疗晚期非小细胞肺癌尤其是肺腺癌的有效靶向药物,安全性可靠。随着EGFR突变检测的普及,EGFR-TKI一线治疗及与化疗放疗联合治疗模式不断成熟,可为晚肺癌患者提供更加具体有效的治疗模式。
[1] Kumar A,Petri E T,Halmos B,et al.Structure and clinical relevance of the epidermal growth factor receptor in human Cancer[J].J Clin Oncol,2008,26(10):1742
[2] Mok TS,Wu Y L,ThongprasertS,etal.Gefitinib or carboplatin-paclitaxel in pulmonary adenocarcinoma[J].N Engl JMed,2009,361 (10):947
[3] Pérez-Soler R,Chachoua A,Hammond L A,et al.Determinants of tumor response and survival with erlotinib in patients with nonsmall-cell lungCancer[J].JClin Oncol,2004,22(16):3238
[4]谭芬来,张力,赵琼,等.国家一类新药盐酸埃克替尼的药理与临床评价[J].中国新药杂志,2009,18(18):1691
[5] Shi Y,Zhang L,Liu X,et al.Icotinib versus gefitinib in previously treated advanced non-small-cell lung cancer(ICOGEN):a randomised,double-blind phase 3 non-inferiority trial[J].Lancet Oncol,2013,14(10):953
[6] Mitsudomi T,Morita S,Yatabe Y,et al.Gefitinib versus cisplatin plus docetaxel in patients with non-small-cell lung cancer harbouring mutations of the epidermal growth factor receptor (WJTOG3405):an open label,randomised phase 3 trial[J].Lancet Oncol,2010,11(2):121
[7] Rosell R,Carcereny E,Gervais R,et al.Erlotinib versus standard chemotherapy as first-line treatment for European patientswith advanced EGFRmutation-positivenon-small-cell lung cancer(EURTAC):a multicentre,open-label,randomised phase 3 trial[J]. LancetOncol,2012,13(3):239
[8] Zhou C,Wu Y L,Chen G,et al.Erlotinib versus chemotherapy as first-line treatment for patients with advanced EGFR mutationpositivenon-small-cell lung cancer(OPTIMAL,CTONG-0802):a multicentre,open-label,randomised,phase 3 study[J].Lancet Oncol,2011,12(8):735
[9]王雷,刘基巍,于佩瑶.盐酸埃克替尼治疗66例晚期非小细胞肺癌的临床研究[J].中国新药杂志,2013,(16):1930
[10]Jänne PA,Wang X,SocinskiM A,etal.Randomized phase II trial of erlotinib alone orwith carboplatin and paclitaxel in patientswho were never or light former smokerswith advanced lung adenocarcinoma:CALGB 30406 trial[J].JClin Oncol,2012,30(17):2063
[11]Wu Y L,Lee JS,Thongprasert S,et al.Intercalated combination of chemotherapy and erlotinib for patients with advanced stage nonsmall-cell lung cancer(FASTACT-2):a randomised,double-blind trial[J].LancetOncol,2013,14(8):777
[12]Goldberg SB,Oxnard GR,Digumarthy S,etal.Chemotherapywith Erlotinib or chemotherapy alone in advanced non-small cell lung Cancerwith acquired resistance to EGFR tyrosine kinase inhibitors [J].Oncologist,2013,18(11):1214
[13]Weber B,WinterdahlM,Memon A,etal.Erlotinib accumulation in brain metastases from non-small cell lung cancer:visualization by positron emission tomography in a patient harboring amutation in theepidermalgrowth factor receptor[J].JThorac Oncol,2011,6(7):1287
[14]Ma S,Xu Y,Deng Q,etal.Treatmentof brainmetastasis from nonsmall cell lung cancerwith whole brain radiotherapy and Gefitinib in aChinesepopulation[J].Lung Cancer,2009,65(2):198
[15]Heon S,Yeap B Y,Lindeman N I,et al.The impact of initial gefitinib or erlotinib versus chemotherapy on central nervous system progression in advanced non-smallcell lung cancerwith EGFRmutations[J].Clin Cancer Res,2012,18(16):4406
(2014-06-27收稿)
Clinicalobservation of icotinib hydrochloride in the treatmentof advanced non-smallcell lung cancer
LIANGShao-ping,WANGHua-qing
(Department of Lymphoma,Cancer Institute and Hospital,Tianjin Medical University,National Clinical Research Center of Cancer, Tianjin Key Laboratory ofCancer Prevention and Therapy,Tianjin 300060,Chin a)
Objective:To observe the clinical effect and toxicity of icotinib in 30 patientswith advanced non-small cell lung cancer (NSCLC).Methods:Thirty patientswith advanced NSCLCwere retrospectively analyzed.Icotinib (125mg,three times a day)was orally taken by patients,to evaluate the short-term response,progression free survival(PFS)and toxicity.Results:Among the 30 patients,no cases experienced complete response(CR),10 cases experienced partial response(PR),14 caseswere with stable diseases(SD),6 cases werewith progression disease(PD),and the tumorobjective response rate(ORR)and disease control rate(DCR)were33.3%(10/30)and 80.0%(24/30),respectively.ECOG and brainmetastasiswere associated with short-term response.At the end of the follow-up period, twenty-four caseshad PD.Themedian PFSwas8.0months,significantly correlated with age,smoking history,ECOG,andmetastasis(P< 0.05).The incidence of side effectswas 43.3%,including rash(16.7%),itch of skin(6.7%),diarrhea(3.3%),heartburn(3.3%),andmild impairof liver function(20.0%).Conclusion:Icotinib hydrochloride iseffectivewith high drug tolerance foradvanced NSCLC.
icotinib hydrochloride;advanced non-smallcell lung cancer;epidermalgrowth factor receptor;molecular target therapy
R734.2
A
1006-8147(2015)01-0051-04
梁绍平(1988-),女,硕士在读,研究方向:肿瘤学;通信作者:王华庆,E-mail:huaqingw@163.com。

