单次静脉注射后多西环素在大鼠血浆和尿液中的药物动力学研究
杨 帆,赵振升,孟小宾,孔 涛,王国永,周变华,郝雪琴(.河南科技大学动物科技学院,河南洛阳47003;.天津瑞普生物技术股份有限公司,天津300300)
单次静脉注射后多西环素在大鼠血浆和尿液中的药物动力学研究
杨帆1,赵振升1,孟小宾2,孔涛1,王国永1,周变华1,郝雪琴1
(1.河南科技大学动物科技学院,河南洛阳471003;2.天津瑞普生物技术股份有限公司,天津300300)
摘 要:选用7只平均体重为250g±31g的健康雄性成年大鼠,进行多西环素单剂量静脉注射(10mg/kg体重)给药途径下的血浆和尿液药物动力学研究。采用高效液相色谱法检测血浆及尿液中的药物浓度,之后分别采用房室分析和速度法计算血浆和尿液中多西环素的药物动力学参数。健康大鼠静脉注射多西环素后,血浆浓度-时间数据的最优拟合模型为二室开放模型。主要药物动力学参数如下:表观分布容积(Vd)为(1 493.48±243.65)mL/kg、分布速率常数(α)为(13.70±5.92)h-1、消除速率常数(β)为(0. 15±0.03)h-1、体清除率(Cl)为(216.06±52.98)mL/h/kg。速度法计算得到的多西环素的药物动力学参数如下:β为(0.13±0.02)h-1、肾排泄速度常数(ke)为(0.08±0.02)h-1、肾清除率(Clre)为(113.35±18. 02)mL/h/kg、肝清除率(Clhe)为(102.71±32.14)mL/h/kg。研究结果表明,多西环素在大鼠体内分布广泛、消除缓慢;此外,大鼠体内多西环素的消除过程中,肝脏和肾脏均发挥了主要作用,且二者作用相当。
关键词:多西环素;大鼠;血浆;尿液;药物动力学
多西环素(doxycycline)是一种半合成的第二代四环素类药物,对革兰阴性菌和阳性菌及一些立克次体、衣原体、支原体、螺旋体及某些原虫均有显著的抑制作用[1]。因其抗菌谱广、抗菌能力强、价格低廉、使用方便,被广泛应用于兽医临床[2]。目前,多西环素的药物动力学报道已见于多种动物[3-7]。但这些研究中均仅以血浆浓度-时间数据来评价多西环素的药物动力学特征,目前国内尚无多西环素在任何动物体内的尿液药物动力学研究报道。为此,本文以大鼠为实验动物,开展了单次静脉注射途径下多西环素的血浆和尿液药物动力学研究,以期更全面地了解多西环素的药物动力学特征。
1 材料与方法
1.1材料
1.1.1试验药品与试剂 多西环素对照品,含量为86%,批号0485-0401,为中国食品药品检定研究院产品;盐酸多西环素注射液:含量规格为5 mL∶0.5g,批号20130417,为洛阳惠中兽药有限公司产品;肝素钠,效价≥140U/mg,为北京奥博星生物技术有限责任公司产品;色谱纯乙腈、甲醇为MERCK公司产品。其他试剂均为国产分析纯。
1.1.2仪器设备 Dionex U-3000型高效液相色谱仪,配备四元泵、Dionex U-3000紫外检测器、自动进样器、柱温箱、Chromeleon色谱工作站为Dionex公司产品;高速台式冷冻离心机为Thermo Fisher Scientific公司产品;感量为0.000 1g AUX 220型电子分析天平为Shimadzu公司产品;pHs-25 型pH计为上海精科雷磁仪器厂产品;XW-80A型旋涡混合器为上海青浦泸西仪器厂产品;MSI型微型混合器为IKA公司产品;4.6 mm×250 mm Hypersil BDS型C18色谱柱,粒径为5μm,为大连伊利特公司产品;60mg/3mL StrataTM-X固相萃取小柱为Phenomenex公司产品。
1.1.3实验动物 雄性Wistar大鼠7只,体重205g~300g,平均体重为250g±31g,购自南方医科大实验动物中心。试验动物购回后,常规适应性饲养1周,自由饮水和采食,饲料为不含任何抗生素和抗菌药的全价鼠粮。
1.2方法
1.2.1试液配制 多西环素标准储备液(1 000μg/mL):准确称取116.3mg多西环素对照品,置于100mL容量瓶中,以甲醇溶解,定容至刻度,-20℃冰箱中避光保存。临用前分取适量,用流动相稀释,配制成7个浓度梯度的标准工作液,浓度范围为2μg/mL~400μg/mL;EDTA-Na2-Mcllvaine缓冲液:准确称取27.548 1g的磷酸氢二钠、12.929 2g的柠檬酸和37.230 8g的EDTANa2,以1L超纯水溶解,经0.45μm微孔滤膜过滤后,置于4℃冰箱中备用。
1.2.2给药及样品采集 首先开展多西环素在大鼠血浆中的药物动力学研究。每只大鼠称重后保定,自尾静脉注射盐酸多西环素注射液,剂量为10 mg/kg体重(以多西环素计,下同),给药后5、10、15、30、45min和1、2、3、4、6、8、12、24、36h分别自每只大鼠的眶下静脉丛采集血液约200μL,用肝素钠进行抗凝,之后以4 000r/min转速离心10min,分离血浆样品,置-20℃冰箱中保存。血浆药物动力学结束10d(洗净期)后,将每只大鼠单独置于代谢笼中适应性饲养4d,之后开展多西环素的尿液药物动力学研究:每只大鼠单剂量静脉注射盐酸多西环素注射液(10mg/kg体重),之后收集给药后0~4、4~8、8~12、12~16、16~22、22h~28h内的尿液样品。准确记录各时间段尿液体积,并预留2mL左右尿样于-20℃冰箱中保存待测。
1.2.3样品前处理 精密量取100μL血浆,加入60μL 0.1 g/mL的抗坏血酸溶液和40μL 180mL/L的高氯酸溶液,涡旋3min,15 000r/inm离心15min,之后将上清液转移至内衬管中,再置于进样瓶中,进行高效液相色谱检测。
准确量取1mL尿液于15mL离心管中,加入5mL Na2EDTA-Mcllvaine缓冲液,8 000r/min离心10min,上清液进一步用StrataTM-X固相萃取小柱净化。净化程序如下:上样前,固相萃取小柱依次以5mL甲醇和5mL水活化平衡;平衡后上样;上样后,再依次以5mL水和5mL 50mL/L的甲醇水溶液淋洗,弃去全部淋洗液,减压抽干;最后用8mL 100mL/L的甲醇乙酸乙酯溶液分3次(3mL+3 mL+2mL)洗脱。收集全部洗脱液,于50℃水浴下以空气吹干。残渣中加入0.5mL流动相,充分涡旋1min后,转移到1.5mL离心管中,15 000r/min离心10min,上清液经0.22μm针头式滤器过滤后,置于尖底进样瓶中。
1.2.4检测方法
1.2.4.1色谱条件 色谱条件如下:BDS型C18色谱柱;柱温为30℃;紫外检测器,检测波长为350nm;流动相为乙腈和0.01mol/L的草酸溶液,两者比例为3∶7(V∶V),流速为1.0mL/min;进样量为50μL。
1.2.4.2标准曲线与线性范围 取1.2.1中的多西环素标准工作液适量,分别加入到空白血浆(100μL)或空白尿液(1mL)样品中,制得血浆及尿液的添加样品,添加浓度范围分别为0.1μg/mL~20μg/mL(血浆)和0.05μg/mL~20μg/mL(尿液)。之后按上述方法进行样品前处理和检测,获得不同添加浓度样品中多西环素的色谱峰面积,最后以峰面积对添加浓度进行线性回归,获得多西环素在血浆及尿液中的标准曲线。
1.2.4.3回收率与变异系数 取100μL空白血浆和1mL空白尿液样品,添加多西环素标准工作液,在标准曲线范围内,分别制得0.1、1、20μg/mL的血浆添加样品及0.05、1、10μg/mL的尿液添加样品,每批每个浓度均同时重复5个样品,共进行3个批次,按上述方法进行样品前处理和检测,同时直接制得3个相当浓度的标准工作液,直接进样。将经过前处理的生物样品所获得的多西环素色谱图峰面积与直接进样得到的峰面积进行比较,计算出多西环素的绝对回收率,并计算批内和批间变异系数。
1.2.4.4检测限和定量限 取大鼠空白的血浆(100μL)和尿液(1mL)样品,添加多西环素标准工作液适量,使得血浆及尿液样品中多西环素的浓度分别为0.025、0.05、0.1、0.5、1、2μg/mL。每个浓度6个平行,按上述方法进行样品前处理和检测,以最低检出浓度计算,3倍信噪比(S/N)为检测限(LOD),10倍信噪比为定量限(LOQ)。
1.2.5药物动力学分析 以WinNonlin软件(5.2. 1版,美国Pharsight公司),利用房室分析法计算多西环素的血浆药物动力学参数,以“AIC最小”为原则,辅以眼观比较来选择最佳房室模型及权重。尿液药物动力学参数则以速度法计算。
2 结果
2.1检测方法的线性范围与标准曲线
以多西环素的浓度(C)为纵坐标,对应的色谱峰面积(S)为横坐标进行线性回归分析,获得血浆及尿液中多西环素的标准曲线分别为C=3.590 2S-0.066 4和C=1.391 5S+0.102 6,相关系数分别为0.999 6和0.999 5。本检测方法的线性范围为0.1μg/mL~20μg/mL(血浆)和0.05μg/mL~20μg/mL(尿液)。
2.2检测方法的回收率和变异系数
本研究所建立的多西环素在大鼠血浆及尿液两种基质中检测方法的回收率及变异系数结果见表1。
表1 大鼠血浆及尿液中多西环素的回收率(±SD,n=5)和变异系数Table 1 Recovery(-x±SD,n=5)and coefficient of variation for doxycycline in plasma and urine samples of rats
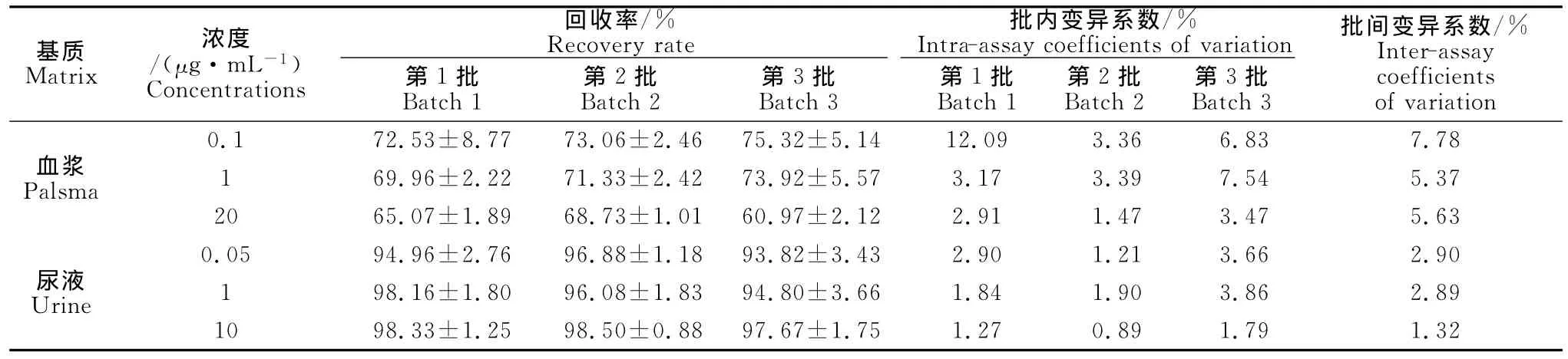
表1 大鼠血浆及尿液中多西环素的回收率(±SD,n=5)和变异系数Table 1 Recovery(-x±SD,n=5)and coefficient of variation for doxycycline in plasma and urine samples of rats
基质Matrix浓度/(μg•mL-1)Concentrations回收率/% Recovery rate 第1批Batch 1 第2批Batch 2 第3批Batch 3批内变异系数/% Intra-assay coefficients of variation 第1批Batch 1 第2批Batch 2 第3批Batch 3批间变异系数/% Inter-assay coefficients of variation血浆Palsma 0.1 72.53±8.77 73.06±2.46 75.32±5.14 12.09 3.36 6.83 7.78 1 69.96±2.22 71.33±2.42 73.92±5.57 3.17 3.39 7.54 5.37 20 65.07±1.89 68.73±1.01 60.97±2.12 2.91 1.47 3.47 5.63尿液Urine 0.05 94.96±2.76 96.88±1.18 93.82±3.43 2.90 1.21 3.66 2.90 1 98.16±1.80 96.08±1.83 94.80±3.66 1.84 1.90 3.86 2.89 10 98.33±1.25 98.50±0.88 97.67±1.75 1.27 0.89 1.79 1.32
2.3检测方法的检测限和定量限
本研究所建立的检测方法在大鼠血浆中的LOD和LOQ分别为0.05μg/mL和0.1μg/mL,尿液中则分别为0.025μg/mL和0.05μg/mL。
2.4多西环素在血浆和尿液中的浓度
大多数大鼠给药后36h血浆中药物浓度即达到LOQ附近,具体的浓度-时间曲线见图1。本研究中,前期一些时间点血浆中多西环素的浓度超出了标准曲线的上限,在检测过程中先以空白血浆对浓度超过标准曲线上限的样品进行了适当稀释后再进行前处理和定量分析。而大鼠单次静脉注射多西环素后累积尿药-时间曲线见图2。
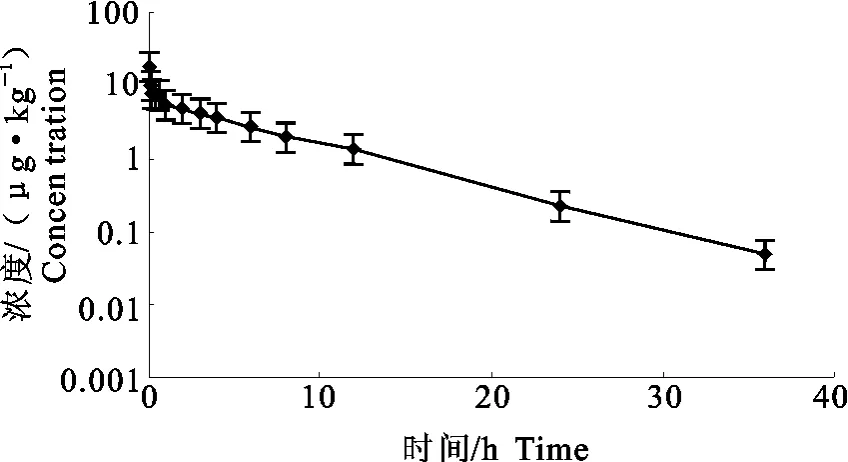
图1 大鼠(n=7)单次静脉注射多西环素(10mg/kg体重)后血浆药物浓度(-x±SD)-时间半对数图Fig.1 Semi-logarithmic plot showing the-x±SD plasma concentration-time profile of doxycycline in rats(n=7)after single intravenous injection at 10mg/kg
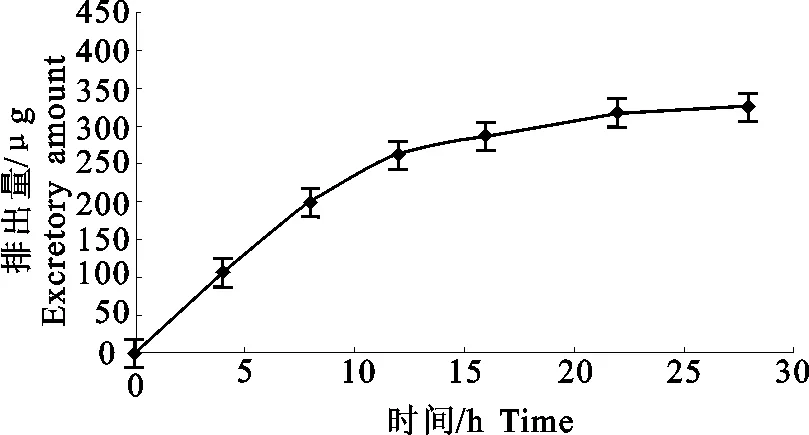
图2 大鼠(n=7)单次静脉注射多西环素(10mg/kg体重)后累积尿药(-x±SD)-时间曲线图Fig.2 Cumulative amount(-x±SD)of doxycycline excreted in urine after single intravenous injection at 10mg/kg in rats(n=7)
2.5血浆及尿液中多西环素的药物动力学参数
血浆浓度-时间数据的最优拟合模型为二室开放模型,权重为1/C2,其中C为检测到的药物浓度。以WinNonlin软件计算得到的多西环素的血浆药物动力学参数见表2。
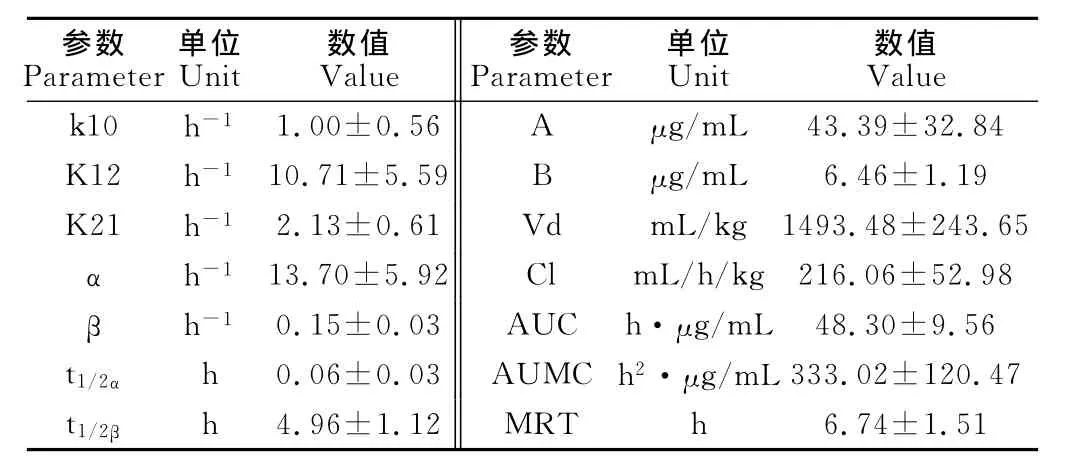
表2 大鼠(n=7)单次静脉注射多西环素(10mg/kg体重)后血浆药物动力学参数(-x±SD)Table 2 Plasma pharmacokinetics parameters(-x±SD)of doxycycline after single intavenous injection at 10mg/kg bw in rats(n=7)
以不同时间段尿液中多西环素排泄率的自然对数对各段采样时间中点作图(图3),利用残数法即可求算出消除速率常数β及keBV1,而V1和B值在血浆药物动力学部分已经求得(表2),因此本研究通过尿药数据计算得到多西环素的β为(0.13±0.02)h-1,ke为(0.08±0.02)h-1,而肾清除率(Clre)可通过ke与表观分别容积(Vd)的乘积计算得到,因此多西环素在大鼠体内的Clre等于(113.35±18.02)mL/h/kg。故而大鼠体内多西环素的非肾清除率(即肝清除率Clhe)应为(102.71±32.14)mL/h/kg。
3 讨论
3.1多西环素的血浆药物动力学
单次静脉注射后,大鼠血浆中多西环素浓度-时间数据的最优拟合模型为二室开放模型,这与Vargas-Estrada D等[8]报道的结果一致,但Michel G等[9]的研究结果却显示大鼠单次灌胃多西环素以后最优拟合模型为有吸收的一室开放模型,这可能与给药途径不同有关。在以往不同种属动物的研究中,猪[10]、鸡[11]、山羊[12]、绵羊[13]等动物体内均采用了二室开放模型来描述多西环素的处置特征。这与多西环素的理化性质有关,多西环素较第1代四环素类药物比,脂溶性更强。因此,其组织分布更广,容易在脂肪组织中蓄积,脂肪组织极易成为其周边室的主要组成部分,这也预示着多西环素在动物体内的消除会较缓慢。
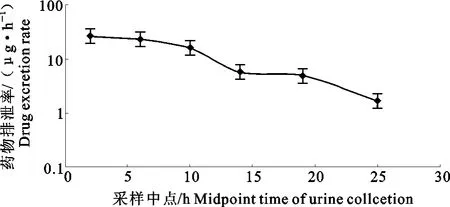
图3 大鼠(n=7)单次静脉注射多西环素(10mg/kg体重)后各时间段内多西环素随尿排泄率与采样时间中点的线性回归图Fig.3 Mean excretion rate of doxycycline versus midpoint time of urine collection curve after single intravenous administration at 10mg/kg bw in rats(n=7)
单次静脉注射后,多西环素在大鼠体内的消除半衰期(t1/2β)为4.96h±1.12h,稍大于Michel D等[9]报道的结果(2.47h~3.85h),这可能和2个研究中所使用的检测方法不同有关。本研究中所建立的高效液相色谱法,血浆中多西环素的LOQ低达0.05μg/mL,而Michel D等的研究中则使用了微生物法,定量限约为0.2μg/mL,无法对消除相后段更多的样品进行浓度定量,因此较难获得足够多的浓度-时间数据对消除相进行准确描述。本研究得出的多西环素的t1/2β与山羊[12](4.11h±0.46h)和肉鸡[11](4.75h±0.21h)体内的结果接近,但远大于猪[10](1.73h±0.1h)、远小于绵羊[13](7.027h~12.11h)体内的结果。这一区别可能与动物种属间的差异有关。单次静脉注射以后,多西环素在大鼠体内的表观分布容积(Vd)为1493.48mL/kg±243.65 mL/kg,与绵羊[13](1.820L/kg~2.690L/kg)和猪[14](1.04L/kg±0.09L/kg)体内的结果接近,但要大于肉鸡[11](0.28L/kg±0.02L/kg)体内的结果,相反小于山羊[12](4.91L/kg±0.13L/kg)体内的结果。考虑到不同动物的体重或体型差别,该结果表明多西环素在大鼠体内分布广泛。
3.2多西环素的尿液药物动力学参数
目前尚无多西环素在大鼠体内尿排泄的报道,本文在确定了多西环素在大鼠体内的处置特点符合二室开放模型的基础之上,以速度法处理了多西环素的尿药数据,计算得到β为(0.13±0.02)h-1、ke为(0.08±0.02)h-1、Clre为(113.35±18.02)mL/h/kg、Clhe为(102.71±32.14)mL/h/kg。该结果说明,大鼠体内肝脏和肾脏清除多西环素的能力相当。Ghani F等[15]也通过类似的方法研究了成年人体内多西环素随尿排泄情况,其研究结果显示人体内多西环素的Clre为(29.4±3.4)mL/h/kg,要远小于大鼠体内的数值,这说明大鼠体内多西环素的肾排泄速度要远快于人体,这可能是由两者间尿液形成及排泄速度间的差别所致。Whelton A等[16]则比较了健康和肾损伤成年男性体内多西环素药物动力学特征间的差别,研究结果表明,两者间肾实质中多西环素浓度没有明显差别,但肾损伤患者体内多西环素的Clre显著降低,这与本研究获得的结果一致,说明在多西环素清除过程中肾脏起到了重要作用。
本研究利用尿液中药物浓度-时间数据计算得到的β与利用血浆浓度-时间数据计算得到的结果非常接近,两者间无显著差异,表明以上两种方法计算结果准确可靠。除速度法以外,还可以应用亏量法计算药物的尿液药物动力学参数,但亏量法需要测定所有经尿液排出的药物总量,需要时间较长,因此本文未采用亏量法计算。大鼠是最常见的实验动物,常用于药物的临床前药物动力学评价研究,但前述讨论部分已表明多西环素在大鼠体内的药物动力学参数与其他动物差异较大,因此有必要进一步开展其他动物体内多西环素的尿液药物动力学研究,以了解多西环素在其他动物体内更全面的药物动力学特征。
目前,血浆是兽医药物动力学试验中最常使用的样品,但采样过程对动物伤害较大,且采样时间点过多时会导致动物血量减少,会影响动物健康及药物处置过程。而相比而言,尿药法取样对动物机体没有损伤,采样方便,因此尿药法在兽医药物动力学分析中具有重要的应用前景。目前尿药法在兽医药物动力学研究中应用较少,本文以大鼠为实验动物,开展了单次静脉注射后多西环素的血浆和尿液药物动力学研究,结果表明尿药法在兽医药物动力学研究中完全可行。同时,本文研究结果还表明,多西环素在大鼠体内分布广泛、消除缓慢;另外,大鼠体内多西环素清除过程中,肝脏和肾脏起到了主要作用,且作用相当。
参考文献:
[1] 王乐乐,邹 明,张启迪,等.氟苯尼考与盐酸多西环素体外联合抑菌效果研究[J].动物医学进展,2013,34(3):85-90.
[2] 赵驻军,蒋禄峰,秦建华.猪附红细胞体病流行病学调查及不同药物治疗效果[J].动物医学进展,2012,33(12):111-115.
[3] 孔宪诚,阎 良,黄建平.LC-MS/MS方法测定人血浆中多西环素浓度[J].中南药学,2014,12(3):231-234.
[4] 赵世明.黄曲霉毒素中毒条件下盐酸多西环素在樱桃谷肉鸭体内药动学研究[D].四川雅安:四川农业大学,2013.
[5] Yang F,Li Z L,Shan Q,et al.Pharmacokinetics of doxycycline in tilapia(Oreochromis aureus x Oreochromis niloticus)after intravenous and oral administration[J].J Vet Pharmacol T-her,2014,37(4):388-393.
[6] Embers M E,Hasenkampf N R,Embers D G,et al.Pharmacokinetic analysis of oral doxycycline in rhesus macaques[J].J Med Primatol,2013,42(2):57-61.
[7] Freeman K S,Thomasy S M,Stanley S D,et al.Population pharmacokinetics of doxycycline in the tears and plasma of northern elephant seals(Mirounga angustirostris)following oral drug administration[J].J Am Vet Med Assoc,2013,243 (8):1170-1178.
[8] Vargas-Estrada D,Gutierrez L,Juarez-Rodriguez I,et al. Pharmacokinetics of doxycycline and tissue concentrations of an experimental long-acting parenteral formulation of doxycycline in Wistar rats[J].Arzneimittelforschung,2008,58(6):310-315.
[9] Michel G,Mosser J,Olle J.Pharmacokinetics and tissue localization of doxycycline polyphosphate and doxycycline hydrochloride in the rat[J].Eur J Drug Metab Pharmacokinet,1984,9(2):149-153.
[10] Gutierrez L,Ocampo L,Espinosa F,et al.Pharmacokinetics of an injectable long-acting parenteral formulation of doxycycline hyclate in pigs[J].J Vet Pharmacol Ther,2014,37(1):83-89.
[11] Anadon A,Martinez-Larranaga M R,Diaz M J,et al.Pharmacokinetics of doxycycline in broiler chickens[J].Avian Pathol,1994,23(1):79-90.
[12] Vargas D,Gutierrez L,Juarez I,et al.Pharmacokinetics after administration of an injectable experimental long-acting parenteral formulation of doxycycline hyclate in goats[J].Am J Vet Res,2008,69(8):1085-1090.
[13] Castro L J,Sahagun A M,Diez M J,et al.Pharmacokinetics of doxycycline in sheep after intravenous and oral administration[J].Vet J,2009,180(3):389-395.
[14] 何家康,祝万菊,周丽光,等.盐酸多西环素缓释注射液在猪体内的药物动力学[J].中国兽医学报,2008,28(2):175-180.
[15] Ghani F,Iqbal T,Shahid M.Renal clearance of endogenous creatinine and doxycycline in male volunteers[J].J Med Sci,2003,3(4):283-288.
[16] Whelton A,Nightingale S D,Carter G G,et al.Pharmacokinetic characteristics of doxycycline accumulation in normal and severely diseased kidneys[J].J Infect Dis,1975,132(4):467-471.
Pharmacokinetics Studies of Doxycycline in Rats′Plasma and Urine after Single Intravenous Administration
YANG Fan1,ZHAO Zhen-sheng1,MENG Xiao-bin2,KONG Tao1,WANG Guo-yong1,ZHOU Bian-hua1,HAO Xue-qin1
(1.College of Animal Science and Technology,Henan University of Science and Technology,Luoyang,Henan,471003,China;2.Ringpu(Tianjin)Biological Pharmaceutical Co.,LTD.,Tianjin,300300,China)
Abstract:Seven healthy adult male Wistar rats,with an average weight of 250g,were used to study the pharmacokinetics characteristics of doxycycline in plasma and urine after intravenous administration at 10mg/kg.The doxycycline concentrations in plasma and urine samples were determind by a high performance liquid chromatography method.Then the plasma concentrations versus time data were subjected to compartmental analysis to obtain its pharmacokinetics parameters in plasma,while rate method was used to calculate the pharmacokinetics parameters in urine.The disposition of doxycycline after single intravenous injection was best described by a two-compartment open model.And the main plasma pharmacokinetics parameters were as flows:the volume of distribution(Vd)was(1493.48±243.65)mL/kg,distribution rate constant(α)was(13.70±5.92)h-1,elimination rate constant(β)was(0.15±0.03)h-1,and body clearence(Cl)was(216.06±52.98)mL/h/kg.The pharmacokinetics parameters of doxcycline derived from rate method were listed below:βwas(0.13±0.02)h-1,renal excretion rate constant(ke)was (0.08±0.02)h-1,renal clearence(Clre)was(113.35±18.02)mL/h/kg,and hepatic clearence(Clhe)was(102.71±32.14)mL/h/kg.In conclusion,doxycycline was distributed extensively and eliminated slowly in rats after intravenous administration.Liver and kidney shared the same abilities for elimination of doxcycline from rats.
Key words:doxycycline;rat;plasma;urine;pharmacokinetics
作者简介:杨 帆(1982-),男,河北卢龙人,讲师,博士,主要从事兽医药物代谢动力学研究。
基金项目:河南科技大学博士启动基金项目(09001677)
收稿日期:2014-12-26
中图分类号:S859.796
文献标识码:A
文章编号:1007-5038(2015)07-0052-05

