干扰素α-2b治疗132例慢性乙型肝炎患者临床观察
涂德幸,胡小雄,邓云梅,易清平
(江西省宜春市人民医院,宜春 336000)
干扰素α-2b治疗132例慢性乙型肝炎患者临床观察
涂德幸,胡小雄,邓云梅,易清平
(江西省宜春市人民医院,宜春 336000)
目的:探讨与验证重组人干扰素α-2b治疗慢性乙型肝炎(CHB)的临床疗效与安全性。方法:研究纳入符合适应证的HBeAg阳性CHB患者108例和HBeAg阴性CHB患者24例,共132例,分别接受重组人干扰素α-2b治疗48周,观察其生化学、病毒学及免疫学应答状况及副作用。结果:治疗结束后,分别有89例HBeAg阳性和19例HBeAg阴性CHB患者谷丙转氨酶和谷草转氨酶恢复正常,总体生化学应答率为81.8%(108/132)。有36例HBeAg阳性和23例HBeAg阴性患者HBV-DNA低于检测下限,总体病毒学应答率44.7%(59/132)。108例HBeAg阳性患者中有45例(41.7%)HBeAg消失,31例(28.7%)出现HBeAg血清转换。且132例CHB患者有14例(10.6%)出现HBsAg血清转换。若以治疗前病毒载量进行分层分析,则高病毒载量组(≥7 log 10 IU/ml)的病毒学应答率(39.1%vs65.0%,P<0.001)和HBeAg血清转率(20.7%vs53.8%,P=0.001)均显著低于低病毒载量组(<7 log 10 IU/ml),而生化学应答率(79.3% vs 87.5%,P=0.264)和HBsAg血清转换率(8.7%vs15.0%,P=0.280)无显著差异。治疗早期感冒样症状、骨髓抑制等副作用常见,整个治疗期间未观察到严重不良事件。结论:普通干扰素α-2b治疗慢性乙型肝炎对初始病毒载量低者使用干扰素治疗可获得较高的应答率,此类人群优先选择干扰素治疗,获得停药机会更大。
病毒性肝炎,乙型,干扰素α,治疗效果,副作用
根据2006年全国乙型肝炎流行病学调查,我国现有慢性乙型肝炎病毒(HBV)感染者约9 300万,其中慢性乙型肝炎(CHB)患者约为2 000万[1]。慢性乙型肝炎治疗的总体首要目标是最大限度地长期抑制HBV复制,若无使用禁忌,各大肝病学会指南均推荐长效干扰素作为抗病毒治疗的首选方案[1-4]。然而在我国,尤其是在中西部落后的地区,基于成本效益考虑,绝大部分患者通常选择普通干扰素。本研究观察了重组人干扰素α-2b治疗132例慢性乙型肝炎的临床疗效与副作用,为普通干扰素治疗CHB提供新的证据。
1 资料与方法
1.1 一般资料 选取2012年2月—2013年3月本院感染科收治的CHB患者132例(HBeAg阳性108例和HBeAg阴性24例)作为研究对象。所有患者均满足《慢性乙型肝炎防治指南》(2010年版)所提到抗病毒治疗一般适应证,且排除血糖及甲状腺功能异常、自身免疫病、妊娠、精神疾病等干扰素使用禁忌证者。并经伦理学论证和患者的知情同意。
1.2 治疗与随访 完成基线病情评估后,对符合干扰素治疗指征的患者首先给予重组人干扰素α-2b注射液(北京凯因科技股份有限公司)2周的强化治疗(5 MIU,1次/d,肌注),若无严重副作用,继续给予常规剂量及用法(5 MIU , 隔日1次,肌注)治疗持续至48周。
若治疗过程中出现严重骨髓抑制(中性粒细胞<0.75×109/L,或血小板<50×109/L)、或生化学异常(谷丙转氨酶或谷草转氨酶>10 ULN,或总胆红素>2 ULN),或其他严重不良反应时,则干扰素减量或停药,予对症治疗待相关指标恢复至安全范围以内再继续干扰素治疗。
治疗过程中,按照中国《慢性乙型肝炎防治指南》(2010版)要求定期进行血细胞分析以及血生化、HBV病毒学标志物、甲状腺功能、血糖、尿液分析等检测,并评估患者的精神状态。
1.3 临床检测 上述各项检测均由本院检验科进行,采用全自动五分类血液分析仪(日本Sysmex XT-2000i)进行血细胞分析;全自动生化分析仪(日本Olympus AU2700)检测谷丙转氨酶(ALT)等生化指标;ELISA法检测HBV血清标志物(上海科华生物工程股份有限公司);实时荧光定量PCR法检测HBV-DNA载量(中山大学达安基因股份有限公司),检测下限100 IU/ml。
1.4 应答判定标准 抗病毒治疗应答的判定标准主要有病毒学应答、血清学应答和生化学应答。病毒学应答指血清HBV-DNA检测不到(PCR法)或低于检测下限, 或较基线下降≥2 log 10 IU/ml;血清学应答指血清HBeAg转阴或HBeAg血清学转换, 或HBsAg转阴或HBsAg血清学转换;生化应答指血清ALT和AST恢复正常。

2 结果
2.1 基线资料 研究纳入慢乙肝病人132例,其中HBeAg阳性108例,HBeAg阴性24例。基线时HBeAg阳性患者的HBV-DNA水平高于HBeAg阴性患者(P<0.001),其余各项人口学、生化学和血液学指标两组比较均无显著差异。见表1。
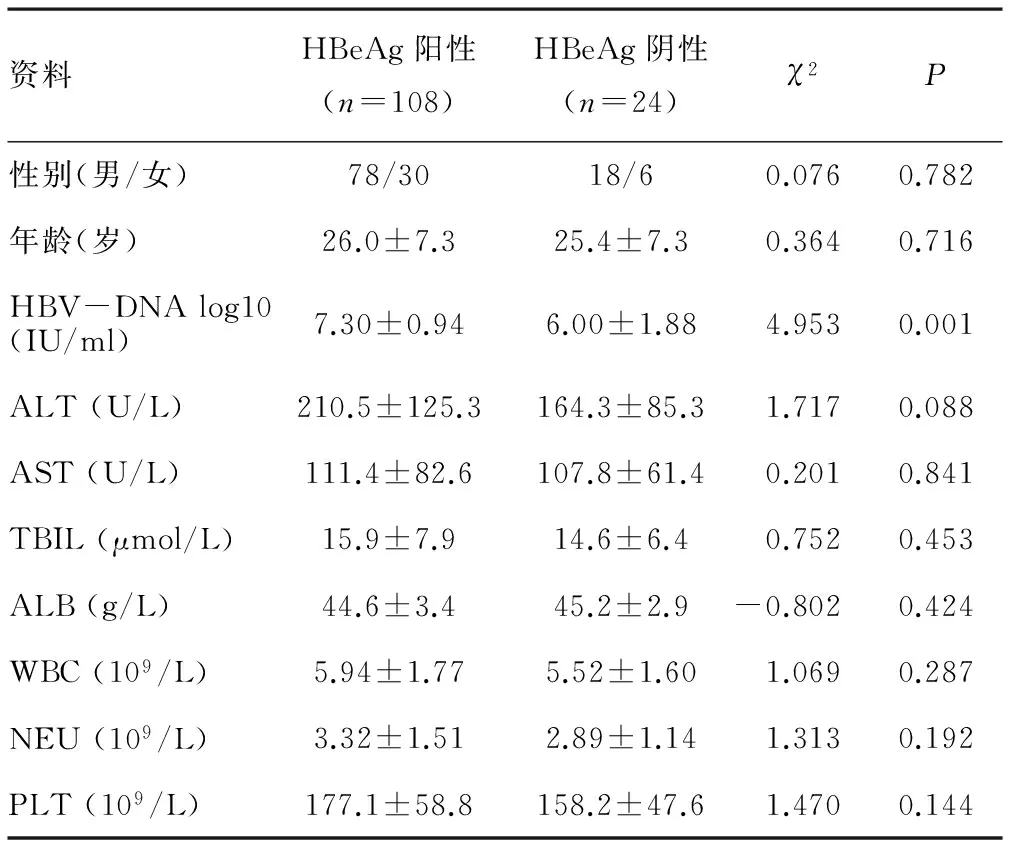
表1 研究人群的基线临床资料特征
注:ALT,谷丙转氨酶;AST,谷草转氨酶;TBIL,总胆红素;ALB,白蛋白;WBC,白细胞计数;NEU,中性粒细胞计数;PLT,血小板计数;HBV-DNA log10,乙型肝炎病毒DNA水平(取常用对数值)。
2.2 生化学应答与病毒学应答 108例HBeAg阳性患者干扰素治疗后4、12、24和48周ALT水平和HBV-DNA载量前后比较均有显著差异(P<0.001); 24例HBeAg阴性患者治疗后4、12、24和48周ALT水平和HBV-DNA载量前后比较无明显统计学差异(P=0.243,P=0.080)。132例CHB患者治疗48周总体生化学应答率为81.8%(108/132),病毒学应答率为44.7%(59/132)。具体情况见表2。
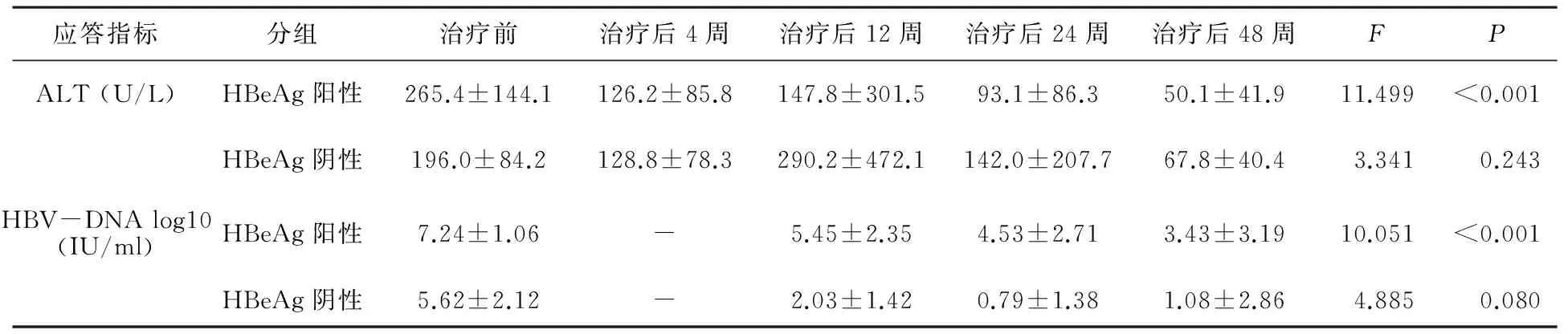
表2 132例CHB患者干扰素治疗前后生化学与病毒学应答状况
注:ALT,谷丙转氨酶;HBV-DNA log10,乙型肝炎病毒DNA水平(取常用对数值)。
2.3 血清学应答 108例HBeAg阳性患者,治疗后12周有4例出现HBeAg血清转换,没有患者出现HBsAg消失;治疗后24周HBeAg消失23例、HBeAg血清转换12例,HBsAg消失7例、HBsAg血清转换5例;治疗后48周HBeAg消失45例、HBeAg血清转换31例,HBsAg消失13例、HBsAg血清转换11例。而24例HBeAg阴性患者治疗后12周有2例出现HBsAg血清转换,治疗至48周有3例患者出现HBsAg血清转换。
若以HBeAg血清转换为标准, 108例HBeAg阳性患者治疗48周的免疫学应答率为28.7%(31/108);若以HBsAg血清转换为观察终点,则132例CHB患者治疗48周的免疫学应答率为10.6%(14/132)。
2.4 基线病毒载量对疗效的影响 按照基线HBV-DNA水平,分为高病毒载量组(HBV-DNA≥7 log10 IU/ml,92例,含HBeAg阳性82例)和低病毒载量组(HBV-DNA <7 log10 IU/ml,40例,含HBeAg阳性26例)进行分层分析。结果见表3。
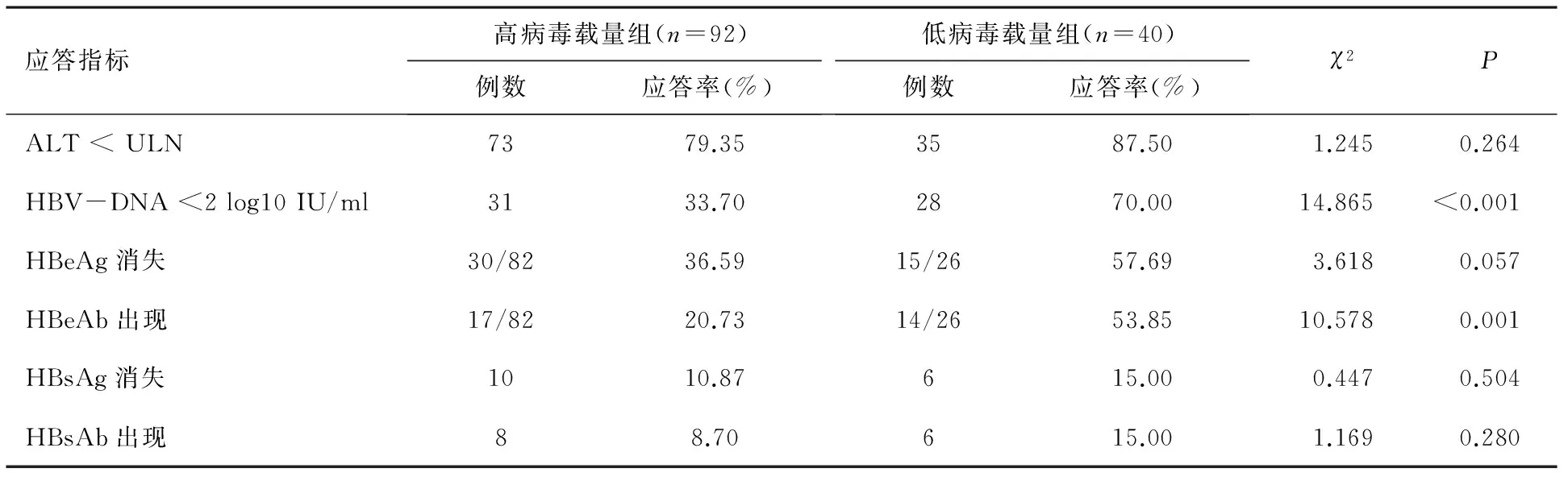
表3 CHB患者基线HBV-DNA载量对干扰素治疗应答的影响
注:ALT,谷丙转氨酶;HBV-DNA log10,乙型肝炎病毒DNA水平(取常用对数值)。
2.5 副作用观察 治疗开始,几乎所有患者均出现不同程度的流感样症状,经对症处理后均可耐受。治疗早期(第1~3周),118例患者出现一过性中性粒细胞减少,其中17例患者小于0.75×109/L,经减量或短暂停药后回升至正常水平,继续治疗后均可耐受;无患者出现严重血小板减少。治疗过程中有9例患者出现生化学突破(ALT>10 ULN),其中5例患者ALT>1 000 U/L,伴轻度胆红素升高或凝血功能改变,经停用干扰素接受护肝治疗后,肝功能指标恢复至安全范围以内,未出现严重肝功能失代偿。1例患者出现甲状腺功能减退,1例患者出现轻度精神抑郁,停用干扰素给予对症处理后均恢复正常。无其他严重不良事件发生。
3 讨论
本研究发现,对HBeAg阳性患者,干扰素α-2b治疗48周后HBV-DNA<100 IU/ml的患者比例为33.3%,HBeAg血清转换率28.7%,这与既往报道的结果[6-8]相似。可见,与核苷(酸)类似物相比,干扰素治疗CHB的优势在于免疫调节,而不是病毒抑制,因此能够获得相对较高的HBeAg血清转换率,甚至是HBsAg血清转换率。与既往研究相比[8],本研究中HBsAg血清转换率偏高,但在HBV-DNA不同载量分组间HBsAg血清转换率差异并不大,考虑其原因可能与采用的国产ELISA检测试剂HBsAb的假阳性有关。
治疗前HBV-DNA水平影响干扰素治疗效果的重要预测因素[9],根据基线HBV-DNA水平将患者重新分组分析,发现低病毒载量组(HBV-DNA<7 log 10 IU/ml)患者的病毒学应答率和HBeAg血清转换率均显著优于高病毒载量组。提示:①严格筛选患者可以提高干扰素治疗慢性乙型肝炎患者的病毒学应答率与HBeAg血清学转换率,对于治疗前病毒载量较低的CHB患者,使用干扰素治疗可获得较高的应答率;②对于基线病毒载量高的CHB患者,单用干扰素治疗未必是最优方案。新近发现干扰素与核苷(酸)类似物联合或序贯治疗,可获得较高的病毒学及免疫学应答率[10],可能与后者的强效抗病毒作用使肌体突破免疫耐受有关[11]。
在本研究中,部分病例治疗24周HBV-DNA转阴或较基线下降>2 log 10 IU/ml的患者,继续治疗至48周时检测发现HBV-DNA阳转或反弹。究其原因,除检测误差外,可能与肌体产生干扰素中和抗体有关。据刘定力等[12]报道,出现病毒学反弹者,检测血清干扰素中和抗体的阳性率高达68.2%。作为多肽类物质,重组干扰素具有一定的免疫原性,可刺激肌体产生结合型和中和型两种抗体[13,14]。中和型抗体可中和体内的重组干扰素,从而降低疗效。通常认为,干扰素中和抗体产生于开始治疗后3~6个月,停止给药后仍可持续3~6个月。因此,干扰素治疗过程中应定期监测中和抗体的产生,及时调整治疗方案。
总之,重组人干扰素α-2b治疗慢性乙型肝炎的整体疗效有限,但进行分层分析可知,对基线病毒载量较低的患者,干扰素治疗效果较好,此类患者通过使用干扰素获得停药的机会更大;对于基线病毒载量高者现有治疗效果整体较差,也是目前研究的热点,可通过序贯治疗、干扰素和核苷类药物联合治疗,核苷类药物间联合治疗等实现更高的获益。
1 中华医学会肝病学分会,中华医学会感染病学分会.慢性乙型肝炎防治指南(2010年版)[J].中华流行病学杂志,2011,32(4):405-415
2 朱鹏飞,赵勇华,李晶媛,等.应用基因芯片筛选慢性乙型肝炎患者PD-1/PD-L通路基因差异表达[J].国际免疫学杂志,2012,35(3):236-241
3 李红霞,郭玉杰,刘丹.慢性乙型肝炎患者负性情绪及影响因素的调查分析及对策[J].中国实用护理杂志,2010,26(8):8-10
4 刘道洁,董培玲,丁惠国,等.IFN-α治疗慢性乙型肝炎疗效与记忆性T细胞的相关性[J].中华微生物学和免疫学杂志,2011,31(3):265-268
5 王银芳.护理干预对慢性乙型肝炎合并糖尿病患者生活质量的影响[J].中国实用护理杂志,2010,26(5):9-10
6 王园园,沈娟,钱湘云.网络互动式健康教育对慢性乙型肝炎患者生活质量的影响[J].中国实用护理杂志,2014,30(3):69-71
7 韦叶生,蓝艳,徐群清,等.慢性乙型肝炎转化生长因子β1基因单核苷酸多态性及单倍型分析[J].中华微生物学和免疫学杂志,2007,27(11):967-971
8 高志良,谢冬英,林炳亮,等.慢性乙型肝炎抗病毒优化治疗策略浅谈[J].中华肝脏病杂志,2012,20(2):154-157
9 杨露绮.从1例慢性乙型肝炎患者治疗过程分析慢性乙型肝炎的治疗策略[J].中华肝脏病杂志,2009,17(9):709-710
10 鲁晓擘,刘浩,徐琴,等.Dubin-Johnson综合征合并慢性乙型肝炎患者脂褐素小体的超微结构特点[J].中华肝脏病杂志,2011,19(3):210-213
11 丁玉平,邹志强,徐学彩,等.乙型肝炎病毒核心抗原与慢性乙型肝炎患者临床病理学特征的关系[J].中华肝脏病杂志,2014,22(3):185-189
12 刘定力,骆抗先,冯筱榕,等.重组α干扰素治疗慢性乙型肝炎病毒学反弹与干扰素中和抗体的相关性研究[J].中华肝脏病杂志,2007,15(6):422-425
13 Sayed S K,Kobeisy M A.The relationship between core promoter mutation of hepatitis B virus,viral load and hepatitis B e antigen status in chronic hepatitis Bpatients[J].Cell Immtmol,2012,276(12):35-41
14 Kim T H,Cho E Y,Oh H J,etal.The degrees of hepatocyte cytoplasmic expression of hepatitis B core antigen correlate with histologic activity of liver disease in the youngpatients with chronic hepatitis B infection[J].J Korean Med Sci,2006,21(4):279-283
2015-04-16
宜春市科技支撑计划( No.JXYC2014KSB015)
R975+.5
A
1006-5687(2015)03-0048-04

