盐酸伊托必利分散片溶出度与稳定性考察
高 茹,王江涛(迪沙药业集团有限公司,威海 264200)
盐酸伊托必利分散片溶出度与稳定性考察
高 茹,王江涛(迪沙药业集团有限公司,威海 264200)
目的 比较盐酸伊托必利分散片与普通片的溶出度及稳定性。方法 采用桨法测定溶出度,紫外分光光度法在258nm处测定吸光度,计算溶出度,并进行稳定性研究。结果 盐酸伊托必利分散片与普通片在5min的累积溶出度分别为81.73%± 1.15%和13.86%±0.5%,30min的累积溶出度分别为93.29%±0.12%和74.54%±0.4%。盐酸伊托必利分散片的溶出度和稳定性优于普通片。结论 盐酸伊托必利分散片溶出度高、质量稳定。
盐酸伊托必利;分散片;溶出度;稳定性
1 仪器与试药
1.1 仪器 U-2910双光束紫外可见分光光度计(日本日立HITACHI);RC806溶出实验仪(天津市天大天发科技有限公司)。
1.2 试药 盐酸伊托必利分散片(标示量50mg,自制,批号131202,131203,131204);普通片(标示量50mg,云南永安制药有限公司,20131026);盐酸伊托必利对照品(中国食品药品检定研究院,质量分数99.9%);水为纯化水。
2 方法与结果
2.1 处方组成 盐酸伊托必利50mg,微晶纤维素80mg,交联聚维酮12mg,羟丙纤维素16mg,乳糖110mg,十二烷基硫酸钠0.25mg,二氧化硅5mg,硬脂酸镁1.25mg,甲基纤维素60mg,聚丙烯酸树脂Ⅳ15mg。
2.2 方法学考察
2.2.1 测定波长的选择 精密称取干燥至恒质量的盐酸伊托必利对照品适量,并称取各辅料可能出现的最大量,加水分散或溶解并稀释成适当质量浓度的溶液,超声过滤,取滤液在200~400nm波长范围内进行紫外扫描,吸收图谱表明,盐酸伊托必利在258nm波长处有最大吸收,辅料在此波长无吸收,故将其检测波长确定为258nm。
2.2.2 标准曲线的建立 精密量取对照品储备液适量,加水稀释制成0.937 5,1.875,3.75和7.5,15 μg·mL-1的溶液。以水为空白,在258nm波长处测定吸光度,其回归方程:A=0.051 8 C-0.007 1,r=0.999 5(n=5)。结果表明,盐酸伊托必利质量浓度在0.937 5~15μg·mL-1范围内线性关系良好。
2.2.3 精密度实验 取2.2.2线性实验项下质量浓度为4.89μg·mL-1的样品溶液,重复在258nm处测定6次,按照吸光度计算RSD为0.03%。
2.2.4 重复性实验 取同一批样品20片,研细,精密称取加水配制成含盐酸伊托必利约5.00μg·mL-1的溶液,共配制6份,于258nm处测定吸光度,其RSD为0.49%。
2.2.5 回收率实验[3]称取处方量的辅料,分别加入处方量的80%,100%和120%的盐酸伊托必利原料(即约40,50和60mg),混匀,每份质量浓度平行配制3份。按照2.3项下方法进行测定,计算回收率,结果平均回收率为99.8%,RSD为0.46%(n=9)。
2.2.6 溶液稳定性实验 取测定溶液(5.55μg·mL-1)在0,2,4,6和8h分别测定吸光度,按照吸光度计算RSD为0.035%,表明溶液至少在8h内稳定[4]。
2.3 溶出度测定 取分散片与普通片各6片,采用篮法,以900mL水为溶出介质,介质温度为37± 0.5℃,转速75r·min-1,分别在实验开始后5,10,15,20和30min取样,精密量取续滤液5mL,置于25mL量瓶中,加水稀释至刻度,摇匀,作为供试品溶液。在258nm波长处测定吸光度,分别计算分散片与普通片在各时间点的溶出百分率,测定结果见表1。
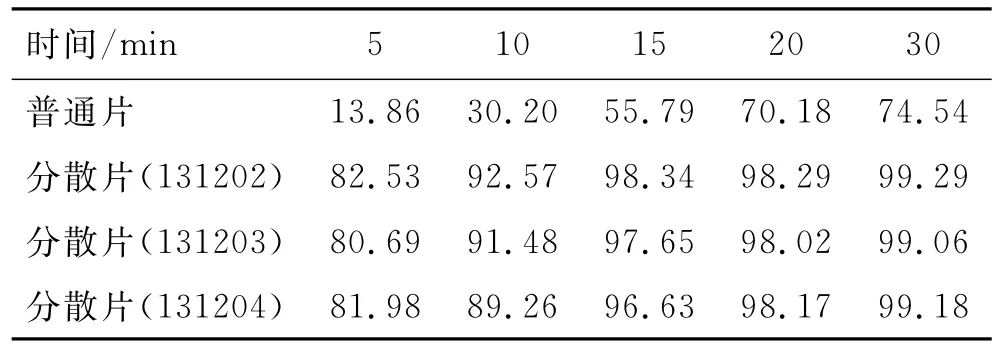
表1 盐酸伊托必利分散片与普通片的累积溶出百分比Tab.1 The cumulative dissolutions percentage of Itopride Hydrochloride Dispersion Tablets and ordinary tablets(n=6)
溶出结果表明,通过在介质水中溶出曲线的对比研究,盐酸伊托必利分散片溶出行为优于普通片。
2.4 稳定性考察 针对该产品对湿极不稳定的特点,按下述方法进行稳定性实验。稳定性实验包括影响因素实验、加速实验和长期留样实验。
2.4.1 影响因素实验 光照实验 样品置于透明密封容器中,放在4 500±500lx光照条件下实验。
高温实验 样品置于避光密封容器中,放在60℃条件下实验。
高湿实验 样品置于避光密封容器内,25℃时在RH(90%±5%)条件下实验。
上述实验分别于0,5和10d取样测定有关物质。其质量对比结果见表2。
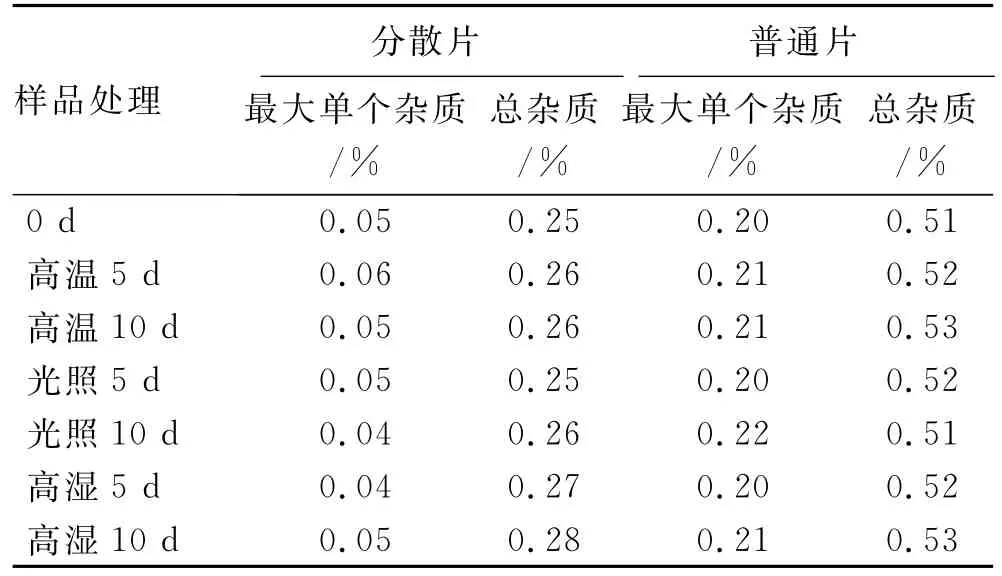
表2 盐酸伊托必利分散片与普通片的影响因素实验结果Tab.2 The impact factors test results of Itopride Hydrochloride Dispersion Tablets and ordinary tablets
结果表明,本品在高温、光照、高湿条件下均较稳定,盐酸伊托必利分散片稳定性优于普通片。
2.4.2 加速及长期留样实验
2.4.2.1 加速实验 将样品模拟上市包装(铝塑),在温度40℃、相对湿度75%的条件下放置6个月,分别于0,1,2,3和6个月时取样测定,结果见表3。
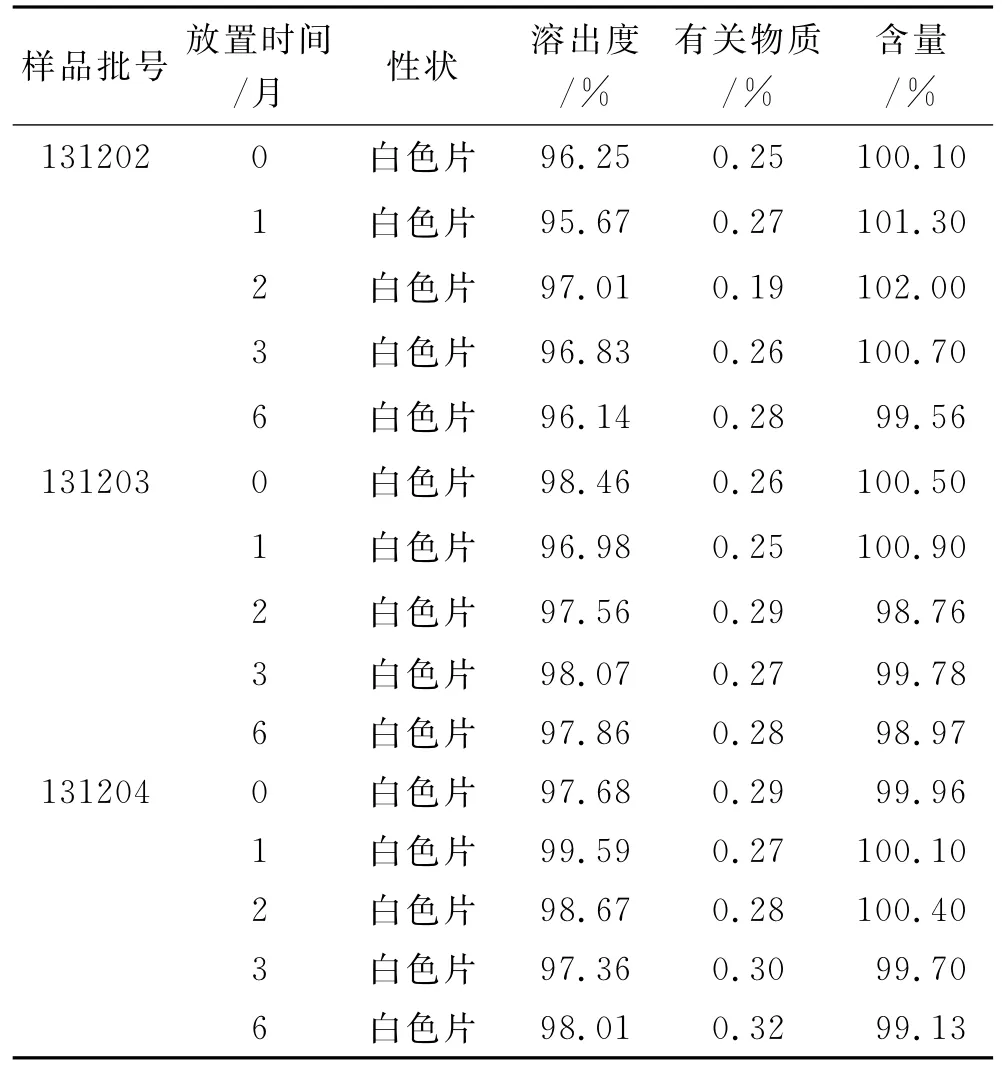
表3 盐酸伊托必利分散片与普通片的加速实验结果Tab.3 The accelerated test results of Itopride Hydrochloride Dispersion Tablets and ordinary tablets
2.4.2.2 长期实验 将3批样品模拟上市包装(铝塑),在温度25℃、相对湿度60%的条件下放置12个月,分别于0,3,6,9和12个月时取样测定,结果见表4。
3 讨论
目前,国内外盐酸伊托必利的主要剂型有片剂、胶囊、颗粒剂、分散片、缓释片,其中分散片的研究还少见报道[5]。国内上市的该品种剂型主要为片剂、胶囊,对吞咽固体药品困难的患者服用很不方便。盐酸伊托必利分散片很好地解决了这一问题,遇水后可迅速分散形成均匀的混悬液,具有吸收快、生物利用度高、不良反应小等优点[6]。盐酸伊托必利分散片溶出速率明显高于市售普通片,提示盐酸伊托必利分散片的吸收比普通片快,并有可能提高药物的生物利用度。

表4 盐酸伊托必利分散片与普通片的长期实验结果Tab.4 The long-term test results of Itopride Hydrochloride Dispersion Tablets and ordinary tablets
由于本品主药极易吸湿,吸湿后诱发主药黏性,可导致溶出慢、生物利用度低、稳定性差;从稳定性实验结果来看,盐酸伊托必利分散片在光照、高温、高湿等影响因素条件及加速、长期条件下有关物质均优于市售普通片。
综上所述,将盐酸伊托必利制成分散片后,不仅可改善稳定性,也可显著促进其体外溶出、体内吸收速度和生物利用度,值得进一步研究。
[1]龙连清.一种盐酸伊托必利分散片组合物:中国,201210086799.1[P].2014-01-29.
[2]陈豪,谭志荣,郭栋,等.高效液相色谱-串联质谱法测定人血桨中伊托必利的浓度[J].中国新药杂志,2008,17(21):1869-1872.
[3]张艳侠,袁转梅,陈育育,等.阿利苯多片溶出度方法的建立及溶出曲线的比较[J].西北药学杂志,2014,29(5):508-546.
[4]刘福利,曾爱国,王云彩,等.阿奇霉素分散片的稳定性研究[J].西北药学杂志,2005,20(5):216-218.
[5]张雪华,郭利民,钟世华,等.紫外分光光度法测定盐酸伊托必利分散片的含量[J].中国现代药物应用,2010,4(9):22-23.
[6]黄胜炎.分散片进展[J].中国药学杂志,1992,27(4):226-228.
Dissolution and stability of Itopride Hydrochloride Dispersion Tablets
GAO Ru,WANG Jiangtao(Disha Pharmaceutical Group Limited Company,Weihai 264200,China)
Objective To compare dissolution and preliminary stability of Itopride Hydrochloride Dispersion Tablets with ordinary tablets.Methods Dissolution was measured using the paddle method.The absorbability was determined by ultraviolet spectrophotometry with detection wavelength at 258nm,and the dissolution was computed.Results The cumulative dissolutions of Itopride Hydrochloride Dispersion Tablets and ordinary tablets at 5minutes were 81.73%±1.15%and 13.86%±0.5%,while 30minuteswere 93.29%±0.12%and 74.54%±0.4%,respectively.Itopride Hydrochloride Dispersion Tablets was better than ordinary tablets in dissolution and stability.Conclusion The technology of preparation for dispersible tablets of Itopride Hydrochloride Dispersion Tablets with good dissolvability and stability.
itopride hydrochloride;dispersible tablet;dissolution;stability盐酸伊托必利为胃肠促动力药,能拮抗多巴胺D2受体增加乙酰胆碱的释放,同时抑制乙酰胆碱酶阻碍已释放的乙酰胆碱分解,从而增强胃、十二指肠动力[1]。临床研究显示,盐酸伊托必利可以成为治疗功能性消化不良及慢性胃炎患者因胃肠动力障碍引起的消化不良症状药物的新选择[2]。在实验过程中发现本品主药极易吸湿,而且有关物质增长较快。因此,为保证样品的质量,本实验对盐酸伊托必利分散片与普通片的溶出度和稳定性进行了比较。
10.3969/j.issn.1004-2407.2015.04.023
R944
A
1004-2407(2015)04-0400-03
2014-12-18)

