蓝翘解毒口服液质量标准的改进
巩伟 李兴东 孙旭 赵庆华 张欣欣 张琨 赵梅
济南军区联勤部药品仪器检验所,山东济南250022
蓝翘解毒口服液质量标准的改进
巩伟 李兴东 孙旭 赵庆华 张欣欣 张琨 赵梅
济南军区联勤部药品仪器检验所,山东济南250022
目的对蓝翘解毒口服液的质量标准进行改进。方法采用薄层色谱法(TLC)鉴别制剂中的板蓝根,气相色谱法(GC)鉴别制剂中的广藿香,高效液相色谱法(HPLC)测定制剂中连翘苷的含量。结果TLC法鉴别供试品色谱中,在与对照药材色谱和对照品色谱相应的位置上显相同颜色的斑点;GC法检测供试品色谱中呈现与对照品色谱峰保留时间相同的色谱峰;HPLC法含量测定中连翘苷在9.387~300.4μg/mL质量浓度范围内线性关系良好(r=0.9999,n=6),加样回收率为99.62%,RSD为1.21%(n=9)。结论本研究建立的方法结果准确,稳定性好,专属性强,改进后的质量标准可用于蓝翘解毒口服液的质量控制。
蓝翘解毒口服液曰薄层色谱法曰气相色谱法曰高效液相色谱法曰板蓝根曰广藿香曰连翘苷
蓝翘解毒口服液为《解放军医疗机构制剂规范》2002年版收载品种[1],临床用于预防和治疗病毒性感冒、病毒性脑炎等。该药处方由板蓝根、芦根、山豆根、郁金、连翘、石膏、石菖蒲、广藿香、荆芥、地黄、知母等11味中药组成。该药原质量标准中仅有针对山豆根和连翘的薄层色谱鉴别等检验项目,无含量测定。在军队医疗机构制剂标准提高工作展开之际,为更有效地控制蓝翘解毒口服液的质量,本试验对其质量标准进行提高,其中采用薄层色谱法(TLC)对板蓝根进行定性分析,气相色谱法(GC)法对广藿香进行定性分析,高效液相色谱法(HPLC)对连翘进行定量分析,现报道如下:
1 仪器与试药
1.1 仪器
GC2010气相色谱仪(日本岛津公司);LC-20AT液相色谱仪(日本岛津公司);AUW220D电子分析天平(日本岛津公司);Synergy-UV超纯水器(法国Millipore公司);TLA-1薄层观察分析仪(湖南长沙克罗玛科技有限公司)。
1.2 试药
板蓝根对照药材(批号:121177-201105),亮氨酸对照品(批号:140687-200401),精氨酸对照品(批号:140685-201003),百秋李醇对照品(批号:110772-201105),连翘苷对照品(批号:110821-201112,含量测定以95.3%计算),以上标准物质均购自中国药品生物制品检定研究院;乙腈、萘为色谱纯(Honeywell),水为自制超纯水,硅胶G薄层板购自烟台市化学工业研究所(批号:120924),其他试剂均为分析纯。蓝翘解毒口服液为济南军区联勤部2014年度抽验制剂品种(规格每支装10 mL,批号:20140108、20140224、20140128、20130923,生产单位分别为解放军第一五四医院、第一五五医院、第一五九医院、第三七一医院,阴性对照制剂委托解放军第三七一医院配制)。
2 方法与结果
2.1 TLC法行板蓝根定性分析
取本品10 mL,蒸干,残渣加稀乙醇2 mL使溶解,作为供试品溶液。另取缺板蓝根的阴性对照制剂10 mL,同法制成阴性对照溶液。另取板蓝根对照药材1.0 g,加稀乙醇20 mL,超声处理20 min,滤过,滤液蒸干,残渣加稀乙醇2 mL使溶解,制成对照药材溶液。再取亮氨酸对照品、精氨酸对照品适量,加稀乙醇制成每1毫升各含0.5 mg的混合溶液,作为对照品溶液。照薄层色谱法[2]附录34-35试验,吸取上述3种溶液各5μL,分别点于同一硅胶G薄层板上,以正丁醇-冰醋酸-水(19∶5∶5)为展开剂,展开,取出,晾干,喷以茚三酮试液,在105℃加热至斑点显色清晰。供试品色谱中,在与对照药材色谱和对照品色谱相应的位置上应显相同颜色的斑点,阴性对照无干扰。薄层色谱图见图1。

图1 板蓝根鉴别薄层色谱图
2.2 GC法行广藿香定性分析
取本品100 mL,置500 mL圆底烧瓶中,加水100 mL与玻璃珠数粒,连接挥发油测定器,自测定器上端加水使充满刻度部分,并溢流入烧瓶为止,再加入环已烷2 mL,连接回流冷凝管,加热回流2 h,冷却,取环已烷液,加入适量无水硫酸钠,振摇,取上清液作为供试品溶液。另取缺广藿香的阴性对照制剂100 mL,同法制备阴性对照溶液。另取百秋李醇对照品适量,加环已烷制成每l毫升含0.1 mg的溶液,作为对照品溶液。照气相色谱法[2]附录38-39试验,用以5%苯基甲基聚硅氧烷为固定相的毛细管柱(柱长为30 m,内径为0.32 mm,膜厚度为0.25μm);柱温为程序升温:初始温度170℃,以每分钟2℃的速率升温至180℃,保持2 min,再以每分钟10℃的速率升温至230℃,保持2 min;进样口温度为230℃;检测器温度为250℃;分流进样,分流比为50∶1。分别吸取对照品溶液、供试品溶液和阴性对照溶液各1μL,注入气相色谱仪。供试品色谱中应呈现与对照品色谱峰保留时间相同的色谱峰,阴性对照无干扰。气相色谱图见图2。

图2 广藿香鉴别气相色谱图
2.3 HPLC法行连翘定量分析
2.3.1 色谱条件
色谱柱:Inertsil ODS3柱(250 mm×4.6 mm,5μm);流动相:乙腈-水(23∶77),流速:1.0 mL/min;检测波长:277 nm;柱温为室温;自动进样器进样,进样量为10μL;理论板数按连翘苷峰计应不低于5000,阴性对照无干扰。液相色谱图见图3。
2.3.2 溶液的制备
2.3.2.1 对照品溶液的制备精密称取连翘苷对照品19.70 mg,置25 mL量瓶中,加70%甲醇定容,摇匀,作为对照品贮备液。精密量取对照品贮备液适量,以70%甲醇为溶剂制成不同质量浓度的对照品溶液。该系列的连翘苷对照品溶液的最终质量浓度分别为9.387、18.77、37.55、75.10、150.2、300.4μg/mL。
2.3.2.2 供试品溶液的制备精密量取本品25 mL,用乙酸乙酯振摇提取6次,每次25 mL,合并乙酸乙酯液,蒸干,残渣加70%甲醇溶解,置10 mL量瓶中,加70%甲醇至刻度,摇匀,作为供试品溶液。
2.3.2.3 阴性对照溶液的制备另取缺连翘的阴性对照制剂25 mL,同法制备阴性对照溶液。
2.3.3 线性关系考察
取“2.3.2”项下配制的系列对照品溶液各10μL,注入液相色谱仪进行测定。以质量浓度(μg/mL)为横坐标、峰面积为纵坐标,绘制标准曲线,得连翘苷的回归方程为Y=456.8X-19.27(r=0.9999,n=6)。结果表明,连翘苷在9.387~300.4μg/mL质量浓度范围内线性关系良好。
2.3.4 精密度试验
精密吸取同一对照品溶液(质量浓度为75.10μg/mL),连续进样6次,连翘苷峰峰面积的RSD为0.82%(n= 6),表明精密度良好。
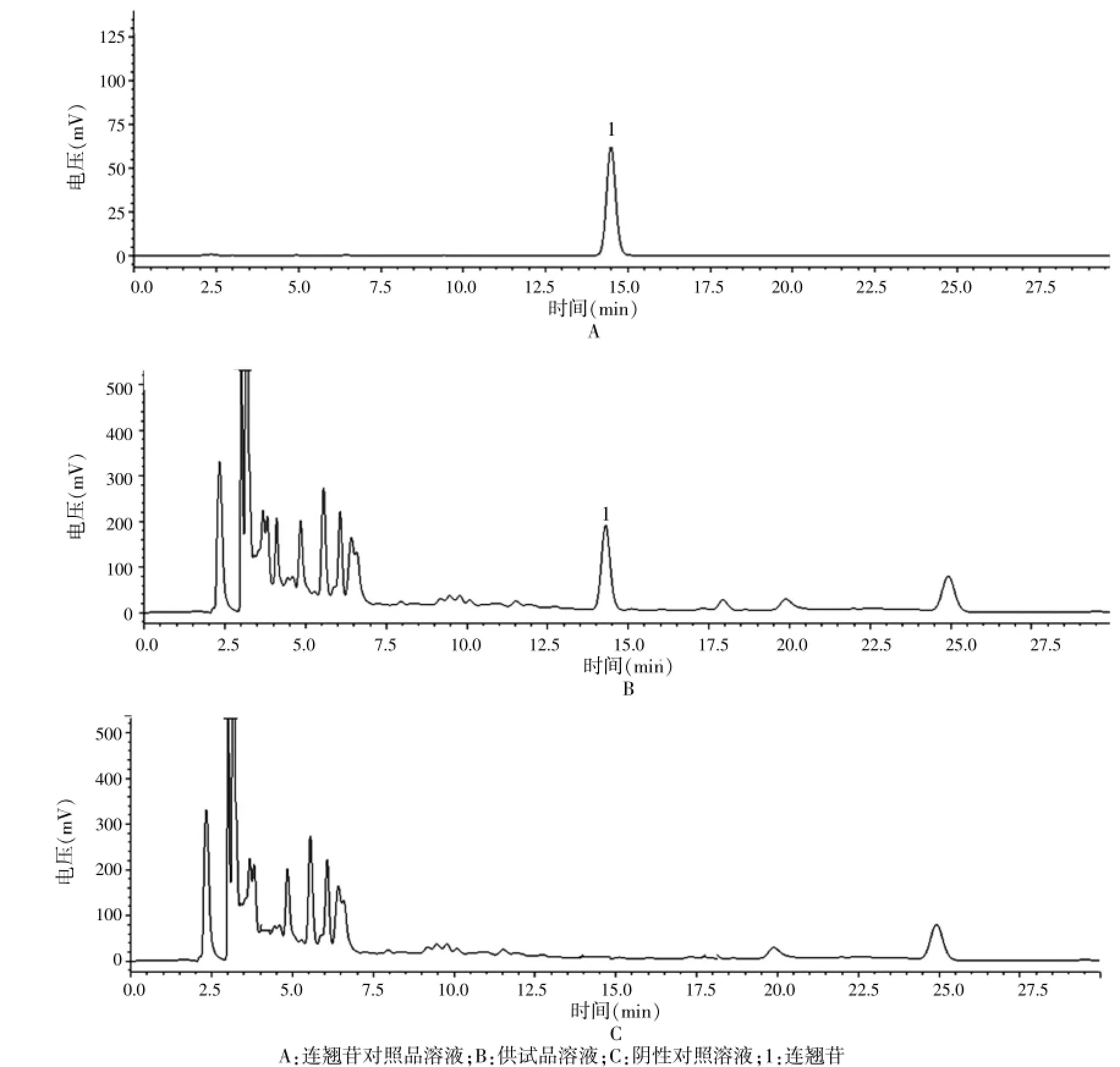
图3 连翘苷含量测定高效液相色谱图
2.3.5 重复性试验
取蓝翘解毒口服液(批号:20130923)25 mL,按“2.3.2”项下方法制备,平行试验6份。结果连翘苷的平均含量为97.28μg/mL,RSD=0.88%(n=6),表明方法重复性良好。
2.3.6 稳定性试验
精密吸取同一供试品溶液10μL,于0、4、8、12、16、24h分别测定峰面积。结果,连翘苷峰面积的RSD为1.15%(n=6),表明供试品溶液在24h内稳定性良好。
2.3.7 加样回收率试验
精密量取已知连翘苷含量的样品(批号:20130923,含量为97.28μg/mL)9份,分别按低、中、高加入连翘苷对照品,按“2.3.2”项下方法制备,测定峰面积并计算回收率,结果见表1。
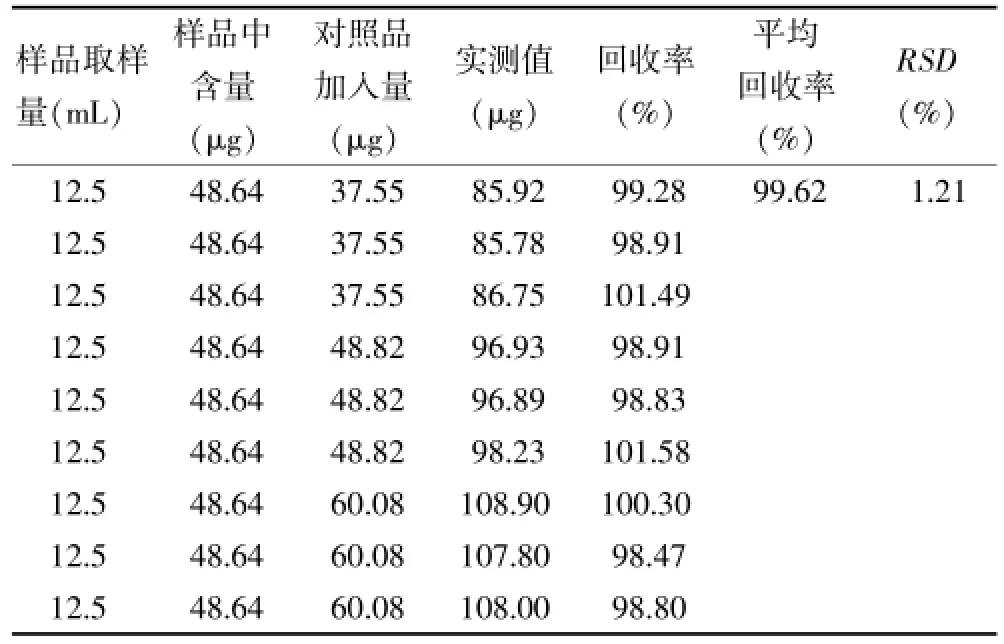
表1 加样回收率试验结果(n=9)
2.3.8 样品含量测定
取4批蓝翘解毒口服液,按“2.3.2”项下方法制备并测定连翘苷的含量,测定结果见表2。
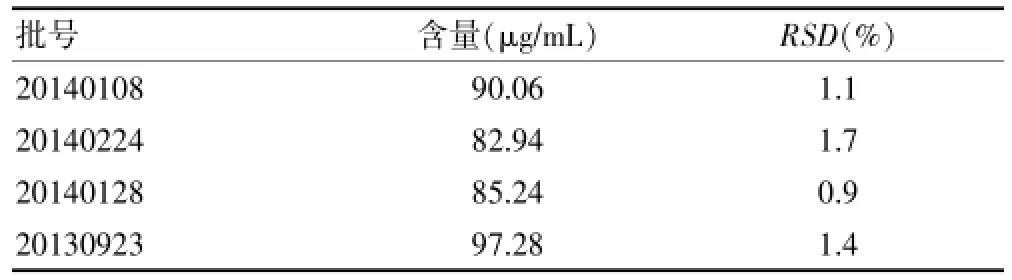
表2 连翘苷含量测定结果(n=2)
3 讨论
该制剂处方中,板蓝根[2]191苦寒清泄,擅清热解毒,更擅凉血利咽,直折里热,连翘[2]159-160性苦微寒,善清降之中兼能升浮宣散,能表里气血俱清,二者共为君药,同行清热解毒,凉血消肿之功;山豆根[2]25-26性苦寒,功专清泄,广藿香[2]42-43辛散温运,芳香化浊,两者一泄一发,相须为用,更助君药之力,共为臣药。根据《国家药品标准(中药)研究制定技术要求》[3],应对上述4味药进行定性定量分析。原质量标准中仅有针对山豆根和连翘的薄层色谱鉴别,无含量测定,本试验在其基础上,拟增加针对板蓝根和广藿香的定性分析,增加针对连翘的定量分析。
3.1 板蓝根的定性鉴别
现代研究表明,板蓝根化学成分丰富[4],抗病毒作用明显[5-8],临床应用广泛[9]。其中,亮氨酸、精氨酸等氨基酸类成分为板蓝根的重要药理活性成分,含量可达8%[10]。本试验通过TLC法对板蓝根进行鉴别[11],方法参照《中国药典》2010年版一部板蓝根鉴别项下方法进行[2]191。原方法对照溶液选用板蓝根对照药材、精氨酸对照品,本试验在此基础上增加了亮氨酸对照品,斑点显色清晰,色谱分离效果良好,操作方便,专属性强,可以有效对之进行鉴别。
3.2 广藿香的定性鉴别
广藿香的药用成分主要是挥发油,广藿香油中含有较多的醇类、酮类、醛类等化合物,其中百秋李醇是其代表性活性成分[12-13]。本试验通过GC法检测制剂中的百秋李醇[14],从而对广藿香进行鉴别。试验中,首先通过挥发油测定法制备挥发油,然后通过GC法鉴别挥发油中的有效成分百秋李醇。GC法检测灵敏度高,专属性强,可以有效地对广藿香进行鉴别。
3.3 连翘苷的定量分析
连翘苷为连翘的主要有效成分之一[15],结合文献报道[16-17],本试验采用HPLC法测定制剂中连翘苷的含量。
制备供试品溶液时,通过乙酸乙酯萃取,可以有效除去制剂中的干扰成分,提高连翘苷的提取率。测定波长、流动相、提取溶剂均参照《中国药典》2010年版一部[2]159-160。选择色谱柱时,考察了Agilentzorbaxextend C18(4.6mm×150mm,5μm)、ShimadzuVP-ODS色谱(150mm×4.6mm,5μm)、InertsilODS3(250mm× 4.6mm,5μm)、KromasilKR100-5-C18(150mm×4.6mm,5μm)等4种色谱柱,结果表明4种色谱柱的峰形、理论板数、分离度均良好,无显著性差异,最终选择InertsilODS3(250mm×4.6mm,5μm)进行方法学考察和样品含量测定。
根据《中国药典》中药质量标准分析方法验证指导原则的要求[2]附录130-131,含量限(幅)度的制订,应根据投料饮片、中间体转移率的实际情况确定。本次测定了4批蓝翘解毒口服液中连翘苷的含量,其值分别为90.06、82.94、85.24、97.28μg/mL,平均值为88.88μg/mL,上述数据为蓝翘解毒口服液中连翘苷的含量限度的确定提供了参考。HPLC法测定结果准确,稳定性好,专属性强,可以有效测定制剂中连翘苷的含量。
综上所述,本试验对蓝翘解毒口服液的质量标准进行了提高,其中TLC法鉴别板蓝根操作方便、专属性强,GC法鉴别广藿香灵敏度高、专属性强,HPLC法测定连翘苷的含量结果准确、稳定性好,可以用于蓝翘解毒口服液的质量控制。因此,可将板蓝根的TLC鉴别、广藿香的GC鉴别、连翘苷的含量测定列入蓝翘解毒口服液的原质量标准中,从而对其进行提高。
[1]解放军总后勤部卫生部.中国人民解放军医疗机构制剂规范[S].北京:人民军医出版社,2002:40-41.
[2]国家药典委员会.中国药典[S].一部.北京:中国医药科技出版社,2010.
[3]国家药典委员会.国家药品标准工作手册[M].4版.北京:中国医药科技出版社,2013:3-17.
[4]孙巍.板蓝根的化学成分和药理作用综述[J].中国医药指南,2014,12(9):35-36.
[5]李莉,杨子峰.板蓝根抗流感病毒多靶点研究思路综述[J].新中医,2014,46(3):202-204.
[6]刘西京,林素静.板蓝根多肽对流感病毒感染小鼠抗病毒作用的研究[J].中国药房,2014,25(7):590-592.
[7]陈凯,窦月,陈智,等.板蓝根抗病毒与抗内毒素等清热解毒药效作用及化学基础研究进展[J].中国方剂学杂志,2011,17(18):275-278.
[8]Xie Z,ShiY,Wang Z,etal.Biotransformation ofglucosinolates epiprogoitrin and progoitrin to(R)-and(S)-Goitrin in Radix isatidis[J].J Agric Food Chem,2011,59(23):12467-12472.
[9]刘建顺.板蓝根中成药临床应用的研究进展[J].中国现代药物应用,2013,7(17):222.
[10]任国萍,田璐,李铮,等.板蓝根药材中氨基酸含量测定研究[J].中国新药杂志,2014,23(1):99-104.
[11]王斌,张腾霄,刘利军,等.国内板蓝根药材质量评价方法的研究现状[J].贵阳中医学院学报,2013,35(2):31-33.
[12]安茜,谢红,王玮,等.广藿香质量控制研究进展[J].武警后勤学院学报:医学版,2013,22(11):1046-1048.
[13]梅清华,陈燕,兰树敏,等.广藿香抑制肠推进药效指纹图谱构建与谱效关系研究[J].中国医药导报,2013,10(35):17-20.
[14]康志英,蔡春玲,连林生,等.抗病毒口服液中广藿香含量测定方法研究[J].中国医药导报,2011,8(2):55-57.
[15]陈玲,李晓,李倩,等.连翘属植物化学成分的研究进展[J].现代药物与临床,2013,28(3):184-188.
[16]张宏伟,龚韬,严文利,等.高效液相色谱法测定不同厂家银翘解毒片中连翘酯A的含量[J].中国医药导报,2013,10(6):102-104.
[17]李延雪,孙菲,邵礼梅.HPLC法测定复方芩兰口服液中连翘苷的含量[J].中国医药导报,2012,9(26):117-118.
Study on the quality standard improve of Lanqiao Jiedu Oral Liquid
GONG Wei LI Xingdong SUN Xu ZHAO Qinghua ZHA NG Xinxin ZHANG Kun ZHA O Mei
Institute for Drug and Instrument Control,Joint Logistics Department of Ji'nan Military Command,Shandong Province, Ji'nan 250022,China
ObjectiveTo improve the quality standard of Lanqiao Jiedu Oral Liquid.MethodsIsatidis radix in the prescription was identified by TLC,while Pogostemonis herba in the prescription was identified by GC.The content of Phillyrin,which derived from Forsythiae fructus,was determined by HPLC.ResultsThe spots in the chromatogram obtained with test solution correspond in position and colour to the spots obtained with the reference drug solution and the reference solution in the TLC test.The retention time of the peaks obtained with the test solution and the reference solution was concordant with each other in the GC test.Phillyrin showed a good linear relationship at 9.387-300.4μg/mL (r=0.9999,n=6)with average recovery of 99.62%(RSD=1.21%,n=9).ConclusionTLC has obvious characteristics with the spots clear and well-separated for Isatidis radix identification.GC has highly sensitive and good specificity for Pogostemonis herba identification.The HPLC method is easy and simple to operate,accurate and stable in results with good specificity.Above all,the improved quality standard is applicable for the quality control of Lanqiao Jiedu O-ral Liquid.
Lanqiao Jiedu Oral Liquid;TLC;GC;HPLC;Isatidis radix;Pogostemonis herba;Phillyrin
R927.2
A
1673-7210渊2015冤01渊c冤-0095-05
2014-10-03本文编辑:卫轲)
军队医疗机构制剂标准提高科研专项课题(编号14ZJZ01-2)。
巩伟(1980-),男,博士;研究方向:药品质量分析。

