糖尿病患者肠道中4 种重要菌群的定量分析
臧文娟,李艳琴,*,李彬春,郭俊杰,赵玉立
糖尿病患者肠道中4 种重要菌群的定量分析
臧文娟1,李艳琴1,*,李彬春1,郭俊杰2,赵玉立2
(1.山西大学生物技术研究所,化学生物学与分子工程教育部重点实验室,山西 太原 030006;2.山西省中医药研究院,山西 太原 030012)
目的:了解正常人群与Ⅱ型糖尿病人,以及Ⅱ型糖尿病人在是否有家族遗传、是否用药治疗和是否伴随肥胖等情况下肠道中拟杆菌、双歧杆菌、柔嫩梭菌和乳杆菌的含量与变化,为预防和治疗Ⅱ型糖尿病开辟新途径。方法:收集上述各类人群粪便样品(每组10人),分别提取样品中微生物的总DNA,运用荧光定量聚合酶链式反应(polymerase chain reaction,PCR)扩增4种重要菌群的特异性片段,计算含量,分析上述菌群的变化差异。结果:正常人群肠道中的拟杆菌和双歧杆菌含量均显著低于Ⅱ型糖尿病人群;柔嫩梭菌和乳杆菌含量均显著高于后者。在Ⅱ型糖尿病人群中,用药患者组和肥胖+高血糖患者组的肠道中拟杆菌和双歧杆菌含量均显著低于未用药患者组和单纯高血糖患者组,而柔嫩梭菌和乳杆菌含量均显著高于后者。有无Ⅱ型糖尿病遗传史对患者肠道内4种菌群的含量均无显著影响。结论:4种重要菌群与Ⅱ型糖尿病的发生和发展有密切关系;用药治疗后的患者肠道中4种重要菌群含量比其他各组更接近正常人群;肥胖易加重Ⅱ型糖尿病病情;而有无Ⅱ型糖尿病家族遗传对这4种菌群的含量几乎没有影响。
糖尿病患者;肠道菌群;定量分析;拟杆菌;双歧杆菌;柔嫩梭菌;乳杆菌
随着社会发展和人们生活方式的改变,糖尿病、肥胖等代谢性疾病迅速发展,据2011年中华糖尿病协会最新调查,中国糖尿病患者高达1亿例,糖尿病及其慢性并发症严重影响了人们的生活质量,给社会及家庭带来沉重的负担,已成为全球突出的社会问题。人体肠道内栖息着大约30个属550多种细菌,其中仅双歧杆菌和拟杆菌就占细菌总数90%以上[1]。肠道菌群约占正常成人粪便质量的60%[2]。众多的共生菌在肠道黏膜形成菌膜,对人体的营养代谢、合成机体必需的微量元素和维生素、免疫防御等方面起着不可替代的作用[3]。肠道菌群在体内发挥着重要作用,完全可称得上是人体后天获得的重要器官——微生物器官。Ⅱ型糖尿病的典型特征是糖代谢紊乱,而近些年肠道菌群对人体代谢的影响备受关注,有研究表明双歧杆菌和乳杆菌等益生菌与宿主间在炎症反应、调节能量平衡方面有着密切关系[4],因此人们推测乳杆菌和双歧杆菌是控制体质量及能量代谢的一个重要因素,且与Ⅱ型糖尿病、肥胖等代谢性疾病的发生发展密切相关[5]。有研究也进一步证明了Ⅱ型糖尿病人肠道中乳杆菌种类和数量低于正常人群[6]。拟杆菌,尤其是多形拟杆菌(Bacteroides thetaiotaomicron)能合成多种糖基水解酶,降解抗性淀粉[7],还能调控肠上皮细胞的炎症反应[8]。梭菌亚群的组成中有一类为丁酸盐产生菌,丁酸盐被认为具有保护肠道抵御结肠癌的作用[9]。由于肠道微生物种类多、数量大、群落结构复杂,通常肠道菌群的定量分析多集中于4类与人体健康相关的特定菌群:拟杆菌属(Bacteroides)、梭菌亚群(Clostridia leptumsubgroup)、双歧杆菌属(Bifidobacteria)和乳杆菌(Lactobacillus)[10-12]。本研究试图通过实时荧光定量聚合酶链式反应(polymerase chain reaction,PCR)[13]对健康个体和Ⅱ型糖尿病患者,以及Ⅱ型糖尿病人在是否有家族遗传、是否用药治疗和是否伴随肥胖等情况下粪便中的拟杆菌、双歧杆菌、柔嫩梭菌及乳杆菌进行定量分析,比较各种Ⅱ型糖尿病患者与健康个体肠道中这4种菌群的差异,希望为以肠道菌群为靶点研究开发新的Ⅱ型糖尿病防治方法提供依据。
1 材料与方法
1.1材料
Ⅱ型糖尿病病例纳入标准:符合世界卫生组织专家咨询报告(WHO/NCD/NCS/99.2)糖尿病诊断标准[14];无肿瘤及肝、肾等脏器严重损害;无甲状腺等其他内分泌疾病;近4周内无腹泻病或其他胃肠道疾病史;排除标本留取量不足或标本留取过程中有污染者。60例Ⅱ型糖尿病患者粪便标本取自2012年10月—2013年1月山西省中医药研究院内分泌科患者,年龄(59±11)岁,彼此无血缘关系,经检测空腹血糖含量指标为(7.82±0.20)mmol/L;依据山西省中医院检验报告单及入院时情况登记表将糖尿病患者分为6组:用药患者组和未用药患者组、有遗传史患者组(父母一方或双方有糖尿病)和无遗传史患者组、肥胖+高血糖患者组(身体质量指数(body mass index,BMI)>25 kg/m2)和单纯高血糖患者组(BMI<25 kg/m2),每组10人,男女各半。每组的病程、年龄、性别、血压等基线资料比较差异均无统计学意义(P>0.05)。健康志愿者纳入标准:无其他脏器严重损害、无甲状腺功能异常等其他内分泌系统疾病,身体健康;无糖尿病;采样前1个月内未服用过抗生素、微生态活菌制剂等;近4周内无腹泻病或其他胃肠道疾病史;无消化道慢性病史,常规体检及粪便常规检查均未见异常。同样自2012年10月—2013年1月采集10例健康志愿者粪便标本,年龄(55±12)岁,经检测空腹血糖含量为(4.97±0.10)mmol/L。
1.2试剂与仪器
2×EasyTaqTMPCR SuperMix、2×TransStart Top Green qPCR SuperMix北京TransGen Biotech公司;Loading Buffer、DNA Marker日本TaKaRa公司;SanPrep柱式DNA胶回收试剂盒、SanPrep柱式质粒DNA小量抽提试剂盒生工生物工程(上海)股份有限公司。PCR引物由北京博迈德生物公司合成,聚丙烯酰胺凝胶电泳(polyacrylamide gelelectrophoresis,PAGE)纯化。
ABI Step One PlusTMReal-Time PCR仪美国ABI公司;凝胶成像系统英国UVItec公司;NanoDrop2000微量紫外分光光度计美国Thermo Fisher Scientific公司;漩涡振荡器、电子天平上海精科公司;移液器德国Eppendorf公司;高速冷冻离心机长沙湘仪公司;PTC-200型PCR仪美国Bio-Rad公司;台式微量离心机江苏其林贝尔仪器制造有限公司;低温冰箱日本Sanyo公司。
1.3方法
1.3.1样品的采集
新鲜粪便样品均于研究对象排便后立即放入无菌EP管内,0.5 h内置于冰箱-20 ℃保存,3 d内完成样品内细菌DNA的提取。
1.3.2各项生理生化指标的测定
对所有研究对象均测定晨起空腹时的体质量、身高和各项血液指标。BMI为体质量/身高2,单位为kg/m2。对研究对象静脉取血样,空腹血糖(glucose,GLU,隔夜空腹所测定的血糖值)、糖化血红蛋白(hemoglobin A1c,HbA1c)、总胆固醇(total cholesterol,TC)、甘油三酯(triglyceride,TG)、高密度脂蛋白(high density lipoprotein,HDL)、低密度脂蛋白(lowdensity lipoprotein,LDL)含量等均采用相对应的试剂盒进行测定。
1.3.3肠道菌群总DNA的提取
将粪便样品在冰上解冻,每例样品称取500 mg,运用苯酚-氯仿抽提法提取人体肠道内菌群基因组总DNA[15],置于-20 ℃冰箱保存。
1.3.4标准质粒和标准曲线的制作
取正常人群肠道菌群基因组总DNA,分别用4种重要菌群特异性引物进行PCR扩增。25 ☒L PCR反应体系:12.5μmol/L上下游引物各0.5 ☒L、DNA模板20 ng、2×EasyTaqTMPCR SuperMix 12.5 ☒L、ddH2O 10.5 ☒L。PCR特异引物见表1,反应程序见表2。将以上4种菌群的PCR产物纯化回收后分别作为目的DNA片段连接至pMDl8-T载体上,重组质粒转化至大肠杆菌XL10宿主细胞中,经蓝白斑筛选,得到阳性克隆后,提取质粒DNA,酶切并经PCR验证。提取鉴定正确的质粒,用微量紫外分光光度计测定其含量,ddH2O系列稀释,作为标准品模板进行荧光定量PCR,绘制标准曲线。

表1 特异菌群的PCR引物序列Table 1 PCR primers of each specific group

表2 特异菌群的PCR反应程序Table 2 PCR program of each specific group
由于肠道微生物菌群的复杂性,该领域的研究者通常利用克隆文库分析得到的各种菌群基因序列信息,针对特定菌群如拟杆菌属[16]、柔嫩梭菌亚群[17]、乳酸菌[18]以及双歧杆菌属[19]等,设计了16S rRNA基因V区的特异引物,这些引物的特异性也被后续的研究所证实[20-21]。目前,表1中所列引物就如16S rDNA通用引物一样,被广泛认可和应用[10,22-24]。
1.3.5实时荧光定量PCR
将待测粪便中提取的DNA样品分别进行4种菌群特异片段的实时荧光定量PCR,使用TransStart Top Green qPCR SuperMix试剂盒,在ABI Step One PlusTMReal-TimePCR仪上进行定量扩增,尽量在避光和低温的条件下进行加样操作。反应程序和特异引物同样参照表1、2。用微量紫外分光光度计测定样品的含量,将样品的DNA含量稀释至100 ng/☒L。实时荧光定量PCR 20 ☒L反应体系:12.5μmol/L上下游引物各0.8 ☒L、2×TransStart Top Green qPCR SuperMix 10 ☒L、质粒或样品DNA 1μL、50×Passive Reference Dye 0.4 ☒L,ddH2O 7 ☒L。将各成分按上述体系加入八联管中,每个样品均同时设定3个平行复孔,每次反应均设标准质粒为阳性对照和阴性对照(ddH2O代替DNA模板)。
由于各粪便样品的含水量不同,再加上提取DNA环节中难以避免DNA部分损失,因此,本实验采用某种菌群的lg(copies)/ng DNA来衡量其含量,而不是用lg(copies)/g粪便样品。
1.4统计学处理
应用SPSS Statistics 19.0统计软件t检验进行数据处理,分析各项指标,比较目标菌群在各组中的差异。
2 结果与分析
2.1正常人群和各类Ⅱ型糖尿病患者生理生化指标的比较分析

表3 各组人群血糖指标测定结果Table 3 Blood glucose indexes in subjects from each group
由表3可知,用药患者组的GLU和HbA1c含量虽高于正常人群组,但已控制在正常人群参考范围内;另外5组患者的血糖指标均显著高于正常人群参考范围;尤其以未用药患者组和肥胖+高血糖患者组的血糖指标最高,除有无遗传史患者组外,其他情况互为相反的组间两两相比均有显著差异。
由表4可知,各组人群的BMI和血脂指标测定结果与血糖指标测定结果基本一致,即用药患者组的BMI和血脂指标虽区别于正常人群组,但已控制在正常人群参考范围内;另外5组患者的指标均显著超出正常人群参考范围;未用药患者组和肥胖+高血糖患者组的血脂指标尤其不正常。由此可以看出,高血糖和高血脂,或糖尿病和肥胖有着密切的正相关性。

表4 各组人群体质量指数和血脂指标测定结果Table 4 BMI and blood lipid indexes of subjects from each group
2.2 各菌群引物的特异性验证及标准曲线
利用文献[16-19]中提供的4种特异菌群引物对本实验的样品材料进行PCR扩增,结果得到长度正确的单一片段。没有发现非特异性产物,证明4种菌群特异引物适合本实验。在此基础上,将特异片段进行克隆、转化。提取鉴定正确的质粒,测定其含量,以ddH2O系列稀释后作为标准品模板进行荧光定量PCR,以lg(copies)为横坐标、Ct值为纵坐标绘制标准曲线,获得4种菌群的线性回归方程,其中拟杆菌为y=-3.397 3x+54.764(R2=1.000);柔嫩梭菌为y=-3.897x+59.917(R2=0.990);乳酸菌为y=-4.046 5x+61.788(R2=0.997);双歧杆菌为y=-3.598x+56.672(R2=0.998)。
2.3 PCR熔解曲线

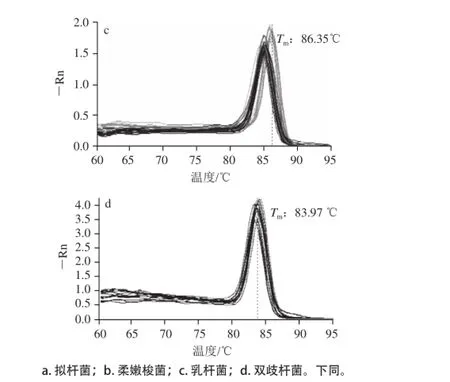
图1 4 种菌群的实时荧光定量PCR熔解曲线Fig.1 Real-time fluorescence quantitative PCR melting curve of four bacterial species
图1为4种菌群的标准品(正常人群)和其他样品的实时荧光定量PCR熔解曲线,通过分析标准品的熔解曲线,确定了拟杆菌、柔嫩梭菌、乳杆菌和双歧杆菌的Tm值分别在83.67、86.2、86.35、83.97℃左右。4种菌群分别在对应的Tm值处有单峰,说明扩增产物正确,且没有发现非特异产物,与荧光染料结合的为目的DNA片段。
2.4 PCR扩增曲线
扩增曲线是描述PCR动态进程的曲线,用于表示荧光强度与模板循环数的关系。由图2可知,本实验4种菌群的扩增曲线均呈光滑“S”形,分为基线期、对数期及平台期3个阶段,无异常扩增,说明4种菌群DNA扩增中采集的荧光信号数据准确。
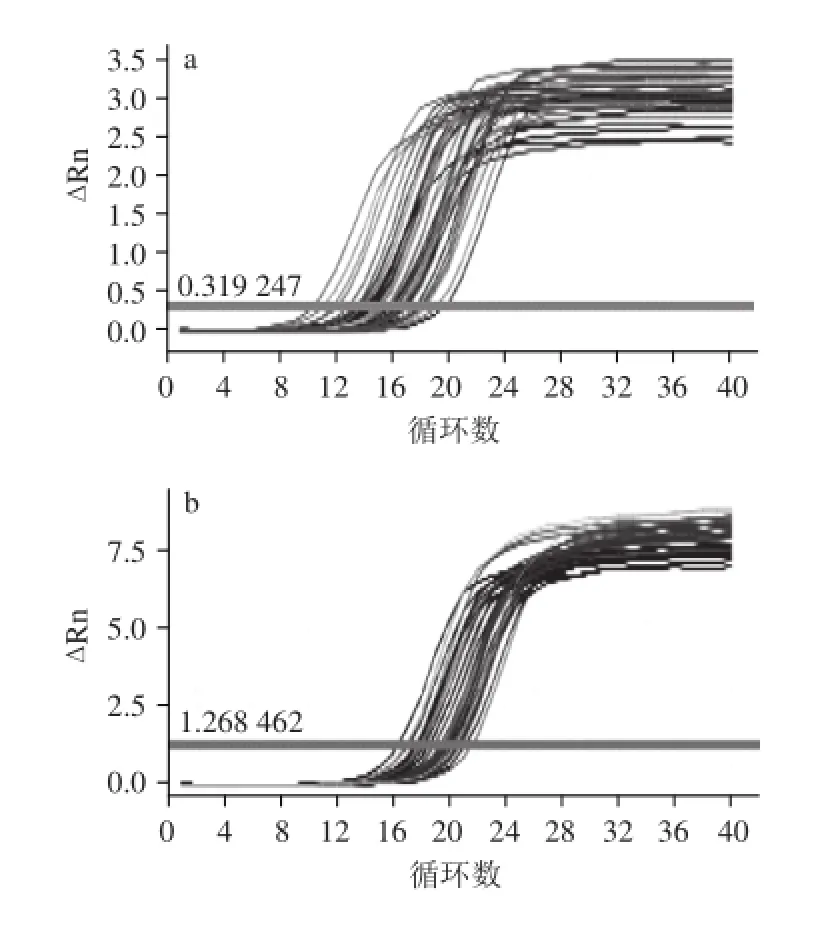

图2 特异菌群的实时荧光定量PCR扩增曲线Fig.2 Real-time fluorescence quantitative PCR amplification plots of specific bacteria
2.5特异菌群的定量检测结果


图3 各组菌群的定量比较结果Fig.3 Quantitative comparison of gut bacterial counts in subjects from each group
由图3可知,各两两比较的组别中4种菌群含量差异表现出高度一致性,即:糖尿病患者组与正常人群组、未用药患者组与用药患者组4种菌群含量的差异均达到极显著水平,肥胖+高血糖患者组与单纯高血糖患者组之间的差异达到显著水平,有遗传史患者组与无遗传史患者组之间无显著差异。各种菌群的相对含量比较结果为:正常人群组的拟杆菌和双歧杆菌含量均极显著低于糖尿病患者组;柔嫩梭菌和乳杆菌含量均极显著高于后者。在Ⅱ型糖尿病人群中,用药患者组和肥胖+高血糖患者组拟杆菌和双歧杆菌含量均显著低于未用药患者组和单纯高血糖患者组,而柔嫩梭菌和乳杆菌含量均显著高于后者。
3 讨 论
目前许多学者认为,肥胖和Ⅱ型糖尿病不能只归因于基因、户外活动减少或营养习惯问题,肠道菌群也影响了宿主营养机制,与肥胖和Ⅱ型糖尿病密不可分。Cani等[25]研究认为,长期肥胖能引起肠道紧密连接蛋白ZO-1和Occludin损坏,使内源性大麻素系统紊乱,进而改变肠道通透性;增加革兰氏阴性菌群比例可导致其细胞壁成分脂多糖的分泌增加。与此同时,菌群比例失调会抑制肠道紧密连接蛋白ZO-1的表达,肠道上皮通透性增加,使得脂多糖不断积累,由肠道进入血液循环,产生“代谢性内毒素血症”[26]。进一步研究发现,脂多糖能诱导全身性慢性炎症的产生和发展[27]。不断积累的氧化应激和慢性炎症可能引起胰岛β细胞的凋亡,最终引起Ⅱ型糖尿病[28]。有研究发现,Ⅱ型糖尿病患者肠道中厚壁菌门数量下降[29]。近些年也有文献报道Ⅱ型糖尿病患者肠道中拟杆菌数量增加[30]。Larsen等[31]研究结果也表明,Ⅱ型糖尿病患者肠道中厚壁菌门菌群的数量显著减少,革兰氏阴性菌群的数量增多。在本研究中,4种菌群中只有拟杆菌为革兰氏阴性菌,且该菌在Ⅱ型糖尿病患者肠道中的含量显著高于正常人群,而属于厚壁菌门的柔嫩梭菌和乳杆菌含量均显著低于后者,这一结果与上述研究[29-31]的结果不谋而合。
另外,在研究人体胖瘦与肠道菌群的关系时,有人发现瘦人消化道内的细菌主要属于拟杆菌,而胖人消化道内的厚壁菌更多;胖人改为进食低热量饮食后,拟杆菌门含量从3%增加到15%,而厚壁菌数量下降[32]。本研究中显示在Ⅱ型糖尿病患者中,肥胖+高血糖患者组拟杆菌含量显著低于单纯高血糖患者组,而柔嫩梭菌和乳杆菌含量均显著高于后者。而且从血糖、血脂指标的测定结果可以看出,肥胖、高血脂与糖尿病间有明显的正相关性。
本研究中,对比是否用降糖药这两组,药物治疗后各血糖、血脂指标均恢复正常,4种菌群的含量与未用药患者组相比也更接近正常人群。之前也有研究表明,降糖药物对肠道菌群具有调节作用[15],但药物对肠道菌群是直接作用还是通过调节宿主代谢的间接作用,还有待更深入的研究。
值得注意的是,Ⅱ型糖尿病患者肠道内双歧杆菌含量较正常人群明显增加,这与多项研究得出的结果[33-34]相矛盾,考虑可能原因为Ⅱ型糖尿病患者机体在高血糖状态下,自身肠道菌群发生应激性改变导致双歧杆菌数量明显增加,以逆转机体慢性炎症反应状态,改善代谢性内毒素血症等,从而造成这一相悖的研究结果。由于肠道微生态系统太过复杂以及研究方法繁多,各项关于肠道菌群的研究结果不尽相同。许多研究显示,补充益生菌后,肥胖、糖尿病患者的胰岛素抵抗、系统性炎症反应状态、代谢性内毒素血症等可得到显著改善[35]。
综上所述,4种肠道菌群在Ⅱ型糖尿病的发生发展中充当了重要角色,其数量的变化与Ⅱ型糖尿病密切相关。越来越多的证据表明,肠道菌群失调在Ⅱ型糖尿病发病机制中起着重要的作用。目前关于家族遗传是否会对Ⅱ型糖尿病患者肠道内菌群结构造成差异的研究尚属空白。本实验结果表明:有无家族遗传史对病人肠道内4种菌群的含量在统计学意义上无影响。肠道菌群的定量分析是了解Ⅱ型糖尿病患者肠道内菌群变化规律的基础,本实验通过初步探讨正常人群与各种糖尿病患者肠道中4种重要菌群含量的差异和变化,有助于从新的角度更全面准确地了解各种病情程度患者肠道菌群的差异,为进一步寻找肠道菌群与Ⅱ型糖尿病之间的关系提供了重要线索,并为理解Ⅱ型糖尿病的发病机制及寻求新的治疗微生态靶点提供了一些资料。
[1]BIAGI E, NYLUND L, CANDELA M, et al. Through ageing, and beyond: gut microbiota and inflammatory status in seniors and centenarians[J]. PLoS ONE, 2010, 5(5): e10667. doi: 10.1371/journal. pone.0010667.
[2]SGHIR A, GRAMET G, SUAU A, et al. Quantification of bacterial groups within human fecal flora by oligonucleotide probe hybridization[J]. Applied and Environmental Microbiology, 2000, 66(5): 2263-2266.
[3]TIIHONEN K, OUWEHAND A C, RAUTONEN N. Human intestinal microbiota and healthy ageing[J]. Ageing Research Reviews, 2010, 9(2): 107-116.
[4]CANI P D, DELZENNE N M. The role of the gut microbiota in energy metabolism and metabolic disease[J]. Current Pharmaceutical Design, 2009, 15(13): 1546-1558.
[5]CANI P D, DELZENNE N M. Gut microflora as a target for energy and metabolic homeostasis[J]. Current Opinion in Clinical Nutrition & Metabolic Care, 2007, 10(6): 729-734.
[6]VALLADARES R, SANKAR D, LI Nan, et al.Lactobacillus johnsoniiN6. 2 mitigates the development of type 1 diabetes in BB-DP rats[J]. PLoS ONE, 2010, 5(5): e10507. doi: 10.1371/journal.pone.0010507.
[7]HOOPER L V, MIDTVEDT T, GORDON J I. How host-microbial interactions shape the nutrient environment of the mammalian intestine[J]. Annual Review of Nutrition, 2002, 22(1): 283-307.
[8]KELLY D, CAMPBELL J I, KING T P, et al. Commensal anaerobic gut bacteria attenuate inflammation by regulating nuclear-cytoplasmic shuttling of PPAR-γand RelA[J]. Nature Immunology, 2004, 5(1): 104-112.
[9]DUNCAN S H, LOUIS P, FLINT H J. Lactate-utilizing bacteria, isolated from human feces, that produce butyrate as a major fermentation product[J]. Applied and Environmental Microbiology, 2004, 70(10): 5810-5817.
[10] 车传燕.人源菌群仔猪模型的建立及其胃肠道粘膜免疫的研究[D].南京:南京农业大学, 2009: 107-117.
[11] 江美玲. 2型糖尿病及其前期状态人群肠道菌群特征分析[D].广州:南方医科大学, 2013: 10-35.
[12] 蒋曼,姚萍,杨涛,等.实时荧光定量PCR法研究溃疡性结肠炎患者肠道双歧杆菌属、柔嫩梭菌属及拟杆菌属量的变化[J].中国微生态学杂志, 2013, 25(11): 1245-1249.
[13]de OLIVEIRA M A, RIBEIRO E G A, BERGAMINI A M M, et al. Quantification ofListeria monocytogenesin minimally processed leafy vegetables using a combined method based on enrichment and 16S rRNA real-time PCR[J]. Food Microbiology, 2010, 27(1): 19-23.
[14]World Health Organization. WHO/NCD/NCS/99.2 Definition, diagnosis and classification of diabetes mellitus and its complications[R]. Geneva: WHO, 1999.
[15] 韩亮.药物干预对先天高血糖小鼠肠道菌群的影响[D].太原:山西大学, 2013: 8-31.
[16]PANG Xiaoyan, DING Dezhong, WEI Guifang, et al. Molecular profiling ofBacteroidesspp. in human feces by PCR-temperature gradient gel electrophoresis[J]. Journal of Microbiological Methods, 2005, 61(3): 413-417.
[17]MATSUKI T, WATANABE K, FUJIMOTO J, et al. Use of 16S rRNA gene-targeted group-specific primers for real-time PCR analysis of predominant bacteria in human feces[J]. Applied and Environmental Microbiology, 2004, 70(12): 7220-7228.
[18]WALTER J, HERTEL C, TANNOCK G W, et al. Detection ofLactobacillus,Pediococcus,Leuconostoc, andWeissellaspecies in human feces by using group-specific PCR primers and denaturing gradient gel electrophoresis[J]. Applied and Environmental Microbiology, 2001, 67(6): 2578-2585.
[19]SATOKARI R M, VAUGHAN E E, AKKERMANS A D L, et al. Bifidobacterial diversity in human feces detected by genus-specific PCR and denaturing gradient gel electrophoresis[J]. Applied and Environmental Microbiology, 2001, 67(2): 504-513.
[20] 申剑.寡果糖对人源菌群仔猪肠道菌群结构和宿主代谢的影响[D].上海:上海交通大学, 2008: 87-102.
[21] 李旻.人体肠道菌群结构与宿主代谢的相关性研究[D].上海:上海交通大学, 2009: 58-96.
[22] 张美玲.两种肠道疾病中肠道菌群结构变化的分子生态学研究[D].上海:上海交通大学, 2007: 96-130.
[23] 魏华.不同外源扰动因素对肠道菌群组成结构影响的研究[D].上海:上海交通大学, 2008: 65-107.
[24] 徐灵筠. 1型糖尿病鼠类模型的肠道菌群分析[D].上海:上海交通大学, 2007: 31-58.
[25]CANI P D, OSTO M, GEURTS L, et al. Involvement of gut microbiota in the development of low-grade inflammation and type 2 diabetes associated with obesity[J]. Gut Microbes, 2012, 3(4): 279-288.
[26]de la SERRE C B, ELLIS C L, LEE J, et al. Propensity to highfat diet-induced obesity in rats is associated with changes in the gut microbiota and gut inflammation[J]. American Journal of Physiology-Gastrointestinal and Liver Physiology, 2010, 299(2): G440-G448.
[27]MEHTA N N, MCGILLICUDDY F C, ANDERSON P D, et al. Experimental endotoxemia induces adipose inflammation and insulin resistance in humans[J]. Diabetes, 2010, 59(1): 172-181.
[28]DONATH M Y, B☒NI-SCHNETZLER M, ELLINGSGAARD H, et al. Islet inflammation impairs the pancreaticβ-cell in type 2 diabetes[J]. Physiology, 2009, 24(6): 325-331.
[29]FURET J P, KONG L C, TAP J, et al. Differential adaptation of human gut microbiota to bariatric surgery-induced weight loss links with metabolic and low-grade inflammation markers[J]. Diabetes, 2010, 59(12): 3049-3057.
[30] 刘晶,王烨,李琳琳,等.新疆维吾尔族、哈萨克族2型糖尿患者群肠道菌群中直肠真杆菌与多形拟杆菌的定量研究[J].中国微生态学杂志, 2011, 23(2): 107-111.
[31]LARSEN N, VOGENSEN F K, van den BERG F W J, et al. Gut microbiota in human adults with type 2 diabetes differs from nondiabetic adults[J]. PLoS ONE, 2010, 5(2): e9085. doi: 10.1371/journal. pone.0009085.
[32]MANCO M, PUTIGNANI L, BOTTAZZO G F. Gut microbiota, lipopolysaccharides, and innate immunity in the pathogenesis of obesity and cardiovascular risk[J]. Endocrine Reviews, 2010, 31(6): 817-844.
[33] 黄旭东,郑晓鹏,郑赵利. 2型糖尿病患者肠道菌群的研究[J].河北医学, 2011, 17(8): 1041-1043.
[34]WU Xiaokang, MA Chaofeng, HAN Lei, et al. Molecular characterisation of the faecal microbiota in patients with type II diabetes[J]. Current Microbiology, 2010, 61(1): 69-78.
[35]PHILIPPE D, FAVRE L, FOATA F, et al.Bifidobacterium lactisattenuates onset of inflammation in a murine model of colitis[J]. World Journal of Gastroenterology, 2011, 17(4): 459-469.
Quantitative Analysis of Important Gut Flora in Diabetic Patients
ZANG Wenjuan1, LI Yanqin1,*, LI Binchun1, GUO Junjie2, ZHAO Yuli2
(1. Key Laboratory of Chemical Biology and Molecular Engineering, Ministry of Education, Institute of Biotechnology, Shanxi University, Taiyuan 030006, China; 2. Shanxi Province Institute of Traditional Chinese Medicine, Taiyuan 030012, China)
Objective: To understand the relative contents and changes ofBacteroides,Bifi dobacterium,Clostridium leptumandLactobacillusin the intestinal flora of healthy people and diabetic patients with and without genetic inheritance, drug treatment or obesity for future prevention and treatment of diabetes. Methods: Fecal samples were collected from the above populations (n= 10). The total DNAs of microorganisms were extracted from the samples, and specific gene fragments from the four intestinal bacteria were amplified by fluorescence quantitative PCR. Differences and changes in these four bacterial species were studied. Results: The relative contents ofBacteroidesandBifi dobacteriumin healthy population were lower than those in diabetic population, while the relative contents ofClostridium leptumandLactobacillusin healthy population were higher than those in diabetic population. Among the diabetic population, the contents ofBacteroidesandBifidobacteriumafter drug treatment were lower than those before drug treatment, while the relative contents ofClostridium leptumandLactobacilluswere higher in patients without drug treatment. The contents ofBacteroidesandBifidobacteriumin obese patients with high blood glucose were lower than those of the patients with high blood glucose alone, while the relative contents ofClostridium leptumandLactobacilluswere higher in the formers. Genetic inheritance had no statistical significance. Conclusion: These four gut bacteria are closely related to the origination and development of diabetes. Their contents in diabetic patients with drug treatment are close to those in healthy population. Obesity aggravates the development of diabetes. Genetic inheritance has no effect on gut flora.
diabetes; gut flora; quantitative analysis;Bacteroides;Bifi dobacterium;Clostridium leptum;Lactobacillus
R587.1
1002-6630(2015)11-0208-07
10.7506/spkx1002-6630-201511040
2014-08-15
山西省科技攻关项目(20120311006-1)
臧文娟(1987—),女,硕士研究生,研究方向为微生物分子生态。E-mail:15581835511@163.com
*通信作者:李艳琴(1960—),女,教授,学士,研究方向为微生物生态。E-mail:yanqin@sxu.edu.cn

