三乙烯四胺修饰β-环糊精交联树脂分离富集/原子吸收法测定大米中的铅、镉
肖 艳,周方钦,彭 佳,廖运霞
(湘潭大学 化学学院 环境友好化学与应用省部共建教育部重点实验室,湖南 湘潭 411105)
铅和镉是两种常见的有毒重金属,可通过生物链在人体内富集,引起慢性中毒,造成对肾脏、肝、肺等的损害,甚至致癌[1]。而环境样品中铅和镉的含量较低,常用的原子吸收光谱法难以直接测定,因此研究高效率的分离富集方法对痕量铅、镉的分析具有重要意义[2]。目前,分离富集铅、镉的常用方法有固相萃取[3-4]、浊点萃取[5]、共沉淀[6]、离子交换法[7]等。其中固相萃取因操作简单、成本低、吸附剂可重复使用等优点而被广泛运用。
β-环糊精(β-CD)因其特有的分子特性与功能,在分离富集中得到广泛关注[8]。但由于疏水区域及催化活性有限,使其应用受到一定限制[9]。为克服β-环糊精的缺点,通常采用化学修饰来提高其性能[10-11],如固载化 β-环糊精[12]、全烷基化 β-环糊精[13]、HP-β-CD[14]、Fe3O4@SiO2- PGMA - β-CD等[15-16]。本文以三乙烯四胺修饰,合成不溶于水的三乙烯四胺-β-环糊精交联树脂(TETA-β-CDP),研究了该分离材料对痕量铅、镉的吸附性能,建立了一种分离富集/原子吸收光谱(FAAS)同时测定大米中铅、镉的新方法。
1 实验部分
1.1 仪器与试剂
AA-6000型原子吸收分光光度计(上海天美科学仪器有限公司);铅、镉空心阴极灯(北京有色金属研究总院),仪器工作条件如表1所示;FT-IR1710型傅立叶变换红外光谱仪(美国PE公司);SHZ(Ⅲ).D循环水式真空泵(巩义市予华仪器有限责任公司);PHS-3D型pH计(上海精密科学仪器有限公司);DZ-IBC型真空干燥箱(天津市泰斯特仪器有限公司);DF-101S集热式恒温加热磁力搅拌器(郑州长城仪器厂)。
Cd2+标准储备液(1 g/L):金属镉采用盐酸(1∶1)溶解配制;Pb2+标准储备液(1 g/L):高纯金属铅采用硝酸(1∶1)溶解配制。醋酸-醋酸钠缓冲溶液(pH 5.5):将0.1 mol/L醋酸钠和0.1 mol/L醋酸溶液按17∶3体积比混合配制而成;β-环糊精(天津市光复精细化工研究所);环氧氯丙烷(EPI,湖南汇红试剂有限公司);对甲苯磺酰氯(TSCL,阿拉丁试剂有限公司);三乙烯四胺(TETA,西陇化工公司);三乙烯四胺为化学纯,其余试剂均为分析纯,实验用水为二次石英蒸馏水。

表1 仪器工作条件Table 1 Working conditions of the instrument
1.2 实验方法
1.2.1 三乙烯四胺修饰β-环糊精交联树脂(TETA-β-CDP)的制备 β-环糊精交联聚合物(β-CDP)的制备:将5 g可溶性淀粉与20 g β-环糊精置于250 mL烧杯中,加入50 mL 20%的NaOH溶液,在50℃水浴上加热溶解,充分搅拌下逐滴加入30 mL环氧氯丙烷,约1 h后成为凝胶状硬块,取出后碾碎,用大量水与丙酮洗涤至中性,过滤抽干,于75℃下真空干燥,得到β-环糊精交联树脂。
TETA-β-CDP的制备:先取10.0 g β-CDP树脂加入50 mL干燥吡啶使其溶胀0.5 h,再加入1.75 g对甲苯磺酰氯,室温搅拌22 h后,用无水乙醇洗涤数次,50℃真空干燥12 h,得淡黄色粉末状的对甲苯磺酰化树脂(TS-β-CDP)。取10.0 g TS-β-CDP于100 mL圆底烧瓶中,加入50 mL苯,回流除去45 mL馏分,加入40 mL三乙烯四胺进行修饰,回流24 h,冷却后过滤,分别用水及氢氧化钠溶液洗涤后,再用水洗涤至中性,抽滤,于50℃下真空干燥10 h,得淡黄色颗粒TETA-β-CDP。
1.2.2 富集与测定 以25 mL的酸式滴定管为自制分离柱,将适量的TETA-β-CDP吸附材料湿法上柱装入一端填有少量脱脂棉的分离柱中,上端塞入少许脱脂棉,装柱高度约60 mm。预富集前,分别用5 mL 0.1 mol/L HNO3和40 mL水清洗该柱,然后用5 mL醋酸-醋酸钠缓冲溶液(pH 5.5)平衡分离柱。将铅镉混合溶液的标准溶液或分析试液(pH 5.5)缓慢倒入分离柱中,调节溶液流出速度为1.0 mL/min。待溶液流尽后,用水洗涤分离柱两次,再用6 mL 0.1 mol/L HCl以0.8 mL/min的流速进行洗脱,采用FAAS测定洗脱液中的Cd2+与Pb2+。
2 结果与讨论
2.1 红外光谱表征
分别测定 β-环糊精(β-CD)、β-环糊精交联树脂(β-CDP)及三乙烯四胺修饰后的β-环糊精交联树脂(TETA-β-CDP)的红外光谱,结果见图1。从图1可以看出,3 432 cm-1处的宽峰为羟基和三乙烯四胺中N—H伸缩振动的重叠吸收峰,2 923 cm-1处为—CH2的反对称变形振动吸收峰,1 569 cm-1处为 N—H的弯曲振动吸收峰,而1 022 cm-1处为β-环糊精的C—O—C键的伸缩振动吸收峰;754 cm-1处为C—N的弯曲振动吸收峰,说明三乙烯四胺已被成功地修饰到β-环糊精交联树脂上。
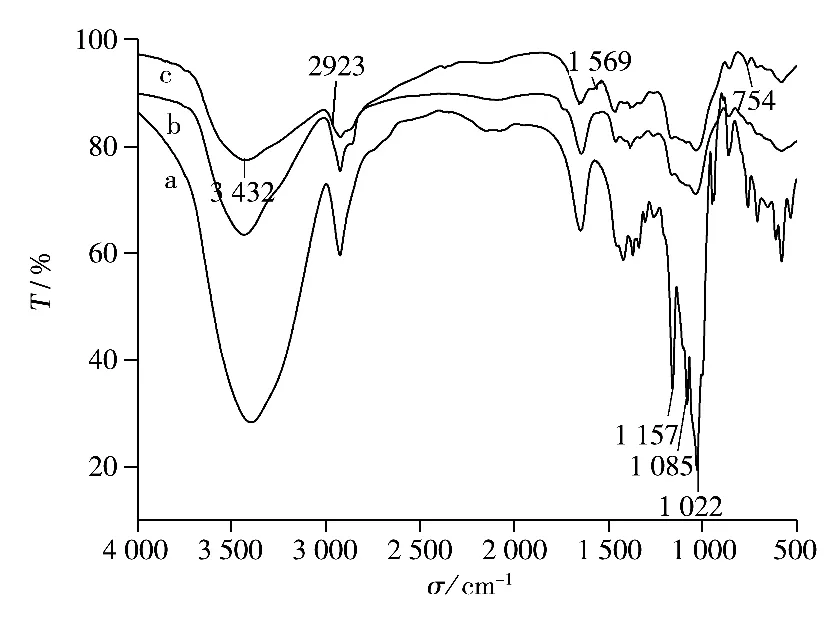
图1 β-CD(a)、β-CDP(b)和TETA-β-CDP(c)的红外光谱Fig.1 FT - IR spectra of β-CD(a),β-CDP(b)and TETA-β-CDP(c)
2.2 TETA-β-CDP吸附率及影响因素的考察

图2 pH值对吸附率的影响Fig.2 Effect of pH value on adsorption rate
2.2.1 溶液pH值的影响 取10 mL浓度分别为0.5,5.0 mg/L的镉和铅混合溶液于25 mL具塞比色管中,用氢氧化钠和盐酸调至不同pH值,按实验方法测定,考察pH值对铅和镉吸附率的影响(如图2)。结果表明,pH 5.5时铅和镉的吸附率达最大值,因此,实验选择上柱液的pH值为5.5。
2.2.2 流速的影响 取10 mL浓度分别为0.5,5.0 mg/L的镉和铅混合溶液,考察不同流速(0.2,0.5,0.8,1.0,1.2,1.5,1.8,2.0,2.5 mL/min)对吸附率的影响,实验结果见图3。当上柱液流速较慢时吸附效果较好,流速高于1.5 mL/min时,吸附率明显下降。在确保吸附率不受影响的前提下,尽量提高样品的分析速度,故实验选择1.0 mL/min作为上柱液流速。
2.2.3 动态饱和吸附容量的测定 控制流速为1.0 mL/min,使铅、镉离子标准混合溶液(pH 5.5,ρ=20 mg/L)连续流过分离柱,每隔5 min测定1次流出液中Pb2+和Cd2+的浓度,当流出液浓度不变时即表明吸附达到饱和。用适量水冲洗分离柱2~3次,再用洗脱剂洗脱被吸附的铅和镉,用FAAS测定洗脱液中铅、镉含量。根据TETA-β-CDP吸附材料的用量,计算出该材料对铅和镉的动态饱和吸附容量分别为22.8,31.3 mg/g。
2.2.4 洗脱剂、洗脱体积及洗脱流速的影响 比较了EDTA,HNO3,HCl,HCl-thiourea,H2SO4,CH3COOH,Na2S2O37种洗脱剂对铅和镉离子的洗脱效果(图4),发现选用0.1 mol/L HCl进行洗脱时的效果最好。为进一步考察洗脱剂用量的影响,同样流速下分别用2,4,6,8,10 mL的0.1 mol/L HCl进行洗脱实验。结果发现6 mL 0.1 mol/L HCl可将吸附的铅和镉完全洗脱。在确定洗脱剂为0.1 mol/L HCl,洗脱剂体积为6 mL的条件下,研究了不同洗脱流速对铅、镉洗脱率的影响。结果发现,当洗脱流速低于1.0 mL/min时,被吸附的铅和镉可完全洗脱,但随着流速的进一步增加洗脱率明显下降,为了保证洗脱完全,实验选择洗脱剂的流速为0.8 mL/min。
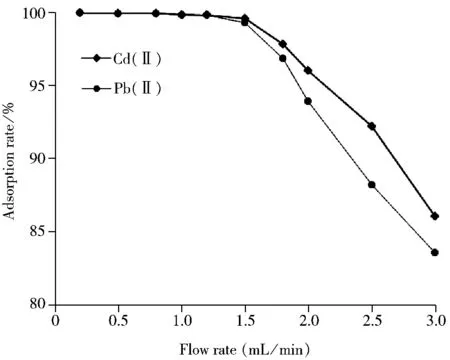
图3 流速对吸附率的影响Fig.3 Effect of flow rate on adsorption rate
2.2.5 分离柱的重复使用实验 将吸附了铅和镉的分离柱用6 mL 0.1 mol/L HCl溶液以0.8 mL/min的流速洗脱,用水清洗至中性后可重复使用。实验表明,重复使用10次后,铅和镉的回收率仍可达到95%。
2.2.6 共存离子的影响 在优化实验条件下,向2 mg/L Pb2+和0.5 mg/L Cd2+混合溶液中加入不同的干扰离子进行测定,考察常见共存离子对测定结果的影响,实验结果见表2。结果表明,按测量误差不超过±5%计,常见共存离子对Pb2+和Cd2+的测定不产生干扰。
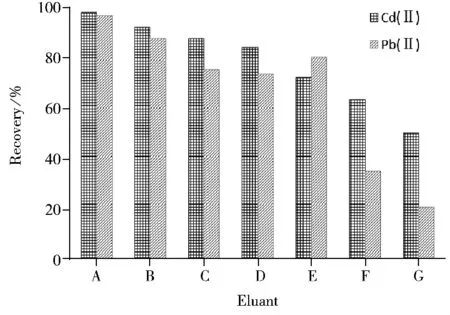
图4 洗脱剂对吸附率的影响Fig.4 Effect of eluants on adsorption rate
2.3 分析特性研究
在最佳实验条件下,分别对不同浓度的Pb2+和Cd2+溶液进行测定,考察其分析特性,结果如表3所示。实验结果表明,在一定的浓度范围内,铅和镉的质量浓度(ρ,mg·L-1)与其对应的吸光度(A)均呈线性关系。对0.5 mg/L Cd2+,5 mg/L Pb2+按实验方法经吸附洗脱后测定,按公式DL=3σ·c/A(其中DL为检出限,σ为11次空白值的标准偏差,c为吸光度大于3σ时对应的待测离子浓度,A为吸光度)计算得到该方法对铅和镉的检出限分别为0.038 mg/L和0.016 mg/L,相对标准偏差(RSD)分别为2.8%和1.7%。

表2 共存离子的影响Table 2 Effect of coexisting ions

表3 分析特性Table 3 Analysis features
2.4 样品分析
准确称取超市购买的大米样品10.0 g,置于25 mL瓷坩埚中,并在其表面覆盖一层薄薄的NaHCO3,先在电炉上炭化完全,再移入马弗炉中于600℃下灼烧8 h,冷却至室温(若个别样品灰化不彻底,则加少量浓硝酸和高氯酸的混合液在电炉上消化完全),加入10 mL 0.5 mol/L HNO3将灰分溶解,并转移至100 mL容量瓶中,用0.5 mol/L的NaOH或HCl调至pH 5.0~6.0后,加入pH 5.5醋酸-醋酸钠缓冲溶液5 mL,以水定容至刻度,摇匀备用。按照实验方法测定大米中铅、镉的含量,同时做加标回收实验,结果见表4。实际大米样品中铅、镉的回收率分别为97.5%~101.0%和95.0%~102.5%,说明本法的准确性较好。我国食品安全国家标准《食品中污染物限量》(GB2762-2012)限定大米中铅和镉的量必须低于0.2 mg/kg,根据测定的结果可知,4种大米中糯米和猫牙米镉含量超标,其他样品中的铅和镉含量均在标准范围之内。
为进一步验证方法的准确性,按实验方法测定了大米成分分析标准物质(GBW10045)中镉和铅的含量分别为(0.190±0.003),(0.069±0.002)μg/g,RSD(n=5)分别为0.83%,0.92%。实验表明,该方法具有良好的准确性。
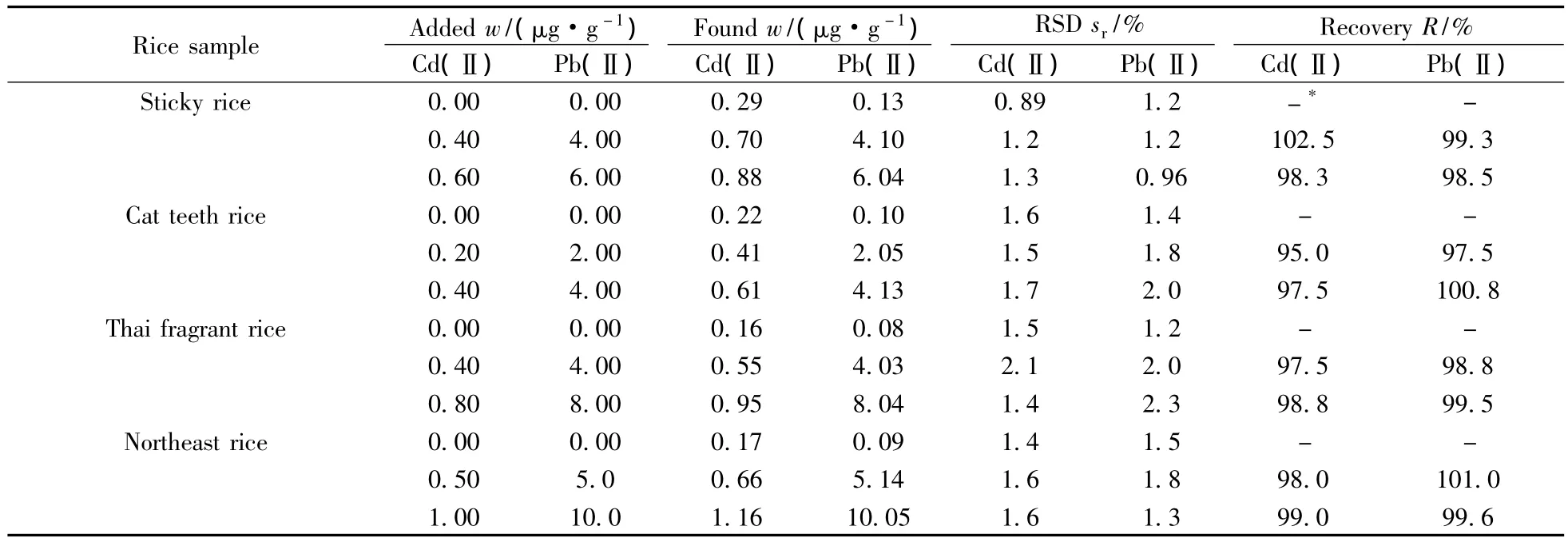
表4 大米中铅、镉的测定及加标回收实验(n=3)Table 4 Determination of Pb2+,Cd2+in rice samples and their spiked recoveries(n=3)
3 结论
本文研制了一种新型分离富集材料TETA-β-CDP,以此为固相萃取吸附剂,结合火焰原子吸收光谱测定,建立了一种同时分离富集与检测痕量Pb(Ⅱ)和Cd(Ⅱ)的新方法,并将其成功应用于大米中痕量铅、镉的测定。本法具有简单、快速、灵敏度高、重现性好等优点,有一定的理论意义和实用价值。
[1]Shen D F,Zhou F Q,Wang Z.J.Anal.Sci.(申东方,周方钦,王珍.分析科学学报),2015,31(1):28-33.
[2]Zhou Q L,Lei Y Q,Guo P R,Pan J C,Wang G H.J.Instrum.Anal.(周巧丽,雷永乾,郭鹏然,潘佳钏,王冠华.分析测试学报),2015,34(2):221-226.
[3]Dang Y F,Ma X G,Zou J P.J.Instrum.Anal.(党永锋,马晓国,邹建平.分析测试学报),2012,31(7):823-827.
[4]Su G J,Zhang G J,Wang Q L.Nat.Sci.J.Xiangtan Univ.(苏国钧,张高剑,王千里.湘潭大学学报:自然科学版),2014,36(2):59-62.
[5]Li S,Wang M,Yang B Y,Gu J P.J.Anal.Sci.(李姗,王梅,杨冰仪,古嘉平.分析科学学报),2015,31(2):188-192.
[6]Zhang Q Y,An G R,Zhao Y Q,Cao X W.Chin.J.Spectrosc.Lab.(张启云,安国荣,赵玉卿,曹晓武.光谱实验室),2012,29(3):1899-1901.
[7]Dai J,Qu J G,Zhang J.J.Instrum.Anal.(戴洁,瞿建国,张经.分析测试学报),2012,31(8):903-908.
[8]Zhang H L,Liu C J,Wang X Z,Zhang X F.Nat.Sci.J.Xiangtan Univ.(张海良,刘婵娟,王行柱,张雪飞.湘潭大学学报:自然科学版),2008,30(1):56-61.
[9]Pan T,Yi B,Chen Q T.Nat.Sci.J.Xiangtan Univ.(潘彤,易兵,谌其亭.湘潭大学学报:自然科学版),2009,31(4):37-40.
[10]Yuan R J,Wang X F,Zhan X Y,Liu Y H,Liu X Y,Cao Y L.Chin.J.Anal.Chem.(袁瑞娟,王雄飞,詹雪艳,刘宇宏,刘晓亚,曹艳玲.分析化学),2013,41(4):559-564.
[11]Shvets O,Belyakova L.J.Hazard.Mater.,2015,283:643-656.
[12]Shen H M,Ji H B,Wu H K,Shi H X.Chin.J.Chem.Org.(沈海民,纪红兵,武宏科,史鸿鑫.有机化学),2014,34:1549-1572.
[13]Zhu X B,Chen F L,Yin M M.J.Instrum.Anal.(朱小波,陈福良,尹明明.分析测试学报),2009,28(4):409-413.
[14]Ma W N,Gu F G,Wang Y,Meng G D L,Wu C Z.J.Chin.Pharm.Sci.,2015,24(1):47-53.
[15]Wang N J,Zhou L L,Guo J,Ye Q Q,Lin J M,Yuan J Y.Appl.Surf.Sci.,2014,305:267-273.
[16]Zhang Y,Wang W,Li Q,Yang Q B,Li Y X,Du J S.Talanta,2015,141:33-40.

