Vogt-小柳原田综合征1例报告并文献复习
张雯雯 史兆博 赵莘瑜 滕军放
郑州大学第一附属医院神经内科 郑州 450052
Vogt-小柳原田综合征(VKH)是一种累及全身多系统的自身免疫性疾病,常侵犯带色素的组织,如葡萄膜、脑膜、内耳及皮肤[1],其发病机制目前尚不明确。主要表现为弥散性葡萄膜炎、神经症状、听力障碍、皮肤脱色素、毛发变白或脱落等[2]。除眼部侵犯以外,神经系统、听力、皮肤、毛发均可受累,首发症状多样,临床中可因其他系统受累症状收治入院,在诊断中漏诊误诊率高。本文对1例以神经系统损害为首发症状患者的诊疗经过进行分析,以提高对该病诊断、治疗的认识。
1 病例资料
1.1 病史资料 患者男性,29岁。以“头痛伴发热10d,意识障碍3d”为代主诉于2014-02-16入我院。10d前饮250 mL白酒后出现持续性头痛,为全头部胀痛,发热,测体温37.5℃,伴头晕、鼻塞、流涕,无恶心、呕吐、意识障碍等,至当地医院就诊,查胸部CT 提示双肺炎症,血常规示白细胞12.36×109/L,中性粒细胞7.79×109/L。给予抗感染及退热药物应用,疗效欠佳。3d前体温最高升至42℃,嗜睡,至“周口市中心医院”查头颅MRI示:双侧颞叶底部内侧异常信号,胼胝体压部异常信号,考虑颅内感染。为求进一步诊治来我院。既往体健,无特殊病史。家族无与患者类似疾病。
1.2 入院体格检查 体温39.1℃,嗜睡,言语清晰,高级智能活动减退。双侧瞳孔等大等圆,直径3.0mm,对光反射灵敏。四肢肌张力正常,肌力5级,双侧腱反射(++)。双侧巴宾斯基征阴性。颈强直,颏下4指,Kernig征阳性。
1.3 辅助检查及治疗 血生化检查未见明显异常。头颅MRI平扫+增强、脑电图未见明显异常。腰椎穿刺测压为190mmH2O,白细胞数为32×106/L,其中淋巴细胞占76%,中性粒细胞占9%,一般单核细胞占9%,激活单核细胞6%。蛋白定性弱阳性,定量为609 mg/L。血肿瘤全套回示巨细胞病毒IgM、IgG 均为阳性。
1.4 诊断及治疗 综合上述资料,患者入院后初步诊断为病毒性脑膜炎,给予脱水降颅压、抗病毒、抗感染、营养神经及其他对症支持治疗。10d后患者头痛症状明显减轻,意识清楚,但诉视物模糊,伴双侧结膜充血,双眼无疼痛、瘙痒等不适,体格检查颈软,双眼结膜充血,双侧瞳孔不等大,左侧5.0mm,右侧3.0mm,对光反射灵敏。测视力:左眼0.6,右眼0.5。行眼底照相、眼底荧光血管造影,考虑双眼全葡萄膜炎。见图1、2。

图1 眼底检查图像

图2 眼底荧光血管造影(FFA)
综合上述病史及相关实验室检查,诊断为小柳原田综合征。因大剂量激素应用恐加重患者肺部感染,给予甲强龙120mg静滴,qd。并给予妥布霉素地塞米松眼液、普拉洛芬滴眼液、复方托吡卡胺滴眼液点眼。治疗10d后,患者诉头痛发热、视物不清症状较前明显好转,双侧瞳孔仍不等大,左侧4.0mm,右侧3.0 mm,对光反射灵敏。复查视力:左眼0.7,右眼0.6。患者出院,院外继续口服泼尼松片30 mg,qd;继续应用妥布霉素地塞米松眼液、普拉洛芬滴眼液、复方托吡卡胺滴眼液点眼。2个月后门诊复查:双侧瞳孔等大等圆,直径3.0mm,对光反射灵敏。双眼视力均为0.9。见图3、4。
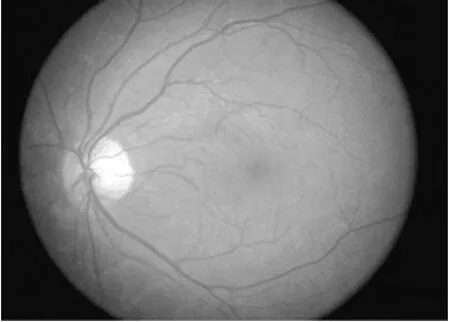
图3 眼底检查图像

图4 眼底荧光血管造影(FFA)
2 文献复习
2.1 发病机制 有关VKH 综合征的病因及发病机制尚不明确。存在3 种假说:遗传假说、炎症假说及自身免疫学说[3]。目前研究多倾向于自身免疫性疾病,认为VKH 综合征的发生是机体对黑色素相关抗原和视网膜S抗原、光感受器间维生素A 类结合蛋白等的自身免疫反应所致[4]。
2.2 临床分期 Moorthy等[1,5]将VKHS 分为4期:(1)前驱期:突然发病,常有感冒症状,如头痛、头晕、耳鸣,严重者有脑膜刺激症状,脑脊液淋巴细胞和蛋白升高。仅持续1~2周,以后逐渐恢复正常;(2)葡萄膜炎期:前驱期后3~5d出现眼部症状,视力高度减退。(3)恢复期:眼部症状逐渐消退,前节可遗留虹膜后粘连,视网膜下液体吸收,视网膜复位。眼底色素脱失形成晚霞样眼底,并有大小不等色素斑和色素脱失斑,视乳头周围有灰白色萎缩晕;(4)慢性复发期:反复发作,迁延不愈,表现为肉芽肿性炎症,发生严重并发症,甚至失明。脱发、白发、白癜风多发生在眼病开始后数周或数月,一般5~6个月恢复。
2.3 诊断标准 目前,VKHS 尚无特异性诊断标准,最新标准为2007年由Rao等[6]在2001年修订诊断标准的基础上修改后提出的。诊断标准如下:(1)病前无眼球外伤或手术史;(2)临床与实验室检查排除其他病因的葡萄膜炎;(3)双眼累及并具有VKH 综合征的急性或慢性期,眼前节或后节的表现;(4)有神经、耳部症状或脑脊液细胞增多;(5)皮肤、毛发改变。完全性VKH:必须出现标准(1)~(5)表现;不完全性VKH:至少出现标准(1)~(3),结合(4)、(5)表现;可疑VKH(单独出现眼部疾患):必须出现标准(1)~(3)表现。
2.4 治疗及预后 VKHS治疗的目标是防止不可逆的视力障碍。早期积极全身系统应用糖皮质激素是VKHS的一线治疗方案[3]。临床上可选择甲泼尼龙1g/d冲击应用3~5 d,减量情况根据个体情况而异,一般激素维持治疗6~12个月。或强的松口服1~2 mg/(kg·d)。严重患者可用免疫抑制剂、生物制剂和抗新生血管生长因子类(VEGFs)药物,为治疗VKHS的辅助用药[7]。对于合并前葡萄膜炎者,使用睫状肌麻痹剂也很重要,散瞳可减轻炎症反应,防止虹膜后粘连,减少并发症发生。同时给予糖皮质激素滴眼和非甾体消炎药滴眼,也有一定疗效[8]。
3 讨论
本例患者29岁,男性。急性起病,以发热、头痛及上呼吸道感染症状,就诊于神经内科,头颅MRI平扫+增强未见明显异常,脑脊液化验淋巴细胞及蛋白升高。由于无眼部阳性体征,体格检查脑膜刺激征阳性,加之辅助检查结果,早期易被误诊为“病毒性脑膜脑炎”,因之后出现结膜充血,视力下降等眼部症状修正诊断。
病毒性脑膜炎是指由各种病毒感染引起脑膜急性炎症的一种感染性疾病。依据病毒感染症状,急性或亚急性起病,以脑膜刺激症状为主要临床表现,脑脊液检查压力正常或轻中度升高,白细胞和蛋白正常或轻度增高,糖氯化物正常。一般病程较短,并发症较少,多成良性过程。少有复发,预后好。
Vogt-小柳原田综合征(VKH)发病机制尚未清楚,普遍认为是自身免疫系统针对分布于皮肤、脑膜、内耳、脉络膜黑色素细胞中的某种抗原产生的迟发型超敏反应。在VKH患者的视网膜下积液中可检测到病毒包涵体,在脑脊液和视丘下部也发现了病毒颗粒,推测病毒可能是由中枢神经系统到达眼部。以神经系统症状为首发症状的患者,可先出现脑膜炎症状及脑脊液改变[5-6],继而出现弥散性葡萄膜炎、听力障碍、皮肤脱色素、毛发变白或脱落等改变。尽早进行视力检查、眼底检查及眼底荧光血管造影等检查有助于确诊VKH。
该病易反复发作,治疗的最新进展主张早期大剂量应用糖皮质激素,从而减少组织渗出、阻止肿胀和减少渗出液,控制炎症反应,治疗时间至少维持6个月以上,否则会导致不同程度的视敏度下降,甚至失明。
临床工作者常因对VKH 的临床特征、病程演变缺乏整体认识及缺乏全面的检查,使患者不能得到及时、系统的治疗,导致病情反复及并发症的发生。有文献统计,VKHS早期误诊、漏诊率高达85%以上,严重影响VWHS的早期治疗及预后[9]。在临床工作中,对于病毒性脑膜炎患者,应积极进行眼底检查,对可疑患者尽早进行眼底荧光血管造影,避免漏诊、误诊,影响患者预后。
[1]Moorthy RS,Inomata H,Rao NA.Vogt-Koyanagi-Harada syndrome[J].Surv Ophthalmol,1995,39(4):265-292.
[2]Wang Fang,Peizeng Yang.Vogt-Koyanagi-Harada syndrome[J].Current Eye Research,2009,233(7):517-523.
[3]Greco A,Fusconi M,Gallo A,et al.Vogt-Koyanagi-Harada syndrome[J].Autoimmunity Reviews,2013,12(11):1 033-1 038.
[4]刘聪慧,郑燕林.Vogt-小柳原田综合征发病机制研究进展[J].眼科新进展,2007,27(11):872-873.
[5]Beniz J,Forster DJ,Lean JS,et al.Variations in clinical features of the Vogt-Koyanagi-Harada syndrome[J].Retina,1991,11(3):275-280.
[6]Rao NA,Sukavatcharin S,Tsai JH.Vogt-Koyanagi-Harada d-isease diagnostic criteria[J].Int Ophthalmol,2007,27(2/3):195-199.
[7]付安琪,李寿玲.Vogt-小柳原田综合征的研究进展[J].临床眼科杂志,2013,21(3):284-287.
[8]王少程,葛庆曼,郑曰忠,等.Vogt-小柳-原田病的临床特点和治疗分析[J].临床眼科杂志,2007,15(2):103-105.
[9]王红,杨培增,钟华红,等.Vogt-小柳-原田综合征漏误诊分析[J].中国实用眼科杂志,2001,19(11):839-841.

