透明质酸降解工艺条件优化*
王鑫,郭瑞琳,王派丽,孟颖,魏静,许丹丹,宋天雪
(哈尔滨商业大学食品工程学院省高校食品科学与工程重点实验室,黑龙江哈尔滨,150076)
透明质酸又称玻璃酸(hyaluronic acid,HA),是一种天然的具有保水功能的酸性黏多糖[1]。广泛存在于动物和人体的组织细胞间质(基质)和某些细菌的荚膜中,具有保持皮肤弹性的功能,能够锁住大量水分子,对皮肤组织具有保湿润滑的作用[2]。HA分子构造为一线性、并无分支的高分子。分子质量能够达到100~150万。低分子质量HA具有促进血管生成的活性,保护人体内肉芽组织免受氧自由基的破坏,并且能够促进伤口愈合[3-4]。高分子质量HA可以抑制巨噬细胞的吞噬能力,而低分子质量HA可促使巨噬细胞表达一些与炎症有关的因子[5]。低分子质量HA能渗透到真皮层,调节皮肤代谢,促进血液循环,有保健、美白作用,低分子质量HA几乎与用于任何种类化妆品[6]。因此,研究高效的降解出低分子质量的HA,使得HA的吸收利用率增加,既含有低分子HA的特性,也能达到高分子HA的作用效果,才更有助于其特殊作用的发挥[7]。本文采用化学法对纯化后的HA进行降解研究,并应用响应面法对降解条件进行优化,以提高产品的利用度。
1 材料与方法
1.1 材料与仪器或材料与设备
新鲜鸡冠市售;HA标品,上海源叶生物科技有限公司;CTAB,北京中生瑞泰科技有限公司;三氯甲烷,天津市天新精细化工开发中心;正丁醇,天津市福晨化学试剂厂;NaCl,天津市北方医化学试剂厂;葡萄糖,天津市进丰化工有限公司;铁氰化钾,天津市北辰方正试剂厂;VC,天津市津北精细化工有限公司;H2O2,天津市化工消毒用品有限公司;NaCO3,天津市晶科化工有限公司;无水乙醇,天津市天力化学试剂有限公司。
微型植物粉碎机,天津市泰斯特仪器有限公司;R-205旋转蒸发器,上海申胜生物技术有限公司;恒温水浴锅,余姚市东方电气仪器厂;SHZ-Dバ循环水式真空泵,巩义市予华仪器有限责任公司;DHG-9123A型电热恒温鼓风干燥箱,上海一恒科技有限公司;TU-1900型紫外可见分光光度计,北京普析通用仪器有限责任公司;ALC-1100.2型电子分析天平,北京赛多利斯仪器系统有限公司;便携数显电子PH计测试笔,北京市立精化学器具有限公司。
1.2 实验方法
1.2.1 HA标准曲线的绘制
准确称取0.025 0 g标准HA于25 mL容量瓶中,定容至刻度,配制成标准溶液。分别量取HA标准溶液0.5、1.0、1.5、2.0、2.5、3.0 mL 置于10 mL 容量瓶中,定容至刻度。以蒸馏水作为空白,在波长为198 nm处测定吸光度。以HA浓度为横坐标,吸光值为纵坐标,绘制标准曲线。
1.2.2 HA提取工艺
将新鲜的公鸡冠用无水乙醇浸泡24 h至鸡冠变硬为止,将鸡冠干燥后粉碎。加入鸡冠粉末6~7倍蒸馏水,搅拌均匀,静置浸泡12 h,收集滤液,滤渣再按同样方法浸泡2次,合并滤液。将滤液不断搅拌,每100 mL滤液加入10 g的固体NaCl,完全溶解后,加入与滤液等体积的三氯甲烷、正丁醇溶液(三氯甲烷∶正丁醇体积比为4∶1),连续搅拌2 h左右,采用分液漏斗静置分层取上层水相待用。取上述待用水相于烧杯中用体积分数90%乙醇浸泡,按照1∶2的比例将二者混合静置沉淀24 h,回收乙醇溶液,沉淀物干燥得HA粗品。
1.2.3 HA纯化方法
HA粗提物溶于0.15 mol/L NaCl中得到0.25%的HA溶液。1倍体积10%CTAB(溶在0.15 mol/L NaCl中)加入4倍体积的0.25%的HA溶液中。调节 pH=9.0,静置 4h。CTAB与 HA生成CTAB-HA复合物沉淀,离心分离。CTAB-HA复合物浸泡在1.5 mol/L NaCl溶液中,置于60℃水浴中静置2 h。CTAB-HA复合物可解离溶解。最终得到较纯的HA液体,干燥后待用。纯化后HA含量计算公式:

式中:W,HA 含量,%;m,HA 质量,g;M,纯化后物质量,g。
1.2.4 糖还原法测定产物的相对分子质量
以0.3 mol/L的Na2CO3溶液为溶剂,配制浓度为0.75 mg/mL的铁氰化钾溶液。采用分析纯葡萄糖配制浓度为1 mg/mL的溶液,并作5个梯度稀释。取各稀释液2 mL,与2 mL上述铁氰化钾溶液于比色管中混合均匀后在沸水浴上反应15 min,冷却,在420 nm波长下测吸光度。以吸光值为纵坐标,以葡萄糖浓度为横坐标,绘制标准曲线。HA的降解产物的相对分子质量的计算公式:

式中:α,降解产物浓度,mg/mL;β,葡萄糖浓度,mg/mL。
1.2.5 降解HA单因素条件的选择
1.2.5.1 H2O2和VC最佳比例的确定
量取5份HA粗品溶液每份5 mL,加入1 mL 0.1 mol/L的VC,用NaOH调节pH至4.0,分别加入2、3、4、5、6、0.1 mol/L 的 H2O2溶液,反应开始,维持pH在4.0,反应15 min。分别取各烧杯中反应液2 mL,与2 mL铁氰化钾-碳酸钠溶液于比色管中混合均匀,在沸水浴上反应15 min冷却。在420 nm波长下测吸光度,根据糖标准曲线方程计算分子质量。
1.2.5.2 pH值对降解的影响
量取5份HA粗品溶液每份5 mL,加入1 mL 0.1 mol/L的 VC,用 NaOH 调节 pH 值在4.0、6.0、8.0、10.0、12.0,再加入4 mL 0.1 mol/L 的 H2O2溶液,反应开始,维持pH恒定,反应15 min,之后方法同1.2.5.1。
1.2.5.3 降解时间对HA降解的影响
量取5份HA粗品溶液每份5 mL,加入1 mL 0.1 mol/L的VC,用NaOH调节pH值至8.0,再加入4 mL 0.1 mol/L的H2O2溶液,反应开始,维持pH值恒定,反应 5、10、15、20、25 min,之后方法同1.2.5.1。
1.2.5.4 H2O2浓度对降解的影响
量取5份HA粗品溶液各5 mL,加入1 mL 0.1 mol/L的VC,用NaOH调节pH值至8.0,分别加入4 mL 1.0、1.2、1.4、1.6、1.8 mol/L 的 H2O2溶液,反应开始,维持pH值在8.0,反应5 min,之后方法同1.2.5.1。
采用Box-Behnken模型,以提取时间、料液比和乙醇浓度为影响透明质酸为主要的考察因子(自变量),分别以 X1、X2、X3表示,并以 +1、0、-1 分别代表自变量的高、中、低水平,按方程X1=Xi-X0/X对自变量进行编码[8]。其中Xi为自变量的编码值,Xi为自变量的真实值,Xo为试验中心点处自变量的真实值,X为自变量的变化步长[9],因子编码及水平见表1。并采用多元回归分析,拟合二次多项式回归模型的Box-Behnken设计试验,进行结果分析。在模型拟合出的最优条件下进行3次重复实验,以验证响应曲面拟合结果的可靠性。

表1 Box-Behnken实验设计因素水平及编码Table 1 Factors and levels of Box-Behnken design
2 结果与讨论
2.1 HA标准曲线绘制结果
在198 nm下测得HA标准曲线,如图1,吸光度与浓度之间的回归方程为:y=7.805 0x+0.080 8(R2=0.998 3),回归方程线性显著,该方程的有效线性范围为0~0.25 mg/mL。

图1 HA标准曲线Fig.1 HA standard curve
2.2 HA纯化结果与分析
由表2可知,提取后HA的含量为58.45%,纯化后HA的含量为82.58%,提高了24.13%,纯化后HA的分子质量为22671.88。
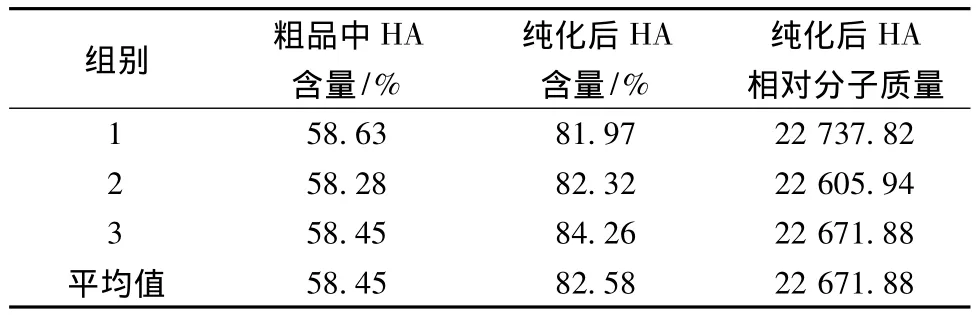
表2 HA提取纯化结果表Tables 2 The extraction and purification results of HA
2.3 葡萄糖标准曲线绘制结果
在420 nm下测得葡萄糖标准曲线,如图2,吸光度与浓度之间的回归方程为:y=0.013 3x-0.002 2(R2=0.992 6),回归方程线性显著,该方程的有效线性范围为0~10mg/mL。采用糖还原法测定产物的相对分子质量,降解前 HA相对分子质量为22 671.88。

图2 葡萄糖标准曲线Fig.2 Glucose standard curve
2.4 降解HA单因素的选择结果分析
2.4.1 料液比单因素的选择结果分析
由图3可知,随着比例的增加,产物的吸光度值达到最低点后有所回升,最后趋于平行,当H2O2和VC添加量不一样时,反应产生的自由基的量也会不同。H2O2和VC对降解都有一定影响,但经实验验证,当和VC添加量比H2O2多时得到的吸光度值低于H2O2比VC多时的吸光度值,因此,VC对降解影响不显著,而H2O2的量对降解的影响相对较大。因此,单因素试验确定出最佳降解的料液比为4∶1。

图3 料液比对HA降解的影响Fig.3 Influence of ratio of Solid-liquid on the degradation of HA
2.4.2 pH值单因素的选择结果分析
以上研究结果多通过顶板结构计算顶板来压时的顶板压力,从而确定支架合理工作阻力,但其计算过程复杂,需要参数众多,具体实践过程中,很多参数难以精确取得。笔者以酸刺沟煤矿6上105-2综放工作面压架事故为背景,通过现场实测和理论分析,对压架机理进行研究,同时对工作面实测矿压数据进行分析处理,基于位态方程,从顶板控制效果出发,研究确定支架的合理工作阻力。
由图4可知,随着pH值的改变,透明质酸降解程度不同,原因是pH会影响羟基自由基的产生,羟基自由基对HA的降解密切相关,在pH 8.0时HA降解程度达到最好。因此,由单因素试验可确定最佳降解pH值为8.0。

图4 pH值对HA降解的影响Fig.4 Influence of pH on the degradation of HA
2.4.3 降解时间单因素的选择结果分析
降解HA主要是靠降解体系内自由基的作用,虽然自由基的作用很强但寿命极短。所以在反应初期分子质量下降很快,随后逐渐趋于下降并趋于稳定。由图5可知,时间越长HA降解的程度降低。在时间5 min时HA降解程度达到最好,若继续延长时间,HA降解的分子质量呈上升趋势。是因为降解时间过长可能使HA成分生物活性受到破坏,有效成分不再被降解,导致实验误差增大。因此,降解时间确定为5min。

图5 降解时间对HA降解的影响Fig.5 Influence of time on the degradation of HA
2.4.4 H2O2浓度单因素的选择结果分析
H2O2的浓度对降解的影响很大,研究中自由基的量通过H2O2的量来表示,当底物浓度一定时,随着自由基量的增加,分子量下降,当下降到一定程度后,分量下降十分缓慢了。由图6可知,随着H2O2的浓度的改变,HA降解程度不同,在H2O2浓度为1.6 mol/L时HA降解程度达到最好。因此,确定最佳降解1.6 mol/L。

图6 H2O2浓度对HA降解的影响Fig.6 Influence of H2O2concentration on the degradation of HA
2.5 响应曲面法优化HA的降解条件结果分析
2.5.1 多元回归分析设计及试验结果分析
采用多元回归分析,拟合二次多项式回归模型的Box-Behnken设计及试验结果见表3。利用 Design Expert软件对表3数据进行多元回归拟合,获得化学法降解鸡冠中提取的HA对降解料液比(x1)、H2O2浓度(x2)和pH(x3)的二次多项回归模型方程为:
Y=2 017.2-460.87x2-806.00x2-177.88x3-108.55x1x2-20.25x1x3-84.5x2x3+1 955.27X12+1 189.02X22+1 345.28X32
其中:Y,相对分子质量;x1,料液比;x2,H2O2浓度mol/L;x3,pH。
从方程的方差分析表4可见,试验所选用的模型高度显著(P<0.000 1),模型的校正决定系数0.978 4,说明该模型能解释97.84%响应值的变化,仅有总变异大约2.16%不能用此模型来解释;相关系数R=0.990 6,说明该模型拟合程度良好,试验误差小,该模型是合适的,可以用此来分析化学降解法对HA的降解程度。从表5的回归方程系数显著性检验可知,模型一次项x1显著、x2极显著、x3不显著;二次项x12(P <0.000 1)、x22(P <0.000 1)、x32(P<0.000 1)极显著;交互项 x1x2,x2x3、x1x3不显著。
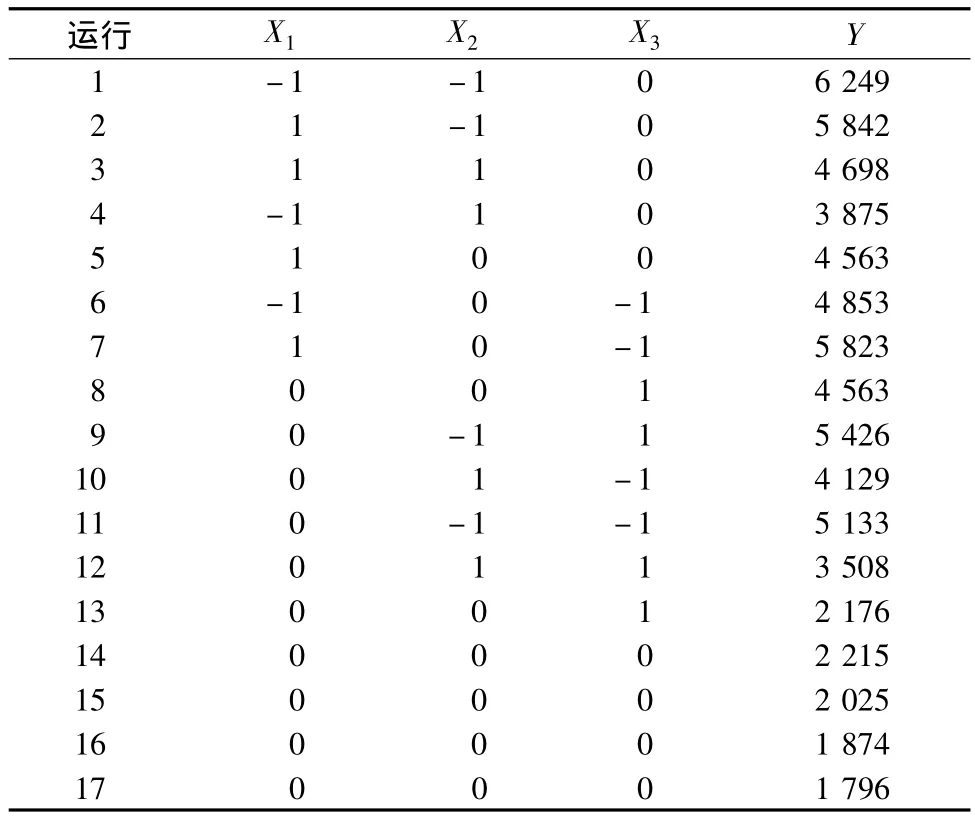
表3 实验设计与结果Table 3 Experimental design and results

表4 响应面模型方差分析表Table 4 Response surface model analysis of variance table
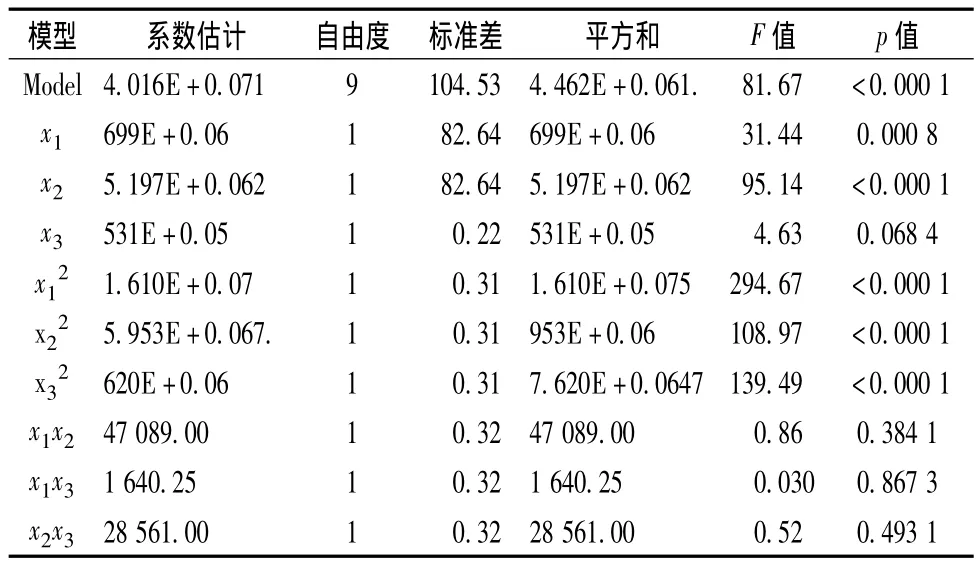
表5 回归方程系数显著性检验Table 5 Significance test of the regression equation coefficients
2.5.2 多元回归方程的响应曲面及其等高线图解结果与分析
由图7可知,料液比和H2O2浓度对降解HA的交互影响效应。从其响应曲面图可以直观的看出两因素的交互作用不显著,随着料液比的增大,HA的降解程度逐渐提高,料液比和H2O2浓度均对降解均有影响,H2O2浓度高比例大降解程度最好,分子量最低点为料液比为4.13∶1,H2O2浓度为1.67 mol/L。

图7 料液比、H2O2浓度及其交互作用对降解HA的响应曲面图Fig.7 Influence of liquid ratio,H2O2 concentration and their interactions on the response surface of the degradation of HA
由图8可知,降解pH和料液比对降解鸡冠中透明质酸的交互影响效应。从其响应曲面图可以看出两因素的交互作用不显著,在实验水平范围内,pH值对透明质酸降解影响不明显,相比料液比的作用更强,两因素交互作用最低点为pH值为8.16,料液比为4.13∶1。

图8 料液比、pH值及其交互作用对降解HA的响应曲面Fig.8 Influence of liquid ratio,pH and their Interactions on the response surface of the degradation of HA
由图9可知,pH与H2O2浓度对降解HA的交互影响效应。从其响应曲面图可以直观的看出两因素的交互作用不显著,在试验水平范围内,H2O2浓度对HA的降解影响大,pH影响程度较小,两项交互作用条件pH为8.16,H2O2浓度为1.67 mol/L时分子量达到最低点。

图9 H2O2浓度、pH值及其交互作用对降解HA的响应曲面Fig.9 Influence of H2O2concentration,pH and their Interactions on the response surface of the degradation of HA
2.5.3 验证试验结果与分析
通过单因素及响应曲面的分析,确定出降解HA最佳工艺条件。料液比为4.13∶1,pH为8.16,,降解时间为5 min;H2O2浓度为1.67 mol/L。根据确定的最佳降解条件进行验证试验,其结果见表6。

表6 验证试验结果表Table 6 The results of Verification test
采用优化后的工艺降解HA,得出该工艺降解透明质酸的分子量为1 764.67。
3 结论
从新鲜鸡冠中提取的粗提物中HA含量为58.45%,经纯化后 HA的含量为82.12%,提高了24.13%,经提取纯化后得到的HA的相对分子质量为2 2671.88,通过响应曲面法对HA的降解条件进行优化,最佳条件为:料液比为4.13∶1,pH 8.16,H2O2浓度为1.67 mol/L。采用优化后的条件降解HA,得出最佳降解条件下降解HA的分质子量为1 764.67。
[1] 郭凤仙,凌沛学,郭学平.透明质酸的生理功能及其在化妆品和美容保健食品中的应用[J].中国商办工业,2002,9:45-46.
[2] 单连海,熊雄,郭海霞.透明质酸的制备及其应用进展[J]. 安魂农业科学,2007,35(11):3 150-3 189.
[3] Trabucchi E,Pallotta S,Morini M,et al.Low molecular weight hyaluronic acid prevents oxygen free radical damage to granulationt issue during wound healing[J].Int J Tisue React,2002,24(2):65-71.
[4] 王彦厚,王凤山,郭学平.低相对分子质量透明质酸的制备及其促血管生成作用[J].中国生化药物杂志,2007,28(2):107-109.
[5] 杨桂兰,郭学平,栾贻宏,不同相对分子质量透明质酸钠的应用[J]. 食品与药品,2005,7(12A):1-3.
[6] 崔向珍,刘爱华,贺艳丽.等.低分子量和寡聚透明质酸研究进展[J]. 食品与药品,2006,8(3):6-9.
[7] 王彦厚,贾雷.透明质酸的制备与临床应用研究进展[J]. 实用药物与临床,2007,10(10):48-85.
[8] Douglas C.实验设计与分析[M].北京:中国统计出版社,2008:589-592.
[9] 袁志发,周静芋.试验设计与分析[M].北京:高等教育出版社,2000:381.

