便携式动脉硬化评估仪
【作 者】曹帅,陈香
中国科学技术大学电子科学与技术系,合肥市,230027
0 引言
动脉硬化是动脉的一种非炎症病变,可使动脉管壁增厚、官腔变小、失去弹性,特别容易发生在动脉血管的弯曲、分叉和狭窄部位。当动脉血管发生硬化后会使人体的某些部位供血不足,从而导致心血管疾病的发生,如冠心病、脑卒中等[1]。动脉硬化程度可以独立反映人体潜在的心血管疾病发病可能性,及早发现动脉血管硬化并采取有效的干预措施是延缓和控制心血管疾病的根本措施[2]。
评价动脉硬化程度的方法有很多种,包括:生化法、血管造影法、超声法、核磁共振法、CT扫描和脉搏波检测法。生化法是通过血糖、血脂等生化指标来间接反映动脉的硬化程度,但这些生化指标并不总与动脉硬化的病变过程同行,无法直接反应动脉的硬化程度。血管造影法、超声法、核磁共振法、CT扫描都较复杂,而且血管造影法和CT扫描对人体是有创的。更重要的是,生化法、血管造影法、超声法、核磁共振法和CT扫描都需要专门复杂的仪器,对操作者的要求也较高,不适合家庭监护。脉搏波检测法是通过检测人体脉搏波,分析它的波形变化或波速的变化,总体反映人体的动脉硬化程度,此种方法简单无创,对操作者没有过高要求。
通过脉搏波传输速度来反应动脉硬化的程度的方法在临床上已经得到了验证,如市场上常见的心血管无创检测仪如法国的COMPLIOR-SP、日本的COLINVP1000/2000等均采用此种方法。但均存在体积庞大、价格昂贵、操作复杂等缺点,不易于家庭监护[3]。为此,有关科研人员在心血管无创检测设备小型化方面做了一些尝试,如Hu Q等[4]研制了一种评估动脉硬化的便携式设备,该设备用压力法仅采集了桡动脉处的脉搏波信号,结合一路心电信号,可反映上肢的动脉硬化程度。Wu HT等[5]研制了一种用于家庭监护的动脉硬化评估设备,该设备利用光电法采集了耳垂处和食指处的脉搏波,结合一路心电信号,可以评估出颈动脉支和上肢动脉的硬化程度,但不能反映下肢的动脉硬化程度。
鉴于现有研究的局限性,本文研制了一种便携式动脉硬化评估仪,它利用压力法采集颈动脉、桡动脉和足背动脉的脉搏波信号,结合一路心电信号,可以较全面的评估人体的颈动脉支、上肢动脉和下肢动脉的动脉硬化程度。
1 硬件实现
便携式动脉硬化评估仪主要由传感器模块、采集板和嵌入式模块构成,如图1所示。传感器模块包括1导联心电模块和3路脉搏波提取模块,用于同步提取人体的心电信号和颈动脉、桡动脉及足背动脉的体表脉搏波信号,模块内包含了放大和滤波电路。采集板由单片机和多通道同步模数转换器构成,单片机通过SPI接口控制多通道模数转换器同步转换多通道的模拟信号,并将转换后的数据通过USB接口以固定的数据格式传输至嵌入式模块。嵌入式模块将接收的数字信号进行显示、存储,并完成人机交互、脉搏波传输速度的计算等任务。
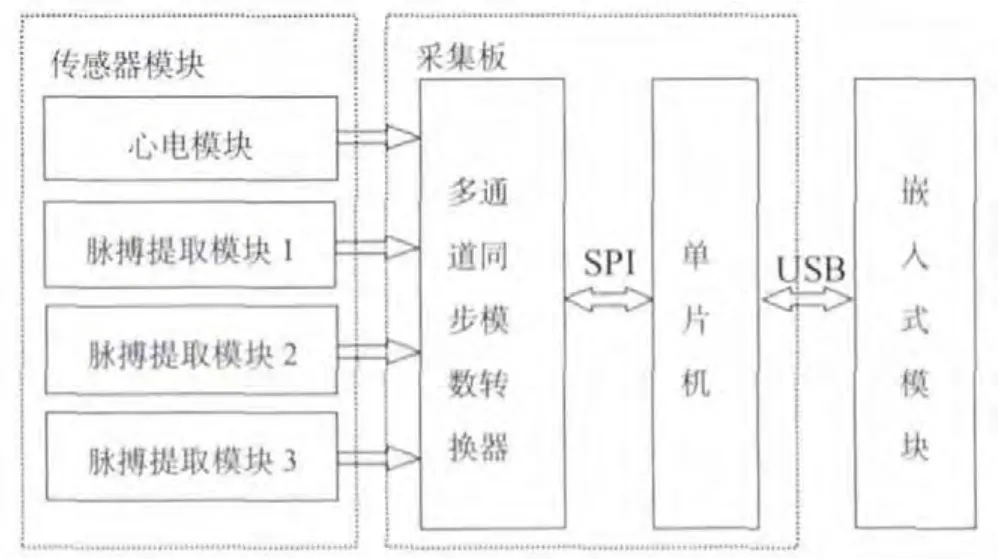
图1 便携式动脉硬化评估仪的总体结构Fig.1 Structure of the portable instrument for arteriosclerosis assessment
1.1 传感器模块
心电模块采用标准I导联,其核心芯片使用了ADI公司低成本的单导联心电模拟前端芯片AD8232。该芯片高度集成化,内部集成了仪用放大器、滤波用运算放大器、右腿屏蔽驱动放大器等器件,仅需要一些少量的外部元件就可以构成所需的心电采集电路,提高了心电模块的稳定性和可靠性。AD8232采用单电源供电,电压范围2.0~3.5 V,供电电流仅为170 mA,具有低功耗的特点。为了获得稳定的R波峰值,心电模块的通带频率设置在7~24 Hz,省去了50 Hz滤波电路,简化了设计。
脉搏波提取模块使用HK-2000B脉搏传感器,如图2所示。该传感器采用高度集成化工艺,将力敏元件(PVDF压电膜)、灵敏度温度补偿元件、感温元件、信号调理电路集成在传感器内部。具有灵敏度高、抗干扰性能强、过载能力大、一致性好、性能稳定可靠、使用寿命长等特点。该脉搏传感器具有完善的信号调理功能,用户不需要在传感器的输出后加滤波等电路,使用简单。HK2000B脉搏传感器提取的脉搏波信号幅度因人而异,而且与传感器的放置有关。为了使信号的幅值满足模数转换器的输入范围,脉搏波传感器的输出信号在转换之前经过了模数转换器内部的可编程增益放大器(PGA)的放大。

图2 脉搏波提取模块实物图Fig.2 Photo of the pulse wave extraction module
1.2 采集板
采集板的核心部件是TI公司的同步模数转换器ADS1198和Silicon Labs公司的单片机C8051F320。
ADS1198具有8通道的16 bit模数转换器,采样率可编程,每通道带有可编程增益放大器,增益调节范围在1~12,每通道的功耗为0.55 mW,具有低功耗的特点。它与外界通信的接口为串行外设接口(SPI),最高通信速率可达20 Mbps。采用同步模数转换器的优点是各通道之间没有采样延迟,增加了脉搏波传输延迟计算的准确性。
单片机C8051F320具有如下主要特点:高速、流水线结构的8051兼容的微控制器内核(可达25MIPS);片内全速、非侵入式的在系统调试接口;通用串行总线(USB)功能控制器,有8个灵活的端点管道,集成收发器和1 kB FIFO RAM;硬件实现的SMBUS/ I2C、增强型UART和增强型SPI串行接口;4个通用的定时器;片内上电复位、VDD监视器和时钟丢失检测器。C8051F320的SPI接口用于与ADS1198的通信,它的USB接口完成与嵌入式模块通信,它运行速度快,方便调试,能很好的满足系统的要求。
1.3 嵌入式模块
嵌入式模块采用LJD-eWin3S,该模块采用低功耗32 bit高速ARM芯片S3C2440A,ARM920T内核,400 MHz主频;接口丰富,带有USB HOST、USB DEVICE、SD卡存储等功能,其中存储容量可达8 GB;8.89 cm高清晰真彩数字屏,支持4线电阻式触摸,分辨率320×240像素。模块上预装了正版WINCE5.0操作系统,支持EVC/VS2005直接开发应用程序,支持MFC等常规WINDOWS应用框架等。LJD-eWin3S适合于工业控制、医疗仪器、监测控制、智能设备等应用,使用方便。
1.4 系统整机集成
系统整机采用分层连接结构,如图3所示,底层为采集板,上层为嵌入式模块,两者通过USB建立通信连接。采集板上一排mini USB接口为传感器接口。

图3 系统整机实物图Fig.3 Photo of the system
2 软件实现
系统的软件实现包括两大部分:单片机C8051F320上的软件实现和嵌入式模块LJD-eWin3S上的软件实现。嵌入式模块的软件实现又包括脉搏波传输速度提取算法实现和人机交互设计的实现。
2.1 单片机上的软件实现
单片机上的软件设计如下:在单片机的片内RAM中申请了2个缓存:发送缓存和采集缓存,发送缓存中存储着上一时刻采集完成的数据,采集缓存用于存放这一时刻正在采集的数据。单片机首先初始化内部资源和8通道同步ADC,直至初始化完成,设置ADC的采样率为500 Hz,ADC会每隔2 ms以外部中断的形式通知单片机读取数据。然后单片机将发送缓存中一帧的数据传输至嵌入式模块直至完成,最后等待中断。在中断服务程序中,单片机读取采集的一帧数据至采集缓存中直至成功,然后交换发送和采集缓存的指针,最后中断返回。在主程序中,单片机从等待中断中跳出后发送新采集的数据。程序将一直循环下去直至单片机接到停止采集命令或系统断电。
单片机每次发送的数据格式是固定的,其发送数据的帧格式,为1个帧头跟随8个通道的数据。其中4 byte的帧头用于区分不同的数据帧。8通道数据为同一时刻采集,每通道数据占2 byte,通道1~4对应心电、颈动脉、桡动脉和足背动脉的数据,剩余的4通道可用于其它的传感器,便于系统的扩展。
2.2 嵌入式模块的脉搏波传输速度获取算法
脉搏传感器的测量点自上而下依次为颈动脉、桡动脉和足背动脉体表可触摸到搏动处。假设胸骨切迹至颈动脉、桡动脉和足背动脉的距离依次为L1、L2、L3。
图4所示为系统采集的某一心电周期内的各路信号,自上至下依次为心电波形和颈动脉、桡动脉、足背动脉的脉搏波信号波形。图中,tcycle为两R波峰值间的时间间隔,即1个心电周期。脉搏波波形上的两个星号“*”依次是脉搏波的波足点和波峰点,它们之间的脉搏波信号段称为上升沿,上升沿上的三角符号点是脉搏波的起搏点。图中△thc、△thr和△thd分别表示心电至颈动脉、桡动脉和足背动脉的脉搏波传输延迟。各路脉搏波传输速度通过如下的公式计算:
心电至颈动脉的脉搏波传输速度:
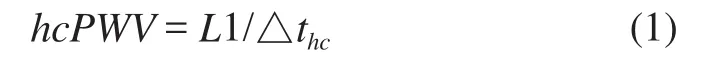
心电至桡动脉的脉搏波传输速度:
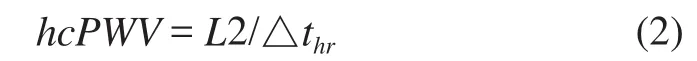
心电至足背动脉的脉搏波传输速度:
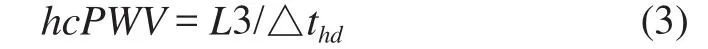
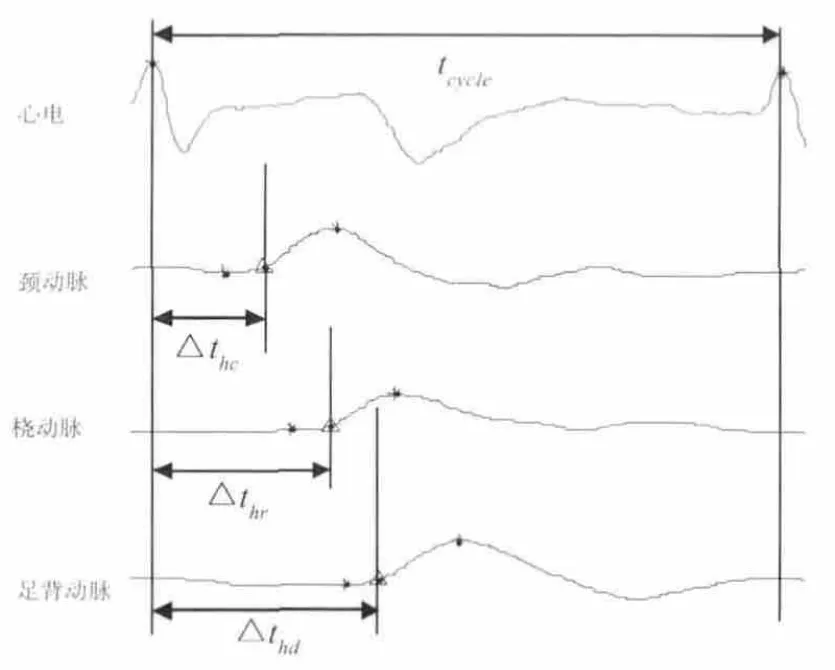
图4 脉搏波传输速度的计算描述图Fig.4 Calculation map of pulse wave velocity
如前所述,计算脉搏波传输速度的关键是计算出脉搏波传输延迟。嵌入式模块的获取脉搏波传输延迟的算法流程如下:取一段同步采集的心电和各路脉搏波信号进行平滑滤波处理,该段信号至少包含2个心动周期;利用阈值法找到心电信号的所有R波峰值点,所设定的阈值可以根据心电信号的特点进行人为的调节,以适应心电信号的个体差异性;依次取上述相邻的R波峰值点间所对各路脉搏波信号段;找到脉搏波信号段的最大值点和最小值点,从最大值点出发沿着脉搏波信号往前寻找到极小值点,将该极小值点与设定的阈值进行比较,判断极小值点是不是要寻找的波足点,直到找到波足点为止,所设定的阈值可以根据脉搏波信号的特点进行人为的调节,以适应脉搏波信号的个体差异性;取脉搏波的上升沿,利用交叉切线法求取脉搏波的起搏点[8],即上升沿的最大斜率的切线与过波足点的水平线之间的交点所对应的脉搏波点位置;计算第一个心电R波峰值点与颈动脉、桡动脉和足背动脉起搏点的时间间隔即传输延迟。该算法具有简单、实用、适用性强的特点,很适合在资源有限的嵌入式模块上实现。
2.3 嵌入式模块的交互设计
嵌入式模块的交互设计主要包括用户信息输入界面、数据显示界面和参数输出界面三大部分,由EVC开发完成。
用户信息输入界面用于受试者在测量前输入信息,包括其编号、性别、年龄、身高、体重、胸骨切迹至颈动脉的体表距离L1、胸骨切迹至桡动脉的体表距离L2、胸骨切迹至足背动脉的体表距离L3。该界面还具有查找功能,若用户的信息已存在,输入用户编号,系统可以调出该用户已有的信息,避免了用户信息的重复输入。
数据显示界面可以实时显示4通道的同步数据。通过观察数据显示界面,用户可以了解每通道的信号质量,对没有信号或信号幅值较弱的通道,用户可以通过调节对应传感器的放置位置或脉搏传感器夹子的松紧性来改善该通道的信号质量,直至每一通道获得较明显的信号为止,再将这些通道的数据同时存储在SD卡中。
参数输出界面用于参数的显示,输出的参数包括心率、hcPWV、hrPWV 和 hdPWV。
3 实验验证
本次实验选取了15名年轻受试者(男12名,女3名),他们的平均年龄为24.07±1.03岁,且没有任何心血管疾病。在实验之前要求他们静坐休息10 min,随后用电子血压计Panasonic EW3106测量受试者的血压,以了解受试者的身体情况。表1列出了受试者的基本信息,用平均值(mean)±标准差(SD)的形式表达。
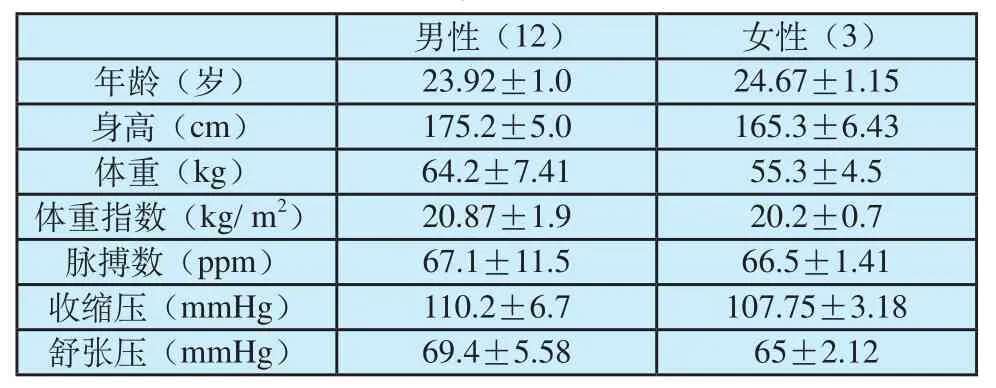
表1 受试者基本信息Tab.1 Subject information
3.1 系统的重复性
随机取某个受试者不同心电周期的各路脉搏波传输速度值作重复性分析。图5给出了不同心电周期的三路脉搏波传输速度值,由图中可见参数值hcPWV、hrPWV、hdPWV的走势趋于平稳。
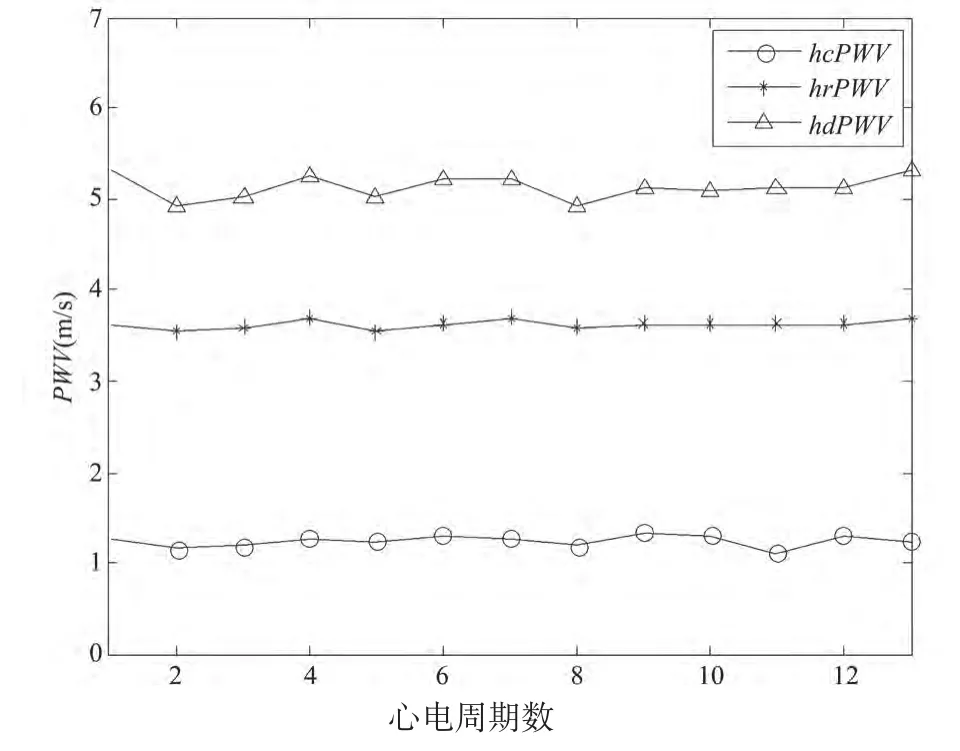
图5 不同心电周期的脉搏波传输速度Fig.5 Pulse wave velocity of different ECG cycles
上述三路脉搏波传输速度的均值和标准差分别为hcPWV=1.2484±0.0620 m/s,hrPWV=3.6308±0.0467 m/s,hdPWV =5.1372±0.1365 m/s。由此可知,每一路脉搏波传输速度的标准差相对于其均值都很小,系统所测各参数的重复性较好。
3.2 系统的准确性
15位受试者的三路脉搏波传输速度值如图6所示,其均值和标准差分别为hcPWV=1.2509±0.2558 m/s,hrPWV=3.5810±0.3269 m/s,hdPWV=5.2774±0.5697 m/s,满足关系hcPWV< hrPWV 图6 不同受试者的脉搏波传输速度Fig.6 Pulse wave velocity of different subjects 本文研制了一种便携式的动脉硬化评估仪器,该仪器具有结构简洁、扩展性好、携带方便,操作简单等特点,非常适合于家庭监护。为了验证设备的重复性和准确性,设备采集了15位受试者的数据,并将其计算的结果与前人的研究进行了对比。实验表明,所研制的便携式动脉硬化评估设备具有良好的重复性和准确性。 本文与上述前人的研究所采用的受试者均为25岁左右的年轻健康人,但是,动脉硬化通常发生在老年人的身上,所以便携式的动脉硬化评估仪器针对的是家中行动不便的老人,下一步需要采集年长的以及有心血管疾病的受试者,并根据计算的参数对动脉硬化程度进行分级,这样才会使得本文研制的便携式动脉硬化评估设备更具实用价值。 [1]DeLoach SS,Townsend RR.Vascular stiffness: its measurement and significance for epidemiologic and outcome studies[J].Clin J Am Soc Nephrol,2008,3(1): 184-192. [2]Park SM.Assessment of arterial stiffness index as a clinical parameter for atherosclerotic coronary artery disease[J].Circulation,2005,69: 1218-1222. [3]黎秀龙,马祖长,张永亮,等.基于波形分析的多种PWV获取系统的设计[J].生物医学工程研究,2011,30(2): 72-77. [4]Hu Q,Pan Q,Shao Q,et al.Design of a portable apparatus for assessing vascular stiffness[C].IEEE BMEI,2009.doi:10.1109/BMEI.2009.5305210. [5]Wu HT.Development of easy operating arterial stiffness assessment instrument for homecare[C].IEEE EMBS,2007: 5868-5871. [6]Li K,Warren S.Initial study on pulse wave velocity acquired from one hand using two synchronized wireless reflectance pulse oximeters[C].IEEE EMBS,2011: 6907-6910. [7]Wu HT,Hsu PC,Chen ZL,et al.A reliable multi-channel measurement based on ECG for atherosclerosis assessment[C].IEEE BMEI,2009: 284-289. [8]Jung DK.Changes of pulse wave velocity in arm according to characteristic points of pulse wave[C].IEEE ICCIT,2007: 821-826.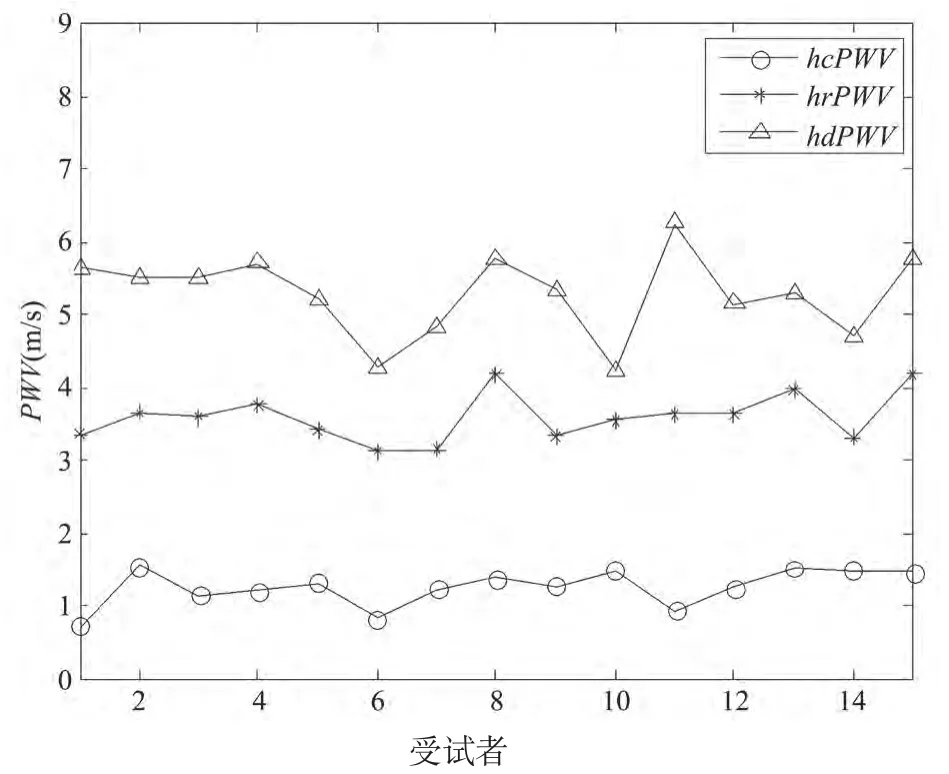
4 总结讨论

