冷冻治疗术对宫颈CINI和HPV感染的疗效观察
石 莹,张秀兴,郭芝亮 (广东省广州市妇女儿童医疗中心,广东 广州 510180)
宫颈癌是最常见的妇科恶性肿瘤,其发病率在女性恶性肿瘤中仅次于乳腺癌,居我国女性生殖系统恶性肿瘤首位[1]。宫颈癌发生之前,必然经历一段漫长的癌前病变期,从宫颈病变到癌的自然演变大约是5~15年[2],医学上统称为宫颈上皮内瘤变(CIN)。根据病变的级别,共分为CINI、CINⅡ、CINⅢ三个级别,大多数级别低的CIN会自然消退或不进展,而级别高的CIN进展为宫颈癌的可能性很大。一种或多种致癌性人乳头瘤病毒(HPV)的持续感染被认为是导致CIN的重要因素,其中,高危型人乳头瘤病毒感染更是宫颈癌发生的必要条件[3]。由于感染HPV的妇女中只有很小部分会发展为宫颈上皮内瘤变甚至宫颈癌,因而宫颈癌仍是可防可治的疾病,其诊断和治疗对预防和降低宫颈癌发生具有极其重要的临床意义。本文将通过对在我院行宫颈冷冻治疗术的1110例患者进行观察与分析,评价宫颈冷冻治疗术对宫颈上皮内瘤变(CIN I)和HPV感染的治疗效果。
1 资料与方法
1.1 一般资料:2010年1月~2012年12月期间,在我院妇科门诊收治行宫颈冷冻治疗术患者共有1110例。其中,宫颈上皮内瘤变(CIN I)128例,HPV感染1个亚型630例,HPV感染2个亚型285例,HPV感染3个以上亚型67例。患者年龄30~64岁。
1.2 方法
1.2.1 仪器:采用TOITU-modelcR-201二氧化碳制冷仪。
1.2.2 实验室方法:HC2(Hybrid Capture 2)、液基细胞学检查法对患者进行检测。
1.2.3 治疗前准备:①选择月经干净后3~7 d进行,以减少出血和感染的机会;②治疗前查阴道分泌物,对有急、慢性外阴及阴道炎的患者,治疗后再作宫颈冷冻治疗;③询问患者有无冷刺激过敏史。
1.2.4 操作方法与技巧:①操作前准备:患者取膀胱截石位,以无菌溶液冲洗外阴和阴道,用窥阴器充分暴露宫颈,使用0.1%安尔碘对宫颈和阴道壁进行消毒;②操作:采用直接接触法,根据宫颈病变的程度和范围选择不同型号的冷冻探头,原则上冷冻探头的形状和面积大小应与宫颈病变面相一致。先将探头准确地放置在病变部位,与组织紧贴后开机降温,将治疗仪探头的温度降至-78℃,肉眼观察到与探头接触的组织形成白色冰霜。随着冷冻时间的延长,逐渐隆起白色冰球。时间控制在80~100 s,用2个冻-融循环,第1个周期冷冻结束。组织完全复温后,接着再重复冷冻一次。冷冻范围应控制在不超出病变约2 mm内。操作完毕关机后需等受冻组织自然复温与探头分开后,方可将探头取出;③疗效判断:宫颈冷冻治疗后6个月、12个月、18个月或24个月进行复查,行宫颈细胞学检查和宫颈HPV检查。痊愈:宫颈细胞学检查和HPV检查连续3次阴性;好转:宫颈HPV分型检查好了一种亚型或两种亚型;无效;宫颈细胞学检查和HPV检查阳性。
2 结果
收治患者中,宫颈CIN I与宫颈HPV感染者共1110例。结果显示,CIN I患者治愈率为95.3%(122/128)。HPV感染者治愈率分别为:1个亚型 97.1%(612/630),2个亚型85.3%(243/285),3个亚型以上52.2%(35/67)。绝大部分患者在冷冻治疗术后6个月或12个月复查行宫颈细胞学检查和HPV检查结果为阴性。大部分患者宫颈冷冻治疗的效果是满意的,总有效率达到96.1%(1067/1110)。见表1。
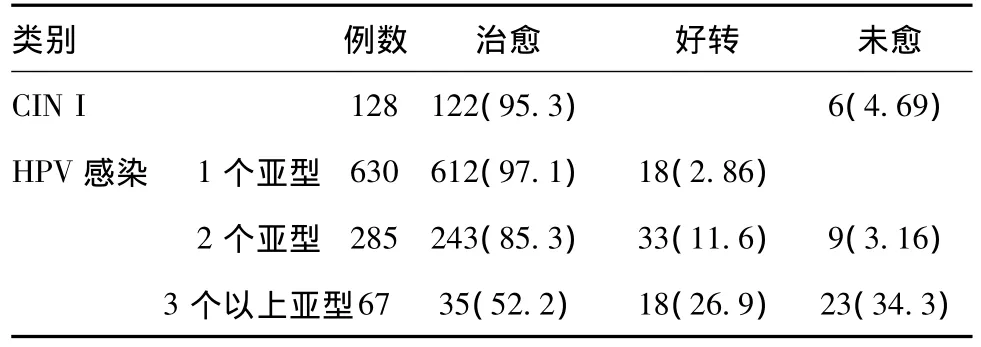
表1 宫颈CIN I和宫颈HPV感染不同程度治疗结果[例(%)]
3 讨论
3.1 冷冻术后注意事项:阴道排液是宫颈冷冻治疗术后最典型、最多见的现象。一般阴道排液的时间持续较长,是宫颈冷冻治疗的主要缺点。治疗后保持外阴清洁,在创面未完全愈合前应禁止性生活2个月,1个月内禁止阴道冲洗、盆浴、游泳等。宫颈冷冻治疗术后2周、2个月均需复诊。如有少量出血,属正常现象,若出血增多,超过月经量或出血时间过长,患者就诊时可及时采用宫颈创面喷凝血酶、阴道塞明胶海绵等方法,尽快止血。
3.2 宫颈冷冻治疗术的原理:宫颈冷冻治疗术的原理是利用超低温在细胞及亚细胞水平产生多方面的变化。癌细胞在-40℃时便不能生存,且温度越低,温度下降得越快,癌细胞就越容易被杀死[4]。采用低温冷冻治疗机进行制冷会快速产生超低温,使宫颈局部病变组织迅速冻结,从而使病变组织细胞内的液体结冰并形成冰晶。此时,细胞将会出现脱水反应,电解质浓度增加,蛋白质出现变性。如此一来,病变组织的局部毛细血管会被阻塞,微循环停止,冷冻区域继发全面缺血、凝固性坏死、透明性变,使坏死组织得以脱落。同时,冷冻复温的过程也对病变组织有破坏作用。最后,病变区域有正常细胞新生,创面得以修复。不少资料皆显示,把该技术用于治疗恶性肿瘤能取得良好效果。
冷冻术用于宫颈病变治疗始于1967年[5],经过四十余年的发展,至今已成为一项成熟可靠的医疗技术。近年来,随着宫颈病变的治疗方法不断增加,宫颈冷冻术在妇科的普及应用有所减少。但由于宫颈冷冻治疗术具有不产生热效应、不刺激增生的特殊性,在宫颈病变、尤其在宫颈上皮内瘤变的治疗中仍有着不可忽视的作用。世界卫生组织曾在2004年的宫颈癌筛查指南中对其给予了充分肯定。
3.3 HPV感染与CIN的关系:宫颈上皮内瘤变(Cervical intraepithelial neoplasias,CIN)是一组与宫颈浸润癌密切相关的癌前期病变的统称。目前几乎所有的流行病学调查与生物学资料都表明,HPV感染是宫颈癌及其癌前病变发病的必要条件[6]。资料显示,高危型HPV感染与子宫颈病变的发生相关,并随病变程度的加重,感染率增高[7]。依据不同型别HPV与肿瘤发生的危险性高低分为低危型HPV和高危型HPV。低危型 HPV 包括 HPV6、11、42、43、44 等类型,常引起外生殖器湿疣等良性病变,包括宫颈上皮内低度瘤变;高危型HPV包括 HPV16、18、31、33、35、39、45、51、52、56、58、59、68 等类型,可引起宫颈癌及其癌前病变[8-9]。HPV感染可使上皮细胞获得较高的增殖活性,也可能通过促进上皮细胞的过度增殖活性而癌变,但HPV阴性者患宫颈癌的风险几乎为零[10]。因此,可以把患者的转阴率作为治愈率的参考。
3.4 HPV感染和CIN I冷冻治疗疗效评价:本组资料共有患者1110例,128例患有宫颈癌前病变CIN I,982例患有HPV感染。从表1可以看出,经冷冻治疗后CIN I的治愈率达到95.3%,效果令人满意。而在HPV感染者中,1个亚型的治愈率最高,达到97.1%,2个亚型的治愈率也达到85.3%,效果依然显著。但3个以上亚型的治愈率只有52.2%。数据显示HPV感染的治疗效果随HPV亚型数量的增加而减少,表明HPV感染的治疗效果可能与HPV亚型数量有关,需进一步观察研究。本次研究数据的总体治愈率达到96.1%,显示宫颈冷冻治疗术对CIN I以及HPV感染两个亚型以内患者有明显的临床疗效,对于宫颈癌前病变与HPV感染的治疗有非常积极的意义,能在治疗宫颈癌前病变的同时,清除HPV感染,阻断宫颈病变进一步发展,降低宫颈癌的发生几率。
3.5 宫颈冷冻术在临床应用中的优势:宫颈冷冻术不需要用电,可在门诊进行治疗,不必加设大量医疗设备,节省空间;成本低廉,不需要额外的设备吸除治疗过程中产生的难闻的气味和可能对健康不利的激光烟柱等;费用较低,具有价格优势;在操作方面,其治疗所需时间短,无需麻醉,治疗过程简捷方便,容易掌握;疗效方面,其效果稳定、显著。本组1110例患者随访超过18个月,无术中和术后并发症的发生。患者在治疗过程中没有明显的疼痛感和出血,术后脱痂均匀无出血,无刺激组织增生,不易导致宫颈狭窄及粘连,对患者影响较少。此外,目前没有证据表明冷冻术治疗宫颈病变会对妊娠产生影响,所以冷冻术可以适用于未生育者。
综上所述,宫颈冷冻术对宫颈上皮内瘤变(CINⅠ)与宫颈HPV感染的疗效显著,尤其适用于病变范围小、级别低、要求保留生育功能的患者,是一种简捷、经济、不良反应少的有效治疗方法。
[1] 王凤岭,王弘锦,张书臣.宫颈癌的分类与治疗[J].中国美容医学,2012,7(3):47.
[2] 高 琼,吴伟民,莫益欢,等.宫颈刮片、阴道镜及HPV检测在宫颈癌筛查中的体会[J].吉林医学,2006,27(7):754.
[3] 赵 静.523例高危型HPV阳性患者液基细胞学及组织学检查结果分析[J].吉林医学,2013,34(25):5125.
[4] 王伦长,涂汉军,秦 军.临床冷冻治疗学[M].郑州:河南科学技术出版社,2005:73.
[5] Crisp WE.Cryosurgery treatment of the uterine cervix[J].AmJ Obstet Gynecol,1970,107(5):737.
[6] 王晓黎,崔红梅.HR-HPV检测、宫颈液基细胞学检查对宫颈病变筛查的评价[J].实用产科杂志,2010,26(8):594.
[7] 杨 杰,王风霞.高危型HPV病毒含量与不同程度子宫颈病变的关系研究[J].中国医学创新,2012,9(34):41.
[8] Stanley M.Immunobiology of HPV and HPV vaccines[J].Gynecologic Oncology,2008,109(2):S15.
[9] Parkin DM,Bray F.Chapter 2:The burden of HPV-related cancers[J].Vaccine,2006,24(3):11.
[10] 赵 虹,卢 丹.冷冻术治疗宫颈高危型人乳头瘤病毒感染疗效研究[J].中国全科医学,2011,14(14):1526.

