银掺杂TNA的光电性能及阻抗谱研究
田 甜,田小亭,周宏伟,白福全,王 强
(1.西北工业大学凝固技术国家重点实验室,西安 710072;2.中国兵器工业第五二研究所,包头 014034)
氧化钛纳米管阵列(Titania Nanotube Arrays,TNA)由于其优异的结构和光电性能而备受关注[1-3],并应用于太阳能染料敏化电池极板材料的研究.太阳能染料敏化电池是一种利用光电转换的低成本能源设备[4],电荷通过光生并在半导体材料与电解质中传导,从而产生电流.对于太阳能电池而言,低的光电子集收效率和低的光电子迁移速率是制约太阳能电池得以应用的两大重要因素.
氧化钛纳米管阵列为大比表面积提高光电子的集收效率和光电子的迁移速率提供了可能,因此,近年来有许多研究致力于氧化钛纳米管阵列在太阳能电池电极应用方面的研究[5-6],研究表明氧化钛纳米管阵列由于其直接依附于金属钛基底表面,可以直接作为光阳极使用,但在光电转换性能方面有待进一步改善和研究[7-9].
早期研究者在研究纳米氧化钛颗粒光电性能时发现,Pt,Au,Ag等纳米金属粒子沉积在纳米氧化钛颗粒表面能够有效提高氧化钛的光电性能[10-11].因为贵金属纳米粒子,如 Au,Ag等,能够在纳米氧化钛颗粒表面产生金属等离子体共振效应,进而增强氧化钛在可见光区域的光电性能[12-14].
氧化钛纳米管阵列作为一种新型结构材料被报导后,对于氧化钛纳米管阵列的掺杂研究,更多的集中在改善氧化钛纳米管阵列的光催化活性,而对于金属粒子掺杂改善其光电性能的研究相对较少.目前,可用于氧化钛纳米管掺银的方法较多,如粒子溅射法、气相沉积法、等离子喷涂法、电沉积法、紫外光诱导沉积法等,但粒子溅射效率较低,气相沉积法与等离子喷涂法成本较高,电沉积法工艺条件难控,且在材料表面形成的是枝状晶体.相较而言,紫外光诱导沉积法具有工艺简单易控、成本低廉、效率较高等优点.因此,本文采用紫外光诱导沉积法对氧化钛纳米管阵列进行掺银,研究了银掺杂后的氧化钛纳米管阵列的光电性能,并通过电化学阻抗谱研究了掺银氧化钛纳米管阵列的电化学性能.
1 实验
1.1 阳极氧化
将钛片(厚2 mm,纯度99.9%)剪切成1 cm×10 cm,封闭并预留研究工作面积1 cm×1 cm,经化学抛光后,依次用丙酮、无水乙醇和去离子水超声清洗,以钛片为阳极,以铂网为对电极,以0.1 mol/L HF和2.0 mol/L H2SO4混合溶液作电解液(试剂均为分析纯),外接直流电源,控制阳极氧化电压为20 V,在室温下进行阳极氧化1 h.氧化结束,立即取出阳极钛片,清洗干燥后得到TNA1.将TNA1放入电阻炉中在500℃下煅烧1 h,随炉冷却后,得到样品TNA2.为便于文章叙述,对不同的样品进行编号,如表1所示.

表1 样品编号
1.2 掺银
将TNA2浸入0.1 mol/L AgNO3+11.89 g/L聚乙二醇+10.1 g/L硝酸钾混合溶液2 min,用点光源光固机进行光沉积 Ag,紫外光波峰值为365 nm,光源强度为1 400 mW/cm2,开启光源后持续照射2 min,重复上述浸泡和照射工作3次后,用去离子水超声清洗样品表面,并在常温下烘干得到TNA3.
1.3 性能表征
样品表面形貌采用JSM-6390A电子扫描显微镜进行表征.光电性质测试在室温下进行,使用CHI660C型电化学工作站进行数据采集,分别以TNA1、TNA2、TNA3为工作电极(有效面积为1 cm2),辅助电极选用箔网,参比电极选用饱和甘汞电极(SCE),电解液为0.01 mol/L Na2SO4溶液,电解池选用石英烧杯,使用氙灯模拟太阳光(AM1.5,光强100 mW/cm2)作外照光源.其中短路电流开路电压曲线(J-V曲线)在-0.8~0.1 Vsce之间进行测量;瞬态光电流测试初始电位选为0.2 V,运行250 s,光源间歇持续时间为50 s.电化学阻抗谱(EIS)测试初始电位选为-0.29 Vsce,振幅为10 mV,频率范围为10 mHz~100 kHz.
2 结果与讨论
2.1 样品形貌分析
图1所示为TNA2表面形貌,从图1可以清晰地看到管口和管壁,其管径约为100 nm.图2(a)为TNA3表面形貌,部分管口被覆盖,且覆盖区域均匀分布于样品表面,部分管口仍然可见,覆盖层表现明显的絮状,图中白色亮区为团簇含银粒子.对材料表面进行能谱分析,如图2(b)所示,管口覆盖层为含银粒子.

图1 TNA2样品的表面形貌
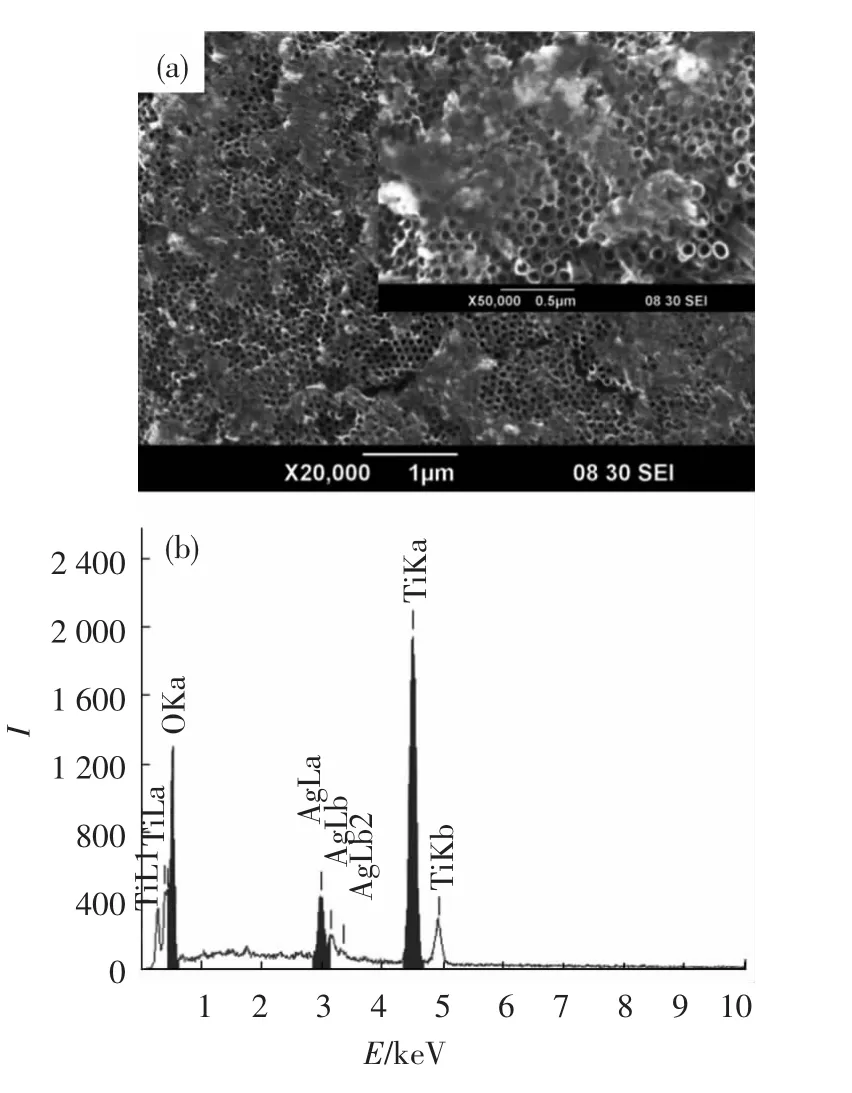
图2 样品TNA3的表面形貌(a)及能谱图(b)
样品表面在沉积银后,利用超声清洗,彻底清除易脱落粒子后,采用X射线衍射仪分析,谱图中未出现含银粒子的衍射峰.但根据硝酸银见光易分解(式(1)),认为管口覆盖层的Ag以单质形态存在.
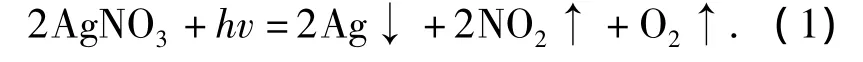
廖海达等[15]在研究银掺杂氧化钛纳米管阵列可见光光催化性能时,将氧化钛纳米管阵列在0.1 mol/LAgNO3溶液中浸泡30 min后,用紫外光照射10 min,获得的样品的XRD谱图中出现了单质银的特征衍射峰.由此可推断本试验样品中的银也是单质形态存在.氧化钛纳米管阵列内部结构难以表征,但结合氧化钛纳米管中空结构的特点,认为在管内可能也有Ag的存在,对于管口未覆盖区域的能谱显示也有银的存在,如图3所示TNA3管口可见区能谱图.
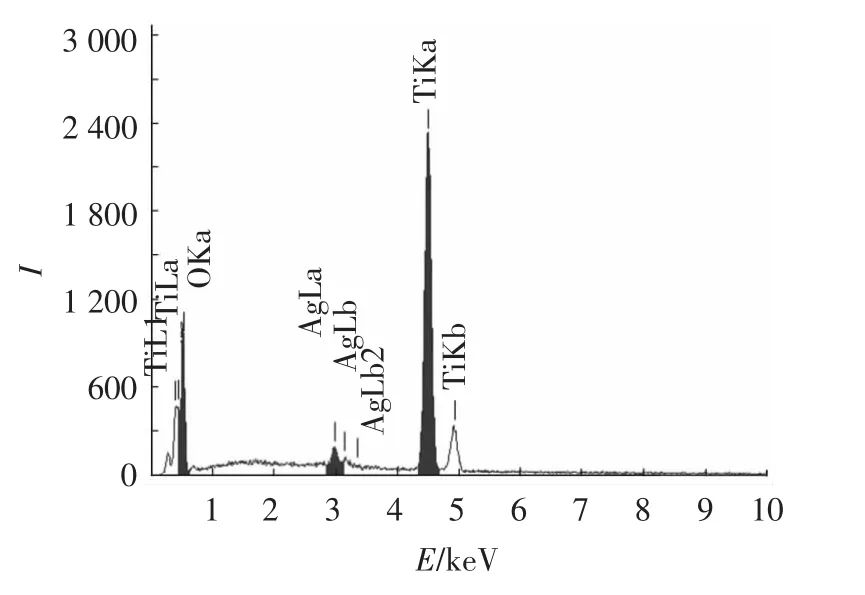
图3 样品TNA3管口可见区能谱图
2.2 样品光电性能分析
图4所示为样品瞬态电流变化图,可以看出TNA2样品(图4中 b曲线)具有较 TNA1样品(如图4中a曲线)更大的电流突变,说明氧化钛纳米管阵列经热处理后具有较好的光敏特征,这是因为经500℃热处理后,其晶体结构已经由无定形态转变为具有更优异光敏特性的锐态型结构[16].TNA3(图4中 c曲线)具有较 TNA2更大的电流突变,说明掺银氧化钛纳米管阵列具有更优异的光敏特征,银的掺杂能有效提高氧化钛纳米管阵列光敏特性.
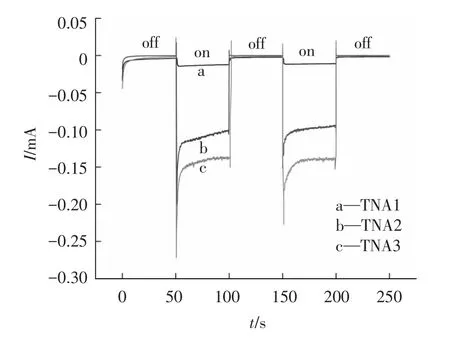
图4 样品的瞬态电流变化曲线
图5所示为样品的J-V图,可以看出,TNA3样品(如图5中c曲线)具有较TNA1和TNA2更大的短路电流,说明掺银氧化钛纳米管阵列具有更高的光电转换效率,银掺杂能有效改善氧化钛纳米管阵列的光电转换性能.
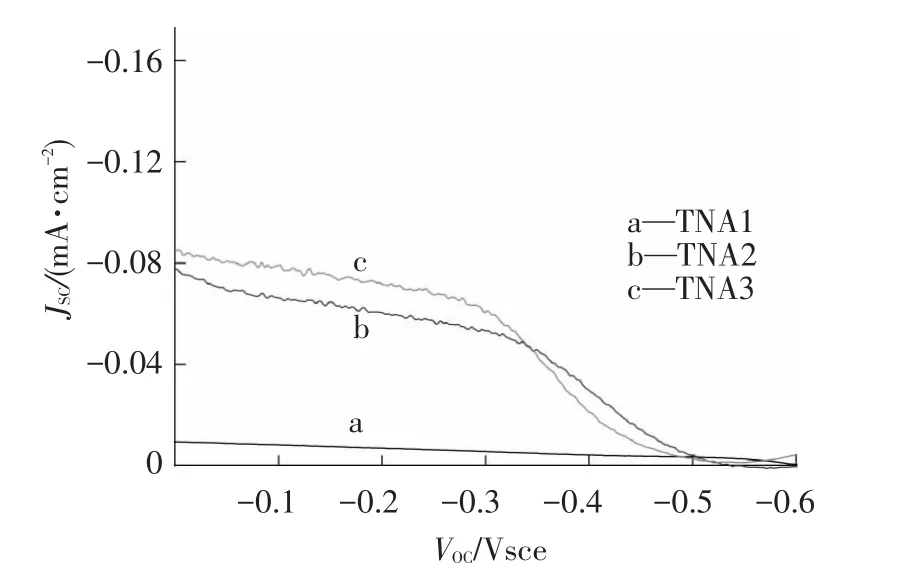
图5 样品的J-V曲线
2.3 样品阻抗谱分析
频率-相位角关系在一定程度上反映材料的电容/电阻特性.图6分别所示为TNA1、TNA2以及TNA3的频率(f)-相位角(θ)关系曲线.从图6中a曲线可以看到,TNA1在0.01~1 Hz的低频范围,相位角向-90°趋近,在1~100 000 Hz的高频范围,相位角向0°趋近,表现出非常明显的高频阻低频电容特性;从图6中b曲线可以看到,TNA2在0.1~10 Hz的低频范围,相位角向-90°趋近,在10~100 000 Hz的高频范围,相位角向0°趋近,表现出高频阻低频电容特性;从图6中c曲线可以看到,TNA3在1~100 Hz的低频范围,相位角向-90°趋近,在100~100 000 Hz的高频范围,相位角向0°趋近,表现出高频阻低频电容特性.
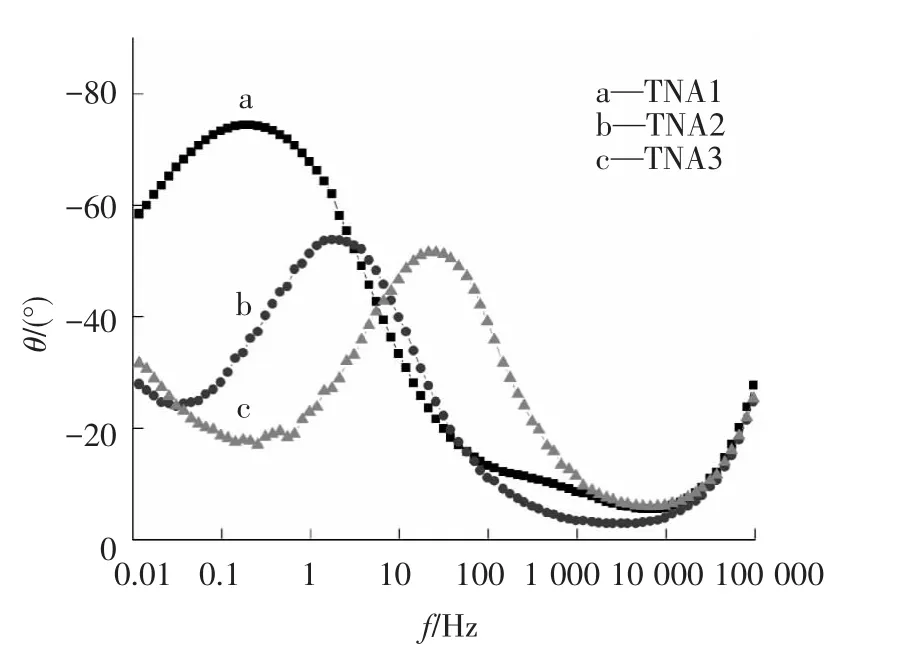
图6 样品相位角-频率关系曲线
3种样品均表现出高频阻低频电容特性,但在频率范围上有明显区别,图中峰值位置相位角最接近-90°,是材料表现电容特性最强的频率区域.TNA1的峰值明显大于样品TNA2及TNA3,且所对应频率更低,说明未热处理的氧化钛纳米管阵列在低频时表现的电容性更加明显,而经热处理的氧化钛纳米管阵列和掺银氧化钛纳米管阵列在低频时表现的电容性较小,这与热处理后氧化钛纳米管具有锐态型结构的氧化钛密切相关,因为锐态型氧化钛本身具有很好的半导体性能.TNA3相位角峰值处对应的频率向高频方向移动,说明掺银对氧化钛纳米管阵列的电化学性能有明显影响,能使其在较高频段(10~100 Hz)表现出一定的电容特性.
图7所示为频率(f)-阻抗(|Z|)关系,可以看出TNA3、TNA2、TNA1在整个频率范围,其阻抗逐渐减小,反应出样品的高频阻低频电容特性.样品TNA3的阻抗在整个频率范围基本上最低,电子在TNA3内部传输的阻力更小.阻抗越小,说明银掺杂能有效提高电子在氧化钛纳米管阵列内部的迁移速率.
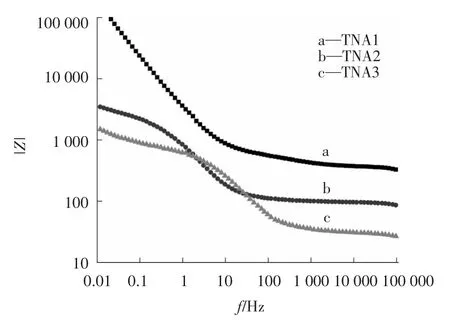
图7 样品的阻抗-频率关系曲线
2.4 掺银改性机理分析
TiO2是一种 n型半导体,其能带隙较宽3.2 eV,只能吸收波长小于387 nm的紫外范围的光子,且由于光生电子来不及转移而与空穴重新复合.有研究表明,用贵金属在氧化钛纳米颗粒表面沉积,能促进电子-空穴的有效分离,显著提高氧化钛的光催化活性[17-19].氧化钛纳米管阵列中空管阵结构以及其大比表面的特点,更有利于贵金属的掺杂改性.对于氧化钛而言,当一个具有一定能量的光子或者大于氧化钛禁带宽度的光子射入时,一个电子由价带(VB)激发到导带(CB),在导带上产生一个高活性电子,在价带上产生空穴,形成载流子,从而表现出氧化钛的光电效应.
氧化钛纳米管阵列经掺银修饰后,Ag的存在改变了氧化钛的电子跃迁和电子转移方式,被激发的电子可直接从费米能级较高的半导体氧化钛转移到费米能级较低的银粒子,或直接表现出光电效应,或进一步跃迁至导带再表现出光电效应.有研究表明[20],贵金属-氧化钛复合体系中,贵金属作为光生电子的接受器,可促进复合系统界面的载流子输运,光生电子在金属表面富积,而空穴则留在氧化钛表面.WU F等[21]在研究Ag掺杂改善氧化钛纳米管阵列的光催化活性时指出,银的掺杂除了能产生表面等离子共振效应,扩大氧化钛纳米管阵列光响应频率范围外,还能有效抑制氧化钛纳米管光生电子与光生空穴的复合.
图8所示为银掺杂改性氧化钛纳米管阵列光电性能示意图,图中示意了电子的跃迁和转移方式.银的介入,降低了电子跃迁需要的激发能量,并增加了光生电子转移的途径,从而有效地提高了氧化钛纳米管阵列的光敏特性和光电转换效率.
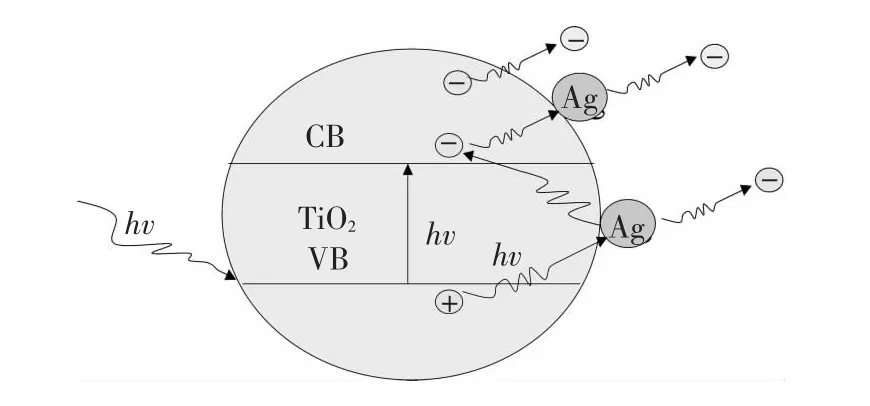
图8 银掺杂作用机理示意图
3 结论
银掺杂能有效提高氧化钛纳米管阵列的光敏特性和光电转换特性,且通过银的掺杂能使氧化钛纳米管在较高频段表现出电容特性.机理分析表明,银掺杂改善氧化钛纳米管阵列的主要原因是降低了电子跃迁需要的激发能量,增加了光生电子转移的途径.
[1] HAGFELDT A,GRATZEL M.Molecular photovoltaics[J].Acc Chem Res ,2000,33(5):269-277.
[2] MOR G K,SHANKAR K,PAULOSE M,et al.Enhanced photocleavage of water using titania nanotube arrays[J].Nano Lett,2005,5(1):191-195.
[3] QUAN X,YANG S,RUAN X,et al.Preparation of titania nanotubes and their environmental applications as electrode [J] .Environ Sci Technol,2005,39(10):3770-3775.
[4] O'REGAN B,GRATZEL M.A low-cost,high-efficiency solar-cell based on dye-sensitized colloidal TiO2films[J].Nature,1991,353:737-740.
[5] STERGIOPOULOS T,GHICOV A,LIKODIMOS V,et al.Dye-sensitized solar cells based on thick highly ordered TiO2nanotubes produced by controlled anodic oxidation in non-aqueous electrolytic media[J] .Nanotechnol,2008,19(23):235602-235607.
[6] XIE Z B,ADAMS S,BLACKWOOD D J,et al.The effects of anodization parameters on titania nanotube arrays and dye sensitized solar cells [J].Nanotechnol,2008,19(40):405701-405705.
[7] CHEN Q W,XU D S.Large scale,noncurling and free standing crystallized TiO2nanotube arrays for dye sensitized solar cells[J].J Phys Chem C,2009,113(15):6310-6314.
[8] LIU Z Y,SUBRAMANIA V,MISRA M.Vertically oriented TiO2nanotube arrays grown on Ti meshes for flexible dye sensitized solar cells[J].J Phys Chem C,2009,113(31):14028-14033.
[9] CHEN C C,JEHNG W D,LI L L,et al.Enhanced efficiency of dye sensitized solar cells using anodic titanium oxide nanotube arrays[J].J Electro Chem Soc,2009,156(9):C304-C312.
[10] CHEN L C ,CHOU T C.Photodecolorization of methyl orange using silver ion modified TiO2as photocatalyst[J]Industrial& Engineering Chemistry Research,1994,33(6):1436-1443.
[11] MOONSIRI M,RANGSUNVIGIT P,CHAVADEJ S,et al.Effects of Pt and Ag on the photocatalytic degradation of 4-chlorophenol and its by-products[J].Chemical Engineering Journal,2004,97(2-3):241-248.
[12] LOGAR M,JAN AR B,ŠTURM S,et al.Weak polyion multilayer-assisted in situ synthesis as a route toward a plasmonic Ag/TiO2photocatalyst[J].Langmuir,2010,26(14):12215-12224.
[13] AWAZU K,FUJIMAKI M,ROCKSTUHL C,et al.A plasmonic photocatalyst consisting of silver nanoparticles embedded in titanium dioxide [J].J Am Chem Soc,2008,130(5):1676-1680.
[14] CHRISTOPHER P,INGRAM D B,LINIC S.Enhancing photochemical activity of semiconductor nanoparticles with optically active Ag nanostructures:photochemistry mediated by Ag surface plasmons[J].J Phys Chem C,2010,114(19):9173–9177.
[15] 廖海达,梁沁沁,程龙,等.银掺杂TiO2纳米管阵列的制备及可见光光电催化性能研究[J].广西民族大学学报,2010,16(3):75-79.LIAO Haida,LIANG Qinqin,CHENG Long ,et al.Preparation of silver-doped TiO2nanotube arrays and its visible light photoelectrocatalysis activity [J].Journal of Guang Xi University for Nationalities,2010,16(3):75-79.
[16] TIAN Tian,XIAO Xiufeng,LIU Rongfang,et al..Study on titania nanotube arrays prepared by titanium anodization in NH4F/H2SO4solution [J].Journal of Materials Science,2007,42(14):5539-5543.
[17] TAUSTER S J,FUNG S C,GARTEN R L.Strong metal-support interactions. Group 8 noble metals supported on titanium dioxide [J].J Am Chem Soc,1978,100(1):170-175.
[18] ILIEV V,TOMOVA D,BILYARSKA L,et al.Photocatalytic properties of TiO2modified with platinum and silver nanoparticles in the degradation of oxalic acid in aqueous solution[J].Applied Catalysis B:Environmental,2006,63(3-4):266-271.
[19] SEERY M K,GEORGE R,FLORIS P,et al.Silver doped titanium dioxide nanomaterials for enhanced visible light photocatalysis[J].J Photoch Photobio A:Chem,2007,189(2-3):258-263.
[20] HOFFMANN M R ,MARTIN S T,CHOI W,et al.Environmental applications of semiconductor photocatalysis[J].Chem Rev,1995,95(1):69-96.
[21] WU F,HU X,FAN J,et al.Photocatalytic activity of Ag/TiO2nanotube arrays enhanced by surface plasmon resonance and application in hydrogen evolution by water splitting [J] .Plasmonics,2013,8(2):501-508.

