次氯酸钠氧化法去除电镀废水中的氨氮
胡小兵*,赵鑫,刘孔辉,叶星
(1.安徽工业大学建筑工程学院,安徽 马鞍山 243032;2.安徽工业大学生物膜法水质净化及利用技术教育部工程研究中心,安徽 马鞍山 243032)
电镀是公认的全球三大污染工业之一,电镀废水成分复杂、有毒物质种类多,如不处理而直接排放,会对环境造成严重污染,危害极大[1]。废水中的铬、镍、铜、镉、锌等采用现有处理技术已能实现回收[2-3]。生产中使用氨水、氯化铵等原料产生的氨氮大量存在于废水中。李冰璟等[4]采用铁碳微电解–水解酸化–好氧膜生物反应器工艺去除电镀废水中的COD(化学耗氧量)和氨氮,但生化处理周期长,运行管理复杂。现有其他处理技术主要是去除电镀废水中的有机污染物,还不能有效去除氨氮[5]。
次氯酸钠(NaClO)是一种常用强氧化剂,已用于多种废水处理[6-7]。张胜利等[8]用NaClO 氧化去除模拟废水中的氨氮,效果显著。顾庆龙[9]使用NaClO 氧化法去除二级生化出水中超标的氨氮,出水氨氮可达标排放。但有关NaClO 氧化法去除难处理工业废水中氨氮的研究尚未见报道。本文拟采用NaClO为氧化剂对电镀废水中的氨氮进行处理,主要考察氧化剂投加量、pH、曝气量等因素对氨氮去除效果的影响,探索NaClO去除电镀废水中氨氮的可行性。
1 实验
1.1 废水来源
苏州某金属工艺品公司电镀综合废水经预沉淀池、折流反应池、调节池、混凝沉淀池等构筑物处理后,除氨氮外,出水中其他指标均符合GB 21900–2008《电镀污染物排放标准》要求。取该公司电镀废水预处理出水为对象进行试验,其氨氮含量为105~115 mg/L,pH 约为1.25。每次试验取200 mL 废水,所用NaClO 溶液的有效氯含量为6%(质量分数)。
1.2 水质分析方法
氨氮按HJ 535–2009《水质 氨氮的测定 纳氏试剂分光光度法》,采用722s 可见分光光度计(上海精密科学仪器有限公司)测定。pH 按GB/T 27500–2011《pH值测定用的复合玻璃电极》,用pHS-25 数显pH 计(上海精密科学仪器有限公司)测定。
2 结果与讨论
2.1 NaClO 溶液投加量对氨氮去除率的影响
初步试验确定了pH=1.25、曝气量为0.40 L/min、反应时间为10 min,在此条件下考察NaClO 溶液的投加量对氨氮去除效果的影响,结果如图1 所示。
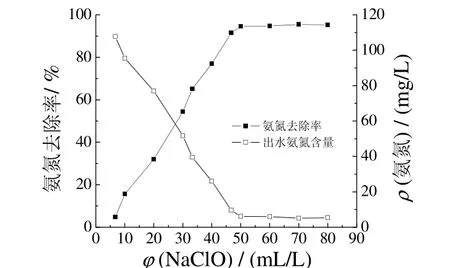
图1 NaClO 投加量对氨氮去除效果的影响Figure 1 Effect of NaClO dosage on removal efficiency of ammonia nitrogen
由图1 可知,氨氮去除率随NaClO 投加量增大而提高,在NaClO 投加量为50 mL/L时出现拐点,随后继续增大NaClO 溶液的投加量,氨氮去除率不再增大,表明废水中能被氧化的氨氮基本已被氧化完全,出水氨氮小于8 mg/L,去除率达94.59%。从理论上分析,要将1 g 氨氮全部氧化需要7.60 g 有效氯[9],则氧化1 L电镀废水中0.11 g 氨氮需要13.9 g NaClO 溶液,即需要15.30 mL 的NaClO 溶液。由于废水中所含氰化物和有机添加剂等还原性物质也要消耗 NaClO,因此NaClO 实际消耗量远超理论消耗量,至少要50 mL/L。
2.2 pH 对氨氮去除率的影响
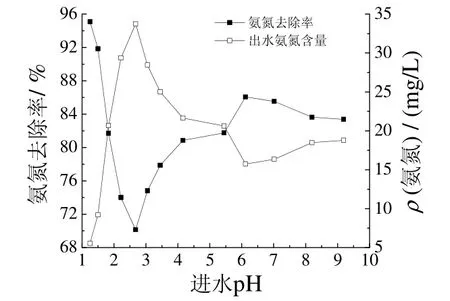
图2 pH 对氨氮去除效果的影响Figure 2 Effect of pH on removal efficiency of ammonia nitrogen
在NaClO投加量为50 mL/L、曝气量为0.40 L/min、反应时间10 min 的条件下,将进水pH 调节至不同值,考察pH 对NaClO 去除氨氮效果的影响,结果如图2所示。由图2 可知,随pH 升高,氨氮的去除率先下降后上升。pH为1.25时,氨氮去除率最高,达95.09%,但在pH为1.25~3.00 范围内迅速下降。由NaClO +H2O → HClO+NaOH 的反应可知,由于pH 升高,NaClO 溶液的氧化性能降低,导致氨氮去除率下降[8,10]。由于NH4+↔ NH3+H+,当pH 趋向于碱性时,水样中的分子态NH3所占比例越高,氨氮越容易被氧化[8],因此,在pH为3.00~6.00 范围内,氨氮去除率随pH升高而增大,峰值达86.07%。当pH 高于6时,随pH升高,氨氮去除率变化不大。因此,低pH 有利于NaClO对氨氮的氧化。
为考察NaClO 氧化对改善废水pH 的作用大小,测定了反应前后pH 的变化,结果如图3 所示。出水pH 随着反应前溶液pH 的增大而增大。在进水pH为1.25~6.00 范围内,反应后溶液pH 大幅升高;反应前溶液pH 大于6时,出水pH 基本稳定,保持在10 左右,高于GB 21900–2008 中pH为6~9 的要求。结合图2 可知,低pH 有利于氨氮的去除,出水pH 也低,可减少后续处理中因调节pH 而投加药剂的成本。因此,进水pH 应控制在1.50 左右为好。
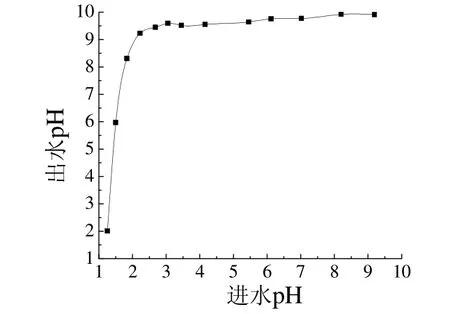
图3 反应前后的pH 对比Figure 3 Comparison of pH before and after reaction
2.3 曝气对氨氮去除率的影响
有研究表明,曝气可加快一些反应的速率,提高反应程度[11-12]。因此,为促进NaClO 对氨氮的氧化,采用曝气的方式进行搅拌,使氧化剂与废水充分混合。在pH=1.50、反应时间为10 min、NaClO 溶液投加量分别为30、40和50 mL/L 的条件下,考察不同曝气量对氨氮去除率的影响,结果如图4 所示。
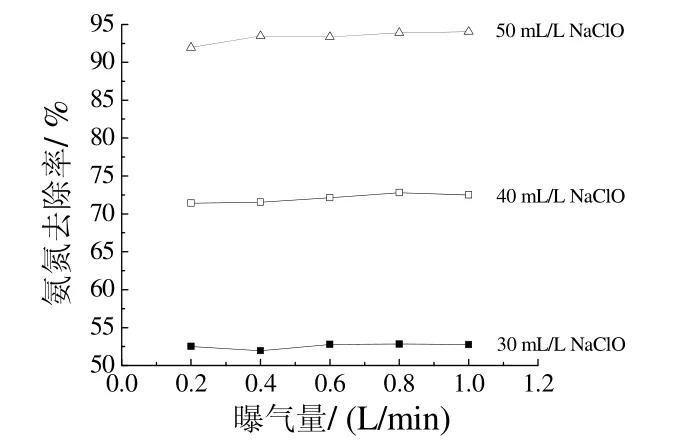
图4 曝气量对氨氮去除效果的影响Figure 4 Effect of aeration rate on removal efficiency of ammonia nitrogen
由图4 可知,曝气量从0.20 L/min 增加到1.00 L/min时,不同药剂投加量下的氨氮去除效果几乎没有变化。这是因为氧气的氧化性能远远低于HClO[7],且由于该反应在短时间内结束,因此曝气对氨氮去除基本没有影响。为再次验证曝气对氨氮去除没有影响,对比了pH=1.50、反应时间为10 min时曝气(曝气量为0.40 L/min)下和机械搅拌(搅拌速率为100 r/min)对氨氮去除率的影响,结果如图5 所示。
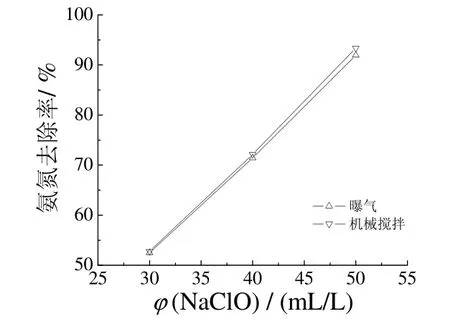
图5 搅拌方式对氨氮去除效果的影响Figure 5 Effect of agitation method on removal efficiency of ammonia nitrogen
由图5 可知,3种投加量在2种搅拌方式下的氨氮去除率基本相同。因此,曝气的作用只是使NaClO 溶液与废水完全混合,不能起促进氧化和提高氨氮去除效率的作用。工程中可使用其他成本较低的混合搅拌方式来代替曝气,或可以在有搅拌的后续处理工艺中投加NaClO,以节约工程成本。
3 结论
(1)NaClO 氧化法能有效去除电镀废水中的氨氮,使出水氨氮指标符合GB 21900–2008 要求,且该工艺运行简单、操作灵活、维护方便。
(2)在pH=1.25、曝气量0.40 L/min、反应时间10 min 以及NaClO 溶液(有效氯质量分数6%)投加量为50 mL/L 条件下,氨氮去除率最高,达到94.59%,出水氨氮仅为6.12 mg/L,且此时的NaClO 溶液投加量较少。综合考虑运行成本、氨氮去除率和有利于出水pH 达标排放,宜将反应前废水pH 控制在1.50 左右。
(3)曝气量对氨氮去除没有影响,曝气对氨氮氧化和去除效率的影响不大,只起与机械搅拌相同的混合作用,因此可采用成本较低的搅拌方式来进行药剂与废水的混合。
(4)实际工程中,药剂与水样的混合时间也是氨氮氧化反应的主要因素之一,因此今后应在中试条件下研究NaClO 溶液与大体积水样的完全混合时间。
[1]王文星.电镀废水处理技术研究现状及趋势[J].电镀与精饰,2011,33 (5):42-46.
[2]陈惠国.论电镀废水治理技术发展动态[J].电镀与环保,2001,21 (3):32-35.
[3]KALIDHASAN S,RAJESH N.Simple and selective extraction process for chromium(VI)in industrial wastewater [J].Journal of Hazardous Materials,2009,170 (2/3):1079-1085.
[4]李冰璟,付丹,赵伟.电镀废水中氨氮及COD 的去除[J].净水技术,2011,30 (5):115-118,154.
[5]赵璇,张蓓,李琛.电镀废水中有机污染物处理研究进展[J].云南化工,2011,38 (2):48-53,57.
[6]杨涛,傅金祥,梁建浩.次氯酸钠预氧化处理微污染水源水的试验[J].工业用水与废水,2005,36 (6):14-16.
[7]陆贤,刘伟京,涂勇,等.次氯酸钠氧化法深度处理造纸废水试验研究[J].环境科学与技术,2011,34 (3):90-92,133.
[8]张胜利,刘丹,曹臣.次氯酸钠氧化脱除废水中氨氮的研究[J].工业用水与废水,2009,40 (3):23-26.
[9]顾庆龙.次氯酸钠氧化法脱除二级生化出水中氨氮的中试研究[J].环境科学与管理,2007,32 (12):97-99,147.
[10]周相武,汪晓军,刘姣,等.次氯酸钠溶液的氧化性研究[J].氯碱工业,2006 (8):28-30.
[11]欧阳超,尚晓,王欣泽,等.曝气对电解除磷的影响研究[J].环境污染与防治,2009,31 (7):30-33.
[12]李庆宇,马楫,马国斌,等.曝气微电解–Fenton 氧化处理制药废水实验研究[J].广东化工,2011,38 (4):153-155.

