水处理实验中邻苯二甲酸酯类快速检测
张 键,宗 姗,周春洪,于林堂
(1.扬州大学 环境科学与工程学院,江苏 扬州 225009;2.扬州市 水利局,江苏 扬州 225009)
邻苯二甲酸酯 (phthalate acid esters,PAEs)又称酞酸酯,是常见的环境激素类污染物,其引起的污染已受到世界各国的普遍关注。邻苯二甲酸酯包括邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二乙酯(DEP)、邻苯二甲酸二丁酯(DBP),邻苯二甲酸二辛酯(DOP)、邻苯二甲酸丁基苄基酯(BBP)和邻苯二甲酸(2-乙基己基)酯(DEHP)。我国新的饮用水标准也已将PAEs列为非常规测定项目[1]。
为培养学生的动手能力,调动学生的学习积极性,提高学生的分析解决问题的能力和创新能力,扬州大学环境科学与工程院实验中心在给水排水和环境工程专业中开设了以曝气生物滤池处理为主要单元、以去除水中邻苯二甲酸酯类为主要指标的水处理实验[2-3]。实验中,邻苯二甲酸酯快速准确检测是实验的重要内容,也是对学生动手能力进行综合训练的途径。
有关邻苯二甲酸酯类的测定方法已有很多[4-8]。我国关于PAEs测定的方法主要为液液萃取-液相色谱法(HPLC)和液液萃取-气相色谱法(GC)。由于学生在实验过程中主要任务是对处理装置性能的了解,为了快速便捷地对水处理实验中的水质进行检验,有必要简化气相色谱检测的预处理工作。本实验采用固相萃取技术-GC检测法,对饮用水中微量PAEs(邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二丁酯(DBP)、邻苯二甲酸二正辛酯(DOP)和邻苯二甲酸(2-乙基己基)酯(DEHP))进行检测,简化了样品预处理工作,建立了一套快速简便、对环境污染少、分离效果好的检测方法。
1 仪器和试剂
仪器:GC-14B岛津气相色谱仪;10柱固相萃取装置(Agilent Technologies,U.S.A),UCT C18(500mg/6ml/50PKG)固相萃取小柱;N-EVAPTM氮吹仪(U.S.A)。
试剂:邻苯二甲酸二甲酯(DMP)(美国Aolocr公司);邻苯二甲酸二丁酯(DBP)(美国Aolocr公司);邻苯二甲酸2-(乙基己基)酯(DEHP)(美国Aolocr公司);邻苯二甲酸二辛酯(DOP)(美国Aolocr公司);正己烷(色谱纯,SCRC国药集团化学试剂优先公司);甲醇(色谱纯,上海市化学试剂一厂)。
2 实验方法
2.1 标准溶液的配制
用微量进样器将高浓度邻苯二甲酸酯标样(单标)精确配置成质量浓度为1 000mg/L的混合标准储备液,再用正己烷逐级稀释为500~50μg/L的标准样品备用。
2.2 气相色谱检测条件
柱型:DB-1石英毛细管柱(30m×0.32mm×0.25μm);载气:高纯氮(纯度≥99.99%),流量为1.0mL/min;进样口温度为250℃;检测器温度为300℃;分流比采用不分流;尾吹气流量为60mL/min;进样量为1μL;柱温(程序升温):开始温度为150℃,保持3min,然后以15℃/min的速度升至300℃,保持4min,共运行18min。根据色谱图中标样保留时间定性,根据峰面积积分对照标准曲线定量。
2.3 操作步骤
(1)实验用水样分别来自江苏省扬州市境内某乡镇水厂的取水河段和实验室水处理实验装置的出水。原水水样内有较多的水藻和悬浮物,为了避免杂质堵塞固相萃取小柱,先用三联过滤仪进行过滤,去除水藻和悬浮物。
(2)将C18固相萃取小柱安装在固相萃取装置上,用2mL左右甲醇通过小柱,浸泡2min,活化小柱,然后用蒸馏水多次洗涤固相萃取柱,将甲醇洗脱,使柱内无甲醇残留。
(3)将1L过滤后的水样缓慢通过固相萃取小柱,流速为8~10mL/min,以保证整个过程中柱子不被抽空;待水样全部通过后,用5mL重蒸馏水清洗柱体,并用平稳的气流继续抽吸10min;最后用10 mL左右正己烷洗脱吸附在小柱上的PAEs,将洗脱液通过无水硫酸钠脱水,贮存于浓缩瓶内,冰箱保存。
(4)将浓缩瓶置于萃取仪上的加热孔洞内,控温80℃;插入萃取针,确保纤维恰好浸入并处于中心位置;将洗脱液用N2浓缩至1.0mL,取浓缩液进行分析;萃取结束后退出纤维拔出萃取针,每次使用时进行空白试验,并确保连接针及纤维的清洁。
(5)为防止接触过塑料制品的试剂、蒸馏水、去离子水对分析结果的干扰,实验前对试剂、实验用水、玻璃仪器等进行净化处理,所用的玻璃器皿需要用清洁剂洗,再水洗、丙酮洗,然后用重蒸的正己烷和二氯甲烷清洗2次,于400℃下焙烘10h,并且测定试剂空白,进行比较和扣除。
3 结果与讨论
3.1 标样的测定
在上述气相色谱条件下,取1μL、质量浓度为10.00μg/L的PAEs混合标准储备液进样。测得的色谱图见图1,PAEs的4种异构体得到较好的分离,经单个标准样品定性,其出峰顺序依次为DMP(6.166 min)、DBP(10.907min)、DEHP(16.168min)和 DOP(16.774min),全程分离时间18min。
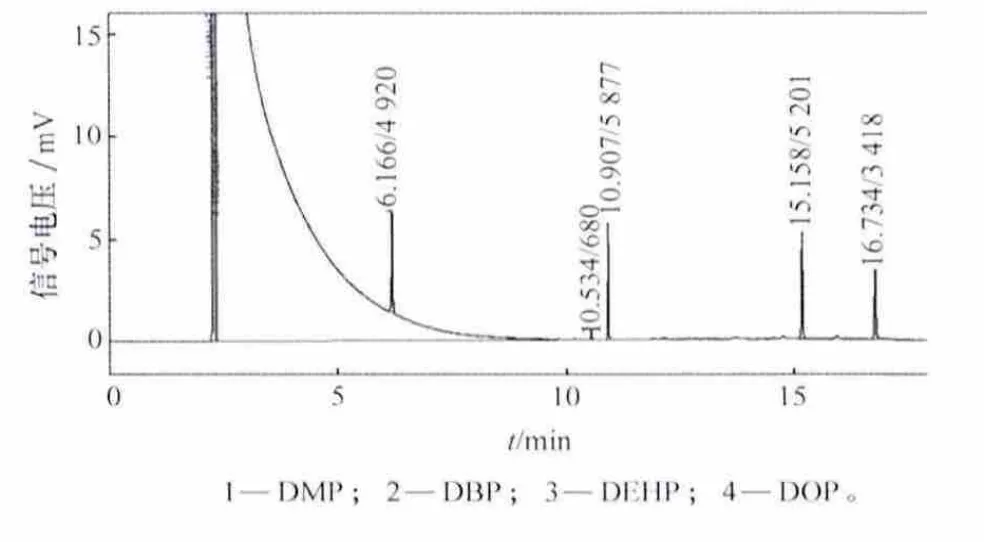
图1 邻苯二甲酸酯的标准气相色谱图
3.2 PAEs的工作曲线
分别 将 0.00、10.00、20.00、40.00、60、80.00、100.00μg/L的PAEs单体标准溶液进样,在选定的气相色谱条件下测定其峰高相应值,扣除空白后作的标准曲线见图2—图5。取3倍噪声的仪器信号所对应的分析的物质量浓度作为方法的检出限,相应的回归方程及其相关系数见表1。
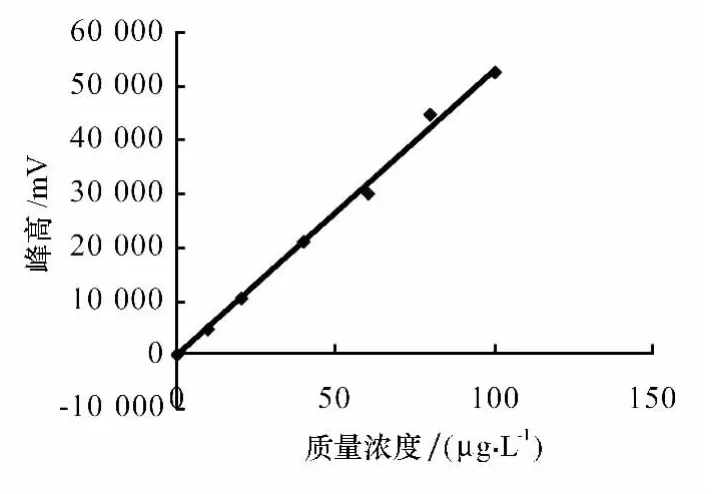
图2 DMP的标准曲线
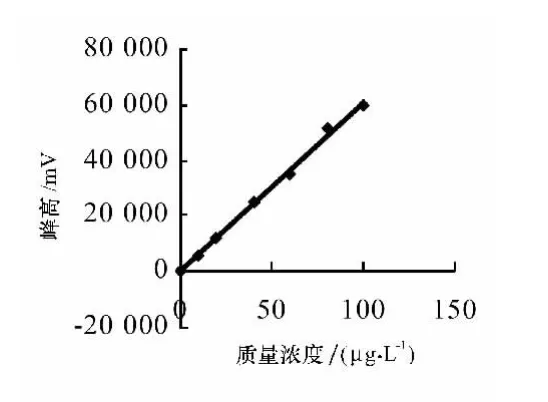
图3 DBP的标准曲线
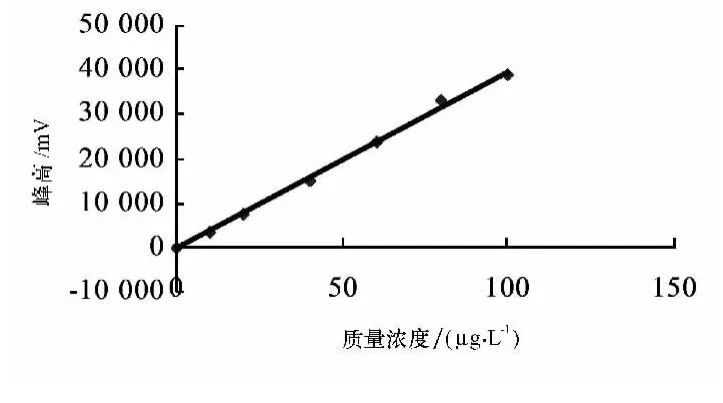
图4 DEHP的标准曲线
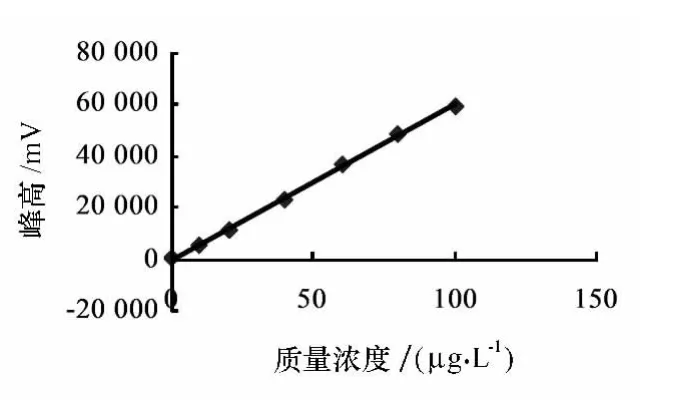
图5 DOP的标准曲线
重复测定混合标准溶液5次,检验方法的精密度,测定的质量浓度c数据见表2。DMP、DBP、DEHP和DOP的相对标准偏差(RSD)分别为3.5%、2.8%、3.4%和3.2%,均小于5%,表明该方法满足仪器分析的误差要求。
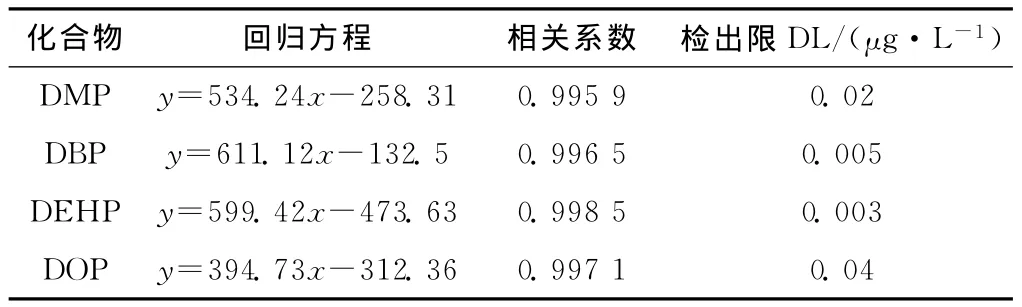
表1 气相色谱测定回归方程和线性关系
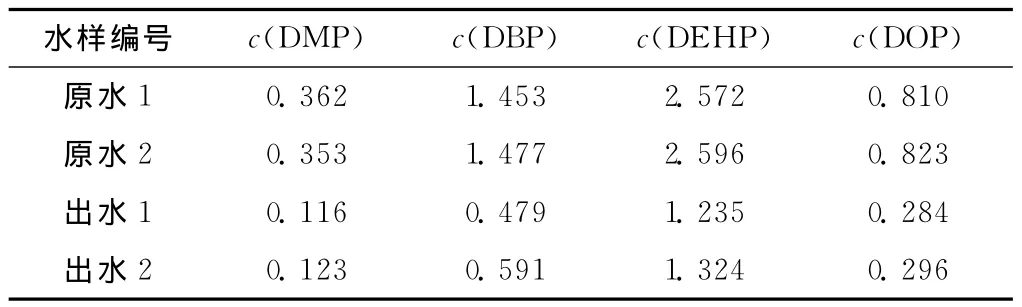
表2 水样PAEs的测定结果 μg/L
3.3 样品回收率和精密度的实验
对原水水样和处理后出水水样进行检测,测定结果见表2(每个样平行测定3次)。向样品中分别添加3个质量浓度的标准中间液:1.00、5.00、10.00μg/L,每个浓度做3个平行,每个平行设1个空白对照,按上述操作步骤预处理后测定回收率,结果见表3。所有水样的回收率都在90%~120%范围内。测定结果表明,本实验所建立的固相萃取-GC检测法是一种准确且适合于水处理实验中PAEs常规检测分析的方法,具有广泛的推广意义。
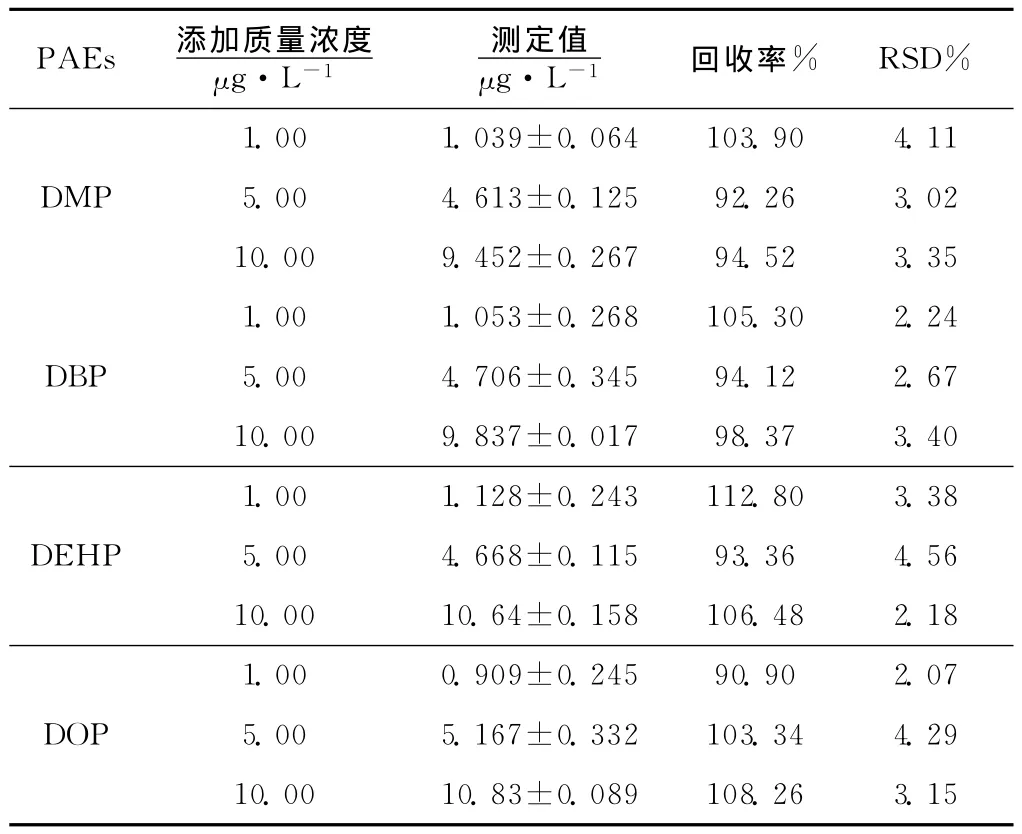
表3 回收率及精密度测定结果
4 结论
水处理实验中采用固相萃取-气相色谱法测定微量邻苯二甲酸酯类物质的方法能有效分离4种邻苯二甲酸酯类异构体,标准曲线线性回归相关系数均大于0.995 9,检测限可达0.003/μg/L,相对标准偏差为2.8%~3.5%,加标回收率为90.9%~112.8%。该方法的分离效果好,灵敏度、回收率高,上述几项指标均满足了学生水处理实验中对PAEs物质的快速测定的要求,且具有较好的可行性及适用性。
(
)
[1]余萍,康强.新旧版《生活饮用水卫生标准》的比较[J].安徽建筑工业学院学报:自然科学版,2009,17(3):80-81.
[2]桑军强,王占生.BAF在微污染源水生物预处理中的应用[J].中国给水排水,2003,19(2):21-23.
[3]吴为中,王占生.水库水源水生物陶粒滤池处理中试研究[J].环境科学研究,1999,12(1):10-14.
[4]Elefteria P.Hollow-fibre liquid-phase microextraction of phthalate esters from water[J].Journal of Chromatography A,2003(999):145-153.
[5]李敏霞,吴京洪,曾玮,等.液相微萃取-气相色谱法测定水样中邻苯二酸酯[J].分析化学研究简报,2006,34(8):1172-1174.
[6]张伟亚,杨左军,王成云,等.新型固相微萃取测定聚氯乙稀玩具制品在模拟人体汗液中的邻苯二甲酸酯增塑剂溶出量[J].化学世界,2003,44(10):520-523.
[7]Gabtiela Prokupkova,Katerina Holadova.Development of a solidphase microextraction method for the determination of phthalic acid esters in water[J].Analytica Chimica Acta,2002(457):211-223.
[8]Jara S,Lysebo C,Greibrokk T,et al.Determination of phthalates inwater samplesusing polystyrene solid-phase extraction and liquid chromatogra-phy quantification[J].Analytica Chemica acta,2000(407):165-171.

