沸石对水中磷吸附性能的初步研究
王 帅,周震峰,刁玲玲
(1.青岛农业大学资源与环境学院,山东青岛266109;2.青岛市环境保护局城阳分局,山东青岛266109)
随着社会进步和工业的快速发展,生活污水和工业废水大量产生并排入地表水体,导致水体中N、P等营养元素浓度升高,引发一系列环境问题。磷在水中有多种形态,包括有机磷酸盐、正磷酸盐和聚合磷酸盐,各种形态之间可相互转化[1]。磷在水中的浓度超过一定的标准,可能会导致水体发生富营养化[2]。目前,在我国的湖泊、水库、湿地等地表水体均存在不同程度的水体富营养化。在我国,已有城市污水处理厂的处理工艺对水中磷的去除率普遍较低,甚至难以达到我国颁布实施的《城镇污水处理厂排放标准》 (GB18918-2002)中的规定[3]。现在国内外常用的除磷方法主要有沉淀法、结晶法、混凝法、生物法、离子交换法和吸附法等[4]。化学法除磷效率较高,但会产生大量化学污泥;生物法除磷操作简单,但效率较低,不能处理浓度高的含磷废水;沉淀法、结晶法运行成本高且水质难达标,后处理困难;吸附法是高效且普遍适用的一种除磷法,它的关键在于吸附剂的选用。沸石具有吸附性、离子交换性、催化和耐酸耐热等性能,在污染处理工艺中应用广泛,国内已有部分学者利用改性沸石对水中磷的吸附性能进行了尝试性的研究工作,并取得了较好的效果[5~6],但由于沸石改性过程成本较高且存在二次污染的可能性,故在实际应用中存在一定的困难。
本研究以不同粒径的沸石为吸附剂,重点分析在不同条件下沸石对水体中磷的吸附效果,旨在探索沸石吸附水中磷的最佳工艺条件,为后续将沸石用于除磷工艺提供参考依据。
1 实验部分
1.1 实验材料
硫酸 (分析纯,莱阳市康德化工有限公司),抗坏血酸 (分析纯),钼酸铵 (分析纯,天津市化学试剂四厂凯达化工厂),酒石酸锑钾 (分析纯,天津市巴斯夫化工有限公司),磷酸二氢钾 (分析纯,天津市巴斯夫化工有限公司),沸石 (市售,用研钵磨碎过48目和20目筛子,分别用D48、D20表示)。
1.2 实验仪器
722E型可见分光光度计 (上海光谱仪器有限公司),TG328B型分析天平 (上海天平仪器厂),HY-5回旋振荡器 (国华电器有限公司),LD4-2低速离心机 (北京医用离心机厂),SHZ-82恒温振荡器 (国华电器有限公司)。
1.3 实验方法
磷的测定采用钼锑抗分光光度法[7~8]。先配100mg/L的磷酸二氢钾储备液,使用时再以蒸馏水稀释至所需浓度的磷酸盐溶液。在锥形瓶中加20ml 5mg/L左右的磷酸盐溶液和一定量的沸石,在20℃下震荡反应60min,振荡频率为240r/min,用离心机分离10min,取上清液于小烧杯中,然后移取5ml于50ml比色管中,加蒸馏水至标线处,然后加1ml抗坏血酸,30s后加2ml钼酸盐,显色15min,由标准曲线求出磷的浓度,计算沸石对磷的吸附量。
2 实验结果与分析
2.1 投加量对磷去除率的影响
分别在8个锥形瓶中依次加入0.5g、1g、2g、3g、4g、5g、7g、9g沸石 D48,再分别加入20ml 5mg/L磷酸盐溶液,在室温下振荡60min,结果见图1。磷的去除率随着沸石量的增加而增加,提高沸石投加量可增大吸附面积和吸附点位数。当沸石量接近7g时,磷去除率变得缓慢,表明吸附趋于平衡。沸石吸附能力有最大负荷,当超过负荷时,沸石就不能继续吸附磷,可能是因为溶液剩余浓度降低,磷在向沸石表面迁移过程中受到阻力,影响了吸附的进行。

2.2 pH对磷去除率的影响
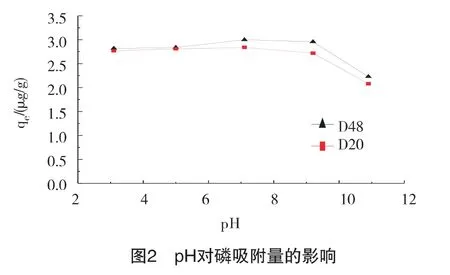
改变磷溶液的pH,保持质量浓度为5mg/L,分别在5个含有20ml 5 mg/L磷酸盐溶液的锥形瓶中加入7g沸石D48和D20,用1mol/L的NaOH和1mol/L的1/2 H2SO4调节溶液的pH分别到3、5、7、9、11,20℃下振荡60min,结果见图2。在相同的pH条件下,沸石D48吸附量略高于D20。在pH为3~9的条件下,沸石D48和D20对水中磷的吸附量均较高,当pH达到11时,吸附量开始明显下降,表明在实际应用中在较大的pH范围内利用沸石对水中磷进行吸附,均可以获得较好的去除效果。
2.3 反应时间对磷去除率的影响
分别在7个含有20ml 5 mg/L磷酸盐溶液的锥形瓶中加入7g沸石D48和D20,20℃下振荡反应时间分别为 3min、5min、10min、15min、30min、45min、60min,结果见图3。

由图3可以看出,沸石对磷的吸附率和吸附量随着反应时间的延长而逐渐升高,当反应时间快接近60min时,磷的去除率增加变得缓慢,这是因为随着时间延长,吸附接近饱和。在最初的15min内,吸附速率随反应时间的延长而快速增长,在60min时,D48和D20的吸附率分别达到了85.9%和79%,随后吸附基本达到平衡。在吸附的过程中,需要保证沸石和溶液有一定的接触时间,以充分利用沸石的吸附能力[9]。开始时吸附较快是因为磷主要吸附在沸石的表面,随着吸附时间的延长,水中磷浓度减小,需通过进入吸附剂的孔隙才能被吸附,因磷通过沸石孔隙的扩散速度减慢,吸附率会随时间缓慢增加,直至达到吸附平衡。根据试验数据和经济效益考虑反应时间宜为60min,可以保证较快的吸附速率,很好地反映吸附过程。沸石D48的吸附性略好于沸石D20,表明粒径越小,吸附性能越好。
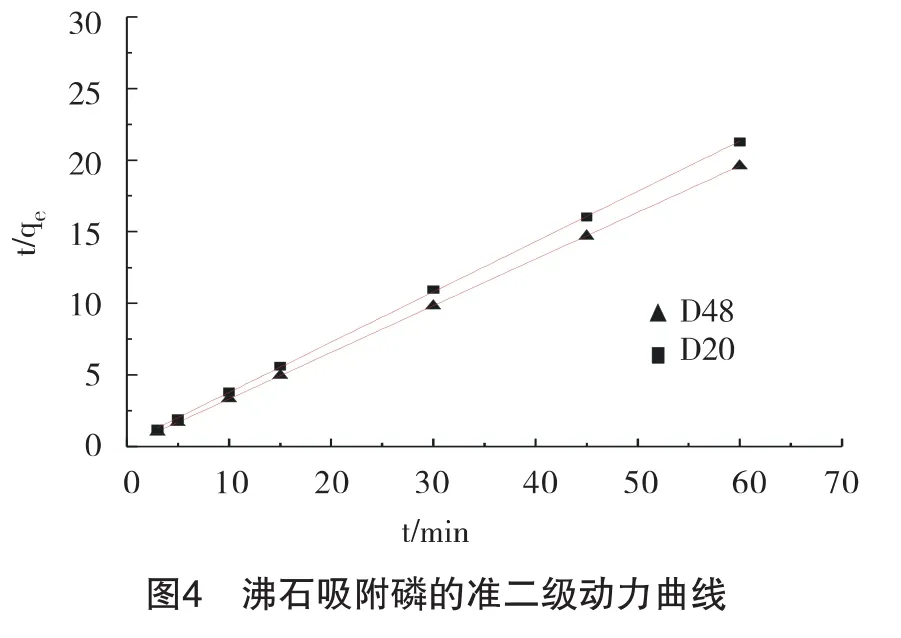

表1 吸附动力学拟合结果
利用拟二级速率方程对吸附动力学过程进行拟合,结果见图4,拟合参数见表1。由表1可知,拟二级速率方程拟合的相关系数非常接近于 1,拟合得到的 qe(D48)=3.07μg/g,qe(D20)=2.847μg/g,与实验 测定结果 qe(D48)=3.06μg/g,qe(D20)=2.82μg/g相差较小,相对误差分别为0.327%和0.957%,D48和D20的相关系数分别为1.0000和0.9998,这与Mahmut Ozacar和Bruno Kostura等的研究结果相一致[10~11],表明D48和D20对磷的吸附动力学规律遵循拟二级动力学模型。沸石对磷的吸附过程符合拟二级速率方程,说明吸附速率受磷浓度的影响大,吸附初期的磷浓度高,吸附速率较快,吸附后期的磷浓度下降,吸附速率变缓,吸附时间延长,吸附逐渐达到平衡。
2.4 温度对磷去除率的影响
称取7g沸石D48和D20各6份于锥形瓶中,分 别 加 入 1mg/L、5mg/L、10mg/L、15mg/L、30mg/L、50mg/L磷酸盐溶液各20ml,温度分别控制在15、20、35℃,振荡60min,结果见图5,拟合参数见表2。
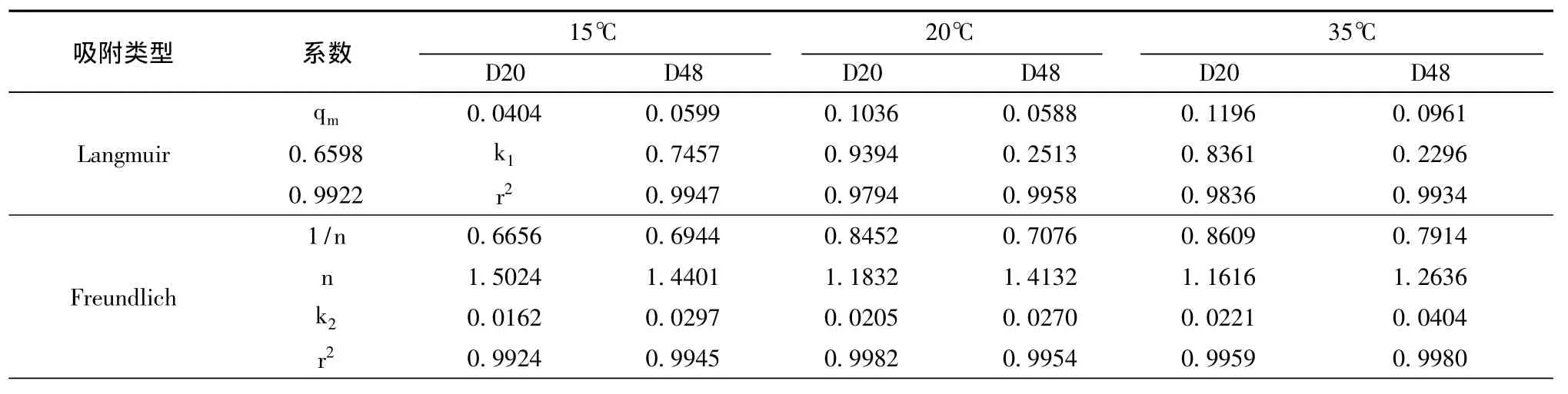
表2 沸石对磷的吸附等温线拟合结果
由图5可以看出,在相同条件下,沸石对磷的吸附量会随着磷的平衡浓度增大而增大,吸附量变化率随着磷的平衡浓度增大而加快[12]。Langmuir和Freundlich方程都能够很好地描述沸石对磷的吸附,其中,Freundlich吸附等温线数据点连起来更符合拟合曲线,说明本实验结果使用Freundlich等温式表征更适宜。由表2可以看出,在不同的温度下,Langmuir方程拟合的相关系数为0.9836~0.9947,而 Freundlich方程的拟合相关系数为0.9924~0.9982,进一步说明沸石对磷的吸附能更好地符合Freundlich方程所描述的规律,属于单分子层吸附[13]。1/n介于易吸附 (1/n=0.1~1)的范围,说明这三种温度都有利于沸石对磷的吸附,且n>1,所以该吸附是优惠吸附。

由表2还可以看出,当吸附温度为15℃时,沸石 D20、D48的吸附系数 k2分别是 0.0162、0.0297,温度为20℃时,粒径D20、D48时的系数k2分别是0.0205、0.027,温度为35℃时,粒径D20、D48的系数k2分别是0.0221、0.0404,在相同的温度条件下,D48的系数明显高于D20,粒径越小的沸石对磷的吸附能力越强。沸石 D48在35℃时吸附能力明显高于20℃、15℃,沸石D20的吸附能力随温度的变化不如D48的变化明显。总体来看,沸石对磷的吸附能力随着温度升高而逐渐增强,沸石的粒径越小,吸附效果越好,去除率越高。
3 结论
(1)沸石对磷的去除率随投加量的增加而升高,当投加量接近7g时,磷的去除率基本稳定。
(2)沸石对磷的吸附量在中性条件下最好,D48和 D20对磷的吸附量分别达到 3μg/g和2.84μg/g,在相同的pH条件下,D48对磷的吸附量高于D20。
(3)在最初的15min内,沸石对磷的吸附速率随反应时间的延长而快速增长,在60min时,D48和D20的吸附率分别达到85.9%和79%,基本达到平衡。吸附动力学过程可以用拟二级速率方程进行拟合,D20和 D48的拟合系数分别为0.9998、1.0000。
(4)在不同的温度下,Langmuir方程拟合的相关系数为0.9836~0.9947,而Freundlich方程的拟合相关系数为0.9924~0.9982,沸石对磷的吸附能更好地符合Freundlich方程所描述的规律。在相同的温度条件下,D48的吸附系数明显高于D20,表明粒径越小的沸石对磷的吸附能力越强。沸石D48在35℃时吸附能力明显高于20℃、15℃,沸石D20的吸附能力随温度的变化不如D48的变化明显。
[1]Correll D L.The Role of phosphorus in the Eutrophication of Receiving Waters[J].Journal of Environmental Quality,1998,27(2):261-266.
[2]金相灿.中国湖泊富营养化[M].北京:中国环境科学出版社,1990:20-30.
[3]Berg U,Donnert D,Ehbrecht A,et al.“Active filtration”for the elimination and recovery of phosphorus from waste water [J].Colloids and Surfaces A:physicochemical and Engineering Aspects,2005,(265):141-148.
[4]李超,朱邦辉.沸石吸附处理含磷废水的研究进展 [J].广东化工,2010,38(3):28-30.
[5]孙兴滨,韩金柱.沸石的改性及除磷性能研究 [J].东北林业大学学报,2010,26(2):162-164.
[6]周明达,张晖,邵凯,等.改性沸石处理含磷废水的实验研究 [J].环境污染与防治,2005,27(2):137-138.
[7]Ozacar Mahmut.Equilibrium and kinetic modeling of adsorption of phosphorus on calcined alunite[J].Adsorption,2003, (9):125-132.
[8]Bruno Kostura,Hana Kulveitova,Juraj Lesko.Blastmmace slaga as sorbems of phosphate from water solutions[J].Water Research,2005,(39):1795-1802.
[9]陈冠军,秦梦华.废纸酶法脱墨的研究进展 [J].生物技术,2002,12(1):40-41.
[10]胡湛波,王双飞.混合办公废纸纤维素酶脱墨的工艺研究[J].造纸科学与技术,2002,22(3):11-15.
[11]张兰泉,崔金贵,肖举强,等.沸石复合吸附剂除磷性能研究[J].兰州铁道学院学报,1999,18(2):116-120.
[12]蒋展鹏.环境工程学[M].北京:高等教育出版社,2005:148-152.
[13]Weber T W,Chakravorti R K.Pore and solid diffusion models for fixed bed adsorbers[J].America Chemical English,2010,56(19):228-238.

