参芪扶正注射液辅助治疗中晚期胃肠道恶性肿瘤的临床疗效分析
罗冬,周定明
(1.重庆三峡中心医院 消化内科,重庆 404000;2.重庆三峡中心医院 普外二科,重庆 404000)
中晚期胃肠道恶性肿瘤患者治疗以放化疗为主的综合治疗为主[1-2]。但是,放化疗引起的不良反应一直困扰学者们和临床医师。为此,学者们和临床医师一直致力于优化中晚期胃肠道恶性肿瘤患者的化疗效果。参芪扶正注射液是采用我国传统补气药物党参和黄芪为主要原料制成的纯中药制剂,在小儿视网膜母细胞瘤化疗和晚期非小细胞肺癌应用中收到满意的效果[3-4]。但是,迄今为止,关于该药在中晚期胃肠道恶性肿瘤患者中应用效果的报道甚少。本研究将参芪扶正注射液应用于90例中晚期胃肠道恶性肿瘤患者,收到满意的效果,现总结报道如下。
1 资料与方法
1.1 一般资料 选取重庆三峡中心医院2011年12月~2012年12月收治的90例中晚期胃肠道恶性肿瘤患者为研究对象。入选条件:①患者经过病理细胞学检查确诊为胃肠道恶性肿瘤;②患者Karnofsky评分在90分以上;③患者均接受放化疗综合治疗;④预计患者生存时间>3个月;⑤患者自愿参加本次调查研究,并签署书面知情同意书;⑥本研究方案经本院医院伦理委员会批准。排除标准:①患者有智力、听力或言语交流沟通障碍;②患者合并精神分裂症和双相障碍等重型精神疾病;③患者不愿意配合接受本研究。运用随机数字表法将中晚期胃肠道恶性肿瘤患者分为对照组和观察组,在对照组45例患者中,肿瘤部位:直肠癌患者19例,结肠癌患者16例,胃癌10例;年龄范围为45~73岁,平均(56.75±16.98)岁;在观察组45例患者中,肿瘤部位:直肠癌患者21例,结肠癌患者14例,胃癌10例;年龄范围为45~74岁,平均(56.87±16.68)岁。2组患者在性别构成、平均年龄和肿瘤部位构成等方面差异无统计学意义。
1.2 方法 2组患者均采用同一放化疗方案,观察组患者则在放化疗开始即联合应用参芪扶正注射液(丽珠集团利民制药厂生产的,国药准字Z19990065)250mL,静脉滴注,连续应用14 d为1个疗程,所有患者均在完成放化疗3个周期后再进行综合评价。
1.3 疗效评定标准[5]疗效标准依据RECIST 1.0版实体瘤客观疗效评价标准对部分缓解(与基线病灶长径总和相比,缩小30%)、完全缓解(所有目标病灶消失)、疾病稳定(基线病灶长径总和有缩小但未达部分缓解标准或有增加但未达进展进展标准)和疾病进展(原靶病灶长径总和增加>20%,且原靶病灶长径总和绝对值增加>5 mm,或出现新病灶)情况进行评估,治疗总有效率=完全缓解率+部分缓解率。
1.4 不良反应评价 抗癌药物不良反应按WHO抗癌药物急性与亚急性不良反应,分为0~Ⅳ级。
1.5 统计学方法 采用SPSS18.0统计软件包进行统计分析,等级资料的比较采用Wilcoxon秩和检验,采用t检验和χ2检验分别对正态计量资料和计数资料进行统计。以P<0.05为差异有统计学意义。
2 结果
2.1 2组患者临床疗效比较 观察组治疗总有效率为95.56%,对照组治疗总有效率为80.00%,差异有统计学意义(P<0.05,见表1)。

表1 2组患者有效率比较[n(%)]Tab.1 Comparison of clinical efficacy between two groups[n(%)]
2.2 2组患者不良反应比较 2组不良反应主要是血液学毒性和消化道不良反应,以Ⅰ~Ⅱ级为主,患者经过对症处理后均耐受,与对照组患者相比,观察组患者在恶心呕吐、腹泻、白细胞减少方面差异有统计学意义(P<0.05,见表2)。
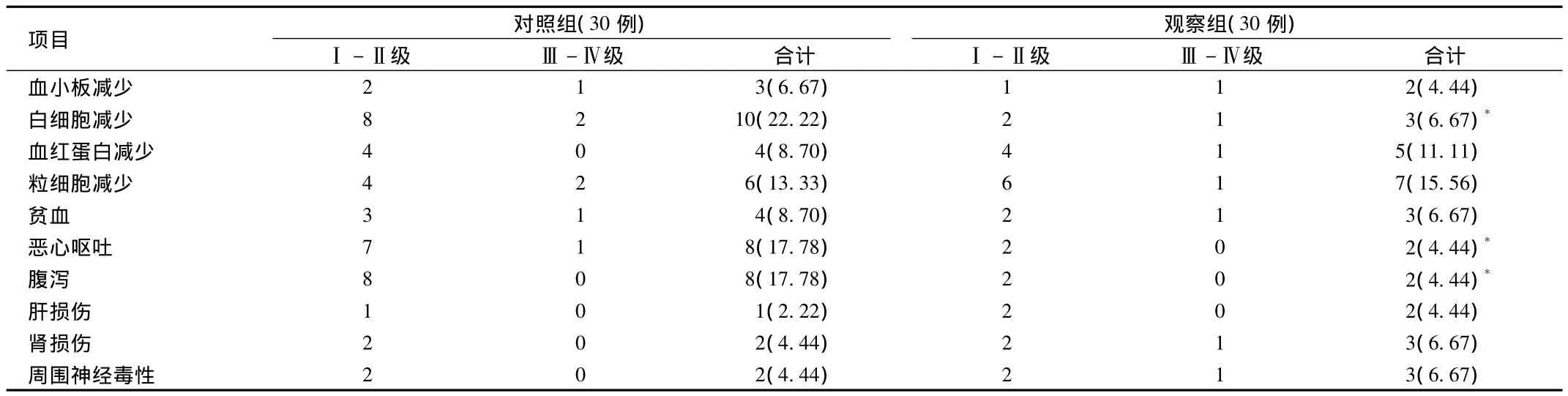
表2 2组患者不良反应比较[n(%)]Tab.2 Comparison of side effects between two groups[(%)]
3 讨论
本研究结果显示:观察组治疗总有效率为95.56%,对照组治疗总有效率为80.00%,差异具有统计学意义(P<0.05)。2组不良反应主要是血液学毒性和消化道不良反应,以Ⅰ~Ⅱ级为主,患者经过对症处理后均耐受,与对照组患者相比,观察组患者在恶心呕吐、腹泻、白细胞减少方面差异有统计学意义(P<0.05)。这与既往研究报道的结果类似[8-9]。究其原因可能与以下因素有关[10-12]:参芪扶正注射液是一种很好的生物免疫调节剂,含内含党参、黄芪为主药,根据中医辨证论治的理论,党参和黄芪意在补气扶正,能够明显增强机体非特异性免疫功能和调节患者体液免疫和细胞免疫,对患者有整体性调节作用。黄芪和党参中的有效成份有多种功效,比如抗肿瘤、抗突变、促进患者造血、保护骨髓功能、提高患者机体免疫功能和应激能力等。其中,党参不但能够提高患者网状内皮系统吞噬功能,而且还能够升高肿瘤患者淋巴细胞转化率。黄芪有促进患者细胞及体液免疫作用[13-14],而且还具有较强的解毒和增强患者免疫功能,同时,还能够明显升高患者白细胞、网状内皮系统、T细胞、LAK细胞、NK 细胞、L-2 抗癌活性[15]。
综上所述,参芪扶正注射液辅助治疗中晚期胃肠道恶性肿瘤临床疗效确切,并减少患者放化疗不良反应。
[1]Park KW,Lim do H,Lee SI.Malignant acanthosis nigricans in a patient with a gastrointestinal stromal tumor[J].Korean J Intern Med,2013,28(5):632-633.
[2]Stockman DL,Miettinen M,Suster S,etal.Malignant gastrointestinal neuroectodermal tumor:clinicopathologic,immunohistochemical,ultrastructural,and molecular analysis of 16 cases with a reappraisal of clear cell sarcoma-like tumors of the gastrointestinal tract[J].Am JSurg Pathol,2012,36(6):857-868.
[3]王一卓,黄东生,史季桐,等.参芪扶正注射液在小儿视网膜母细胞瘤化疗中的临床应用[J].儿科药学杂志,2013,19(8):8-11.
[4]盛蕾,方英立,徐森,等.参蔑扶正注射液辅助化疗治疗晚期非小细胞肺癌的系统评价[J].中国新药与临床杂志,2013,32(1):1-9.
[5]王为民,孔凡良,李成发,等.参芪扶正注射液联合多西他赛和顺铂治疗晚期非小细胞肺癌临床观察[J].安徽医学,2011,32(7):939-941.
[6]Hu QD,Zhang Q,Chen W,etal.Human development index is associated with mortality-to-incidence ratios of gastrointestinal cancers[J].World J Gastroenterol,2013,19(32):5261-5270.
[7]Zhou B,Zhang M,Wu J,etal.Pancreaticoduodenectomy versus local resection in the treatment of gastrointestinal stromal tumors of the duodenum[J].World JSurg Oncol,2013,11(1):196.
[8]Zhao JM,Wu AZ,Shi LR.Clinical observation on treatment of advanced gastric cancer by combined use of Shenqi Fuzheng injection,docetaxel,flurouracil and calcium folinate[J].Zhongguo Zhong Xi Yi Jie He Za Zhi,2007,27(8):736-738.
[9]Dai Z,Wan X,Kang H,etal.Clinical effects of shenqi fuzheng injection in the neoadjuvant chemotherapy for local advanced breast cancer and the effects on T-lymphocyte subsets[J].J Tradit Chin Med,2008,28(1):34-38.
[10]张文慧,王军,谭雅琴,等.参芪扶正注射液辅助化疗治疗老年胃癌30 例临床观察[J].包头医学院学报,2012,28(1):86.
[11]李武军,乐涵波,陈志军.参芪扶正注射液辅助化疗对肺癌患者急性化疗不良反应的影响[J].中国中医急症,2013,22(12):2142-2143.
[12]陈华兴.参芪扶正注射液辅助化疗治疗恶性肿瘤的临床疗效分析[J].肿瘤药学,2013,3(2):143-146.
[13]余胜珠,杨光华,冯金梅.参芪扶正注射液联合化疗治疗恶性肿瘤86 例临床观察[J].中西医结合学报,2006,4(1):84-86.
[14]任海华,钟方晓.参芪扶正注射液配合化疗治疗晚期恶性肿瘤的临床疗效观察[A].第二届国际中西医结合、中医肿瘤学术研讨会论文汇编[C].2004:825-827.
[15]李宁,杨卫兵.参芪扶正注射液配合化疗治疗中晚期恶性肿瘤疗效观察[J].四川中医,2005,23(7):44-45.

