胃癌的分子靶向治疗药物研究进展Δ
刘文婷,曹邦伟(首都医科大学附属北京友谊医院肿瘤科,北京 100050)
胃癌(Gastric cancer,GC)、胃食管连接部恶性肿瘤(Gastroesophageal junction,GEJ)是世界范围内第二大肿瘤性致死原因。肿瘤的发生率和分布与地域差异密切相关,远端胃腺癌主要发生于东欧、亚洲和南美,而近端胃癌和胃食管连接部肿瘤多发于西欧和北美。这是由于远端胃癌的发生与幽门螺旋杆菌感染以及一些营养和经济危险因素相关;相反的,近端胃和胃食管连接部腺癌的发生则与肥胖、反流性食管炎密切相关,致使其在西欧、北美发病率较高[1]。
1 目前晚期胃癌的治疗手段
外科手术以及内镜下黏膜切除术(Endoscopic mucosal resection,EMR)仍然是上消化道局部肿瘤的治疗标准。然而,大部分患者就诊时已为晚期。根据MAGIC试验[2]和ACCORD试验[3],在西欧,新辅助化疗已经成为GEJ/GC患者的标准治疗。新辅助化疗一般应用铂类联合氟尿嘧啶,或是包含紫杉类、蒽环类的三药联合方案。此外,新辅助放化疗是治疗胃食管连接部和远端食管腺癌的另一种选择方案。其中,部分患者可通过新辅助化疗可达到病理完全缓解(Pathological complete response,pCR)。同时,在北美,术后放化疗通过SWOG试验已成为胃癌的标准治疗方案[主要应用于未进行彻底淋巴结清扫的病人(D0或D1术式)][4]。在亚洲人群中,胃切除术和D2式淋巴结清扫术后的辅助化疗可延长总生存期(Overall survival,OS)。然而,超过50%的局部进展期GEJ/GC患者应用目前已有的多模式治疗最终仍然会复发。在远处转移的患者中,姑息化疗可延长患者的生存期。相关研究证实,在以铂类和氟尿嘧啶类为基础的化疗方案中加入紫杉醇可提高客观缓解率和疾病控制率。尽管如此,远处转移患者的中位生存时间仍停滞在12个月左右。
2 靶向治疗药物治疗胃癌的研究进展
近年来多种靶向治疗药物的不断研发,以其良好的疗效及低毒性应用于临床。
2.1 作用于生长因子受体的靶向药物
生长因子受体是位于质膜上的酪氨酸激酶受体蛋白。在胃肠道肿瘤中,目前已有两种不同药理学机制的药物应用于其靶向生长因子受体:(1)单克隆抗体(Monoclonal antibodies,moAbs):锚定于生长因子细胞外的抗原决定簇上,从而阻止配体-受体相互作用和受体二聚化激活。另外,单克隆抗体的一些特殊同型可以引发相关免疫机制,如抗体依赖性细胞毒作用(Antibody-dependent cellular cytotoxicity,ADCC)、补体依赖性细胞毒作用(Complement-dependent cytotoxicity,CDC),或是通过补充免疫系统的相关效应器细胞,从而消除抗体标记细胞。抗体或重组受体抗体结合蛋白可能也参与中和血管内皮生长因子(Vascular endothelial growth factor,VEGF)等促进肿瘤进展的配体。(2)小分子化合物:通过进入细胞内干扰酪氨酸激酶受体的酶功能或细胞内信号分子,从而阻止异常信号的传导[5],其在肿瘤细胞中的作用机制见图1。

图1 表皮因子受体抗体抑制剂作用机制
2.1.1 靶向作用于内皮生长因子受体(Endothelial growth factor receptor,EGFR)的抗体。西妥昔单抗(Cetuximab)和帕尼单抗(Panitumumab)已被证实,无论其单药或者与化疗联合均对转移性结直肠癌有效。此外,西妥昔单抗联合放疗或与铂类联用,使转移或复发的头颈部鳞状细胞癌(Head and neck squamous cell carcinoma,HNSCC)患者均可获益。
在转移性GC/GEJ中抗-EGFR单克隆抗体被广泛研究。一些Ⅰ期和Ⅱ期临床试验证实单克隆抗体联合化疗可获得良好的疗效及可耐受的不良反应。基于这些结果,两项研究进展期GEJ/GC的大型Ⅲ期临床试验得以进行。EXPAND试验对比了西妥昔单抗联合卡培他滨+顺铂,卡培他滨、顺铂联合西妥昔单抗组,其疾病进展期(Progression-free survival,PFS)、总生存期(Overall survival,OS)、总缓解率(Overall response rate,ORR)与对照组相比均无统计学差异[6]。REAL-3试验采用EOX方案(表柔比星+奥沙利铂+卡培他滨)±帕尼单抗也得出了相似的结果[7]。与此同时,抗-EGFR单克隆抗体在局部GC/GEJ的新辅助放-化疗或辅助化疗中的作用正被进一步探究(如NeoPECX试验,NCT01234324;SAKK75/08试验,NCT01107639)。
2.1.2 靶向作用于人类表皮生长因子受体2(HER2)的抗体。曲妥珠单抗和帕妥珠单抗通过触发受体的内化和介导抗体依赖细胞介导的细胞毒性作用(ADCC)过程,阻止HER2的异源二聚化。曲妥珠单抗单药或联合内分泌治疗已被证实可使HER2阳性的乳腺癌患者在辅助或姑息治疗中获益。基于此背景,ToGA试验[8]观察了曲妥珠单抗联合含以顺铂/氟尿嘧啶为基础的化疗的大规模随机对照试验应用于转移性HER2阳性的GC/GEJ的患者。试验结果显示,曲妥珠单抗的加入明显提高了ORR,同时PFS、OS的延长也具有统计学意义。在一项探索性事件后分析中得出,HER2高表达(免疫组化3+)或表达意义不明确(免疫组化2+)但基因扩增(FISH+)的患者在其中受益最大。因此,曲妥珠单抗联合以顺铂/氟尿嘧啶为基础的化疗成为HER2阳性的转移性GEJ/GC的标准治疗方案。Her-FLOT试验(NCT01472029)等正在进一步探索曲妥珠单抗在HER2阳性的局部进展期GEJ/GC患者围手术期治疗中的作用。相对于曲妥珠单抗,帕妥珠单抗是作用于HER2/ERBB2受体不同抗原决定簇的单克隆抗体。最近,基于CLEOPATRA试验,帕妥珠单抗联合曲妥珠单抗及多西他赛被用于HER2阳性的转移性乳腺癌的一线方案。正在进行的NCT01774786试验探索帕妥珠单抗+曲妥珠单抗联合化疗对于HER2阳性的转移性GEJ/GC的价值。
2.1.3 EGFR和HER2的酪氨酸激酶抑制剂。EGFR的酪氨酸激酶抑制剂(Tyrosine kinase inhibitors,TKIs)厄洛替尼(Erlotinib)、吉非替尼(Gefitinib)与泛-ERBB的TKIs阿法替尼(Afatinib)已被证实在转移性EGFR突变的非小细胞肺癌中有良好疗效。在一些小型Ⅰ期、Ⅱ期临床试验中,探索了厄洛替尼和吉非替尼单药或与化疗联合在GEJ/GC中的作用,但其不佳的结果导致未能进行Ⅲ期临床探索。关于阿法替尼在晚期胃癌中的Ⅱ期临床试验NCT00970138研究了144例二线化疗失败的晚期胃癌患者,试验的首要终点OS和次要终点PFS都得到了阳性结果[9]。相关的Ⅲ期临床试验正在进行中。
拉帕替尼(Lapatinib)是针对EGFR和HER2的双靶点靶向药物,其联合卡培他滨、曲妥珠单抗或与内分泌治疗联用适用于HER2阳性的晚期乳腺癌患者。LOGIC试验研究了拉帕替尼联合卡培他滨+奥沙利铂在HER2阳性的GEJ/GC患者中的一线治疗,但该临床试验的主要终点OS却无统计学差异,试验结果失败。探究拉帕替尼联合紫杉类在亚洲ERBB2阳性的胃癌患者中的作用同样在主要试验终点上得到了失败的结果。
2.2 作用于间质上皮转化因子的靶向药物
间质上皮转化因子(Mesenchymal epithelial transition,MET)受体酪氨酸激酶正常情况下表达于人体干细胞,它在胚胎发育和伤口愈合过程中扮演重要角色。肝细胞生长因子(Hepatocyte growth factor,HGF)的天然受体是由间质细胞分泌。但是,除了在这些正常过程中发挥作用之外,HGF/MET信号也会促进肿瘤迁移、侵袭和血管形成。约10%~15%的胃癌患者出现MET基因扩增,还有高达30%的患者存在MET蛋白表达增高,这两种情况均与预后呈负相关。多项肿瘤样本的回顾性研究显示MET表达与抗-MET靶向抗体的作用呈正相关。最近,两项关于抗-MET单克隆抗体Onartuzumab和Rilotumumab联合化疗MET过表达的进展期GEJ/GC患者的大型Ⅲ期随机对照试验正在进行。MetGastric(NCT01662869)试验共纳入800例患者,给予FOLFOX6(氟尿嘧啶+奥沙利铂+叶酸)联合或不联合Onartuzumab。另一项临床试验RILOMET-1(NCT01697072)则是在纳入的450例MET表达阳性的进展期GEJ/GC患者中给予ECX(表柔比星+顺铂+卡培他滨)联合或不联合Rilotumumab作为一线方案。
2.3 哺乳动物雷帕霉素靶蛋白复合物抑制剂
哺乳动物雷帕霉素靶蛋白(mTOR)是近年来发现的一种非典型丝氨酸/苏氨酸蛋白激酶,它是PI3K/Akt通路的下游分子,可接受生长因子、营养、能量等多种信号,是细胞生长和增殖的关键调节分子。西罗莫司和依维莫司可用于进展性肾细胞癌的治疗。此外,依维莫司还适用于胰腺内分泌癌或与芳香化酶抑制剂联用治疗激素受体阳性的转移性乳腺癌。GRANITE-1试验是一项比较依维莫司作为GC/GEJ二线或三线用药的大规模多中心安慰剂对照的Ⅲ期临床试验,虽然中位PFS和疾病缓解率在依维莫司组都得以延长,但试验的主要终点OS却未见延长。正在进行的Ⅲ期临床试验RAD-PAC(AIO-STO-0111,NCT01248403)比较了胃癌的二线治疗中依维莫司联合培美曲塞的作用,让我们期待其结果。
2.4 抗血管生成药物
异常的肿瘤血管生成是癌症的重要特点,在肿瘤进展过程中肿瘤组织的低氧和营养消耗环境促使血管生成。由肿瘤细胞和基质细胞分泌的VEGF在肿瘤组织新生血管生成中起重要作用。常见的抗血管生成药物包括moAbs贝伐单抗和TKIs索拉非尼、舒尼替尼。其对肿瘤细胞的作用机制见图2。
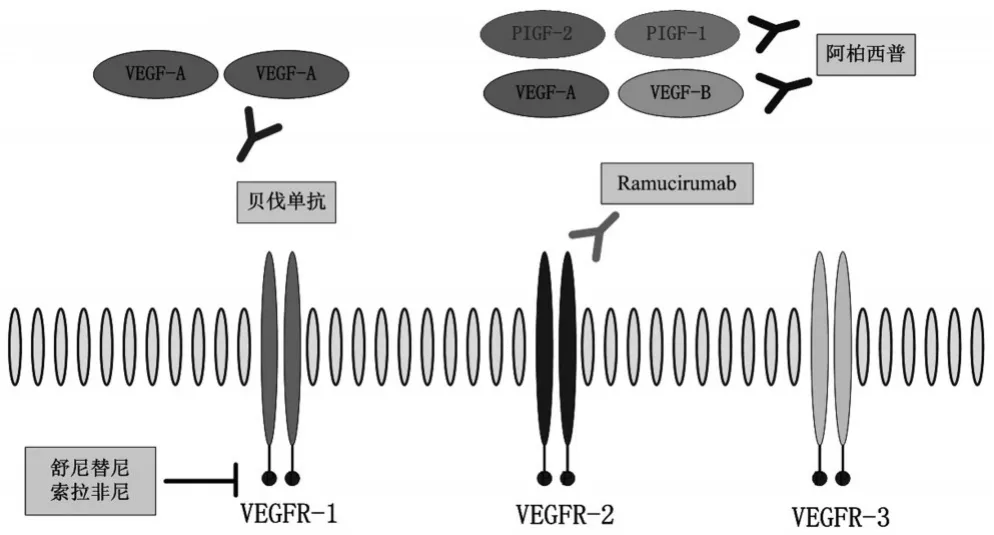
图2 抗血管生成药物的作用机制
2.4.1 抗VEGF单抗。目前贝伐单抗已应用于结直肠癌、卵巢癌、非小细胞肺癌以及与干扰素联用应用于肾癌。在欧洲,其还可应用于转移性乳腺癌。大型的Ⅲ期临床试验AVAGAST研究了贝伐单抗联合卡培他滨和顺铂在姑息化疗中对GC/GEJ患者的作用。在贝伐单抗组,中位PFS和ORR都有延长,但试验的主要终点OS却未得到阳性结果[10]。一项该试验的回顾性亚组分析显示:高表达VEGF-A、同时低表达神经纤毛蛋白质-1的患者获益更多。
2.4.2 TKIs。舒尼替尼和索拉非尼是多靶点TKIs,可直接作用于VEGF受体和其他TKIs。索拉非尼联合铂类化疗在GC/GEJ的Ⅱ期临床试验获得了有益的结果。Ⅲ期临床研究正在进行中。
2.4.3 抗VEGF抗体(VEGFR)单抗。抗VEGFR单抗Ramucirumab在Ⅲ期临床试验REGARD中得到了良好的结果。试验中Ramucirumab组中位PFS和OS都得到了提高。另一个关于Ramucirumab的Ⅲ期临床试验RAINBOW比较了紫杉醇联合Ramucirumab或安慰剂,主要试验终点OS在试验组中延长了2个月(9.63个月vs.7.36个月)。
3 结语
晚期胃癌的化学治疗尚无明确的标准方案,联合分子靶向治疗已是未来的治疗趋势[11]。目前,大部分靶向治疗药物仅是针对单一信号通路或靶点发挥作用,而胃癌的发生、发展过程是多环节共同作用的结果,故我们应将多靶点靶向药物作为后期的研究方向。靶向药物大多价格昂贵,且延长总生存期有限,因此寻找其相关的疗效标志物以筛选优势人群同样也是今后研究的重要方向[12]。
[1]Catalano V,Labianca R,Beretta GD,et al.Gastric cancer[J].Crit Rev Oncol Hematol,2009,71(2):127-164.
[2]Cunningham D,Allum WH,Stenning SP,et al.Perioperative chemotherapy versus surgery alone for resectable gastroesophageal cancer[J].N Engl J Med,2006,355(1):11-20.
[3]Ychou M,Boige V,Pignon JP,et al.Perioperative chemotherapy compared with surgery alone for resectable gastroesophagealadenocarcinoma:an FNCLCC and FFCD multicenter phase Ⅲ trial[J].J Clin Oncol,2011,29(13):1715-1721.
[4]Smalley SR,Benedetti JK,Haller DG,et al.Updated analysis of SWOG-directed intergroup study 0116:a phaseⅢtrial of adjuvant radiochemotherapy versus observation after curative gastric cancer resection[J].J Clin Oncol,2012,30(19):2327-2333.
[5]张圣林,刘春丽,王淑萍,等.分子靶向药物治疗胃癌的研究进展[J].广东医学,2012,33(7):1026-1029.
[6]Lordick F,Kang YK,Chung HC,et al.Capecitabine and cisplatin with or without cetuximab for patients with previously untreated advanced gastric cancer(EXPAND):a randomised,open-label phase 3 trial[J].Lancet Oncol,2013,14(6):490-499.
[7]Waddell T,Chau I,Cunningham D,et al.Epirubicin,oxaliplatin,and capecitabine with or without panitumumab for patients with previously untreated advanced oesophagogastric cancer(REAL3):a randomised,open-label phase 3 trial[J].Lancet Oncol,2013,14(6):481-489.
[8]Bang YJ,Van Cutsem E,Feyereislova A,et al.Trastuzumab in combination with chemotherapy versus chemotherapy alone for treatment of HER2-positive advanced gastric or gastro-oesophageal junction cancer(ToGA):a phase 3,open-label,randomised controlled trial[J].Lan⁃cet,2010,376(9742):687-697.
[9]Li J,Qin S,Xu J,et al.Apatinib for chemotherapy-refractory advanced metastatic gastric cancer:results from a randomized,placebo-controlled,parallel-arm,phase Ⅱtrial[J].J Clin Oncol,2013,31(26):3219-3225.
[10] Ohtsu A,Shah MA,Van Cutsem E,et al.Bevacizumab in combination with chemotherapy as first-line therapy in advanced gastric cancer:a randomized,double-blind,placebo-controlled phase Ⅲ study[J].J Clin Oncol,2011,29(30):3968-3976.
[11] 高丹丹,刘磊.晚期胃癌化疗及分子靶向治疗研究进展[J].中国肿瘤临床,2012,39(23):1978-1981.
[12] 曹怀刚.食管胃癌的靶向药物治疗进展[J].实用癌症杂志,2011,26(5):536-539.

