HPLC法测定鲜食葡萄采后贮藏过程中糖分的变化∗
林江丽,朱亚娟,王金霞,封顺,王吉德
(新疆大学 化学化工学院,新疆石油天然气精细化工教育部和自治区重点实验室,新疆 乌鲁木齐 830046)
葡萄果实中除水分之外,糖含量最高,其中以葡萄糖、果糖为主.葡萄果实在贮藏期间由于自身代谢,会消耗葡萄果实内的糖分[1].目前,市售葡萄大都采用SO2缓释保鲜剂并辅以低温贮藏,抑制酶活性以延长贮藏期,但SO2也能与葡萄果实中的还原糖等化合物发生反应[2],这在一定程度上也影响贮藏过程中果实中糖含量的变化.
糖含量的检测方法有比色法[3,4],旋光法,气相色谱法[5]、液相色谱法[6]等.高效液相色谱法因其操作简便,可快速、准确地分析各种单糖和多元醇,因此近年来用液相色谱法测定食品中糖的组成和含量得到了快速发展[7∼11].关于葡萄中的白藜芦醇,花青素及多酚等的研究报道较多,但对其糖分的测定未见报道.本实验采用液相色谱法对不同时期,不同贮藏条件下鲜食葡萄中的糖分进行测定,并对不同贮藏期果实中糖含量的变化趋势进行分析,为鲜食葡萄采后贮藏中葡萄风味品质的评价提供参考.
1 材料与方法
1.1 材料
供试材料为新疆常见的红提葡萄,采自新疆三坪农场红提葡萄种植园.采摘后的葡萄采用两种贮存方式:第一种方式为葡萄样品直接进行低温冷藏贮存(Blank);第二种方式为葡萄样品使用SO2缓释型保鲜纸并辅以低温冷藏贮存(SO2处理).为了对鲜食葡萄样品贮藏过程中糖分的变化规律进行研究,定时对两种贮存方式的葡萄样品进行采样,直至葡萄样品完全失去食用价值.
1.2 仪器和试剂
LC-10Avp高效液相色谱仪(日本SHIMADZU公司制造),Coulter Avanti J-25高速离心机(美国 BECKMAN公司制造),DF-101S集热式磁力加热搅拌器(金坛市医疗仪器厂生产),葡萄糖,果糖,蔗糖为国产分析纯,乙腈为Dikama公司色谱纯,实验用水均为电阻率不低于18.2 MΩ.cm−1的高纯水.
1.3 标准溶液的配置
参照文献[6],准确称取葡萄糖、果糖各0.500 0 g,共同转移至100 mL容量瓶中,用高纯水定容至刻度,得到葡萄糖、果糖浓度分别为5.00 mg/mL的混标贮液.用逐级稀释法配制葡萄糖、果糖浓度为1.00~5.00 mg/mL的梯度混标溶液.同时配制葡萄糖、果糖浓度均为5.00 mg/mL的单标溶液,待测.
1.4 色谱分析条件
色谱柱:Inertsil NH2(5µm,4.6×250 mm)柱;柱温:室温;流动相:乙腈:水=75:25(v/v);真空泵脱气;流速:0.8 mL/min;进样量:20µL.
1.5 样品处理
准确称取20.00 g葡萄样品置于三角瓶中,加入30 mL高纯水,80oC水浴15 min,冷却后高速离心15 min,残渣加入20 mL高纯水再提取,合并上清液,定容至100 mL.用一次性注射器抽取提取样液,过0.22µm滤膜过滤、NH2柱分析.每个样品重复五次.
2 结果和讨论
2.1 流动相和提取剂的选择
根据葡萄糖和果糖分子的化学结构特点,我们选择极性较大的溶剂水和乙腈作为流动相.由实验结果可知,当乙腈和水的比例为75:25(v/v)时,葡萄糖和果糖得到很好的分离.
葡萄样品中葡糖糖和果糖的提取溶剂选用水,文献报道也有选用乙醇作为提取溶剂,但是两者在分离效果、速度、以及准确度、回收率上并没有明显的差别,因此本实验选用水做提取剂.
2.2 标准曲线的绘制
取葡萄糖、果糖标准溶液2、4、6、8、10 mL,分别用高纯水定容至10 mL,从中分别取20µL进样,采用HPLC-RI方法进行分析,以峰面积Y(mV)为纵坐标,标样浓度X(mg/mL)为横坐标,绘制标准溶液曲线,计算线性回归方程.结果见表1
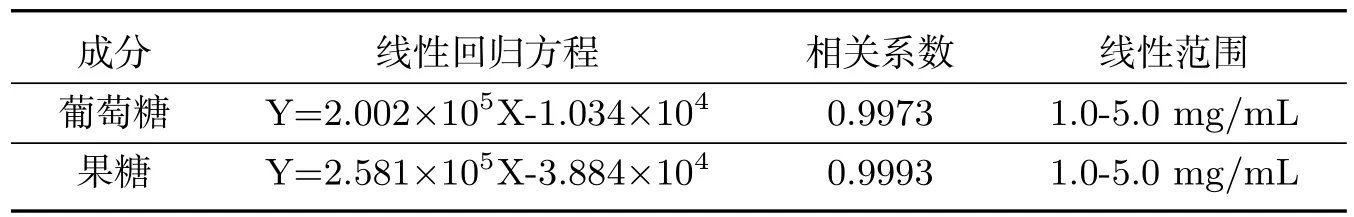
表1 线性回归方程,相关系数,线性范围
2.3 精密度实验
对待测的鲜食葡萄提取液,同一样品重复进样五次,测定峰面积,并计算相对标准偏差(RSD)来考查其测定的精密度,得出两种糖的RSD为0.52%~1.22%,说明精密度良好.结果见表2.
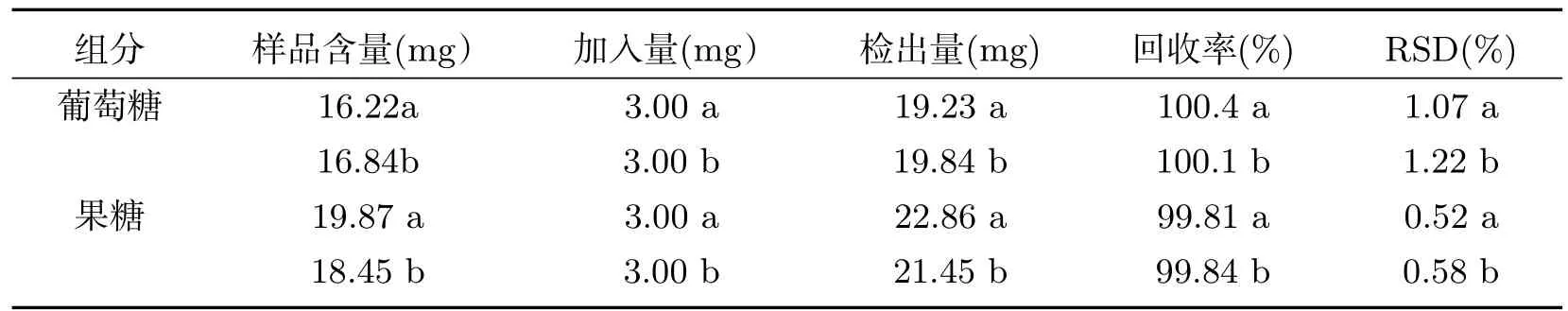
表2 方法的精密度和回收率
2.4 回收率实验
采用加标样回收法,选取贮存30天的葡萄样品,每样取2份,一份加入果糖、葡萄糖的标样,一份不加,按实验方法平行测定五次,计算回收率(回收率为:添加标样样品的测出量减去样品测出量,再除以加入的标样量),结果见表2.实验表明两种糖的平均回收率为99.81%~100.4%,说明该方法具有较高的准确度.
2.5 葡萄样品的分析
按照上述色谱条件,将糖分标样和葡萄样品提取液进行液相色谱分析,进样20.0µL,糖分标样和葡萄样品色谱图如图1.从图1可知,葡萄果实中主要以葡萄糖、果糖为主,不含有蔗糖.同时对两种不同贮藏方式(Blank和SO2)不同贮藏期的葡萄样品提取液进行分析,根据测定的葡萄糖、果糖的色谱峰峰面积,代入工作曲线计算其含量,得到葡萄糖、果糖在贮藏60 d内的糖分变化趋势如图2.
从图2可得,经SO2处理的葡萄果实在贮藏前7天含糖量较空白葡萄样品要高,可能是由于SO2在保鲜过程中,抑制酶活性的变化,从而抑制糖代谢的过程;但是7天后呈逐渐下降的趋势,其中葡萄糖含量的下降程度高于葡萄果实中果糖含量的下降趋势,这可能是由于果实中的部分葡萄糖与SO2发生化学反应而使葡萄糖的含量发生变化.
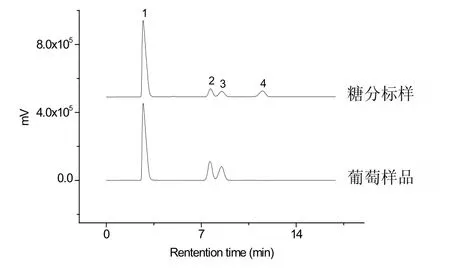
图1 葡萄样品和糖分标样色谱图(1溶剂2葡萄糖3果糖4蔗糖)
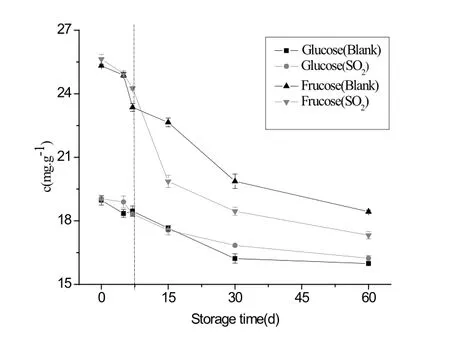
图2 贮藏期间葡萄糖和果糖含量的变化(贮藏温度:0oC)
3 小结
本研究建立了高效液相色谱法测定葡萄果实中糖的组分和含量的方法,相关系数分别为0.997 3和0.999 3,相对标准偏差为0.52%~1.22%,加标回收率为99.81%~100.4%,是一种简便、快速、准确的方法.本方法适于葡萄及葡萄制品中糖的组分及其含量分析,具有实用价值.

