制药洁净厂房过渡空间的原理及其运用
顾锋
(中美上海施贵宝制药有限公司,上海 200240)
何为过渡空间?过渡空间是用于说明两个毗邻房间或区域的关系的通用术语,这种关系是说明进入一个房间或空间时另一个房间需要进行控制。例如,在走廊和工艺房间(如:制粒、压片等)之间的物流气闸室或人员更衣脱衣的缓冲间,在那里必须维持一定的压差,实行出入管制。物料和人员的过渡空间旨在维护不同的房间之间的净化等级和设施分级,防止交叉污染;产品质量和员工的安全保护也是通过过渡空间来实现。
GMP 的核心就是防治药品生产中的混批、混杂、污染和交叉污染。我们在评估医药制剂生产的质量风险时,厂房设施的合理设计和实施,是我们规避生产质量风险及EHS (环境、健康和安全)风险的最基本、最重要的前提。其中包括:合适的空间设计、合理的人流物流设计、恰当的隔离设计以及合适的建筑装修材料的使用。所以,过渡空间、清洗间、称量室、取样间等的设计必须得到重视,这些区域常常被认为是容易产生交叉污染的地方。但是,过渡空间是工厂设计中的基本布局,是防止交叉污染重要的措施。特别是许多跨国制药公司在设计多品种生产的口服制剂车间时,往往采用国际制药工程协会的工程设计指南,采取一次集中更衣,二次更衣分散在各制造单元的地方的做法,那么过渡空间的确定就显得特别重要了。
常见的过渡空间有:
(1)不同净化级别区域之间的人员过渡空间(人流缓冲室或气闸);
(2)不同净化级别区域之间的物流过渡空间(物流缓冲室或气闸);
(3)设施控制等级为1~4级的人员和物料共用过渡空间;
(4)设施控制等级为5级的人流过渡空间;
(5)设施控制等级为5级的物流过渡空间。
1 设施控制等级
那么,什么是设施控制等级(Facility control grade– FCD)呢?这要根据EHS关于物料和产品的暴露控制等级和对人体的有害等级来决定。相对而言,制药厂厂房设施设计内容中的GMP 风险将更加深远地影响产品质量。但是,制剂生产过程就是对大量化学活性原料API(Active Pharmaceutical Ingredients)进行化学或者物理方式的处理[1],而且大多数生产活动由生产人员直接参与,所以,对人员和环境的保护也格外重要。现代制药企业在设计时不但要考虑质量的风险,也要考虑EHS的风险和防范措施,例如:原料在称量和取样中使用的层流罩(Downflow booth)就是为保护人员的健康设置的。
暴露控制等级是根据职业接触限值(Occupational Exposure Limit,OEL)来决定的。OEL指劳动者在职业活动过程中长期反复接触,对绝大多数接触者的健康不引起有害作用的容许接触水平,是职业性有害因素的接触限制量值。OEL是根据API物料的物料安全数据表(MSDS)等实验数据得到的,中国国家标准GBZ2—2007《工作场所有害因素职业接触限值》列出了一些工作场所空气中化学物质的容许浓度。但许多制药厂特定的化学物质的OEL则是制药厂的研发部门自己研究得到的。暴露控制等级旨在帮助人们控制健康危险,暴露控制等级定义了化合物在空气中的浓度以及存在条件,即在这个浓度下,所有工作人员反复接触该化合物而对健康几乎无不良影响。
暴露控制等级有很多分类方法,一般由各制药公司的EHS部门确定的。表1是一个常用小分子药物的暴露控制等级分类的例子,其OEL是通过每个工作日8~10 h、每周40 h的时间计算后得到的加权平均浓度。
根据该厂房所要生产的药物的暴露控制等级,确定厂房设计的设施控制水平FCD。设施控制等级则规定了某一操作环境中既定的制药生产工艺的风险水平,它考虑了多项因数,包括但不限于API的职业接触限值和暴露控制等级、所用产品的数量、暴露时间、API处理的产品形式等。根据设施控制等级来规定针对物料、设备和人员移动的气闸和前厅形式,设施控制等级是确定过渡空间形式的依据。表2是一个设施控制等级分类的例子。
2 过渡空间的净化要求
过渡空间用作不同净化级别区域的物料、设备和人员进出的过渡,因此,过渡空间必须要有合适的面积、结构和布局,满足物料、设备和人员的移动。过渡空间的空调净化级别必须与相邻房间的较高净化级别一致。国际制药工程协会(International Society for Pharmaceutical Engineering-ISPE)关于洁净度的等级中还增加了现场监控区和出入控制区的概念[2]。ISPE是全球领先的制药领域非营利组织,致力于培养和发展科学、工程以及质量体系人才,从而促进安全和有效药物产品的发展与生产。ISPE根据GMP的原则发展了一系列关于制药厂工程设计的指南和标准,帮助制药企业在设计、建造新的设施和厂房改建使用,所以,现场监控区和出入控制区的净化等级为大多数跨国制药公司接受采纳。表3为ISPE与其他国家或组织关于净化等级的对照表。
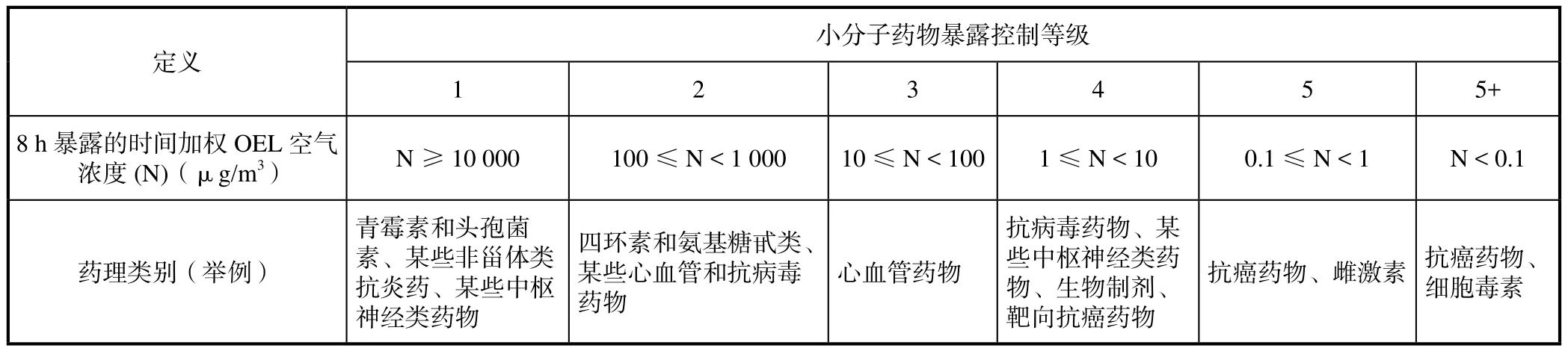
表1 小分子药物暴露控制等级(举例)
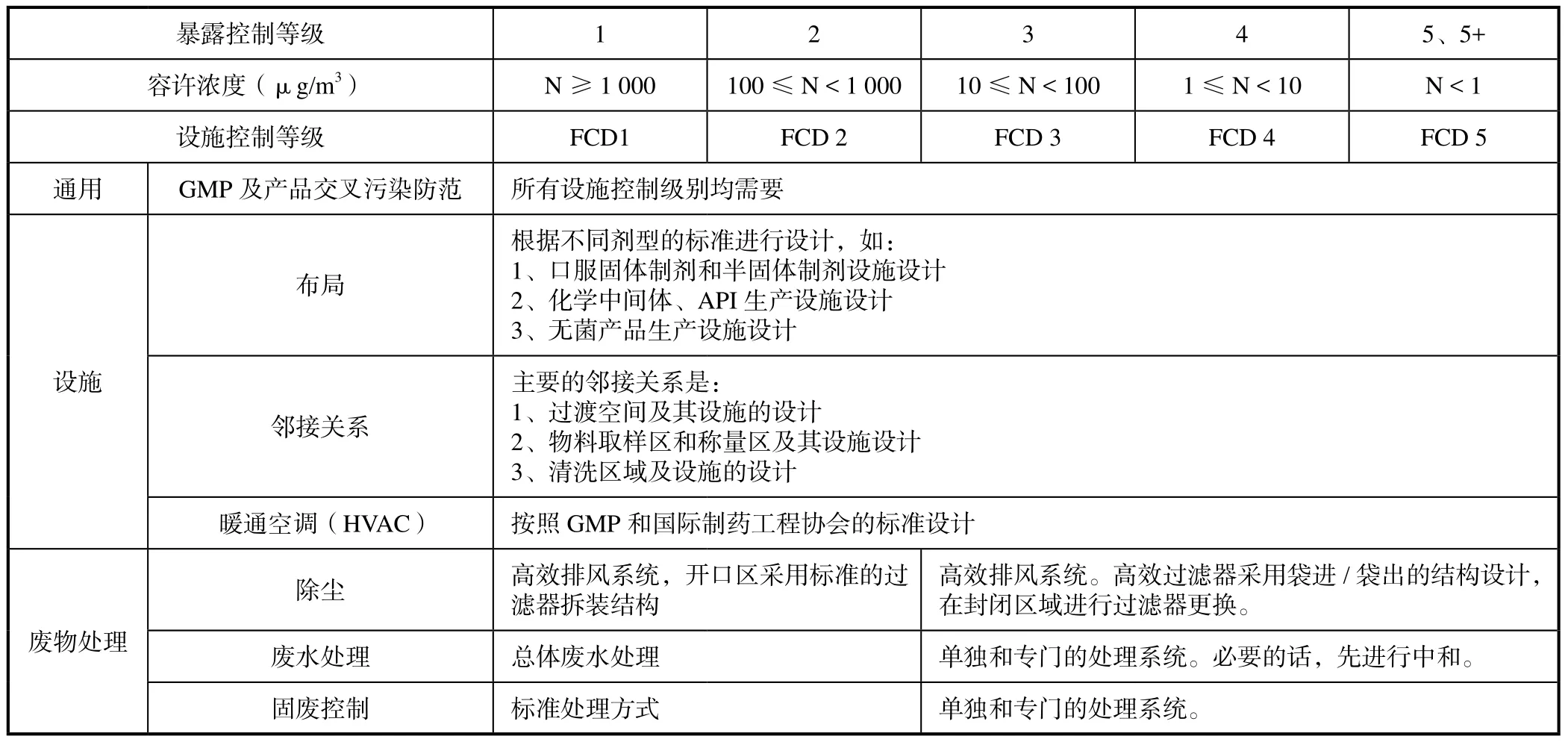
表2 设施控制等级FCD及控制要求(举例)
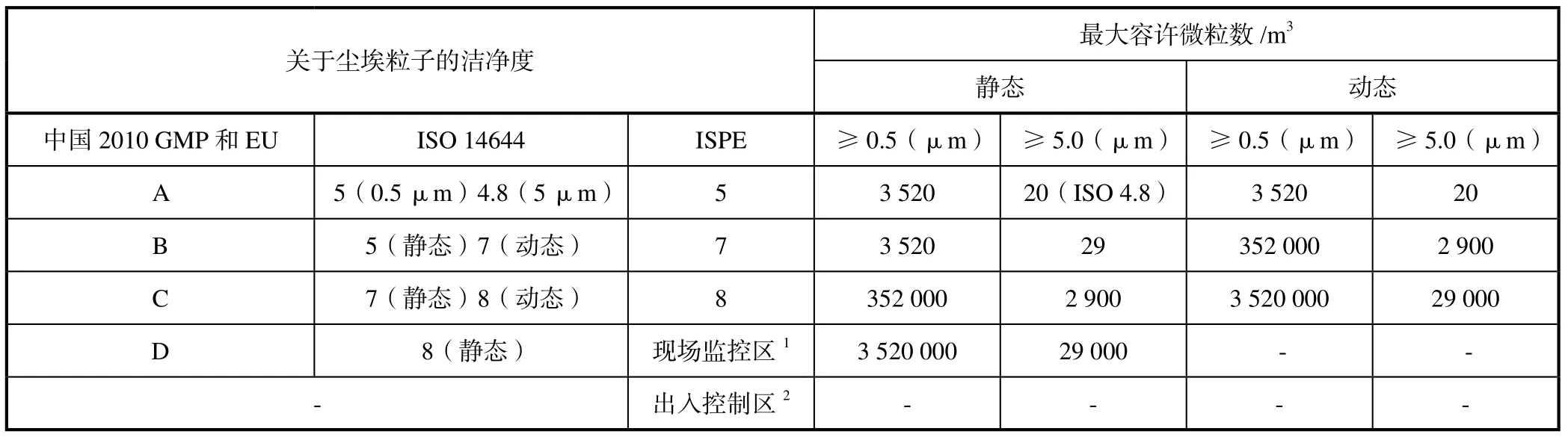
表3 ISPE与其他国家或组织关于净化等级的对照表
受控环境指预先规定的环境净化级别,旨在符合医药行业的ISPE的标准:5级、7级、8级、现场监控区和出入控制区。
ISPE定义的控制未定级(Controlled Not Classified- CNC)区域:指那些可清洁的、需要进出控制的、配置通风过滤的非无菌生产区域,那里没有产品暴露于环境中或与人员接触。因此不需进行环境粒子监控。根据需要,自行决定控制程序和人员衣着的等级。控制未定级可以分为二种类型:
(1)现场监控区(CNC w/LM),相当于国际标准组织ISO的8级(静态)以及EU(欧盟)D级。现场监控区指设施中的那些区域,如:称量配料、制造区、包装开口区。那里产品直接暴露在环境中或人员中,因此需要规定净化级别和控制程序并且需要进行监测,防止净化级别降级或者产品的交叉污染。需要监测的项目是尘埃粒子和微生物以及房间的压差。
药品生产是指从物料的接受、经过完整的工艺处理和包装、再到完工成为成品的所有操作。这些操作是在单独的工艺房间或区域中进行的,工艺房间是主要的生产空间,在那里进行敞开的、半封闭或全封闭的单个工艺生产,包括:API原料、生物制剂、口服固体制剂/半固体制剂的生产过程。生产区域由多个主要生产空间组成的区域,生产区域可能是专注于针对专用产品或连续生产安排的工艺系统。还可能具备用于多种产品同时生产的条件。对口服固体制剂和半固体制剂来说,现场监制区至少包括但不限于以下生产操作单元:来料取样、称量/配制、制粒、粉碎、混合、压片/装囊、中间体取样、溶液配制、包衣/印字、开口区包装/灌装、设备清洗/干燥、就地清洗/清洁、进出控制区走廊和生产区域之间的人流与物流缓冲间等。
(2)出入控制区(CNC w/LM)指设施中的那些区域,如:过渡空间和走廊,那里没有潜在的产品暴露在环境中或人员中,但是,此区域中的环境或活动可能直接或间接影响产品质量,需要在设计时考虑或采取控制措施,保护产品和物料以及将接触产品或成为产品一部分的组分。
对口服固体制剂和半固体制剂来说,出入控制区至少包括单不限于以下生产操作支持单元:设备存储(包裹/密封的设备)、机器零部件存储(包裹/密封的机器零部件)、受污染设备暂存(密封或包裹)、清洁设备暂存(密封或包裹)、与直接服务于生产区的过渡空间接邻的工艺进入通道、主通道和工艺进入通道之间进出控制的过渡空间等。
未定级(无净化)区:无潜在的暴露于环境或人员的产品或产品接触面的区域。主要是支持生产操作的区域,必须有与生产通道区分开来的单独通道,包括卫生间和淋浴设施。这些区域至少包括但不限于:普通办公室、QC实验室、一更衣、卫生间和淋浴设施、仓库存储区、货物收发、通用进出通道、休息室、闭口区包装、机修等。
3 过渡空间的压差控制
厂房建造时可能已考虑到整个建筑物的压力控制,即建筑物保持正压以防止外界未经过处理的空气渗透。但是,单个房间或区域由于操作内容不同,其压力关系可能是正值也可能负值。这些压力关系可以保持空间洁净,以及防止生物的和高活性物料污染。这些生物的或高活性物料在进出工艺房间时,这些过渡空间(气闸)就发挥了重要作用[3]。
气闸压力控制的类型见图1。

图1 气闸压力类型
3.1 级差型
级差型(也称为Cascade-瀑布型),在只考虑洁净度而无须污染控制的情况下须采用这种方式。在这种情况下,气流从洁净度高的区域(房间)流向邻近洁净度低的区域(房间)。洁净度每相差一级,设计的房间的压差在两边门关闭的情况应大于15 Pa。实际运行时房间的压差在两边门关闭的情况应大于10 Pa(GMP要求),在级差增压方式下,测量的压差是穿过气闸的不是穿过每个门的最低压差。如图2所示。
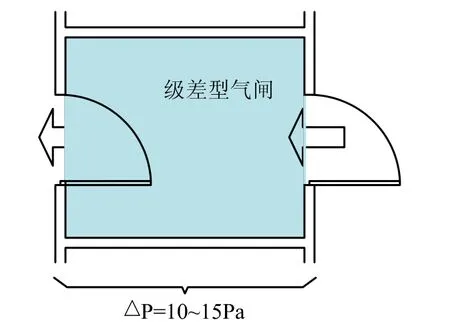
图2 级差型压力关系
3.2 正压型
正压型(也称为Bubble-泡泡型),在必须同时考虑洁净度和污染控制的情况下采用这种方式。两边门都关闭时,通过每个门的空气压差是不同的。如图3所示。
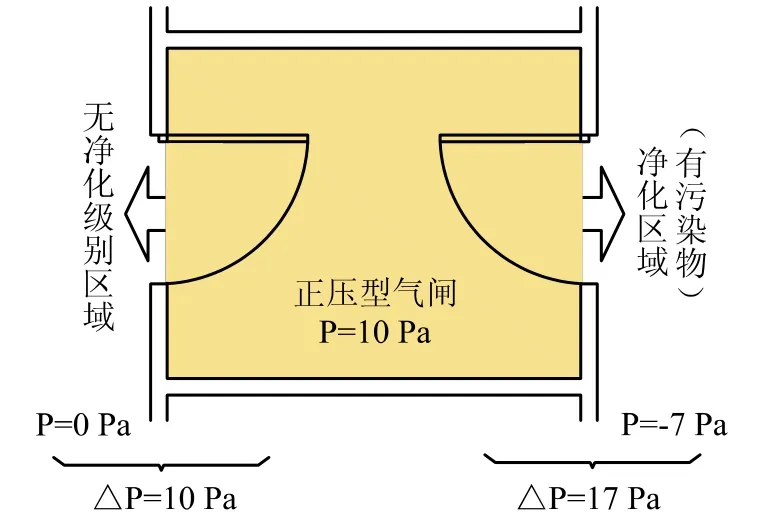
图3 正压型压力关系
3.3 负压型
负压型(也称为Sink-水槽型);两边门都关闭时,通过每个门的空气压差也是不同的。如图4所示。
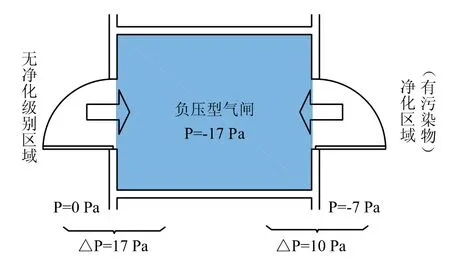
图4 负压型压力关系
4 过渡空间的运用举例
4.1 设施控制等级为1~3级的工艺环境:合用的人员和物料的过渡空间,两者均为双向流动(进出同一房间),为物料、人员双向进出的正压型气闸(图5)。
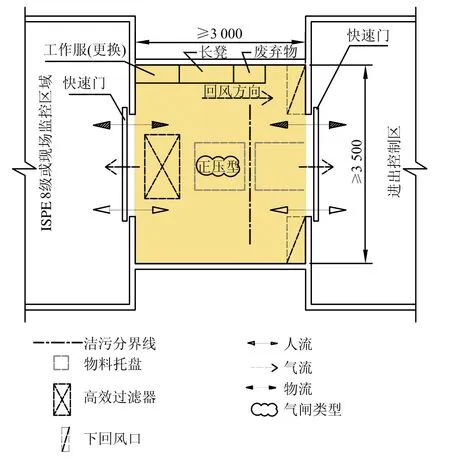
图5 合用的人员和物料的过渡空间
要点:
(1)房间最小面积——按图5所标尺寸计。
(2)高效送风口位于洁净度高的一侧,回风口位于洁净度较低的一侧且为下回风。
为控制污染,空调回风口的位置和结构是非常重要的。回风应采用下回风,回风口的位置应该置于离地面300 mm之内,回风口的面风速不大于2.0 m/s,回风管道的风速不大于4.3 m/s,连接弯管的半径应大于150 mm以便清洁。至少离地面1 500 mm长的回风管及弯管应采用304不锈钢(若焊接风管,则采用304 L不锈钢)。在含尘浓度高或湿度高的房间中,回风(排风)管必须向下倾斜,以便于排水。图6为典型的下回风(嵌入式)安装示意图。
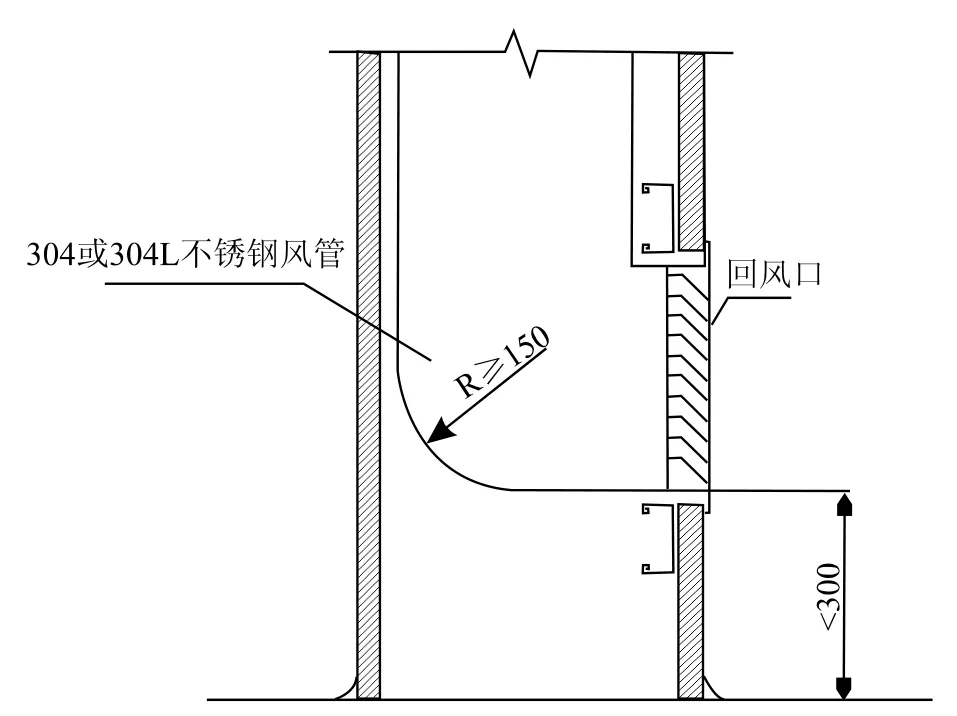
图6 典型的下回风口安装示意图
(3)维持空气压差是保证洁净度关键因素之一。
(4)通向高风险洁净区域(ISPE第5和7级)的物流气闸和人员前厅的门必须联锁。
(5)图7所示的门为快速卷帘门,目的是能快速的开关,迅速恢复气闸的压差(开门后压差恢复时间也是环境验证的内容之一),并且保证房间面积。图7为这种净化用快速卷帘门的外形,已有国内企业开发生产。物流气闸也可以采用普通的平开门。

图7 快速卷帘门外形
4.2 设施控制等级为1~4级的工艺环境[4]:分开的人员和物料的过渡空间,均为双向流动的正压型气闸(图 8)。
要点:
(1)专用的物料双向流动过渡空间。
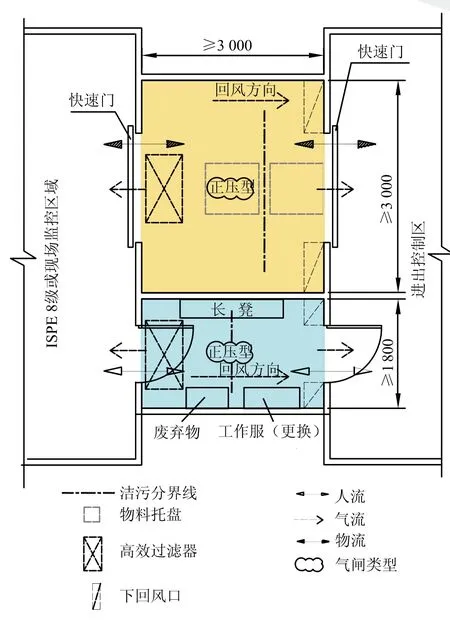
图8 分开的双向流动人员和物料的过渡空间
(2)由于较高的悬浮尘埃粒子浓度,需配备单独的双向流动人流缓冲间,在那里进行再次的更衣和脱衣。
(3)其余要点同前(物料、人员双向进出的正压型气闸)。
4.3 设施控制等级为5级的工艺环境:单独的物流气闸(双向流动)和人流气闸(单向流动),5+级的人员出口还需配置风淋室(图9)。
要点:
(1)由于高活性化合物的操作,采用单独的双向物流过渡空间以及单独的单向人流过渡空间,在那里进行再次的更衣和脱衣。
(2)人员出口要求:
①对专门的5级设施控制等级,人员离开先要通过风淋室然后进入脱衣区。
②对4级和5级共用的设施控制等级,设计时需考虑风淋室。当4级使用时,人员离开可直接进入脱衣区;当5级及5+级使用时,人员离开先要通过风淋室然后进入脱衣区。
(3)其余要点同前(物料、人员双向进出的正压型气闸)。
4.4 设施控制等级为1~4级的无菌生产工艺环境(ISPE 5级和7级的洁净度):单独的物流气闸(单向流动)和人流气闸(单向流动),一步脱衣出口(图10)。
要点:
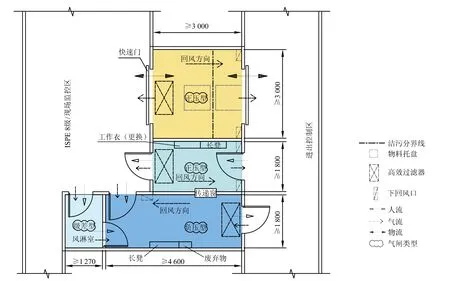
图9 双向流动物料过渡空间和单向流动人员过渡空间
(1)由于无菌工艺操作设置单独的单向流动物流气闸和人员缓冲室,在那里进行再次的更衣和脱衣。
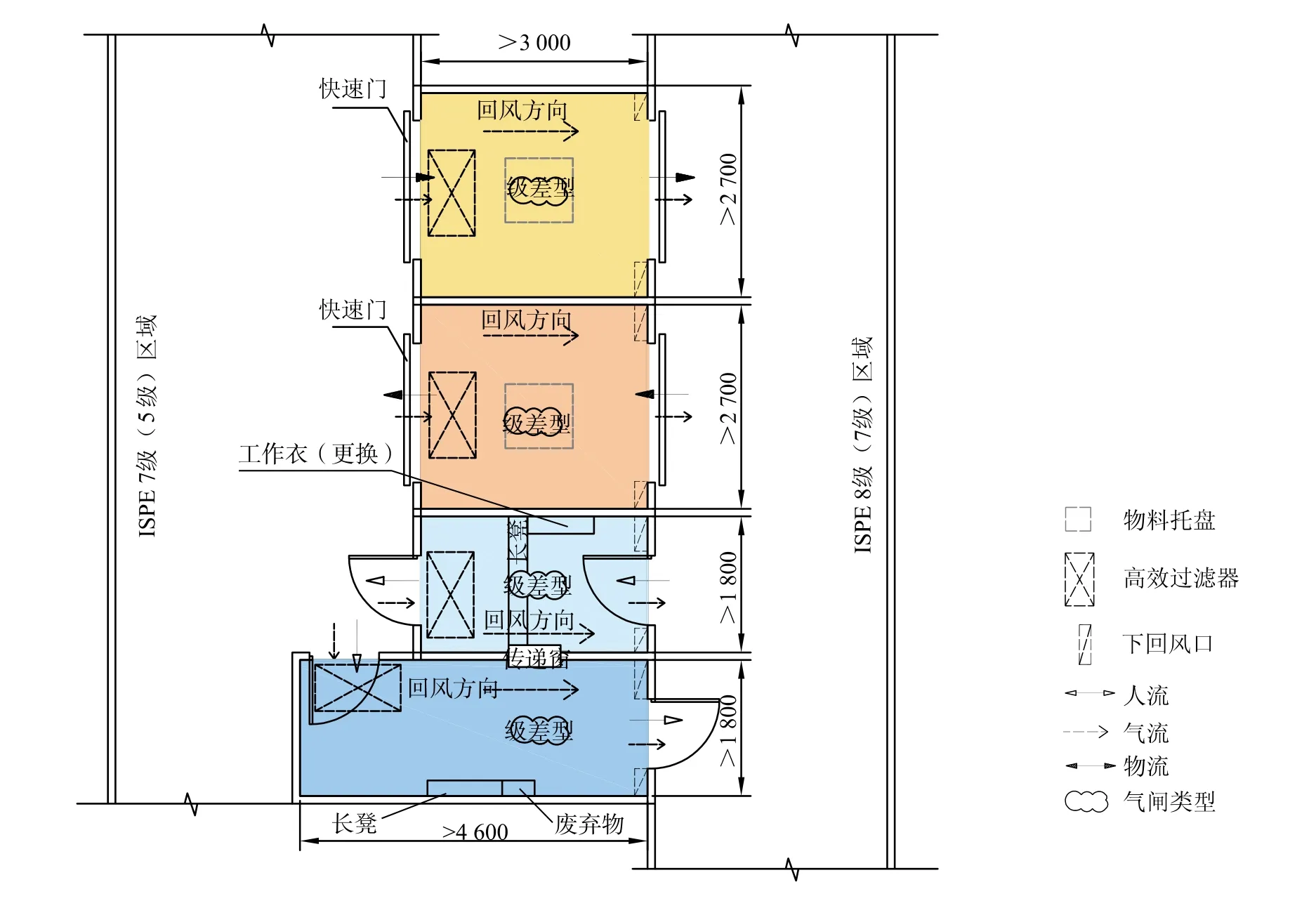
图10 单独的物流气闸(单向流动)和人流气闸(单向流动)
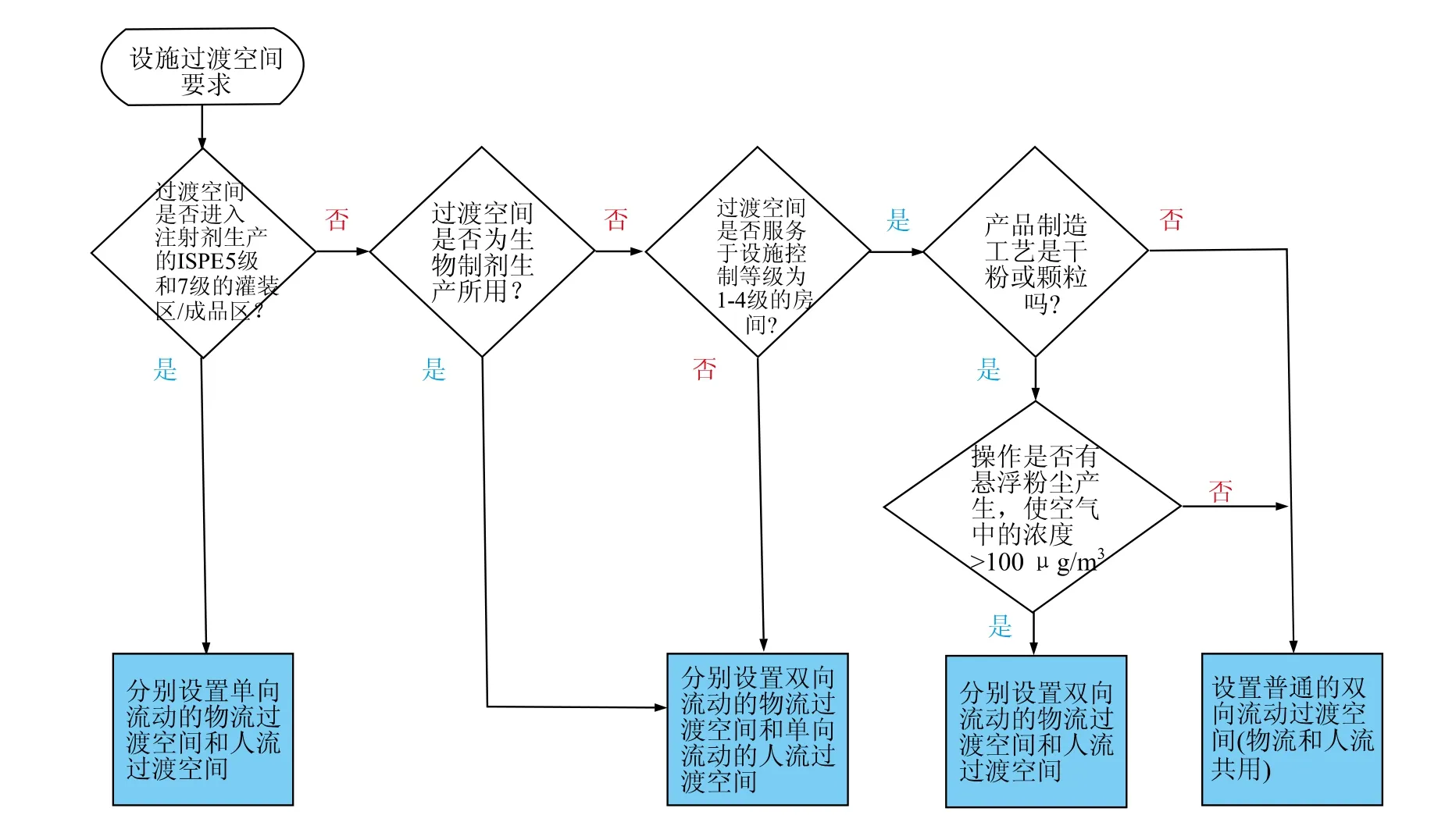
图11 过渡空间类型选择流程图
(2)其余要点同前(物料、人员双向进出的正压型气闸)。
可以利用图11的流程图来选择合适的过渡空间类型。
5 结束语
综上所述,制药洁净厂房过渡空间选择的流程为:根据所生产的物料(主要是活性物料API)的MSDS确定职业接触限值OEL——确定暴露控制等级——确定设施控制等级——确定合适的过渡空间类型。从原理上来看,(半)固体口服制剂生产的洁净走廊应是进出控制区(CNC w/AFAC),单从符合中国的GMP来看,一般还是设计成现场监制区(D级),在这种情况下,人员过渡区的更衣实际上是三次更衣。过渡空间在防止交叉污染方面,除了需要合理布局外,其装饰材料的选择、空调净化系统的设计、压差维持控制等也至关重要。
除硬件条件外,过渡空间还必须要有控制程序,如:SOP,说明物料、人员、设备和废物通过过渡空间的移动方式,以清除污染源并保证产品的质量。
[1] ISPE[M]. Baseline Guideline: Active Pharmaceutical Ingredients(Second Edition- Revision to Bulk Pharmaceutical Chemicals Guideline), Volume 1.
[2] ISPE[M]. Good Practice Guide: Heating, Ventilation, and Air conditioning.
[3] 百度文库. 空调系统GMP 实施指南[M]:158-160
[4] ISPE[M]. Baseline Guideline: Oral Solid Dosage Forms, Volume 2.

