硫酸四氨合铜结晶过程的粒度控制技术
张 楠,冯璐璐,柳沛宏
(中北大学化工与环境学院,山西 太原 030051)
硫酸四氨合铜(copper sulfate-ammonia complex),俗称络氨铜、硫酸四氨络合铜,化学式为[Cu(NH3)4]SO4。硫酸四氨合铜用途广泛,在工业上常被用作媒染剂[1],在碱性铜中是电镀液的主要成分。在农业上是一种高效、安全的广谱杀菌剂,对真菌、细菌性病害均有较好的防效,同时还可以作为植物生长激素,在施药条件下,能有效促进植物生长,明显提高作物产量[2]。硫酸四氨合铜还可作为催化剂,例如在六硝基联苄转化为六硝基茋的反应中加入硫酸四氨合铜,可使反应得率(以六硝基联苄计)大于65%[3]。
目前,硫酸四氨合铜的制备方法主要有直接合成法与沉淀法[4]。直接合成法是将CuSO4·5H2O和Na2SO4加入蒸馏水中,然后通入一定量的氨气而制备。这种方法操作简单,生产成本较低,但是使用大量的氨气会对环境造成严重的污染。沉淀法是先将CuSO4·5H2O溶于蒸馏水中,然后加入氨水与其反应,最后利用乙醇作为溶析剂使生成的硫酸四氨合铜沉淀出来[5]。这种方法虽然生产成本略高,但是对环境污染小。因此,本研究采用沉淀法制备硫酸四氨合铜。
晶体材料的粒度影响其性能。超细材料因其特有的量子尺寸效应、宏观量子隧道效应等特征[6-7],常常具有块状材料所不具有的优异性能,例如高催化性、奇异的电磁及光学性质等,其制备与性能研究近年来受到了功能材料研究者们的广泛重视[8-10]。
研究硫酸四氨合铜晶体粒度及其分布的控制技术,制备特定粒径的产品,对于改善其性能和进一步拓展其应用具有十分重要意义[11]。
1 实验部分
1.1 实验原理
在制备超细粒子时,沉淀法[12]是常用的方法。所谓沉淀法,通常是先在溶液中将不同化学物质混合,然后往混合溶液中加入适当的沉淀剂以制备化合物。其原理是在难溶电解质的溶液中,溶解的阴阳离子的离子积大于该难溶物的溶度积Ksp,这种物质就会沉淀下来[13]。沉淀物的粒径取决于核形成与核成长的相对速度,核形成速度低于核成长速度时生成的颗粒数就少,平均粒径就变大。
沉淀剂的加入方式主要有3种:正加法,将沉淀剂加入到混合溶液中;反加法:将混合溶液加入到沉淀剂中;并流滴加,将混合溶液与沉淀剂同时加入到容器中。
1.2 原料
五水硫酸铜(分析纯),无水乙醇(分析纯),氨水(分析纯),蒸馏水(实验室自制)。
1.3 仪器及装置
DF-101S集热式恒温加热磁力搅拌器,YP502N电子天平,SHZ-CA循环水式多用真空泵,HH-1电热恒温水浴锅,S312恒速搅拌器,Φ300mm真空玻璃干燥器,BT-2002激光粒度分布仪(μm级),BT-90纳米激光粒度分布仪。
1.4 硫酸四氨合铜晶体制备
1)称取一定量的CuSO4·5H2O,用蒸馏水配制成适当浓度的溶液,加入到三口烧瓶中。保持体系的温度在25℃,搅拌的同时向烧瓶中缓慢加入氨水,溶液中出现沉淀,继续加氨水,沉淀逐渐消失,当混合液完全清澈时反应结束。其化学反应方程为:
CuSO4+4NH3·H2O=[Cu(NH3)4]SO4·H2O
2)量取一定量的乙醇(作为沉淀剂),将反应式(1)的溶液与之混合,搅拌一定时间,析出沉淀。减压过滤、干燥,得到目标产物。利用BT-2002 和BT-90激光粒度分布仪测定其粒度分布。
1.5 制备工艺对晶体粒度及分布的影响
研究了搅拌方式、沉淀方法、表面活性剂的种类与加量,以及反应液与乙醇用量比等因素对硫酸四氨合铜晶体粒度及分布的影响,实验条件见表1。

表1 实验条件表Table 1 The table of experimental condition
2 结果与讨论
用激光粒度仪测定了不同工艺及操作条件下所得硫酸四氨合铜晶体的粒度(用中位径表征)及分布,粒度数据见表2,粒度分布曲线见图1~13。

表2 不同实验条件制得的硫酸四氨合铜晶体的粒度Table 2 The size of different experimental conditions produced
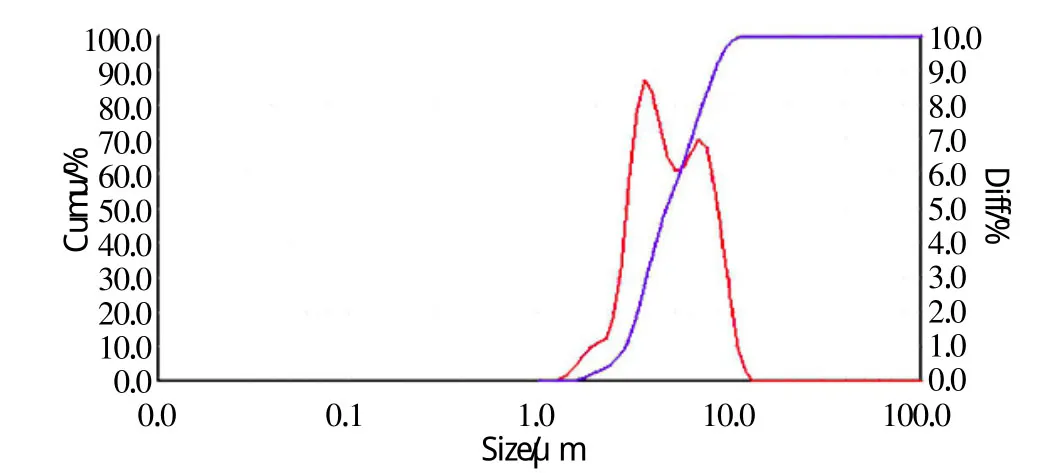
图1 实验1所得晶体粒度分布曲线Fig.1 The crystal size distribution curve of 1

图2 实验2所得晶体粒度分布曲线Fig.2 The crystal size distribution curve of 2

图3 实验3所得晶体粒度分布曲线Fig.3 The crystal size distribution curve of 3
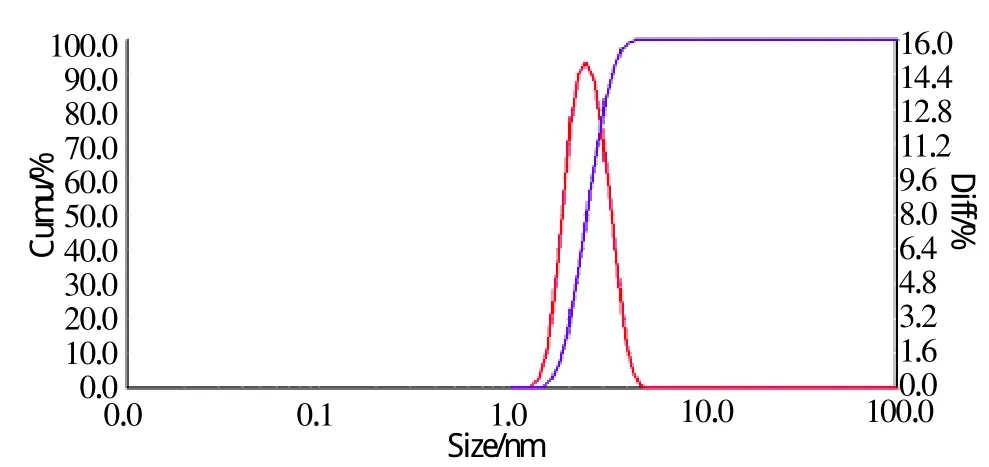
图4 实验4所得晶体粒度分布曲线Fig.4 The crystal size distribution curve of 4
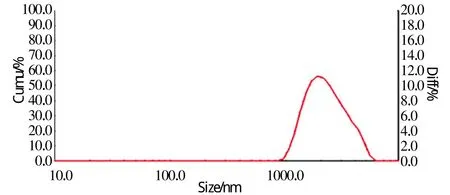
图5 实验5所得晶体粒度分布曲线Fig.5 The crystal size distribution curve of 5

图6 实验6所得晶体粒度分布曲线Fig.6 The crystal size distribution curve of 6

图7 实验7所得晶体粒度分布曲线Fig.7 The crystal size distribution curve of 7

图8 实验8所得晶体粒度分布曲线Fig.8 The crystal size distribution curve of 8
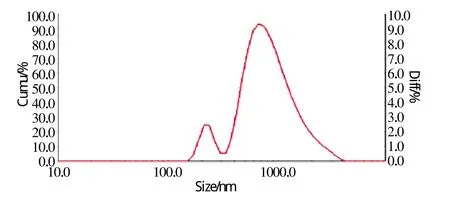
图9 实验9所得晶体粒度分布曲线Fig.9 The crystal size distribution curve of 9
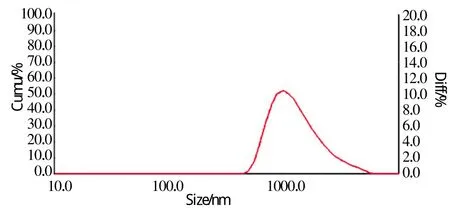
图10 实验10所得晶体粒度分布曲线Fig.10 The crystal size distribution curve of 10
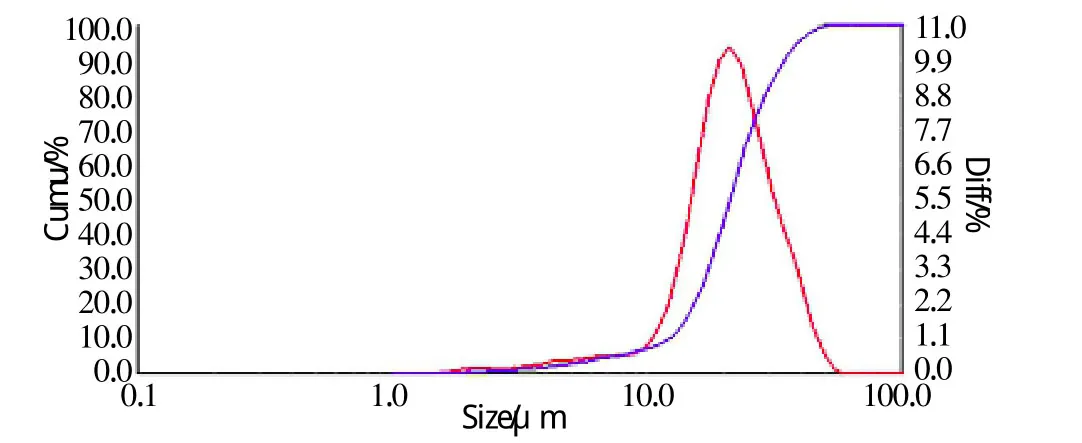
图11 实验11所得晶体粒度分布曲线Fig.11 The crystal size distribution curve of 11

图12 实验12所得晶体粒度分布曲Fig.12 the crystal size distribution curve of 12
由以上图表可以看出,不同实验条件下得到的粉体粒度是不一样的。图4、5、6、8、10和 11均出现单一峰,说明这些样品为球形粉体或近球形,图7和9出现2个正态分布峰,说明样品为非球形颗粒,且不同方向的尺寸相差较大。
2.1 搅拌强度的影响
对比实验1与4、6与10,可发现搅拌强度越大,晶体粒度越小。不同的搅拌会造成不同的剪切力,从而将液体撕裂成不同粒度的液膜、液丝和液滴,产生不同相界面,使相间传质速率不同[14]。磁力搅拌器由于转子体积小,搅拌引起的剪切力较小,使得成核过程在非均匀微观条环境中进行,从而微观混合状态严重,导致粒度分布不均匀,而且粉体粒径较大。机械搅拌器的搅拌叶半径大,转速也更快,加快了传质,与磁力搅拌器相比效果更好。高速分散器转速更快,造成巨大的剪切力,使得微观混合和传质过程得到极大强化。所以在3种搅拌方式中,高速分散器搅拌效果最好。
2.2 滴定方式的影响
实验1、2和3数据表明,反向滴加所得粉体最小,说明反向滴加方式有利于硫酸四氨合铜分子的分散,成核中心多,晶体颗粒小。
2.3 表面活性剂的影响
对比实验1、11和12,7、8、9和10发现,不合适的表面活性剂使产品平均粒径更大,分布更广;合适的表面活性剂可以有效缩小晶粒尺寸,产生极化,从而缩短了离子间的距离[15]。
制备硫酸四氨合铜所需要的表面活性剂是阳离子表面活性剂。阳离子表面活性剂溶于水后发生电离,与亲油基相连的亲水基带正电荷的,从而与硫酸四氨合铜结合成键起到空间位阻作用,阻碍粉体团聚。但是表面活性剂的用量过多会对粉体的性能产生不良的影响, 因此表面活性剂的加入量也不是越多越好。
2.4 沉淀剂加量的影响
实验4、5和7表明,沉淀剂越多,产品粒度就越小。沉淀剂越多,[Cu(NH3)4]2+浓度越低,反应瞬间晶核形成速度较快,由于成核速度明显高于晶核生长速度,使得粒子尺寸较小;当反应浓度过高时,由于粒子密度高,布朗运动使得粒子由于相互碰撞而长大,同时团聚现象加重。因此分散剂越多,所得粒径越小。
3 结论
采取沉淀法制备硫酸四氨合铜晶体时,反向滴加、高速搅拌以及加入适当的表面活性剂有利于小粒径晶体的形成。较佳的工艺条件是:采用反向滴加方式,以高速分散器为搅拌装置,加入阳离子表面活性剂十二烷基三甲基氯化铵,且表面活性剂的量要大于其临界胶束浓度。
[1] 石莉萍,刘纯,王丽君.硫酸四氨合铜的制备及组成测定的实验研究[J].沈阳教育学院学报,2002(4):113-114.
[2] 黄中强,蒋毅明.硫酸四氨合铜制备工艺研究[J].广西师范大学学报:自然科学版,1999(3):69-71.
[3] 宁培毅.用铜氨络合物制造六硝基芪[J].现代兵器,1980(6):41.
[4] 陈玲.硫酸四氨合铜的制备及成分测定[J].广东化工,2011,38(11):124-125.
[5] B.Morosin.The Crystal Structures of Copper Tetrammine Complex A.Cu(NH3)4, SO4.H2O and Cu(NH3)4SeO4[J].Acta Cryst., 1969.
[6] 杨柯,等译.发展中的材料研究(美)[M].沈阳:辽宁科学技术出版社,1994:70.
[7] Allen,T., Particle Size Measurement, Poeder Technology Series, 3rd Edn[M].London: Chapman and Hall,1981.
[8] Shamlou, P.A., Handling of Bulk Solids[M].Theory and Practice,Butterworth & Co.Ltd.,1988.
[9] 盖国胜.超细粉碎与分级技术进展[J].中国粉体技术,1995(1):22-26.
[10] REN Jun, LU Shouci, SHEN Jian, et al.Research on the composite dispersion of ultrafine powder in air[J].Materials Chemistry and Physics, 2001(69): 204-209.
[11] McCave I N, Syvitski J P M.Principles and methods of geological particle size analysis [C].Cambridge: Cambridge University Press, 1991:2-21.
[12] Wang Hongqiang, Li Caihong, Zhao Haigang, Liu Jinrong.Preparation of nano-sized flower-like ZnO bunches by a direct precipitation method[J].Advanced Powder Technology,2013(24): 599-604.
[13] 徐华蕊,李凤生,陈舒林,宋洪昌.沉淀法制备纳米级粒子的研究[J].化工进展,1996(5):29-31.
[14] 李艳,刘有智,张丽萍.超重力法制备纳米材料的研究现状[J].化学工业与工程技术,2006,27(3):4-6.
[15] 邱关明.结晶化学[M].武汉:华中工学院出版社,1986.

