海洋抗肿瘤药物Ecteinascidin-7 4 3的研究新进展
马满玲,康传哲,杨丽杰
(1.哈尔滨工业大学 基础交叉学科研究院,黑龙江 哈尔滨 150006;2.哈尔滨医科大学 附属第一医院 药学部,黑龙江 哈尔滨150001)
海洋抗肿瘤药物Ecteinascidin-7 4 3的研究新进展
马满玲1,2,康传哲2,杨丽杰2
(1.哈尔滨工业大学 基础交叉学科研究院,黑龙江 哈尔滨 150006;2.哈尔滨医科大学 附属第一医院 药学部,黑龙江 哈尔滨150001)
目前对海洋抗肿瘤药物的研究已经成为全世界普遍关注的热点,海洋天然产物现已成为临床抗癌药物的重要来源。Ecteinascidin-743是从加勒比海海鞘Ecteinascidia turbinata中分离提取得到的海洋生物碱,抗肿瘤活性明显高于目前临床上广泛使用的抗肿瘤药物,对多种肿瘤细胞如白血病、卵巢癌、软组织肉瘤、黑素瘤、宫颈癌、乳腺癌、结直肠癌、肾癌、前列腺癌、肺癌及非小细胞肺癌等有明显抑制活性,是首个成功应用到临床的海洋抗肿瘤药物。本文检索近年相关文献,对该药的合成、药理及临床研究进展作一综述。
海洋抗肿瘤药物;Ecteinascidin-743;抗肿瘤活性
据世界卫生组织(WHO)最近公布的数据显示,全球每年癌症死亡人数约为700万,占死亡人数的13%,且发病率呈逐年上升趋势。然而,目前临床上仍没有安全有效的治疗方法和抗肿瘤药物,开发和探寻新型抗肿瘤药物具有重要意义。目前对海洋抗肿瘤药物的研究已经成为全世界普遍关注的热点,海洋天然产物现已成为临床抗癌药物的重要来源。
目前,对海洋抗肿瘤药物的研究已经成为开发新型抗肿瘤药物研究的热点。Ecteinascidin-743(Et-743)是从加勒比海海鞘Ecteinascidia turbinata中分离提取得到的四氢异喹啉类海洋生物碱。研究发现Et-743的抗肿瘤活性明显强于目前临床上使用的抗肿瘤药物如紫杉烷类、喜树碱类、顺铂、阿霉素及甲氨蝶呤等;明显抑制多种肿瘤细胞活性如白血病、卵巢癌、软组织肉瘤等肿瘤细胞[1-5]。2007年欧洲药品管理局(EMEA)正式批准Et-743作为治疗晚期软组织肉瘤药物上市,商品名Yondelis(Trabectedin)。本文对Et-743的合成、药理、临床等方面的研究进展进行综述。
1 Ecteinascidin-743(Et-743)
1969年sigel等[2]首次发现加勒比海海鞘的乙醇粗提物具有较强的抗肿瘤活性,于是该提取物在随后的十几年里成为众多专家研究的热点,致力于对该提取物中的分离鉴定。由于分离活性物质和鉴定结构的技术要求,当时的科学技术水平无法满足,最终均未获得进展。直到1986年伊利诺伊斯大学的Rinehart教授带领的科研团队从海鞘中首次分离鉴定出一系列具有强抗肿瘤活性的Ecteinascidins生物碱类化合物,Et-743在该类生物碱化合物中含量最多,药理活性最强[6]。1990年,由于现代生物技术的发展,尤其是二维核磁共振技术的发展。Rinehart和Wright两个小组同时确定了Et-743的分子结构[6-7](见图1)。
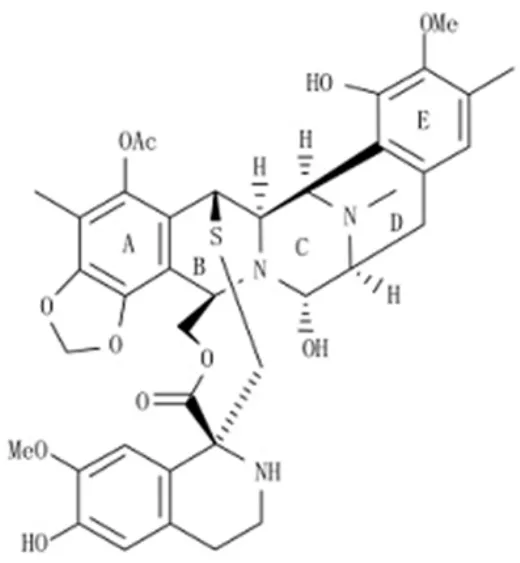
图1 ET-743的分子结构示意图Figure 1 Schematic molecular structure of ET-743
Et-743的化学分子结构非常复杂,其骨架结构是哌嗪并双四氢异喹啉环,含3个四氢异喹啉结构单元,七个手性中心。另外,Et-743在环外还有独特的硫桥结构。Et-743抗肿瘤作用的药效团主要是2个四氢异喹啉环,通过与DNA的小沟结合,导致DNA的一个鸟嘌呤残基烷基化,从而破坏DNA双螺旋结构,使DNA构象改变,使得肿瘤细胞难以分裂增长。
2 Et-743的化学合成研究
由于Et-743具有显著的抗肿瘤活性,以及其独特新颖的化学结构,引起了化学家及药理学家的广泛关注,成为近年天然抗肿瘤产物研究的热点之一。在海鞘中Et-743的含量极低,为了满足药效及临床实验对药物的需求,合成化学家对Et-743的合成研究进行了大量的探索。Et-743结构复杂,到目前为止,仅有四个研究小组完成了对Et-743的化学全合成。E.J.Corey研究小组于1996年首次完成了Et-743的全合成研究,他们以Sesamol为原料,通过运用经典的分子内Mannich反应和Strecker反应构建五环骨架结构,经过四十多步反应,得到目标化合物的总收率为0.53%[8]。但因为两个前体化合物的合成非常繁琐、合成步骤较昂贵、产率低限制了该方法的应用。2002年,Fukuyama课题组完成了Et-743的立体专一性全不对称合成研究,他们通过四组分Ugi缩合反应、分子内Heck反应及随后酚-醛环化构建五环结构,整个路线经历了40多步反应,以总收率为0.78%得到目标化合物[9]。2006年,Zhu等[10]报道了Et-743的全合成,他们以3-甲基儿茶酚为原料,以D-C-B顺序构环,整个路线共经历31步,总收率为1.7%。与前两条合成路线相比,此合成路线不需要苛刻的反应条件,利于大量制备,而且总产率也相对提高。随后,Danishefsky 等[11]也于2006年完成了Et-743的全合成,以B-C-D顺序构环,通过分子内Pictet-Spengler反应构建C、D环,但是该步产率仅为42%~58%。总体而言化学合成反应步骤繁琐,反应条件苛刻,产率低,不适应于大规模工业化生产,因而化学全合成方法在现阶段很难解决药源问题。
此外,还有一些未完成的全合成研究,这些研究虽然最终未能得到目标产物Et-743,但是其在五环骨架的构建及其他功能基团的修饰方面都取得了创造性的研究成果[12-14]。2000年,Cuevas等[15]以天然产物Cyanosafracin B为原料,利用该分子与Et-743具有相似的五环骨架和五个正确的手性中心,通过修饰分子中相应部位的取代基,进行半合成研究,共经过21步反应,得到Et-743的总收率1.0%。由于荧光假单胞菌通过发酵的方法可以大量获得Cyanosafracin B,从而解决了药源供应问题。由于具有了充足的药物来源,Et-743相关的一系列药效学研究、药代学研究及药物安全性评价等研究得以顺利进行。目前,上市的Yondelis(Trabectedin)就是通过类似物Cyanosafracin B半合成获得的。
3 Et-743的生物合成研究
在对Et-743进行化学合成研究的同时,很多科学家也对Et-743生物合成进行了深入的研究。2000年R.G.Kerr等[16]首次完成了Et-743的生物合成研究,以酪氨酸和L-DOPA为起始原料,利用从海鞘Ecteinascidiaturbinata中提取出来的酶催化通过化学合成方法合成出的环肽,成功合成出了Et-743。从而证明了Et-743的生源合成途径,即由天然的苯丙氨酸类化合物经生物转化而来(见图2)。
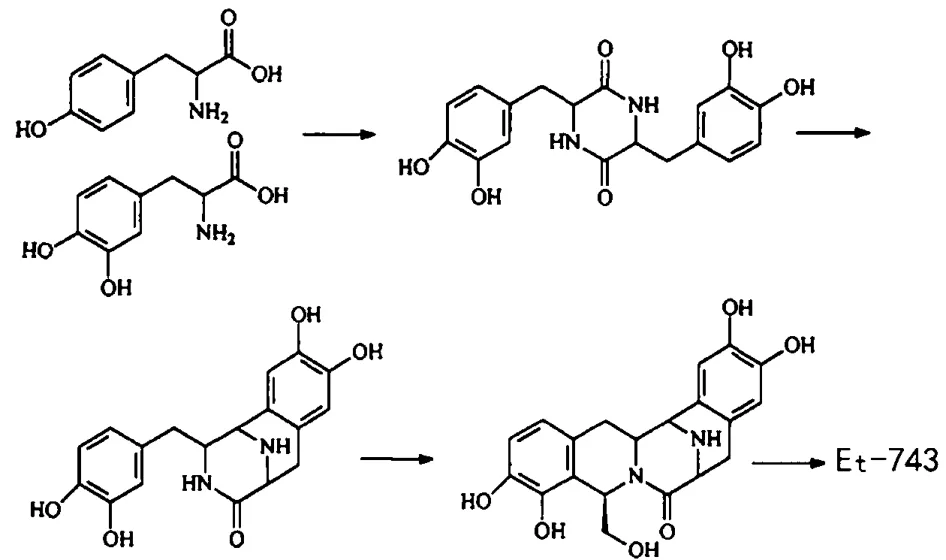
图2 ET-743的生物合成路线Figure 2 Biosynthesis route of ET-743
4 Et-743的药理学研究
4.1 Et-743的作用机制[17-18]至今为止,虽然还未完全阐明Et-743抗肿瘤活性的作用机制,但是相关研究发现,Et-743有独特的多重作用机制:(1)Et-743为烷化剂,主要作用于脱氧核糖核酸,但烷基化的机理与传统的烷化剂不同,主要通过使DNA双螺旋小沟处的鸟嘌呤的N-2发生烷基化,从而阻断DNA的复制和合成,抑制肿瘤细胞分裂生长;(2)使耐药关键基因(包括致癌基因)和细胞生长关键基因的表达被选择性地抑制;(3)抑制遗传修复途径:Et-7434可以诱导转录基因致使DNA丝状体断裂,使肿瘤细胞死亡;(4)干扰细胞周期而致使p 53依赖性细胞程序化死亡;(5)扰乱肿瘤细胞微管网络;(6)Et-743可以和DNA结合蛋白及转录因子相互作用;(7)Et-743的可以作用于拓扑异构酶,高浓度Et-743可以在DNA和拓扑异构酶之间引起交联等。
4.2 Et-743的体外抗肿瘤活性 Et-743体外抗肿瘤活性测试表明:对白血病、宫颈癌、肺癌、乳腺癌、卵巢癌、软组织肉瘤等都有显著的抗肿瘤活性。其抗肿瘤活性显著比目前临床上的一线抗肿瘤药物高。Et-743与多柔比星等抗肿瘤药物显示协同作用[19]。Et-743对L 1210小鼠白血病肿瘤细胞株的IC 50值为0.5 ng/mL[20]。
4.3 Et-743的体内抗肿瘤活性 体内抗肿瘤活性研究发现通过腹腔及静脉给药时,Et-743可使卵巢癌、白血病、黑色素瘤、乳腺癌、非小细胞肺癌等多种肿瘤裸鼠的存活率显著提高,疗效与剂量呈良好的相关性,未出现药物致死现象;分别连续给药治疗效果远不如间歇给药治疗,对顺铂耐药的卵巢癌细胞的裸鼠Et-743同样有效[21]。腹腔或静脉给予Et-743[27µg/(kg·d)]治疗P 338白血病小鼠,使其生命延长率达148%,有效血药浓度为15 µg/kg[22]。Et-743治疗MX-1晚期乳腺癌,采用最佳剂量给药,23天后完全缓解率达90%[23],表明Et-743对白血病和乳腺癌具有显著抗肿瘤活性。
5 Et-743的临床研究
Et-743的I期临床研究:Et-743的I期临床研究表明Et-743对软组织肉瘤呈现良好的抗肿瘤活性。I期实验中,25例软组织肉瘤患者接受Et-743治疗后,56%的患者病情得到了很好的控制[24]。试验中发现,Et-743的剂量限制性毒性(DLT)主要表现为血液毒性和肝毒性,包括血小板减少、中性粒细胞减少、转氨酶异常,但都在可控、耐受范围内。
Et-743的II期临床研究:II期临床试验中Et-743用于多种肿瘤的治疗如卵巢癌、直肠癌、乳腺癌、黑素瘤和软组织肉瘤等,但对卵巢癌和软组织肉瘤治疗效果最为显著。Et-743对于异环磷酰胺和多柔比星等化疗药物无效的病人同样有效。患者对Et-743耐受性良好,剂量限制毒性(DLT)不累积、可逆和可控,没有心脏和神经毒性;Et-743治疗软组织肉瘤能显著提高病人的存活率[25-28]。
Et-743的III期临床研究:在III期临床实验中,Et-743用于软组织肉瘤和卵巢癌的治疗。189例晚期软组织肉瘤患者,通过连续静脉注射Et-743治疗,结果表明:13.5%的患者肿块减少,17%的患者延长了疾病的稳定性,6个月后存活率为25%-30%,10个月后的存活率为50%,一年后的存活率为45%[29-30]。2005-2009年欧洲多中心扩展临床试验共有1404例软组织肉瘤采用连续静脉注射Et-743治疗,504名有效评价病例中,8%的患者得到了完全或部分缓解,33%的患者疾病的稳定性得到了有效控制,一年后的存活率为45%[31]。
2001年5月Et-743作为治疗软组织肉瘤的孤药被欧盟人用医药产品委员会批准进入临床研究;2003年10月又被批准作为治疗卵巢癌的孤药;2007年欧洲药品管理局(EMEA)正式批准Et-743作为治疗晚期软组织肉瘤药物在27个欧盟国家上市,2009欧洲药品管理局(EMEA)批准Et-743作为治疗卵巢癌药上市,后又被批准在欧洲和加拿大等地区治疗复发卵巢癌。而FDA认为该药缺乏充足的不良反应资料,而至今未批准其在美国上市。
6 小结与展望
Et-743是第一个成功上市的海洋抗肿瘤药物,从发现到上市历经近40年,从Et-743的研发过程我们可以发现:(1)Et-743具有独特新颖的化学结构和多重作用机制,显著的体内外抗肿瘤活性,是一种新型的海洋抗肿瘤药物;(2)Et-743药源不足,是其深入开展体内活性、临床试验研究的瓶颈;(3)Et-743分子结构复杂,化学合成往往需要特殊的反应条件和试剂,合成路线繁琐复杂、产率低,很难实现工业化生产。
Et-743的研究给我们带来了以下一些启示:(1)从海洋生态系统筛选和提取天然活性物质成为抗肿瘤药物研究的重要途径。(2)海洋天然抗肿瘤药物研究需要多领域、多学科合作,化学研究者与肿瘤药理研究者合作,能加快海洋天然抗肿瘤药物研究;(3)现代生命科学技术以及药物筛选、化学合成和制备技术的发展,将有利于海洋天然抗肿瘤药物进一步研究和开发。Et-743海洋抗肿瘤药物的上市使我们相信,未来会有越来越多的海洋天然抗肿瘤药物进入市场,为人类的抗癌事业提供更多新的选择。
[1] Brett A,SchroederEve T,Rodler Elizabeth T.Clinical benefit of trabectedin in uterine adenosarcoma[J].Med Oncol,2013(30):501-503.
[2] Sigel MM,Wellham LL,Lichter W,et al.In food-drugs from the sea prodeedings 1969[C].Youngken HW Jr.Ed.Washington DC:Marine Technol Soc,1970:281-294.
[3] Atmaca H,Bozkurt E,Uzunoglu S,et al.A diverse induction of apoptosis by trabectedin in MCF-7 (HER 2-/ER+) and MDA-MB-453 (HER 2+/ER-) breast cancer cells[J].Toxicol Lett,2013,221(2):128-136.
[4] Papaioannou D,Rafia R,Stevenson MD,et al.Trabectedin for the treatment of relapsed ovarian cancer[J].Health Technol Assess,2011,15(1):69-75.
[5] Preusser M,Spiegl-Kreinecker S,Ltsch D,et al.Trabectedin has promising antineoplastic activity in high-grade meningioma[J]. Cancer,2012,118(20):5038-5049.
[6] Rinehart KL,Holt TG,Fregeau N,et al.Ecteinascidins 729,743,745,759 B, and 770:potent antitumor agent from the Caribbean tunicate Ecteinascidia turbinate[J].J Org Chem,1990,55(15):4512-4515.
[7] Wright AE,Forleo DA,Gunawardana GP,et al.Antitumor tetrahydrodisoquinoline alkaloids from the colonial ascidian Ectdinascidia turbinate[J].J Org Chem, 1990,55(15):4508-4512.
[8] Corey EJ,Gin DY,Kania RS.Enantioselective total synthesis of ecteinascidin 743[J].J Am Chem Soc,1996,118(38):9202-9203.
[9] Endo A,Yanagisawa A,Abe M,et al.Total synthesis of ecteinascidin 743[J].J Am Chem Soc,2002,124(23):6552-6554.
[10] Chen J,Chen X,Bois-Choussy M,et al.Total synthesis of ecteinascidin 743[J].J Am Chem Soc,2006,128(1):87-89.
[11] Zheng S,Chan C,Furuuchi T,et al.Stereospecific formal total synthesis of ecteinascidin 743[J].Angew Chem Int Ed Engl,2006,45(11):1754-1759.
[12] Fishlock D.Williams RM.Synthetic studies on Et-743.Asymmetric stereocontrolled construction of the tetrahydroisoquinoline core via radical cyclization on glyoxalimine[J].J Org Lett,2006,8(15):3299-3301.
[13] Fishlock D.Williams RM.Synthetic studies on Et-743.Assembly of the pentacyclic core and a formal total synthesis[J].J Org Chem,2008,73(24):9594-9600.
[14] Gonzalez JF,Salazar L,Cuesta E,et al.Sysnthesis of phthalascidin analogs[J].Tet rahedron,2005,61(31):7447-7455.
[15] Cuevas C,Perez M,Martin MJ,et al.Synthesis of phthalascidin analogs[J].Org Lett,2000,2(16):2545-2548.
[16] Menchaca R,Martínez V,Rodríguez A,et al.Synthesis of natural ecteinascidins (ET-729,ET-745,ET-759 B,ET-736,ET-637,ET-594) from cyanosafracin B[J].J Org Chem,2003,68(23):8859-8866.
[17] Aune GJ,Furuta T,Pommier Y.Ecteinascidin 743:a novel anticancer drug with a unique mechanism of action[J].Anticancer Drugs,2002,13(6):5452-5551.
[18] Takano M,Ikeda Y,Kudoh K,et al.Complete remission of recurrent ovarian clear cell carcinoma by chemotherapy with bevacizumab,trabectedin and oxaliplatin[J].J Obstet Gynaecol Res,2013,39(4):872-875.
[19] Meredith K,Chuk MD,Alberta Aikin RN,et al.A phase I trial and pharmacokinetic study of a 24-hour infusion of trabectedin (Yondelis,ET-743) in children and adolescents with relapsed or refractory solid tumors[J].Pediatric Blood & Cancer,2012,59(5):865-869.
[20] Germano G,Frapolli R,Belgiovine C,et al.Role of macrophage targeting in the antitumor activity of trabectedin[J].Cancer Cell,2013,23(2):249-262
[21] Monk BJ,Dalton H,Benjamin I,et al.Trabectedin as a new chemotherapy option in the treatment of relapsed platinum sensitiveovarian cancer[J].Curr Pharm Des,2012,18(25):3754-3769
[22] Charytonowicz E,Terry M,Coakley K,et al.PPARγ agonists enhance ET-743-induced adipogenic differentiation in a transgenic mouse model of myxoid round cell liposarcoma[J].J Clin Invest,2012,122(3):886-898.
[23] Rath CM,Janto B,Earl J,et al.Meta-omic characterization of the marine invertebrate microbial consortium that produces the chemotherapeutic natural product ET-743[J].ACS Chem Biol,2011,6(11):1244-1256.
[24] Schoffski P,Wolter P,Clement P,et al.Trabectedin(ET-743):evaluation of its use in advanced soft-tissue sarcoma[J].Future Oncol,2007,3(4):381-392.
[25] Cesne AL,Judson I,Maki R,Trabectedin is a feasible treatment for soft tissue sarcoma patients regardless of patient age:a retrospective pooled analysis of five phase II trials[J].Br J Cancer,2013,109(7):1717-1724
[26] Grosso F,Jones RL,Demetri GD,et al.Efficacy of trabectedin (ecteinascidin-743) in advanced pretreated myxoid liposarcomas:a retro spective study[J].Lancet Oncol,2007,8(7):595-602.
[27] Roylance R,Seddon B,McTiernan A,et al.Experience of the use of trabectedin(ET-743,Yondelis) in 21 patients with pretreated advanced sarcoma form a single centre[J].Clin Oncol(R Coll Radiol),2007,19(8):572-576.
[28] Krasner CN,Poveda A,Herzog TJ,et al.Patient-reported outcomes in relapsed ovarian cancer:results from a randomized Phase III study of trabectedin with pegylated liposomal doxorubicin (PLD) versus PLD alone[J].Gynecol Oncol,2012,127(1):161-167.
[29] Schur S,Lamm WK,Stler WJ,et al.Trabectedin in patients with metastatic soft tissue sarcoma:a retrospective single center analysis[J].Anticancer Drugs,2013,24(7):725-730.
[30] Genniqens C,Jerusalem G.Trabectedin (ET-743/Yondelis) for treating soft tissue sarcomas and ovarian cancer[J].Rev Med Liege,2011,66(7-8):452-455.
[31] Csaba Gajdos,Anthony Elias.Trabectedin:Safety and Efficacy in the Treatment of Advanced Sarcoma[J].Clin Med Insights Oncol,2011,(5):35-43.
Progress in the studies on marine antitumor drugs ecteinascidin-743
MA Man-ling1,2, KANG Chuan-zhe2, YANG Li-jie2
(1. Academy of Fundamental and Interdisciplinary Sciences, Harbin Institute of Technology, Harbin 150006, China; 2. The First Affiliated Hospital of Harbin Medical University, Harbin 150001, China )
At present the study of Marine antineoplastic drugs has already become the focus of concern around the world, Marine natural products has become an important source of clinical anti-cancer drugs. Ecteinascidin-743 from the Caribbean sea squirts Ecteinascidia turbinata extraction have been the ocean alkaloid, antitumor activity is signi fi cantly higher than the current widely used clinical antitumor drugs, inhibit a wide variety of tumor cell activity such as leukemia, ovarian cancer, soft tissue sarcoma, melanoma, cervical cancer, breast cancer, colorectal cancer, kidney cancer, prostate cancer, lung cancer and non-small cell lung cancer and other tumor cells, is the fi rst successful application to the oceans, clinical antitumor drugs. In this paper, the drug synthesis, pharmacological and clinical research progress were reviewed.
marine antineoplastic drugs; ecteinascidin-743; antitumor activity
R 9
A
1005-1678(2014)01-0147-03
马满玲,女,博士,硕士生导师,主任药师,研究方向:医院药学和临床药学,Email:mamanling@126.com。

