盐酸平阳霉素水溶蜡棒的研制及含量测定
刘娟,闫军,王凤山
(1.山东大学 药学院,山东 济南 250012;2.山东商业职业技术学院,山东 济南 250103;3.济南市皮肤防治院,山东 济南 250001)
盐酸平阳霉素水溶蜡棒的研制及含量测定
刘娟1,2,闫军3,王凤山1△
(1.山东大学 药学院,山东 济南 250012;2.山东商业职业技术学院,山东 济南 250103;3.济南市皮肤防治院,山东 济南 250001)
目的制备盐酸平阳霉素的水溶蜡棒,并建立蜡棒中盐酸平阳霉素含量测定方法。方法采用正交设计试验对蜡棒基质的配比及制备条件进行筛选,用高效液相色谱法对蜡棒中平阳霉素的含量进行测定。结果盐酸平阳霉素蜡棒基质处方为平平加与硬脂酸聚烃氧(40)脂质量比为1∶1,在温度70℃时加入主药,搅拌时间为20 min,制成蜡棒;高效液相色谱法测定蜡棒中盐酸平阳霉素含量在34.4~172 μg/mL线性关系良好,回归方程为y=8298.9 x-34996(r=0.9999),平均回收率为102.67%(n=9)。结论盐酸平阳霉素水溶蜡棒的制备工艺简单,性质稳定;利用高效液相色谱法测定蜡棒中平阳霉素含量的方法简便、快速,结果准确。
盐酸平阳霉素;水溶蜡棒;制备;高效液相色谱;含量测定
平阳霉素是从我国浙江平阳县土壤中的放线菌培养液中分离得到的抗肿瘤抗生素,经研究与国外的博来霉素(Bleomycin)成分相近。国产平阳霉素系博来霉素Aj单体,主要抑制胸腺嘧啶核苷酸掺入DNA,并与DNA结合使之破坏。另外,它也能使DNA单链断裂,并释放出部分游离核碱,进而破坏DNA模板,阻止DNA复制[1]。平阳霉素为白色疏松块状物或无定形固体,几乎无臭,引湿性强;易溶于水和甲醇,微溶于乙醇,在丙酮、氯仿和乙醚中几乎不溶。平阳霉素适应症为头颈部各部位鳞状上皮癌、皮肤癌、食道癌等[2]。缺点是半衰期短,临床应用时需一次给药4~20 mg,可静脉注射、肌内注射和瘤内注射,每日给药1次或隔日给药1次,最少需连续应用20 d以上[3]。目前有文献可查的蜡棒制剂有地蒽酚、蒽林的蜡棒制剂,并且蜡棒制剂的治疗效果要好于软膏制剂[4-5],平阳霉素有微球制剂、凝胶剂、栓剂、膜剂等[6-8],其蜡棒制剂未见报道。
本实验通过筛选平阳霉素合适的基质,制备易吸收并且使用方便的水溶性蜡棒,为临床提供一种新的、适用的、治疗银屑病的外用制剂。水溶性蜡棒应用时不需用手直接接触药物本身,从而可减少药物的浪费及对手部皮肤的刺激。
1 材料与方法
1.1 仪器与试剂 Waterse 2695高效液相色谱仪(配有Waters 2489紫外检测器),沃特世科技(上海)有限公司;85-2控温磁力搅拌器,金坛市医疗仪器厂;GY-1型果实硬度计,艾德堡仪器有限公司;FRQ-1008 HT 超声波清洗器,杭州法兰特超声波有限公司。
注射用盐酸平阳霉素(批号:121102),天津太河制药有限公司;平平加O-15(批号:11010979),江苏省海安石油化工厂;硬脂酸聚烃氧(40)脂(批号:20111101),南京威尔化工有限公司;甲醇和乙腈为色谱纯,Merck KGaA;水为娃哈哈纯化水。
1.2 方法
1.2.1 正交设计筛选蜡棒基质处方 因为硬脂酸聚烃氧(40)脂的熔点在46℃~51℃[9],平平加O-15熔点在32℃~35℃[10],加入药物时需先加热使基质熔融,且基质熔融时间随温度升高而缩短。因此,选取影响因素中加热温度为60℃、70℃、80℃。因为平阳霉素性质不稳定,需考察在以上三种加热温度下,温度、搅拌时间是否会使药物分解。因此实验采用了平平加质量(A)、S 40质量(B)、基质加热温度(C)、搅拌时间(D)4个因素,每个因素取3个水平(见表1)的L9(34)正交实验设计表进行实验设计。

表1 正交试验设计各因素水平表Tab.1 Experiment scheme of orthogonal design
按所指定的因素水平选用L9(34)正交试验表确定平阳霉素水溶蜡棒处方。将一定量的硬脂酸聚烃氧(40)脂和平平加在指定温度(±2℃)下加热融化,每组加入相同量的平阳霉素药物,于磁力搅拌器上按时间充分搅拌,使药物分散均匀,冷却,即得所需蜡棒。提取每组蜡棒中的平阳霉素,测定药物含量,并对结果用极差分析法进行分析。
按正交试验设计筛选出的最佳处方制备3批样品,对其进行硬度检查、延展性测试、皮肤刺激性试验以及耐热、耐寒试验。
1.2.2 平阳霉素蜡棒中药物含量的测定
(1)色谱条件 Agilent C8色谱柱(4.6 mm×150 mm,5µm),以己烷磺酸钠溶液(取己烷磺酸钠1.88 g与乙二胺四醋酸二钠1.96 g,加0.08 mol/L醋酸溶液使溶解并稀释至1000 mL,用氨溶液调节pH值至4.3)为流动相A;以甲醇-乙腈(7:3)为流动相B,检测波长为 254 nm,柱温25℃,流速1.0 mL/min,进样量20µL[11-12]。
(2)对照品溶液及供试品溶液的制备 取平阳霉素原料药约2 mg,精密称定,置于25 mL量瓶中,加水溶解并稀释至刻度,使成约80µg/mL的对照品溶液溶液。
取0.1%盐酸平阳霉素蜡棒样品2 g(相当于平阳霉素2 mg),提取,加水定容至25 mL,摇匀,制成约80µg/mL的供试品溶液。
(3)标准曲线的制备 取平阳霉素原料药约8.6 mg,精密称定,置于25 mL量瓶中,加水溶解并稀释至刻度,使成0.344 mg/ml的溶液,作为储备液。分别精密量取储备液1.0、1.5、2.0、3.0、4.0、5.0 mL,各置10 mL量瓶中,加水分别稀释至刻度,摇匀,即成浓度为34.4、51.6、68.8、103.2、137.6、172µg/mL的系列溶液。精密量取上述溶液各20µL,注入液相色谱仪,按照2.3.1的色谱条件,以峰面积与盐酸平阳霉素质量浓度(μg/mL)做线性回归。
(4)精密度试验 取对照品溶液3份,分别稀释至20、40、80µg/mL,取这三种浓度溶液按照2.3.1的色谱条件,每种浓度连续进样5次,每次20μL,记录峰面积。
(5)重复性试验 取同一批样品5份,按供试品溶液制备方法处理样品,按照2.3.1的色谱条件,分别进样20µL,记录峰面积积分值,进行分析。
(6)回收率试验 取蜡棒空白基质,精密称定,按照处方工艺,分别配成主药浓度为标示量的80%,100%,120%的模拟蜡棒样品各3份。按照供试品溶液制备方法,制成供试品溶液,取各浓度供试品溶液20µL,按照2.3.1的色谱条件,注入高效液相色谱仪,按外标法以峰面积计算含量,计算样品中平阳霉素回收率。
(7)样品含量测定 同一条件下制0.1%平阳霉素蜡棒3批,按供试品溶液制备方法处理,每批次进样3次,测平阳霉素含量。
1.2.3 统计学方法 数据处理采用SPSS 19.0软件,对正交实验数据采用极差分析法处理。
2 结果
2.1 平阳霉素蜡棒处方筛选情况 采用L9(34)正交试验结果及采用极差分析法对数据进行分析的结果见表2。
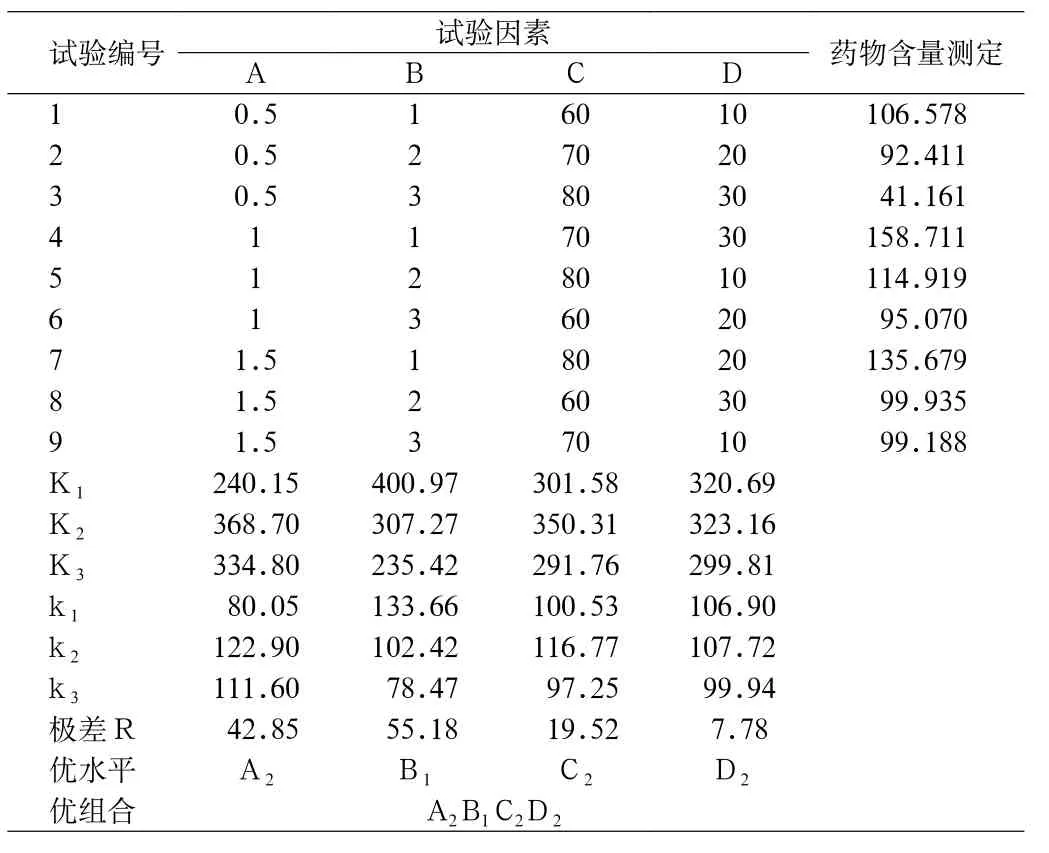
表2 正交试验结果与结果分析Tab.2 Experiment results of the orthogonal design
由表2结果可知,各因素对处方影响的顺序分别为B>A>C>D,根据药物含量选出最优组合为:平平加1 g,S40 1g,温度为70℃时加入主药,搅拌时间为20 min合适。
按正交试验设计筛选出的最佳处方制备3批样品,对其进行硬度检查、延展性测试、皮肤刺激性试验以及耐热、耐寒试验,结果符合标准[13]。
2.2 平阳霉素蜡棒中药物含量的测定情况
2.2.1 标准曲线的制备 取平阳霉素原料药制备的系列浓度溶液,按照2.3.1的色谱条件,以峰面积与盐酸平阳霉素质量浓度(μg/mL)做线性回归,回归方程为y=8298.9 x-34996(r= 0.9999),结果表明盐酸平阳霉素在34.4~172µg/mL浓度范围内线性良好。
2.2.2 精密度试验 3份不同浓度对照品溶液峰面积积分值的RSD分别为1.00%、0.22%、0.24%,结果精密度良好,说明方法可靠。
2.2.3 重复性试验 取同一批样品5份的供试品溶液,峰面积积分值RSD为3.3%,表明结果重复性良好。
2.2.4 回收率试验 主药浓度为标示量的80%,100%,120%的模拟蜡棒样品的供试液,计算平阳霉素回收率,结果见表3。

表3 加样回收试验结果Tab.3 The results of recovery
2.2.5 样品含量测定 同一条件下制备的3批0.1%平阳霉素蜡棒测得其平阳霉素平均含量为分别为98.03µg/g、95.29µg/g、99.18µg/g,RSD为2.05%,说明测定方法可靠。
3 讨论
平阳霉素注入人体,主要分布于皮肤及肺部[14],主要副作用有发热、胃肠道反应(恶心呕吐、食欲不振)、口腔炎,特别是肺毒性较严重[15]。所以考虑将平阳霉素改为外用剂型以治疗皮肤疾病,减小副作用。平阳霉素存在皮肤反应(色素沉着、角化增厚、皮炎、皮疹等)[15],制成蜡棒制剂,应用时不需用手直接接触药物本身,从而可减少药物的浪费及对手部皮肤的刺激。由于平阳霉素水溶液24 h内药物含量会发生显著变化[16],所以在选择外用制剂基质时,不适宜选择含水基质。本研究研制的平阳霉素水溶蜡棒选取的基质为硬脂酸聚烃氧(40)脂,用平平加调节蜡棒硬度。在蜡棒整个制备过程中没有水,药物性质稳定。因为硬脂酸聚烃氧(40)脂为表面活性剂,可以在水、乙醇或乙醚中溶解,所以洗除方便。
文献记载平阳霉素在25℃下性质稳定,15℃~25℃下原料药粉2年不降低效价[14],但是蜡棒的储存温度过高或过低都会有发硬现象,延展性变差,不适宜涂抹,所以平阳霉素水溶蜡棒的保存温度应控制在15℃~25℃。
采用HPLC法对蜡棒中盐酸平阳霉素的进行含量测定的测定条件参考了2010版药典二部中“盐酸平阳霉素”章节[12]。本次实验利用HPLC法测定平阳霉素含量时,对流动相中己烷磺酸钠溶液浓度、乙二胺四醋酸二钠浓度、pH值、甲醇-乙腈的配比进行摸索和筛选,在所建立的色谱条件下平阳霉素保留时间合适,比药典方法保留时间大大缩短,且峰形较好。
[1] 闫军,杨延安,李昌生,等.平阳霉素凝胶剂的制备与临床观察[J].中国药房,2011,12(1):27-28.
[2] 甄永苏,李电东.抗肿瘤抗生素平阳霉素研究与临床应用40年[J].中国抗生素杂志,2009,34(10):577-580.
[3] 赵勇.平阳霉素制剂的制备技术[J].健康必读杂志,2011,4(4):340.
[4] 张福仁,邵长庚,马道铭,等.蒽林蜡棒与蒽林软膏治疗银屑病的对照研究[J].临床皮肤科杂志,1991,(5):247-248.
[5] Saraswat A,Agarwal R,Katare OP,et al.A randomized,double-blind,vehicle—controlled study of a novel liposomaldithranol formulation in psoriasis[J].J Dermatolog Treat,2007,18(1):40-45.
[6] 陈启蒙,李璐,韩志霞,等.紫外分光光度法测定平阳霉素膜剂含量[J].天津医科大学学报,2005,11(2):190-191.
[7] 闫军,赵桂华,李昌生.平阳霉素栓的制备及临床应用[J].中国医院药学杂志,2001,21(12):757-758.
[8] 吕伟,张晓红,高扬.平阳霉素及其微球制剂的研究进展[J].现代生物医学进展.2011,11(8):1589-1590.
[9] 国家药典委员会.中华人民共和国药典(二部)[S].北京:中国医药科技出版社,2005:912.
[10] Chemical Book——平平加O-15 性质[OL].http://www.chemicalbook.cn/Pro ductChemicalPropertiesCB 32126200.htm.
[11] 杨倩,吴燕,袁雯玮,等.梯度洗脱HPLC法测定盐酸平阳霉素及注射药物中的有关物质[J].中国抗生素杂志,2009,34(8):481-484.
[12] 国家药典委员会.中华人民共和国药典(二部)[S].北京:中国医药科技出版社,2010:659-660.
[13] QB/T 1977-2004,唇膏[S].
[14] 闫军,张君仁,王海钠.平阳霉素霜的研制[J].中国药业,2001,10(1):46-47.
[15] 王文锦.平阳霉素作用机制和临床应用[J].中国肿瘤临床,1992,19(3):223-224.
[16] 李成玲,张古英,刘艳辉.平阳霉素与利多卡因及氯化钠注射液配伍的稳定性考察[J].中国药师,2004,7(10):787-788.
Preparation of pingyangmycin water-soluble wax stick and the content determination
LIU Juan1,2,YAN Jun3,WANG Feng-shan1△
(1.School of Pharmaceutical Sciences, Shandong University, Jinan 250012, China; 2.Shandong Institute of Commerce and Technology, Jinan 250103,China; 3.Jinan Hospital for Skin Diseases Preven tion and Treatment, Jinan 250001, China)
Objiective To prepare pingyangmycin water-soluble wax stick and to establish its content determination method。MethodThe formula was optimized by orthogonal experiment and the content of pingyangmycin in wax stick was determined by high performance liquid chromatography (HPLC)。ResultsThe formula of pingyangmycin wax stick matrix was optimized as 1 g of alcohol ethoxylate and 1 g of S 40. Pingyangmycin was added when the temperature of the matrix raised to 70℃ and stirred for 20 min. The linear range of pingyangmycin determined by HPLC was 34.4~172 μg/mL,the regression equations was y=8298.9 x-34996(r= 0.9999),and the average recovery of pingyangmycin was 102.67 (n=9)。ConclusionThe Preparing procedure of pingyangmycin water-soluble wax sticks is simple and stable. The HPLC method for determining the content of pingyangmycin in water-soluble wax sticks is simple, fast and accurate.
pingyangmycin;water-soluble wax stick;preparation;high performance liquid chromatography;content determination
R 285;TQ 464.1
A
1005-1678(2014)01-082-03
刘娟,女,讲师,制药工程,E-mail:sdliujuan@163.com;王凤山,通信作者,教授, E-mail: fswang@sdu.edu.cn。

