热电池用NiS2的水热合成及放电性能
林保山,曹晓晖,杨少华,陈威宏
(1.沈阳理工大学 环境与化学工程学院,辽宁 沈阳 110159;2.辽宁省特种储备电源工程技术研究中心,辽宁 沈阳 110159)
热电池是一种利用机械激活装置或电激活装置使电解质瞬间熔融并对外输出电流的一次储备电池[1]。热电池广泛应用于智能武器当中,热电池阴极活性物质的好坏是热电池性能优劣的关键。立方晶系NiS2是一种热电池用阴极材料,材料的微观结构、颗粒大小、形貌对其物理性能、化学性能和电化学性能有显著的影响。目前,NiS2的主要制备方法:(1)超声热喷涂技术:Xiao-Feng Zhou等[2]用超声喷雾器将硫脲和NiCl2·6H2O从加热的通有氩气的石英管中喷涂到玻璃板上,分别在330℃、470℃下制备出四面体和圆锥体NiS2。(2)溶剂热法:Qian Xuefeng等[3]用NiCl2·6H2O与Na2S3制备出NiS2,该方法虽然操作简单,但是使用的有机溶剂易燃、易爆、有毒。(3)闪蒸法:I.J.Ferrer等[4]真空下将金属镍闪蒸到基体上350℃硫化20h,即获得NiS2薄膜。(4)水热法:水热法是一种较为普遍的化学合成方法,利用该方法合成FeS2和CoS2的文献较多。谢玲玲等[5]利用水热法合成黄铁矿型CoS2并研究了pH对产物结构和形貌的影响。吴荣等[6]利用水热合成FeS2并对其结构进行研究。NiS2同属黄铁矿型金属硫化物,形成机理较为相似,尚飞等[7]利用水热法一步合成NiS2。
本文采用水热合成法制备出不同形貌、不同颗粒大小的NiS2,并将其作为热电池阴极活性物质制备成单体电池进行放电性能测试。
1 实验
1.1 NiS2的制备
NiCl2·6H2O、Na2S2O3·5H2O、EDTA-2Na、CS2、盐酸、无水乙醇、氢氧化钠均为分析纯试剂。称量一定量的EDTA-2Na,投入盛有70mL去离子水的100mL的烧杯中,使其充分溶解。然后依次加入NiCl2·6H2O、Na2S2O3·5H2O,其中n(NiCl2·6H2O):n(Na2S2O3·5H2O)=1/2,并用磁力搅拌器搅拌。利用PHS-25型pH计,通过加入盐酸或氢氧化钠调节溶液pH,使其分别为1、4、7、9、11、13,充分混合后,转移至内衬为聚四氟乙烯的100mL的管式釜中,密封后置于鼓风干燥箱中,在140℃下加热24h后,自然冷却至室温。滤出黑色沉淀物,依次用稀盐酸、CS2、无水乙醇、去离子水洗涤2~3次,在70℃下真空干燥6h,经研磨制得NiS2粉体。
1.2 性能表征
采用日本D/max-RB型X射线衍射仪对样品进行物相分析(CuKα辐射,光阑系统为DS=SS=1°,RS=0.1mm,靶电压:40kV,靶电流:100mA。测角仪半径185mm,采用θ-2θ连续扫描方式,步长0.02°,扫描速度6°/min);采用日立S-3400N型扫描电子显微镜观察样品表面形貌;采用BT-9300ST激光粒度分布仪测试样品的粒度分布;采用DTA-100全自动微机差热议测试样品热解温度。
1.3 热电池单体电池的制备
阴极材料制备:将NiS2与LiCl-KCl、碳纳米管、MgO、LiSi以一定的比例充分混合,得到所需阴极材料。
在手套箱中,采用粉末压片制备工艺,将其装配成单体电池,放入通有惰性气体高纯氩气的管式炉中加热,使其电解质熔融从而激活,采用LAND电池测试系统(CT2001A)对单体电池进行放电测试。
实验分为三组:第一组阴极活性物质为不同形貌的NiS2在450℃、100mA/cm2时恒流放电;第二组不同形貌的NiS2制备成单体电池放电电流为100mA/cm2,每30s施加一次强度为1500mA/cm2的脉冲电流,脉冲宽度为1s;第三组为近立方体型NiS2锂化前后制备的单体电池在450℃、100mA/cm2时恒流放电。
2 结果与讨论
2.1 XRD分析
图1为反应温度在140℃时,溶液初始pH不同时所得样品NiS2的XRD谱图。
所得样品XRD谱图与黄铁矿型立方晶系NiS2标准衍射谱图(PDF card no.11-99)对比可见,不同pH下所得的样品的主相都是NiS2,有少量杂质出现。其中当初始反应体系pH=1、4时,XRD谱图中显示在低角度处出现了少量较弱的S8和S的晶面特征衍射峰;酸性时,产物中有硫杂质生成,在一定程度上降低了产物中NiS2的纯度。pH=7、9时XRD谱图中没有出现明显杂质,说明pH=7、9时产物纯度较高。而当pH=11、13时,产物中有Ni(OH)2生成。

图1 在140℃时、不同pH下合成样品的XRD图
2.2 SEM分析
图2为不同pH下水热合成样品的SEM图。

图2 不同pH合成的NiS2的SEM图
由图2可见:pH=1、4时,产物NiS2形貌均为近立方体型,颗粒尺寸为1μm左右,同时呈现出一定的团聚现象;pH=7的中性溶液时,产物形貌及颗粒尺寸均发生了显著变化,形成的NiS2均为球形,颗粒尺寸明显增大;当pH大于9时,球形颗粒周围产生许多细小的粉末,且随着pH的增大而更加显著,这可能与产物中生成较多的Ni(OH)2有关。
2.3 粒度分析
图3为不同pH下水热合成的NiS2粒度分布曲线。
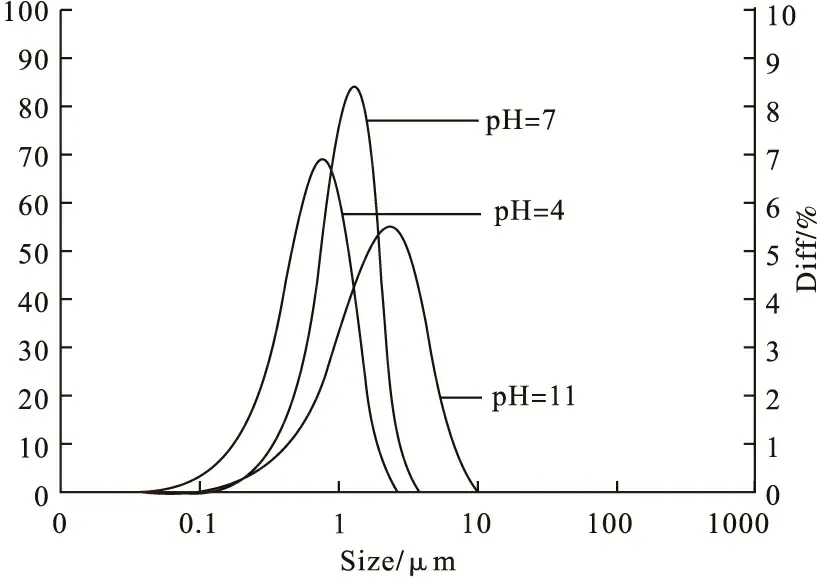
图3 不同pH合成的NiS2粒度分布曲线
由图3可见:中性条件(pH=7)下合成的球形NiS2颗粒尺寸最大;碱性条件(pH=11)下合成的片形结构NiS2颗粒尺寸最小;酸性条件(pH=4)下合成的近立方体NiS2颗粒大小居中。片形、球形、近立方体型平均颗粒尺寸约为0.803μm、1.376μm、2.371μm,颗粒尺寸与SEM测得尺寸基本一致。
2.4 差热分析
图4为水热合成的FeS2、NiS2的DTA曲线。

图4 水热合成的FeS2、NiS2的DTA曲线
由图4可见:NiS2分解温度明显高于FeS2,FeS2、NiS2最高分解温度分别为590℃、650℃,NiS2比FeS2分解温度高60℃。热电池的工作寿命由热寿命决定,因此分解温度越高加热粉量越多,其热寿命越长,从而热电池工作寿命越长,所以NiS2比FeS2更适合于长寿命热电池。
2.5 热电池单体电池放电性能
图5为阴极活性材料为不同pH合成的NiS2制备的单体电池在450℃时100mA/cm2恒流放电曲线。
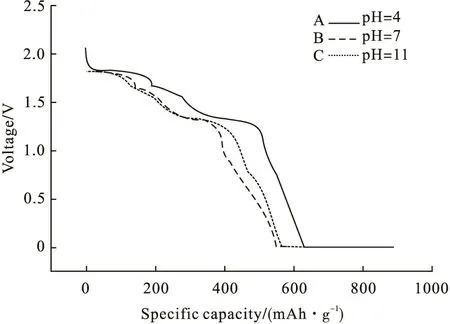
图5不同pH合成的NiS2单体电池在100mA/cm2恒流放电曲线
由图5可见:pH=4合成的近立方体型NiS2制备的单体电池放电电压高于pH=7和pH=11合成的球形、片形NiS2制备的单体电池放电电压,第一放电平台为1.84~1.85V;pH=7和pH=11合成球形、片形的NiS2制备的单体电池第一放电平台为1.82~1.83V,约高出0.02V。另外,pH=4合成的近立方体型NiS2制备的单体电池放电比容量明显高于pH=7和pH=11合成的球形、片形NiS2制备的单体电池放电比容量,终止电压为1.5V时:pH=4、pH=7、pH=11合成的近立方体型、球形、片形NiS2制备的单体电池放电比容量分别为293.8mAh/g、214mAh/g、211.1mAh/g。
pH=4合成的近立方体型NiS2制备的单体电池放电性能明显优于pH=7和pH=11合成的球形、片形NiS2制备的单体电池放电性能,主要原因是颗粒尺寸较小,比表面积较大。比表面积对极化的影响较大:比表面积越大,实际工作电流密度越小;阴极极化越小,极化电压降越小。因此pH=4合成的近立方体型NiS2制备的单体电池具有较高的放电电压和较大的放电比容量。pH=11时片形NiS2颗粒尺寸虽然最小,但是含有Ni(OH)2影响其放电性能。
图6为不同pH合成的NiS2制备的单体电池脉冲内阻变化曲线。
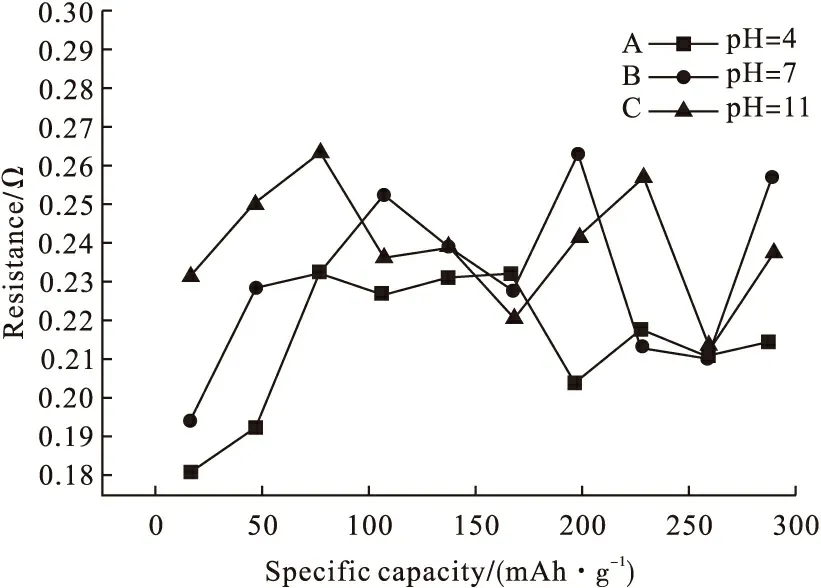
图6不同pH合成的NiS2制备的单体电池脉冲内阻变化曲线
由图6可知,pH=4合成的近立方体型NiS2制备的单体电池脉冲内阻比pH=7和pH=11合成的球形、片形NiS2制备的单体电池脉冲内阻小,这进一步说明了近立方体型NiS2制备的单体电池放电电压与放电比容量比球形、片形高的原因。
图7为近立方体型NiS2锂化前后单体电池在450℃、100mA/cm2恒流放电曲线。

图7 近立方体型NiS2锂化前后单体电池恒流放电曲线
由图7可见:锂化后有效地消除了放电初期产生的电压尖峰,且第一放电平台几乎没有变化,而放电比容量较锂化前有所提高;终止电压为1.5V时,锂化前后放电比容量分别为293.8mAh/g、321.2mAh/g。
3 结论
本文以EDTA-2Na为螯合剂,NiCl2·6H2O和Na2S2O3·5H2O为反应物,在不同pH下,140℃时恒温24h水热合成不同形貌的NiS2。XRD与SEM分析表明,在酸性条件(pH=1、4)时合成样品为近立方体型NiS2。中性条件(pH=7)时合成样品为球形NiS2。碱性条件(pH=9、11)时合成样品为片形NiS2。激光粒度分析表明,随着pH增大颗粒尺寸先增大后减小。结果表明,pH可以调节产物的形貌和颗粒尺寸的大小。
差热分析表明,NiS2最高分解温度比FeS2高60℃,高的分解温度使得材料的热寿命长,因而制备的热电池工作寿命高于商用的FeS2热电池。不同形貌的NiS2制备成单体电池放电时,近立方体型NiS2放电电压及放电比容量都优于球形和片形,近立方体型NiS2制备的单体电池第一放电平台为1.84~1.85V,球形、片形的NiS2制备的单体电池第一放电平台为1.82~1.83V。近立方体型、球形、片形NiS2制备的单体电池放电比容量分别为293.8mAh/g、214mAh/g、211.1mAh/g。近立方体型NiS2锂化后放电性能优于未锂化,锂化后材料的放电比容量提高了27.4mAh/g。
[1]陆瑞生,刘效疆.热电池[M].北京:国防工业出版社,2005:267.
[2]Zhou Xiaofeng,Lin Lin,Wang Wei,et al.Shape evolution of NiS2minicrystals via thermodynamic controlled growth[J].J Cryst Growth,2011,(314):302-305.
[3]Qian Xuefeng,Li Yadong,Xie yi,et al.The synthesis and morphological control of nanocrystalline pyrite nickel disul?de and cobalt disulide[J].Mater Chem Phys,2000,(66):97-99.
[4]Ferrer I J,Sanchez C J.Synthesis of NiS2thin films electrical and optical properties[J].Mater Process Tech,1999,(92):239-242.
[5]谢玲玲,吴荣,李锦,等.pH值对水热合成黄铁矿型CoS2微晶的影响[J].J inorg chem,2011,27(1):95-99.
[6]吴荣,郑毓峰,张校刚,等.EDTA辅助水热合成FeS2/NiSe2复合纳米晶及其薄膜光电性质[J].物理学报,2004,53(10):3493-3497.
[7]尚飞,蒋莉,简基康,等.水热合成NiS2粉晶及Rietveld结构精修[J].J Synth.Cryst,2008,37(4):937.

