两种隐形眼镜对护理液中薄荷醇的吸收及释放研究
周方晴,曹阳,韩雪莲,许茜
(1.东南大学 公共卫生学院,江苏 南京 210009; 2.海昌隐形眼镜有限公司,江苏 丹阳 212331)
除作为外用制剂辅料使用外,薄荷醇(menthol)亦可作为清凉剂加入眼部制剂,以期减轻眼部刺激,缓解眼部干涩、灼热感[1]。研究[2-3]显示,薄荷醇可明显增加外用制剂中药物的透皮吸收率。若隐形眼镜片护理液中加入薄荷醇,镜片浸泡时则可能吸收其中的薄荷醇,而佩戴该镜片时其可能会释放至眼中。那么此时的薄荷醇是否会因其促吸收作用而带来一定的使用安全问题?国内外均未见相关的研究报道。因此,基于对薄荷醇特性的全面考虑,有必要研究隐形眼镜片对护理液中薄荷醇的吸收和释放程度,以评估其导致的眼部刺激或致敏作用的可能性,保证使用安全。
本研究拟建立隐形眼镜护理液和模拟眼内环境的ISO标准盐溶液(ISO10344)[4]中薄荷醇的检测方法,并进行隐形眼镜片对护理液中薄荷醇的吸收情况(是否)及吸收程度(多少),以及经浸泡的隐形眼镜片在模拟眼内环境的ISO标准盐溶液中薄荷醇的释放情况(是否)及释放程度(多少)的测试,为含薄荷醇的隐形眼镜护理液的安全性评价提供依据。
1 材料与方法
1.1 材料
受试样品均由海昌隐形眼镜有限公司提供,包括:J1102809隐形眼镜片(非离子型,含水量38%)、G1105599隐形眼镜片(离子型,含水量55%);隐形眼镜护理液(批号2120003);阴性样品液(除不含薄荷醇外,其他成分均按护理液配方配制的溶液);ISO标准盐溶液(pH 7.0等渗缓冲盐水溶液)。薄荷醇标准品(供含量测定用),面积归一化法测得百分含量为99.80%(中国药品生物制品检定所);色谱纯甲醇(德国默克公司)。
1.2 仪器和器材
气相色谱仪(日本岛津公司GC2010);固相萃取仪(美国Supelco公司Visiprep-DL);C18固相萃取小柱(50 μm,50 mg,迪马公司);精密分析天平(感量0.01 mg,瑞士梅特勒公司);超声清洗仪(济南巴克超声波科技有限公司)。
1.3 试验方法
1.3.1 色谱条件
色谱柱:DB-624毛细管气相色谱柱(0.32 mm×30 m,固定液膜厚1.8 μm,美国Agilent公司);检测器:火焰离子化检测器(flame ionization detector,FID);柱温(程序升温方式):初温80 ℃,3 min;温度上升速率4 ℃·min-1;终温150 ℃,3 min。进样口温度250 ℃;检测器温度250 ℃;氮气流速9.5 ml·min-1,氢气流速40 ml·min-1,空气流速400 ml·min-1,尾吹气流速30 ml·min-1。
1.3.2 护理液中薄荷醇鉴别及浓度测定
精密量取质量浓度为1 mg·ml-1的薄荷醇标准贮备溶液适量,加甲醇稀释制得质量浓度为50 μg·ml-1的标准溶液;精密量取5 ml护理液,以5 ml·min-1的速度经过固相萃取小柱(事先以0.5 ml蒸馏水和0.5 ml甲醇依次活化2次),0.5 ml甲醇洗脱,取1 μl洗脱液进样,按1.3.1之色谱条件行气相色谱分析,与1 μl薄荷醇标准溶液进样分析后所得的保留时间比较,以鉴别样品中的薄荷醇,并记录其峰面积,计算样品中的薄荷醇质量浓度(μg·ml-1)。
1.3.3 吸收试验
1.3.3.1 隐形眼镜片准备 以专用镊子取出隐形眼镜片,置吸水纸上将其表面水分轻轻拭干,之后精密称取并记录100片隐形眼镜片总质量(m总,mg)。如此法平行准备3份,共300片隐形眼镜片。
1.3.3.2 吸收试验容器对薄荷醇的吸收试验 取干燥洁净的1 000 ml广口试剂瓶,准确加入已测得薄荷醇的原始质量浓度(ρ0 h,μg·ml-1)的500 ml护理液,加盖密封,置于(25±2)℃的恒温水浴中,在2、4、6、8、12、24 h分别以移液管精密量取5 ml护理液,依1.3.2项下自“以5 ml·min-1的速度经过固相萃取小柱”起操作,分别计算各时间点护理液中薄荷醇的测得质量浓度(ρ2 h、ρ4 h、ρ6 h、ρ8 h、ρ12 h、ρ24 h,μg·ml-1),与ρ0 h比较,评价试验容器对薄荷醇的吸收情况和吸收程度。每个时间点取样结束后,即补充5 ml同温度[(25±2)℃]护理液,使护理液总体积不变。如法同时进行3只试验容器的吸收试验,容器标好序号。
取Opadry中药薄膜包衣材料适量,加水制成浓度为12%的包衣液,采用流化床包衣机对羚黄宝儿未包衣素丸(投料量750 g)进行包衣。
1.3.3.3 吸收试验 如1.3.3.1表面拭干并精密称重的100片隐形眼镜片,将其放入序号与1.3.3.2一一对应的容器中,准确加入500 ml已准确测得薄荷醇原始质量浓度(ρ0 h,μg·ml-1)的护理液,加盖密封,置于(25±2)℃的恒温水浴中,在2、4、6、8、12、24 h分别精密量取5 ml护理液,依1.3.2项下自“以5 ml·min-1的速度经过固相萃取小柱”起操作,分别计算各时间点护理液中薄荷醇的测得质量浓度(ρ2 h、ρ4 h、ρ6 h、ρ8 h、ρ12 h、ρ24 h,μg·ml-1),与ρ0 h比较,并结合1.3.3.2的测试结果,评价隐形眼镜片对薄荷醇的吸收情况和吸收程度。每个时间点取样结束后,即补充5 ml同温度[(25±2)℃]护理液,使护理液总体积不变。如法平行进行3份,共300片隐形眼镜片的吸收试验。
1.3.3.4 吸收试验结果计算 单位质量(mg)的干镜片吸收薄荷醇的质量(μg)设为m吸收,即m吸收=500×(ρ0 h-ρ吸收平衡)/m总,其中ρ吸收平衡为镜片吸收薄荷醇达到平衡时的质量浓度。
1.3.4 释放试验
1.3.4.1 隐形眼镜片准备 以专用镊子将1.3.3.3吸收实验结束后的隐形眼镜片取出,置吸水纸上将其表面水分轻轻拭干。从每份100片隐形眼镜片中随机挑出50片分为5组,每组10片,进行释放试验。
1.3.4.2 释放试验容器对薄荷醇的吸收试验 精密量取标准贮备溶液适量,加ISO标准盐溶液稀释制成每1 ml中含0.1 μg薄荷醇的模拟样品溶液,原始质量浓度准确测定后记为ρ0 h(μg·ml-1)。
取干燥洁净的50 ml广口试剂瓶,准确加入如上所述的模拟样品溶液10 ml,加盖密封,置于(37±2)℃的恒温水浴中。在2、4、6、8、15 h分别精密量取5 ml护理液(每个时间点从1只容器中取样,下个时间点从另外的容器取样),依1.3.2项下自“以5 ml·min-1的速度经过固相萃取小柱”起操作,分别计算各时间点护理液中薄荷醇的测得质量浓度(ρ2 h、ρ4 h、ρ6 h、ρ8 h、ρ15 h,μg·ml-1),与ρ0 h比较,评价试验容器对薄荷醇的吸收情况和吸收程度。如法平行进行15只试验容器(共分为3组,以便进行3份释放平行试验,每组5只)的吸收试验,每只容器按组别和考察时间点标好序号。
1.3.4.3 释放试验 取1.3.4.1处理的5组隐形眼镜片,将其分别放入5只经1.3.4.2吸收测试的50 ml广口试剂瓶中,每只容器中准确加入ISO标准盐溶液10 ml,得5组释放试验用样本,加盖密封,置于(37±2)℃的恒温水浴中。在2、4、6、8、15 h分别精密量取ISO标准盐溶液5 ml(注意容器序号与1.3.4.2一一对应,每个时间点从考察吸收时间相同的容器中取样,下个时间点从另外的经相应时间点考察吸收情况的容器中取样),依1.3.2项下自“以5 ml·min-1的速度经过固相萃取小柱”起操作,分别计算各时间点ISO标准盐溶液中薄荷醇的测得质量浓度(ρ2 h、ρ4 h、ρ6 h、ρ8 h、ρ15 h,μg·ml-1),并结合1.3.4.2的测试结果,评价隐形眼镜片对其可能吸收的薄荷醇的释放情况和释放程度。如此法进行3份平行试验。
1.3.4.4 释放试验结果计算 单个镜片释放薄荷醇的质量设为m释放(μg),即m释放=10×ρ释放平衡/m总,其中ρ释放平衡为镜片释放达到平衡时的质量浓度,ISO标准盐溶液中的薄荷醇质量浓度(μg·ml-1)。
2 结果与分析
2.1 吸收试验
2.1.1 吸收试验容器对薄荷醇的吸收试验
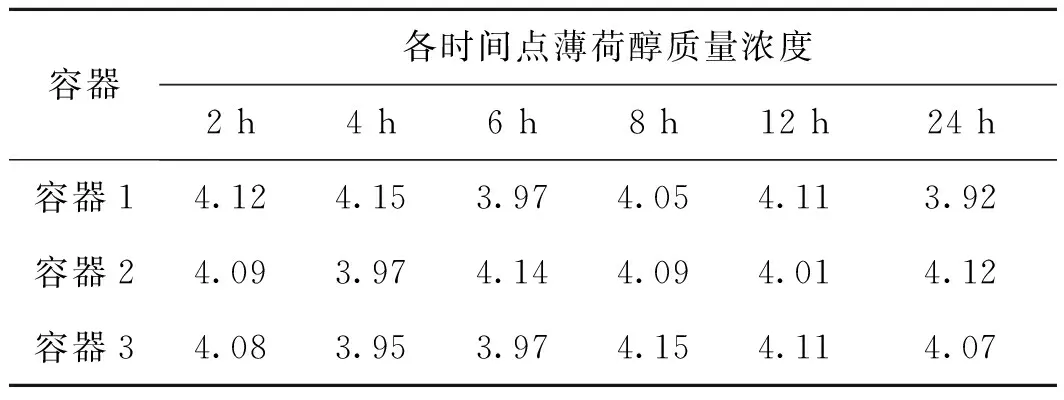
考察吸收试验所用容器时,各时间点护理液中薄荷醇的测得浓度见表1所示。护理液中薄荷醇原始浓度ρ0 h测得值为4.10 μg·ml-1。
每个容器在各时间点时护理液中薄荷醇的测得浓度,经t检验(置信度为95%)差异均无统计学意义,且与ρ0 h相比差异亦无统计学意义。结果提示,吸收试验所用各容器对薄荷醇无吸收或吸收可忽略不计。
表1容器吸收试验各时间点测得护理液中薄荷醇的质量浓度μg·ml-1
Tab1Containerabsorptionexperimenttesttheconcentrationofthementholinfunctionalcaresolutionateachtimepointμg·ml-1
容器各时间点薄荷醇质量浓度2 h4 h6 h8 h12 h24 h容器14.124.153.974.054.113.92容器24.093.974.144.094.014.12容器34.083.953.974.154.114.07
2.1.2 隐形眼镜片对护理液中薄荷醇吸收试验
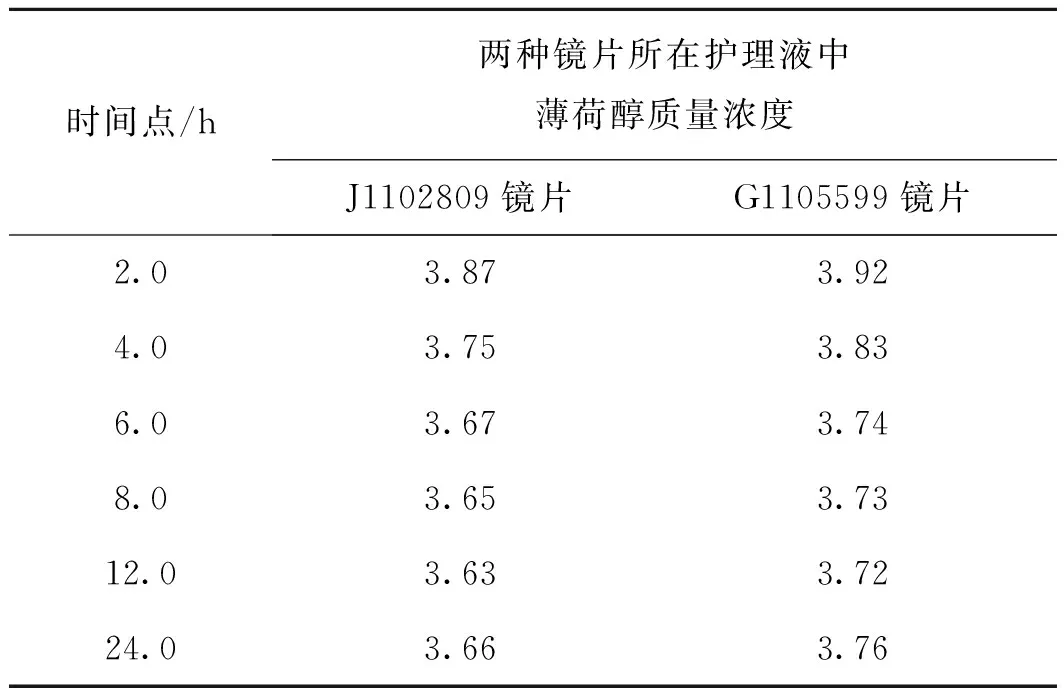
J1102809和G1105599隐形眼镜片在吸收试验各时间点测得护理液中薄荷醇的平均浓度(μg·ml-1)如表2所示。两种隐形眼镜片的测试结果经t检验(置信度为95%),各时间点质量浓度与起始的相比差异均有统计学意义,表明两种镜片对护理液中的薄荷醇均吸收;而ρ6 h、ρ8 h、ρ12 h、ρ24 h间差异无统计学意义,提示两种镜片均在6.0 h对薄荷醇的吸收即达平衡。ρ吸收平衡则以ρ6 h、ρ8 h、ρ12 h、ρ24 h的平均值计,J1102809和G1105599隐形眼镜片的ρ吸收平衡分别为3.65 μg·ml-1和3.74 μg·ml-1,表明100片浸泡于500 ml的护理液中共吸收薄荷醇分别为225 μg和180 μg。测得100片J1102809和G1105599干镜片的总质量分别为1 902.7 mg和1 493.4 mg,则计算得其单位质量(mg)干镜片吸收薄荷醇的质量分别为0.118 2 μg和0.120 5 μg。
表2隐形眼镜片吸收试验各时间点测得护理液中薄荷醇的平均质量浓度(n=3)μg·ml-1
Tab2Contactlensabsorptionexperimenttesttheconcentrationofthementholinfunctionalcaresolutionateachtimepoint(n=3)μg·ml-1
时间点/h两种镜片所在护理液中薄荷醇质量浓度J1102809镜片G1105599镜片2.03.873.924.03.753.836.03.673.748.03.653.7312.03.633.7224.03.663.76
2.2 释放试验结果
2.2.1 释放试验容器对薄荷醇的吸收试验
考察释放试验所用容器时,各时间点ISO标准盐溶液加标制成的模拟样品溶液中薄荷醇的测得浓度如表3所示。ISO标准盐溶液加标模拟样品溶液中薄荷醇原始质量浓度ρ0 h测得值为0.095 μg·ml-1。
表3容器释放试验各时间点测得护理液中薄荷醇的质量浓度
μg·ml-1
Tab3Containerreleaseexperimenttesttheconcentrationofthementholinfunctionalcaresolutionateachtimepoint

μg·ml-1
每个容器在各自时间点时ISO标准盐溶液加标模拟样品溶液中薄荷醇的测得浓度,经t检验(置信度为95%)差异均无统计学意义,且与ρ0 h亦无显著差异。结果提示,释放试验所用各容器对薄荷醇无吸收或吸收可忽略不计。
2.2.2 隐形眼镜片吸收薄荷醇的释放试验
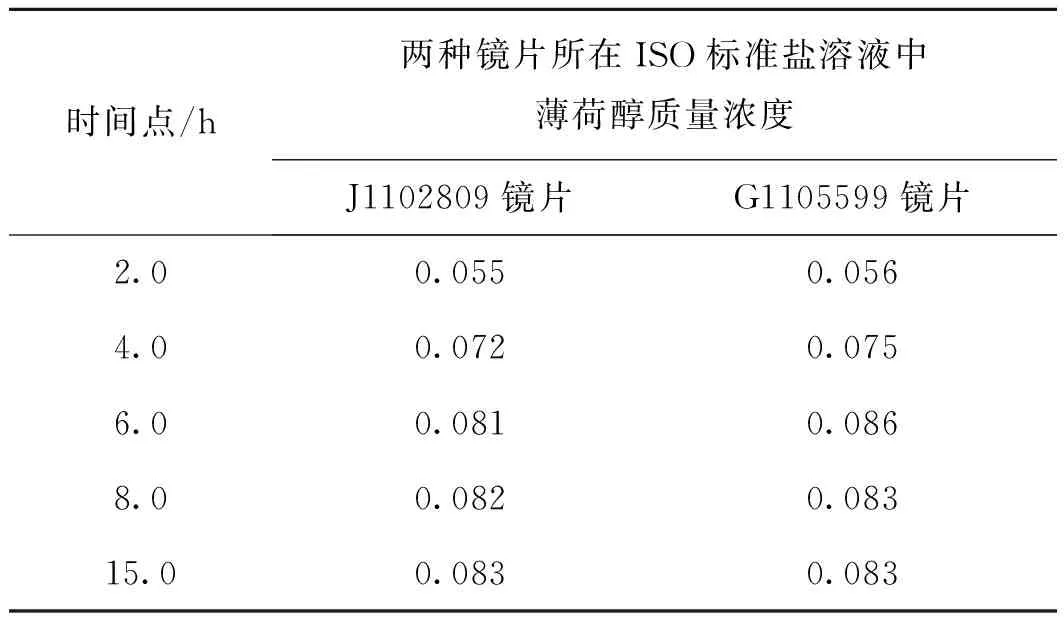
J1102809和G1105599隐形眼镜片在释放试验各时间点测得薄荷醇的平均质量浓度(μg·ml-1)如表4所示。结果表明,两种镜片在ISO标准盐溶液中均会释放之前在护理液中浸泡时吸收的薄荷醇。其检测结果经t检验(置信度为95%),ρ2 h、ρ4 h与ρ6 h、ρ8 h、ρ15 h间差异有统计学意义,而ρ6 h、ρ8 h、ρ15 h间差异无统计学意义,提示两种镜片在6.0 h对薄荷醇的释放均即达平衡。ρ释放平衡则以ρ6 h、ρ8 h、ρ15 h的平均值计,J1102809和G1105599镜片的ρ释放平衡分别为0.082 μg·ml-1和0.084 μg·ml-1,则单个J1102809和G1105599镜片释放薄荷醇的质量分别为0.082 μg和0.084 μg,计算得单位质量(mg)的J1102809和G1105599干镜片释放薄荷醇分别为0.004 3 μg和0.005 6 μg。
表4隐形眼镜片释放试验各时间点测得薄荷醇的平均浓度值(n=3) 两组孕鼠的平均摄食μg·ml-1
Tab4Contactlensreleaseexperimenttesttheconcentrationofthementholinfunctionalcaresolutionateachtimepoint(n=3)μg·ml-1
时间点/h两种镜片所在ISO标准盐溶液中薄荷醇质量浓度J1102809镜片G1105599镜片2.00.0550.0564.00.0720.0756.00.0810.0868.00.0820.08315.00.0830.083
3 总 结
本研究的两种隐形眼镜片分别为高含水离子型和低含水非离子型,是具有一定代表性的试验样本。研究结果表明,两种镜片对护理液中的薄荷醇虽有少量的吸收,在模拟眼内环境的ISO标准盐溶液中均只有微量的释放,提示含薄荷醇护理液的使用具有安全性。
[1] 胡士高,俞佳,宁黎丽,等.眼用制剂中添加清凉剂的思考[J].中国现代应用药学,2010,27(1):38-39.
[2] 程阔菊,王晖,陈垦.薄荷醇的安全性研究[J].辽宁中医杂志,2010,37(2):377-380.
[3] 齐红艺,李莉,吴纯洁.薄荷醇促渗透作用的研究进展[J].时珍国医国药,2006,17(9):1176-1178.
[4] ISO10344:1996《光学和光学仪器接触镜测试用盐溶液》[S].

